Chemie ist überall um dich herum - von den Atomen... Mehr anzeigen
Melde dich an, um den Inhalt zu sehenKostenlos!
Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Knowunity KI
Fächer
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Alle Themen anzeigen
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Alle Themen anzeigen
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Alle Themen anzeigen
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Alle Themen anzeigen
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Alle Themen anzeigen
1,600
•
Aktualisiert May 13, 2026
•
Celina Schürmann
@celinaschrmann_pfkr
Chemie ist überall um dich herum - von den Atomen... Mehr anzeigen


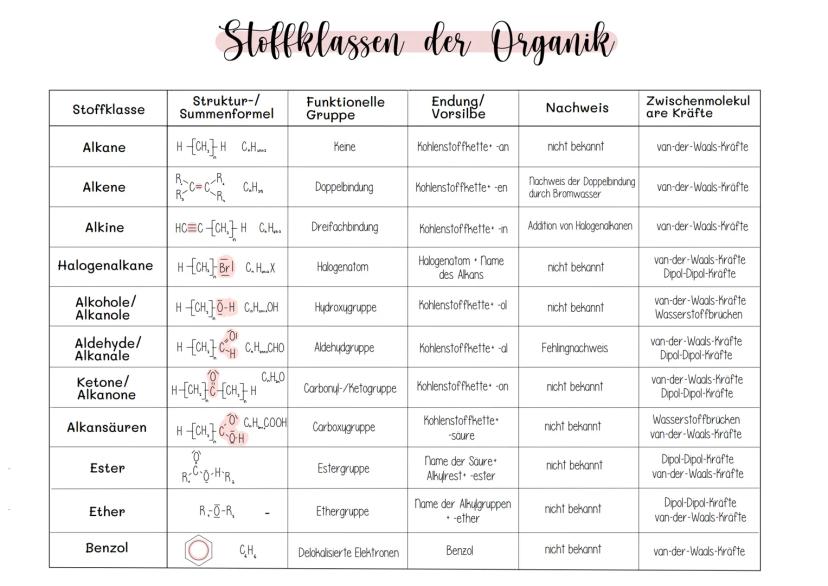




Das ist dein Starterpack für die Chemie im Abitur! Hier findest du alles Wichtige auf einen Blick, von Atommodellen bis zu organischen Verbindungen. Die Konzepte bauen logisch aufeinander auf.
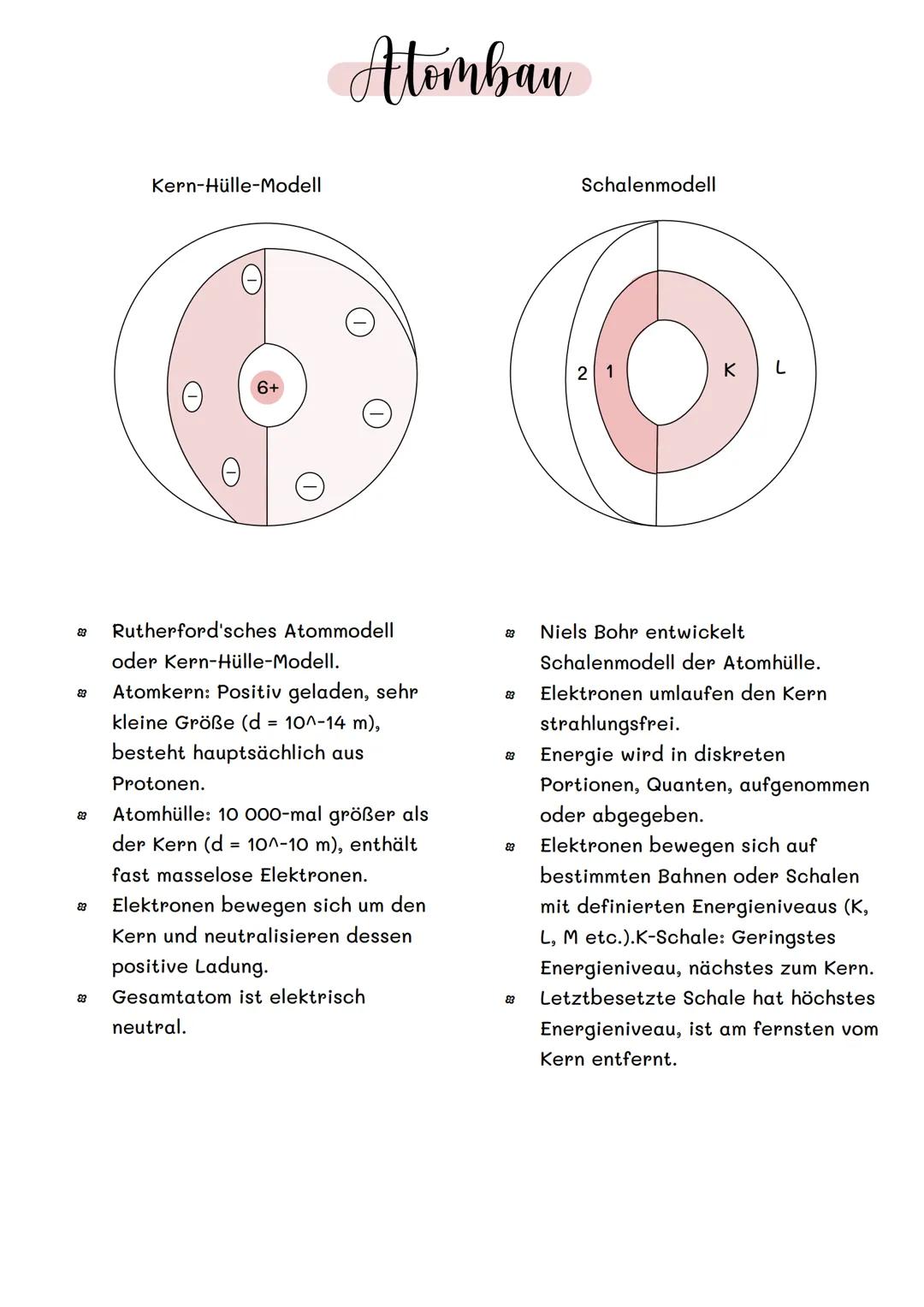
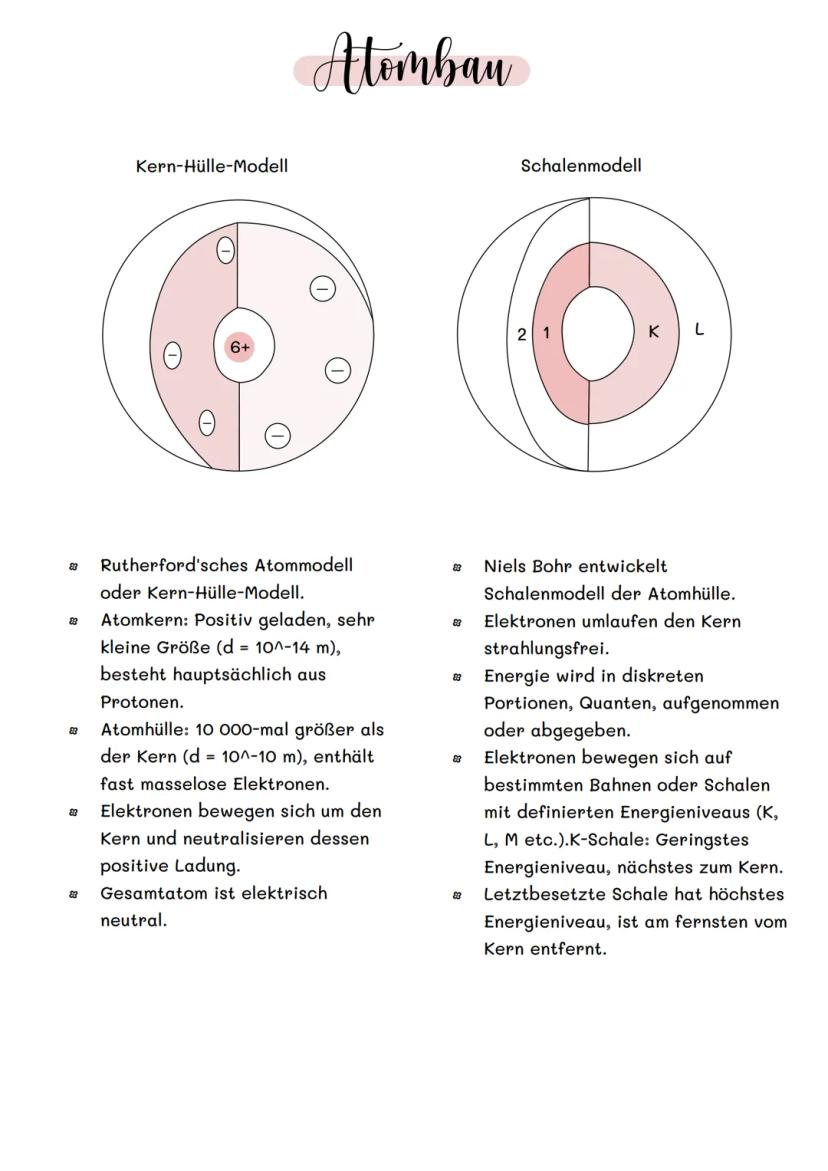
Das Rutherford'sche Atommodell zeigt dir den Grundaufbau: Ein winzig kleiner, positiv geladener Atomkern (nur 10⁻¹⁴ m groß) sitzt im Zentrum. Um ihn herum bewegen sich Elektronen in einer 10.000-mal größeren Atomhülle (10⁻¹⁰ m).
Niels Bohr entwickelte das Schalenmodell weiter. Die Elektronen kreisen nicht wild umher, sondern bewegen sich auf festen Energieniveaus - den K-, L-, M-Schalen. Je näher zum Kern, desto weniger Energie haben die Elektronen.
Die K-Schale ist dem Kern am nächsten und hat das niedrigste Energieniveau. Die äußerste Schale bestimmt die chemischen Eigenschaften des Atoms - sie ist für Reaktionen entscheidend.
Merktipp: Stell dir die Schalen wie Stockwerke vor - je höher, desto mehr Energie!
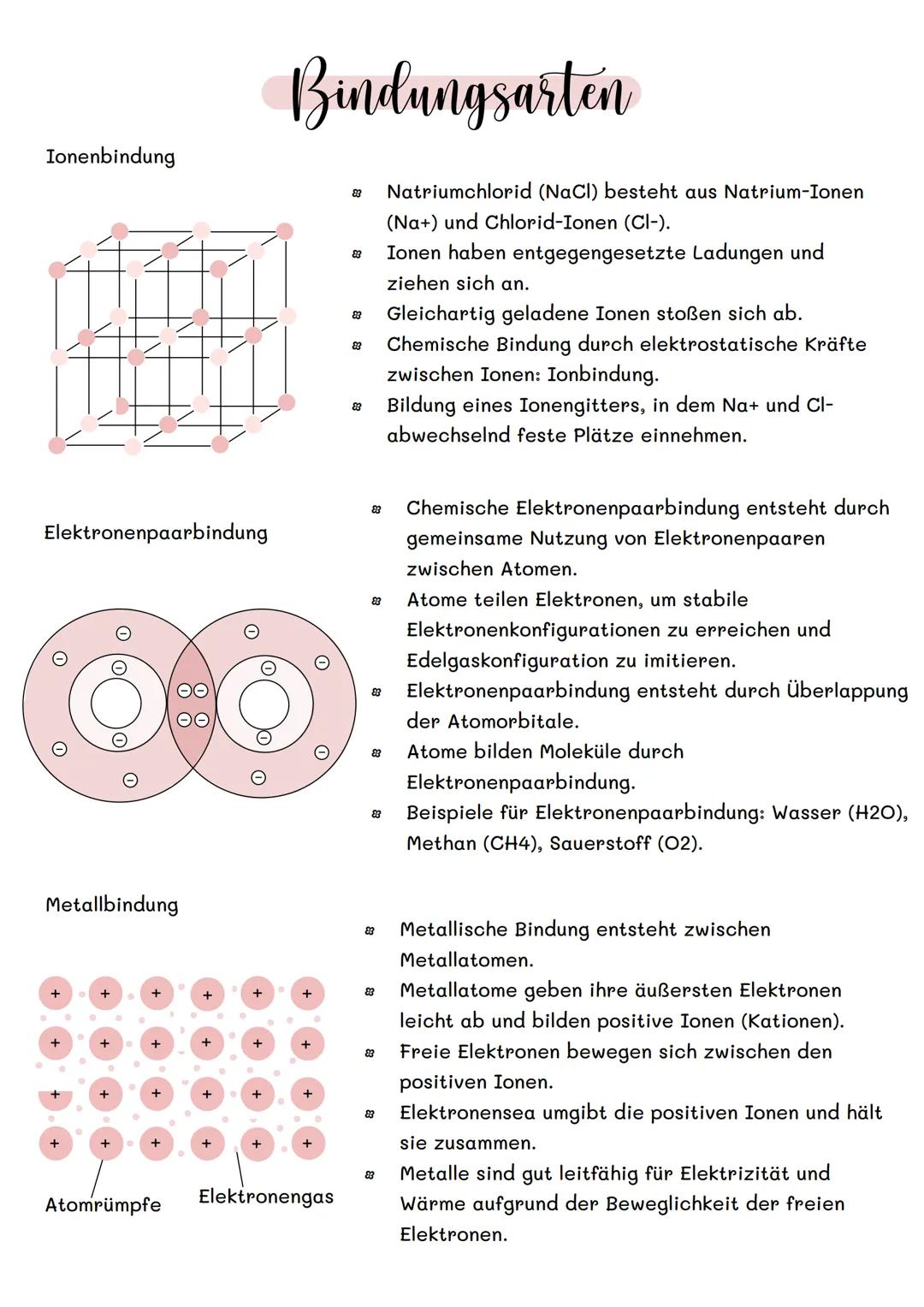
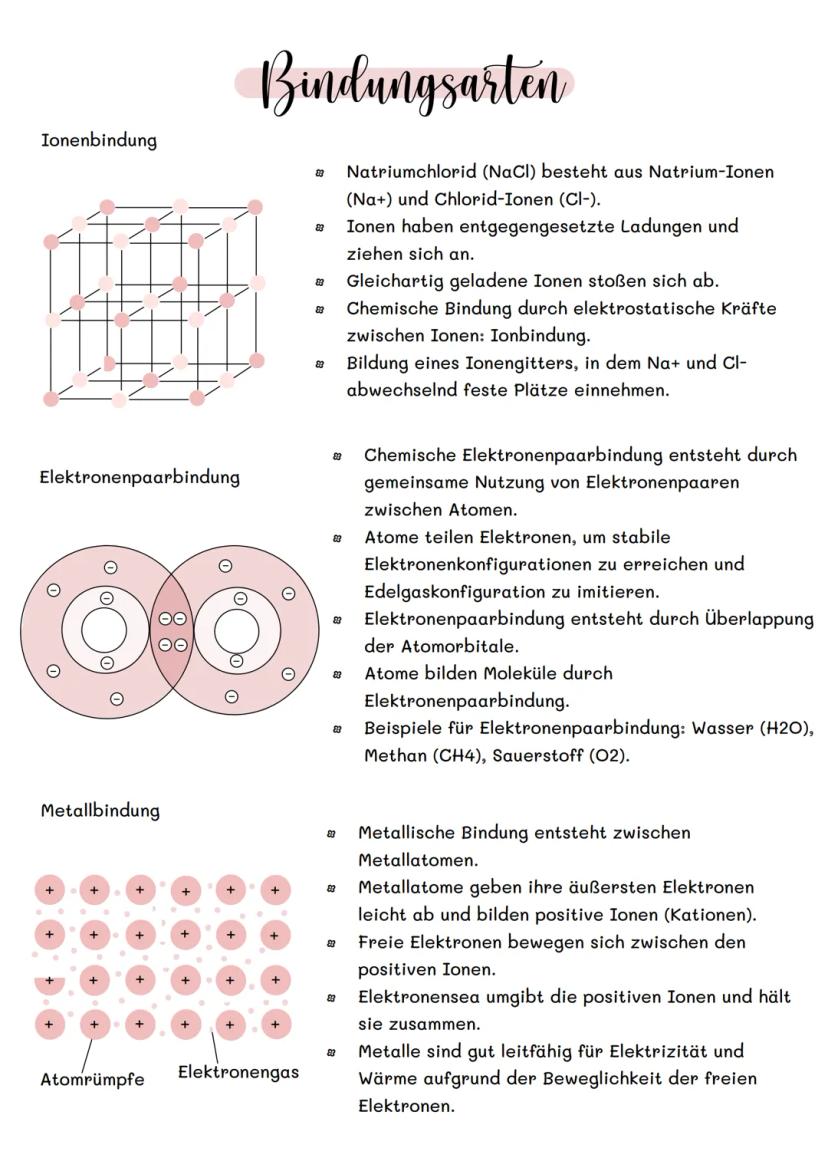
Ionenbindung entsteht, wenn Atome Elektronen komplett abgeben oder aufnehmen. Natriumchlorid (NaCl) ist das perfekte Beispiel: Na⁺-Ionen und Cl⁻-Ionen ziehen sich durch elektrostatische Kräfte an und bilden ein Ionengitter.
Bei der Elektronenpaarbindung teilen sich Atome Elektronen, anstatt sie abzugeben. So entstehen Moleküle wie Wasser (H₂O) oder Methan (CH₄). Die Atome "kooperieren", um die stabile Edelgaskonfiguration zu erreichen.
Metallbindung funktioniert anders: Die Metallatome geben ihre äußeren Elektronen ab und bilden ein "Elektronenmeer". Diese frei beweglichen Elektronen halten die positiven Ionen zusammen und machen Metalle leitfähig.
Praxistipp: Ionenbindung = Geben/Nehmen, Elektronenpaarbindung = Teilen, Metallbindung = Elektronenmeer
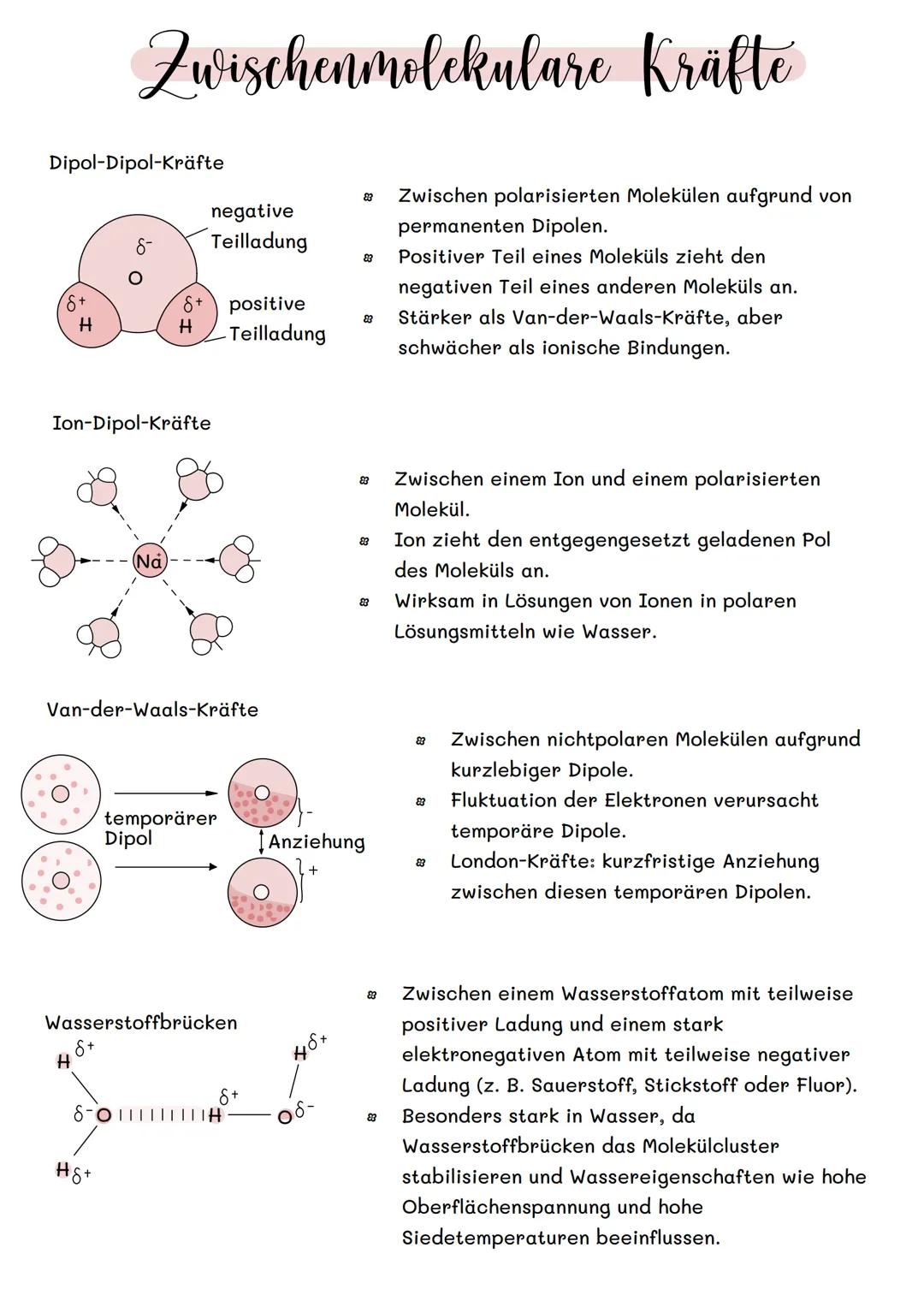
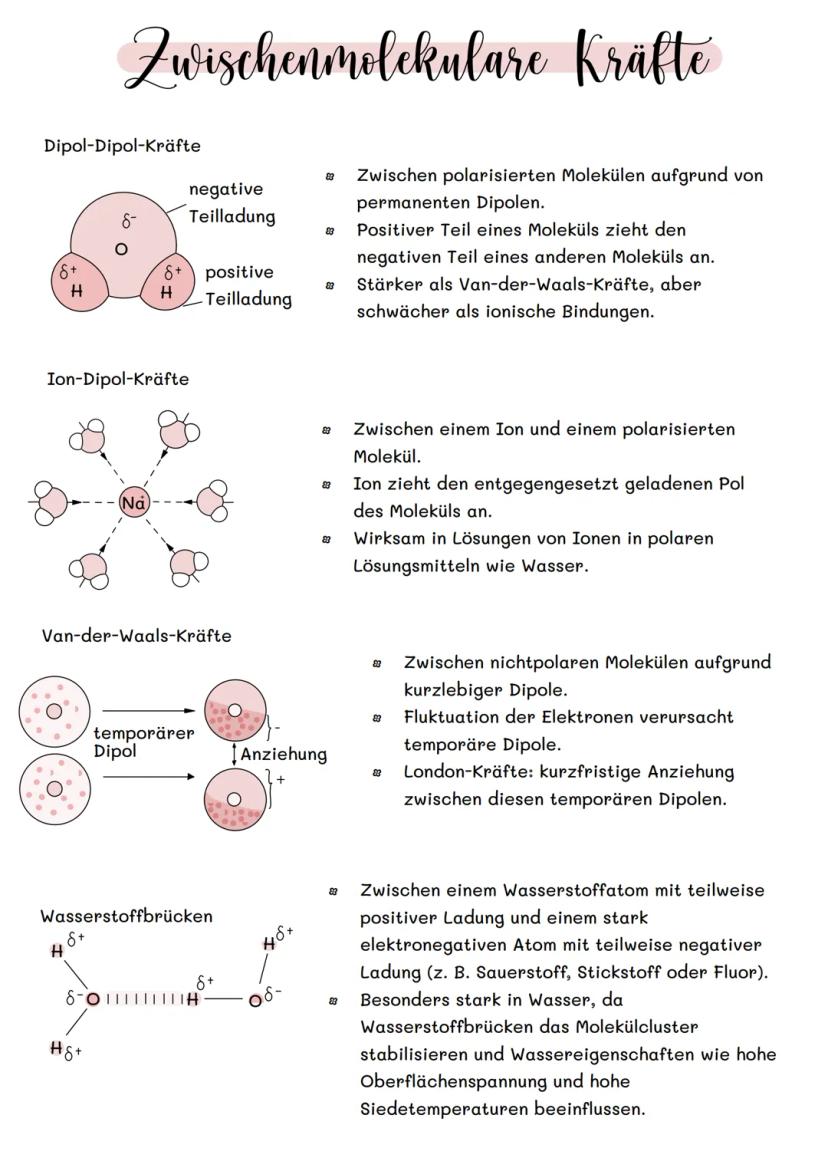
Dipol-Dipol-Kräfte wirken zwischen Molekülen mit permanenten Ladungsunterschieden. Der positive Teil eines Moleküls zieht den negativen Teil eines anderen an - wie kleine Magnete.
Van-der-Waals-Kräfte sind die schwächsten Kräfte. Sie entstehen durch kurzzeitige Elektronenbewegungen, die temporäre Dipole erzeugen. Selbst unpolare Moleküle können sich so anziehen.
Wasserstoffbrücken sind besonders stark. Sie bilden sich zwischen Wasserstoff und stark elektronegativen Atomen wie Sauerstoff oder Stickstoff. Deshalb hat Wasser so ungewöhnliche Eigenschaften!
Ion-Dipol-Kräfte treten auf, wenn Ionen auf polare Moleküle treffen - wichtig beim Lösen von Salz in Wasser.
Eselsbrücke: Wasserstoffbrücken sind wie starke Freundschaften - selektiv aber sehr stabil!

Stöchiometrisches Rechnen läuft immer nach dem gleichen Schema ab: Reaktionsgleichung aufstellen, Stoffmengen berechnen , Verhältnisse vergleichen, gesuchte Werte ermitteln. Die wichtigste Formel ist n = m/M.
Für Nachweisreaktionen musst du drei Klassiker kennen: Wasser macht weißes Kupfersulfat blau. Sauerstoff lässt einen glimmenden Holzspan wieder aufflammen. Wasserstoff knallt in der Knallgasprobe.
Das EPA-Modell (Elektronenpaarabstoßungsmodell) erklärt Molekülformen. Elektronen stoßen sich ab und nehmen den größtmöglichen Abstand zueinander ein - deshalb haben Moleküle bestimmte räumliche Strukturen.
Lerntipp: Übe stöchiometrische Rechnungen mit konkreten Beispielen - das Schema wird schnell zur Routine!
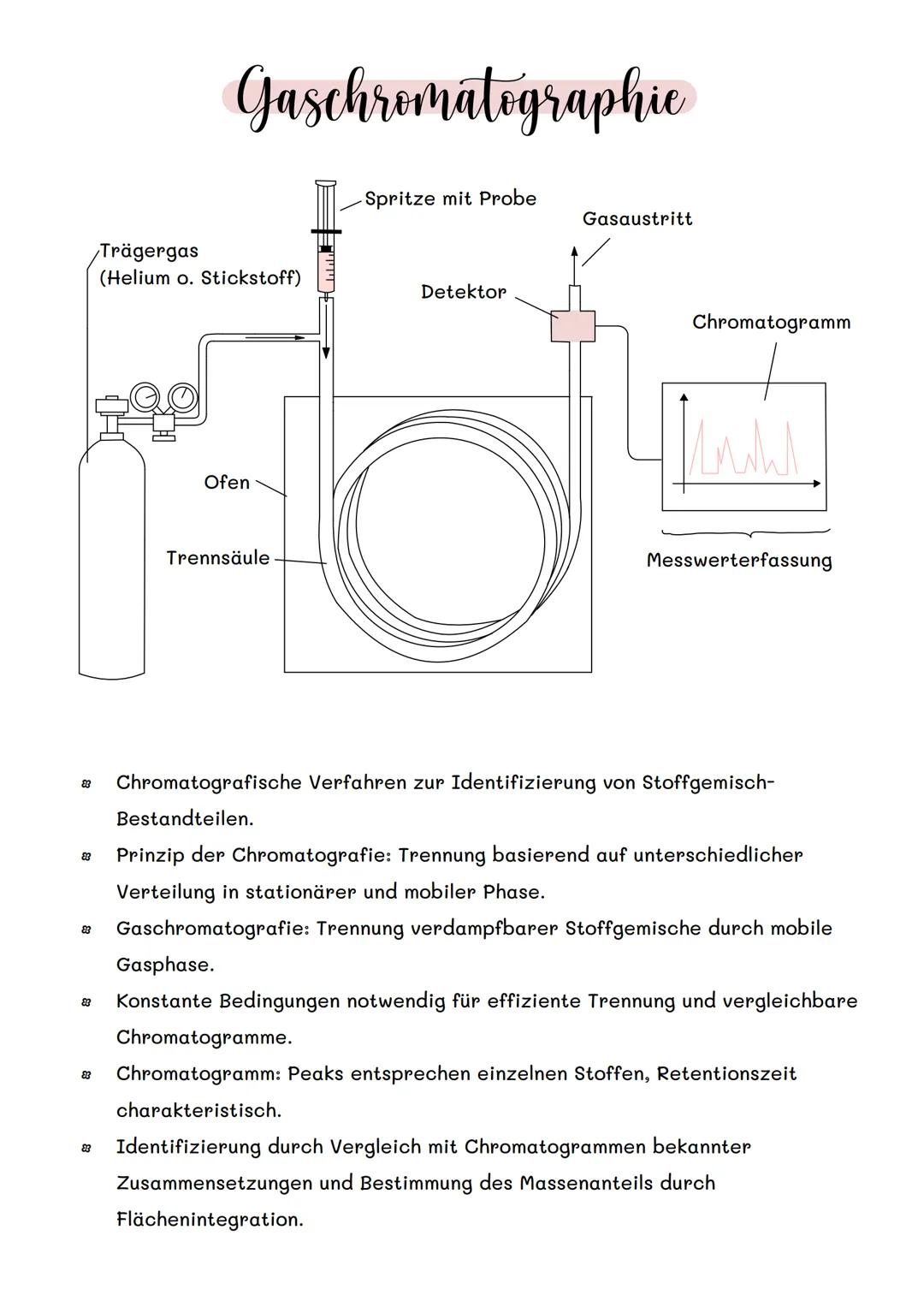
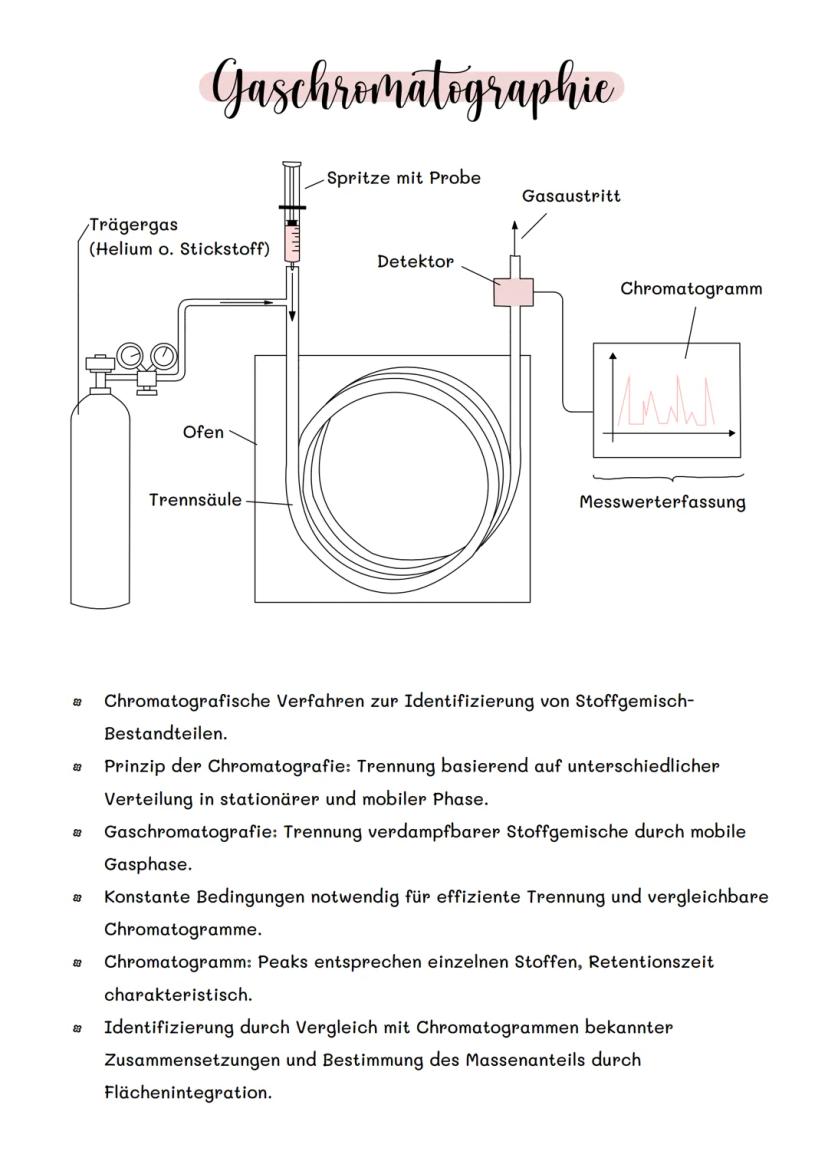
Gaschromatographie ist wie ein molekularer Fingerabdruck-Scanner. Das Verfahren trennt verdampfbare Stoffgemische durch eine mobile Gasphase (meist Helium oder Stickstoff), die durch eine Trennsäule fließt.
Das Prinzip basiert auf unterschiedlicher Verteilung zwischen stationärer und mobiler Phase. Jeder Stoff hat eine charakteristische Retentionszeit - die Zeit, die er braucht, um durch die Säule zu wandern.
Das Chromatogramm zeigt Peaks für jeden Stoff. Durch Vergleich mit bekannten Referenzen kannst du Stoffe identifizieren und über die Peakflächen sogar Mengenanteile bestimmen.
Konstante Bedingungen (Temperatur, Druck, Gasfluss) sind entscheidend für reproduzierbare Ergebnisse.
Anwendung: Forensik nutzt Gaschromatographie zur Analyse von Drogen, Sprengstoffen oder Brandbeschleunigern!
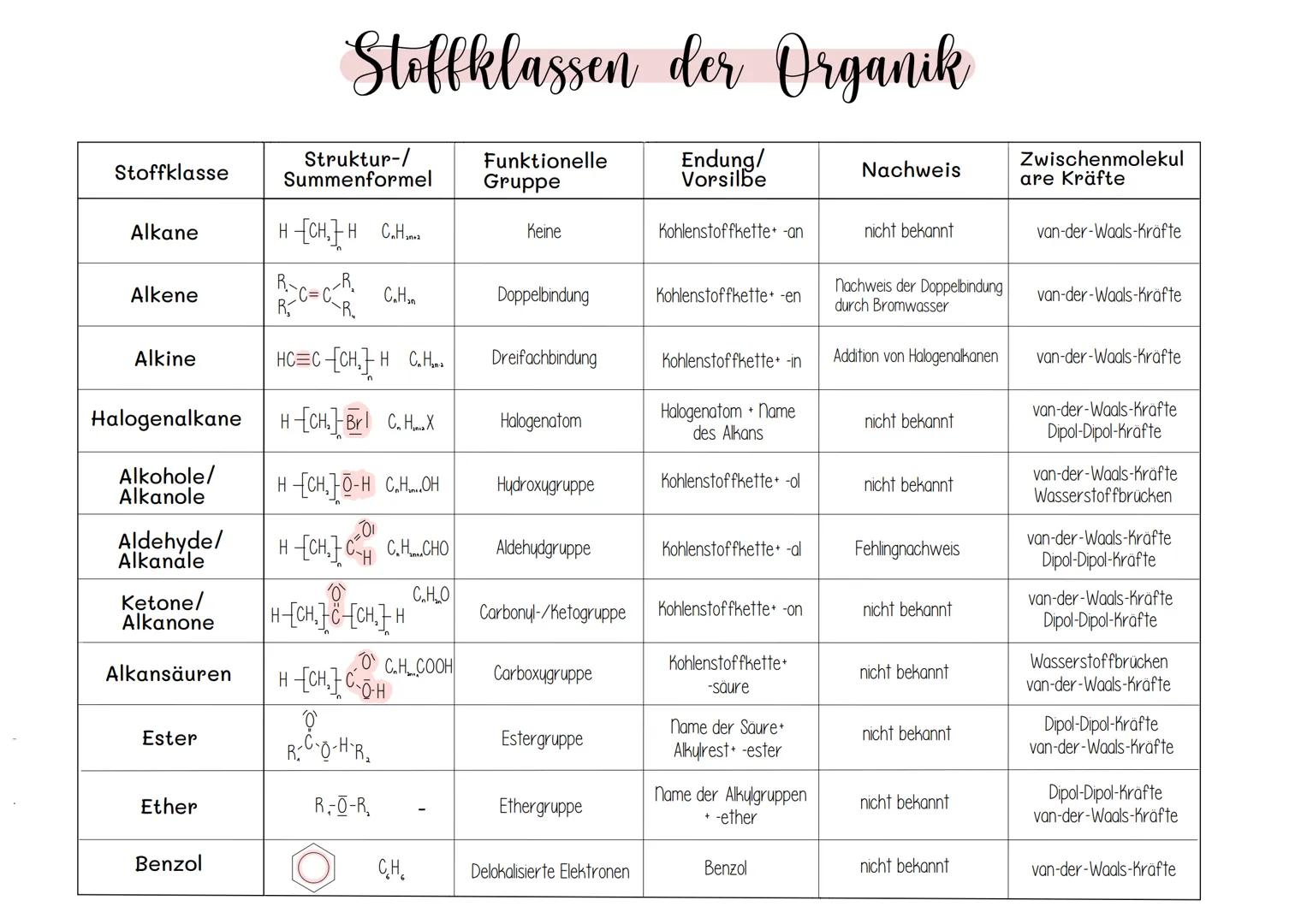
Alkane (CₙH₂ₙ₊₂) sind die Grundbausteine mit Endung "-an". Alkene haben Doppelbindungen und Alkine Dreifachbindungen . Alle drei zeigen hauptsächlich Van-der-Waals-Kräfte.
Alkohole und Alkansäuren können Wasserstoffbrücken bilden - deshalb sind sie oft wasserlöslich und haben höhere Siedepunkte. Die Hydroxyl- bzw. Carboxylgruppe macht den Unterschied.
Aldehyde und Ketone enthalten die Carbonylgruppe und zeigen Dipol-Dipol-Kräfte. Aldehyde lassen sich mit der Fehling-Reaktion nachweisen.
Ester und Ether sind Sauerstoffverbindungen mit charakteristischen Eigenschaften. Benzol ist der Grundkörper der Aromaten mit delokalisierten Elektronen.
Merkhilfe: Die funktionelle Gruppe bestimmt Name, Eigenschaften und zwischenmolekulare Kräfte!

Erdgas besteht hauptsächlich aus Methan (CH₄) mit über 90% Anteil. Dazu kommen geringe Mengen Ethan, Propan und Butan. Es ist leichter als Luft und brennt sauber.
Erdöl ist ein komplexes Gemisch aus Kohlenwasserstoffen. Die Hauptbestandteile sind Alkane (Paraffine), aber auch Alkene und Aromaten wie Benzol sind enthalten. Schwefel-, Stickstoff- und Sauerstoffverbindungen kommen als Nebenbestandteile vor.
Die Zusammensetzung variiert je nach Lagerstätte und geologischer Formation. Durch Raffination entstehen verschiedene Produkte: Benzin, Diesel, Heizöl, Schmierstoffe und Petrochemikalien.
Beide Rohstoffe sind entstanden aus organischem Material unter hohem Druck und hohen Temperaturen über Millionen von Jahren.
Faktencheck: Deutschland importiert über 95% seines Erdöls - Recycling und alternative Energien werden immer wichtiger!

Fraktionierte Destillation trennt Rohöl nach Siedepunkten. Im Destillationsturm steigen leichte Komponenten nach oben (Erdgas bei 20°C), schwere bleiben unten (Bitumen über 400°C). Dazwischen liegen Benzin, Kerosin und Diesel.
Cracken spaltet große Moleküle in kleinere auf. Thermisches Cracken nutzt hohe Temperaturen und Druck. Katalytisches Cracken arbeitet bei niedrigeren Temperaturen mit Katalysatoren.
Das Ziel ist die Herstellung leichter Kohlenwasserstoffe wie Benzin und Diesel aus schweren Ölfraktionen. Katalytisches Cracken ist selektiver und energiesparender.
Der kontinuierliche Prozess erzeugt verschiedene Fraktionen mit spezifischen Siedebereichen. Jede Fraktion hat unterschiedliche Anwendungen in Industrie und Alltag.
Umweltaspekt: Moderne Raffinerien arbeiten an effizienteren Verfahren, um weniger Energie zu verbrauchen!

Bei der Nomenklatur bestimmt die funktionelle Gruppe die Endung . Die längste Kohlenstoffkette mit der funktionellen Gruppe wird zur Hauptkette. Seitenketten bekommen die Endung "-yl".
Die Schritte: Hauptkette finden, durchnummerieren, Seitenketten alphabetisch ordnen, gleiche mit Di-, Tri-, Tetra- zusammenfassen. So entstehen systematische Namen wie 2-Methylpropan.
Isomere haben gleiche Summenformel, aber unterschiedliche Strukturen. Beispiel C₄H₁₀: Butan (gerade Kette) und 2-Methylpropan (verzweigt).
Cis-trans-Isomerie tritt bei Doppelbindungen auf. Cis bedeutet gleiche Seite, trans gegenüberliegende Seite der Substituenten. Diese räumlichen Unterschiede können völlig verschiedene Eigenschaften bewirken.
Prüfungstipp: Zeichne dir Strukturformeln auf - so siehst du Isomere sofort!
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Celina Schürmann
@celinaschrmann_pfkr
Chemie ist überall um dich herum - von den Atomen in deinem Handy bis zu den Molekülen in deinem Lieblingsgetränk. Diese Zusammenfassung zeigt dir die wichtigsten Grundlagen der Chemie, die du für dein Abitur brauchst.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Das ist dein Starterpack für die Chemie im Abitur! Hier findest du alles Wichtige auf einen Blick, von Atommodellen bis zu organischen Verbindungen. Die Konzepte bauen logisch aufeinander auf.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Das Rutherford'sche Atommodell zeigt dir den Grundaufbau: Ein winzig kleiner, positiv geladener Atomkern (nur 10⁻¹⁴ m groß) sitzt im Zentrum. Um ihn herum bewegen sich Elektronen in einer 10.000-mal größeren Atomhülle (10⁻¹⁰ m).
Niels Bohr entwickelte das Schalenmodell weiter. Die Elektronen kreisen nicht wild umher, sondern bewegen sich auf festen Energieniveaus - den K-, L-, M-Schalen. Je näher zum Kern, desto weniger Energie haben die Elektronen.
Die K-Schale ist dem Kern am nächsten und hat das niedrigste Energieniveau. Die äußerste Schale bestimmt die chemischen Eigenschaften des Atoms - sie ist für Reaktionen entscheidend.
Merktipp: Stell dir die Schalen wie Stockwerke vor - je höher, desto mehr Energie!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Ionenbindung entsteht, wenn Atome Elektronen komplett abgeben oder aufnehmen. Natriumchlorid (NaCl) ist das perfekte Beispiel: Na⁺-Ionen und Cl⁻-Ionen ziehen sich durch elektrostatische Kräfte an und bilden ein Ionengitter.
Bei der Elektronenpaarbindung teilen sich Atome Elektronen, anstatt sie abzugeben. So entstehen Moleküle wie Wasser (H₂O) oder Methan (CH₄). Die Atome "kooperieren", um die stabile Edelgaskonfiguration zu erreichen.
Metallbindung funktioniert anders: Die Metallatome geben ihre äußeren Elektronen ab und bilden ein "Elektronenmeer". Diese frei beweglichen Elektronen halten die positiven Ionen zusammen und machen Metalle leitfähig.
Praxistipp: Ionenbindung = Geben/Nehmen, Elektronenpaarbindung = Teilen, Metallbindung = Elektronenmeer

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Dipol-Dipol-Kräfte wirken zwischen Molekülen mit permanenten Ladungsunterschieden. Der positive Teil eines Moleküls zieht den negativen Teil eines anderen an - wie kleine Magnete.
Van-der-Waals-Kräfte sind die schwächsten Kräfte. Sie entstehen durch kurzzeitige Elektronenbewegungen, die temporäre Dipole erzeugen. Selbst unpolare Moleküle können sich so anziehen.
Wasserstoffbrücken sind besonders stark. Sie bilden sich zwischen Wasserstoff und stark elektronegativen Atomen wie Sauerstoff oder Stickstoff. Deshalb hat Wasser so ungewöhnliche Eigenschaften!
Ion-Dipol-Kräfte treten auf, wenn Ionen auf polare Moleküle treffen - wichtig beim Lösen von Salz in Wasser.
Eselsbrücke: Wasserstoffbrücken sind wie starke Freundschaften - selektiv aber sehr stabil!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Stöchiometrisches Rechnen läuft immer nach dem gleichen Schema ab: Reaktionsgleichung aufstellen, Stoffmengen berechnen , Verhältnisse vergleichen, gesuchte Werte ermitteln. Die wichtigste Formel ist n = m/M.
Für Nachweisreaktionen musst du drei Klassiker kennen: Wasser macht weißes Kupfersulfat blau. Sauerstoff lässt einen glimmenden Holzspan wieder aufflammen. Wasserstoff knallt in der Knallgasprobe.
Das EPA-Modell (Elektronenpaarabstoßungsmodell) erklärt Molekülformen. Elektronen stoßen sich ab und nehmen den größtmöglichen Abstand zueinander ein - deshalb haben Moleküle bestimmte räumliche Strukturen.
Lerntipp: Übe stöchiometrische Rechnungen mit konkreten Beispielen - das Schema wird schnell zur Routine!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Gaschromatographie ist wie ein molekularer Fingerabdruck-Scanner. Das Verfahren trennt verdampfbare Stoffgemische durch eine mobile Gasphase (meist Helium oder Stickstoff), die durch eine Trennsäule fließt.
Das Prinzip basiert auf unterschiedlicher Verteilung zwischen stationärer und mobiler Phase. Jeder Stoff hat eine charakteristische Retentionszeit - die Zeit, die er braucht, um durch die Säule zu wandern.
Das Chromatogramm zeigt Peaks für jeden Stoff. Durch Vergleich mit bekannten Referenzen kannst du Stoffe identifizieren und über die Peakflächen sogar Mengenanteile bestimmen.
Konstante Bedingungen (Temperatur, Druck, Gasfluss) sind entscheidend für reproduzierbare Ergebnisse.
Anwendung: Forensik nutzt Gaschromatographie zur Analyse von Drogen, Sprengstoffen oder Brandbeschleunigern!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Alkane (CₙH₂ₙ₊₂) sind die Grundbausteine mit Endung "-an". Alkene haben Doppelbindungen und Alkine Dreifachbindungen . Alle drei zeigen hauptsächlich Van-der-Waals-Kräfte.
Alkohole und Alkansäuren können Wasserstoffbrücken bilden - deshalb sind sie oft wasserlöslich und haben höhere Siedepunkte. Die Hydroxyl- bzw. Carboxylgruppe macht den Unterschied.
Aldehyde und Ketone enthalten die Carbonylgruppe und zeigen Dipol-Dipol-Kräfte. Aldehyde lassen sich mit der Fehling-Reaktion nachweisen.
Ester und Ether sind Sauerstoffverbindungen mit charakteristischen Eigenschaften. Benzol ist der Grundkörper der Aromaten mit delokalisierten Elektronen.
Merkhilfe: Die funktionelle Gruppe bestimmt Name, Eigenschaften und zwischenmolekulare Kräfte!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Erdgas besteht hauptsächlich aus Methan (CH₄) mit über 90% Anteil. Dazu kommen geringe Mengen Ethan, Propan und Butan. Es ist leichter als Luft und brennt sauber.
Erdöl ist ein komplexes Gemisch aus Kohlenwasserstoffen. Die Hauptbestandteile sind Alkane (Paraffine), aber auch Alkene und Aromaten wie Benzol sind enthalten. Schwefel-, Stickstoff- und Sauerstoffverbindungen kommen als Nebenbestandteile vor.
Die Zusammensetzung variiert je nach Lagerstätte und geologischer Formation. Durch Raffination entstehen verschiedene Produkte: Benzin, Diesel, Heizöl, Schmierstoffe und Petrochemikalien.
Beide Rohstoffe sind entstanden aus organischem Material unter hohem Druck und hohen Temperaturen über Millionen von Jahren.
Faktencheck: Deutschland importiert über 95% seines Erdöls - Recycling und alternative Energien werden immer wichtiger!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Fraktionierte Destillation trennt Rohöl nach Siedepunkten. Im Destillationsturm steigen leichte Komponenten nach oben (Erdgas bei 20°C), schwere bleiben unten (Bitumen über 400°C). Dazwischen liegen Benzin, Kerosin und Diesel.
Cracken spaltet große Moleküle in kleinere auf. Thermisches Cracken nutzt hohe Temperaturen und Druck. Katalytisches Cracken arbeitet bei niedrigeren Temperaturen mit Katalysatoren.
Das Ziel ist die Herstellung leichter Kohlenwasserstoffe wie Benzin und Diesel aus schweren Ölfraktionen. Katalytisches Cracken ist selektiver und energiesparender.
Der kontinuierliche Prozess erzeugt verschiedene Fraktionen mit spezifischen Siedebereichen. Jede Fraktion hat unterschiedliche Anwendungen in Industrie und Alltag.
Umweltaspekt: Moderne Raffinerien arbeiten an effizienteren Verfahren, um weniger Energie zu verbrauchen!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Bei der Nomenklatur bestimmt die funktionelle Gruppe die Endung . Die längste Kohlenstoffkette mit der funktionellen Gruppe wird zur Hauptkette. Seitenketten bekommen die Endung "-yl".
Die Schritte: Hauptkette finden, durchnummerieren, Seitenketten alphabetisch ordnen, gleiche mit Di-, Tri-, Tetra- zusammenfassen. So entstehen systematische Namen wie 2-Methylpropan.
Isomere haben gleiche Summenformel, aber unterschiedliche Strukturen. Beispiel C₄H₁₀: Butan (gerade Kette) und 2-Methylpropan (verzweigt).
Cis-trans-Isomerie tritt bei Doppelbindungen auf. Cis bedeutet gleiche Seite, trans gegenüberliegende Seite der Substituenten. Diese räumlichen Unterschiede können völlig verschiedene Eigenschaften bewirken.
Prüfungstipp: Zeichne dir Strukturformeln auf - so siehst du Isomere sofort!
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
43
Smart Tools NEU
Verwandle diesen Lernzettel in: ✓ 50+ Übungsfragen ✓ Interaktive Karteikarten ✓ Komplette Probeklausur ✓ Aufsatzgliederungen
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer