Bei chemischen Reaktionen spielt Energie eine zentrale Rolle - mal... Mehr anzeigen
Melde dich an, um den Inhalt zu sehenKostenlos!
Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Knowunity KI
Fächer
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Alle Themen anzeigen
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Alle Themen anzeigen
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Alle Themen anzeigen
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Alle Themen anzeigen
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Alle Themen anzeigen
220
•
Aktualisiert Apr 20, 2026
•
kk
@zoldyckxc
Bei chemischen Reaktionen spielt Energie eine zentrale Rolle - mal... Mehr anzeigen
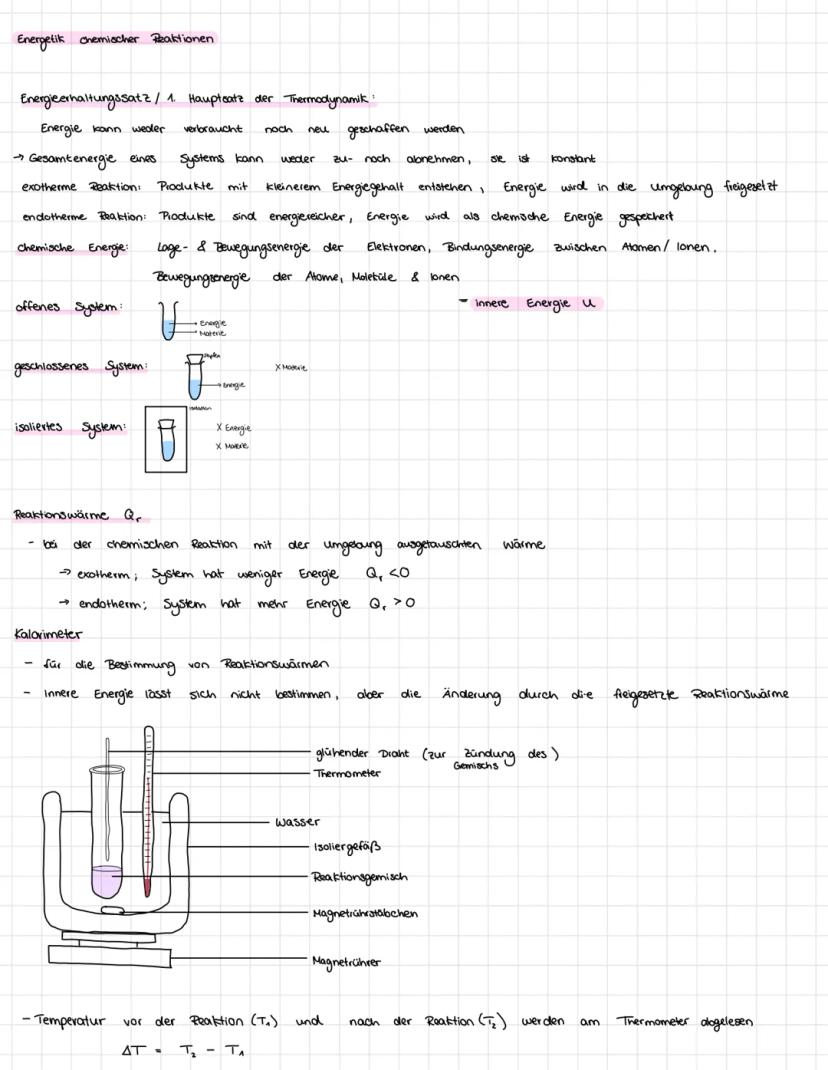




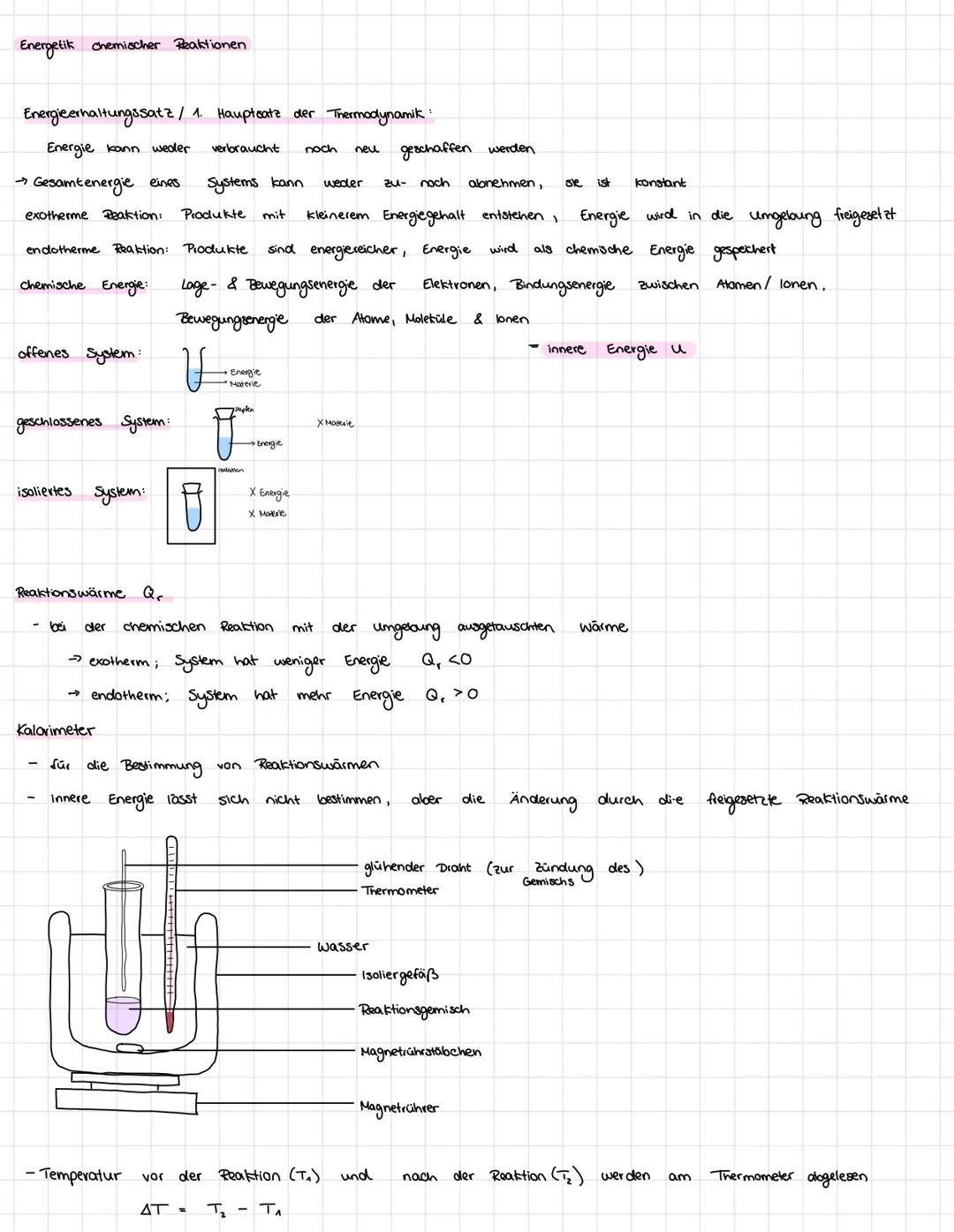
Energie kann weder vernichtet noch aus dem Nichts entstehen - das ist der 1. Hauptsatz der Thermodynamik. Bei chemischen Reaktionen ändert sich nur die Art, wie Energie gespeichert ist.
Exotherme Reaktionen setzen Energie frei, weil die Produkte weniger Energie enthalten als die Ausgangsstoffe. Endotherme Reaktionen brauchen dagegen Energiezufuhr, da die Produkte energiereicher sind.
Die chemische Energie steckt in den Bindungen zwischen Atomen und der Bewegung aller Teilchen. Mit einem Kalorimeter könnt ihr messen, wie viel Wärme bei Reaktionen frei wird oder benötigt wird - das nennt man Reaktionswärme Qᵣ.
Merktipp: Exotherm = Energie raus (negatives Qᵣ), Endotherm = Energie rein (positives Qᵣ)
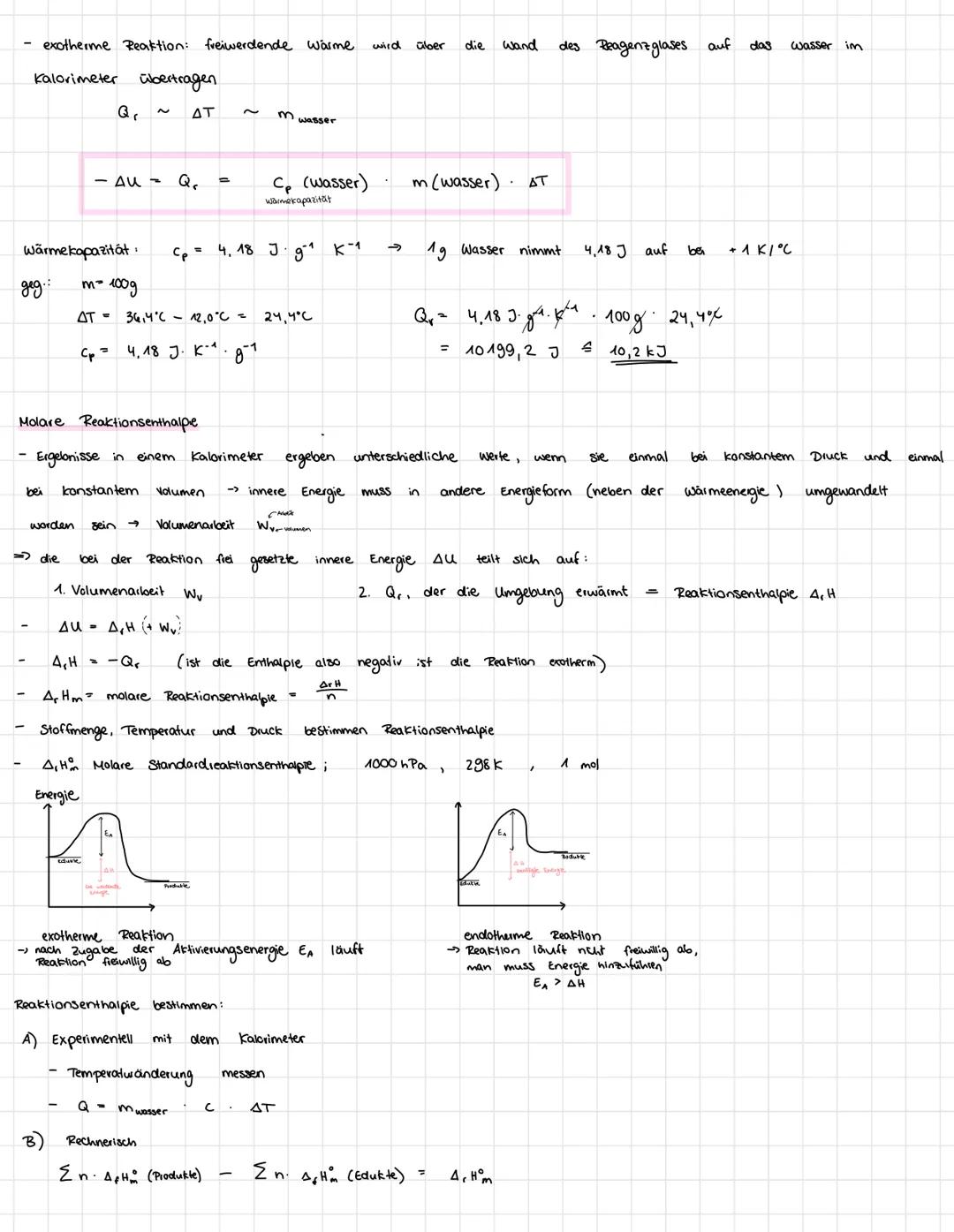
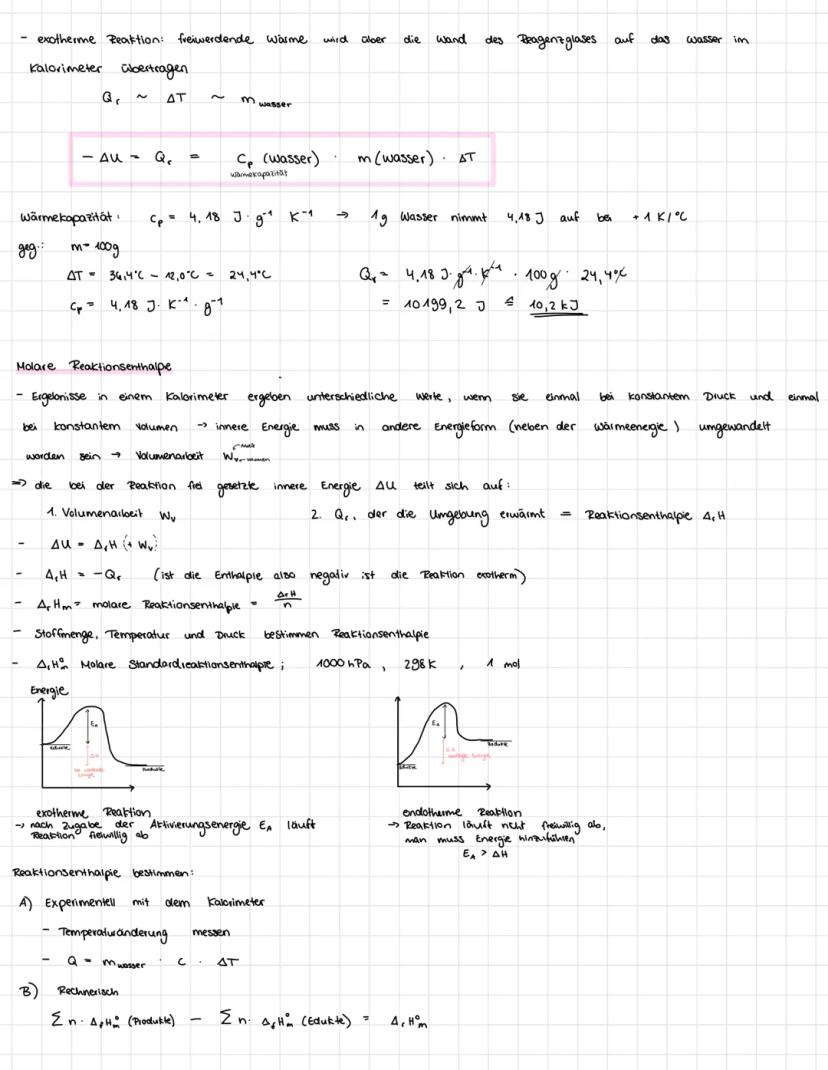
Manchmal könnt ihr Reaktionsenthalpien nicht direkt messen - aber berechnen geht immer! Der Satz von Hess besagt: Es ist egal, welchen Reaktionsweg ihr nehmt, die Gesamtenergie-änderung bleibt gleich.
Die Formel dafür lautet: ΔᵣH°ₘ = Σ Δf H°ₘ (Produkte) - Σ Δf H°ₘ (Edukte). Die Bildungsenthalpie Δf H°ₘ zeigt, wie viel Energie nötig ist, um 1 Mol eines Stoffes aus seinen Elementen zu bilden.
Beim Lösen von Salzen wirken zwei Kräfte gegeneinander: Die Gitterenergie (endotherm, braucht Energie) und die Hydratationsenthalpie (exotherm, setzt Energie frei). Je nachdem was überwiegt, wird die Lösung warm oder kalt.
Praxistipp: Handwärmer werden warm (exotherm), Kältekompressen werden kalt (endotherm) - beides durch Löse-vorgänge!

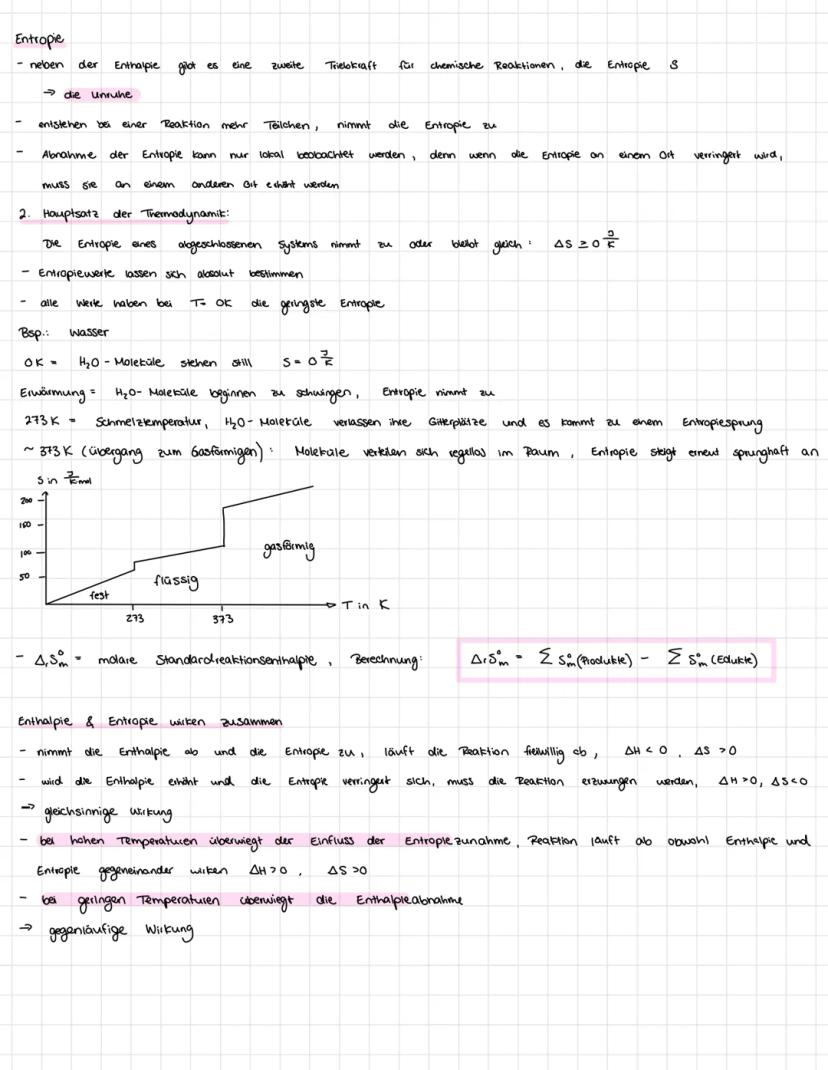
Neben der Energie gibt es noch einen zweiten "Motor" für Reaktionen: die Entropie S - ein Maß für Unordnung. Der 2. Hauptsatz der Thermodynamik besagt: Die Entropie nimmt in abgeschlossenen Systemen immer zu.
Bei 0 K stehen alle Teilchen still . Mit steigender Temperatur bewegen sie sich mehr, die Entropie steigt. Beim Schmelzen und Verdampfen gibt es regelrechte Entropiesprünge, weil die Teilchen plötzlich viel mehr Bewegungsfreiheit haben.
Enthalpie und Entropie können zusammen oder gegeneinander wirken. Bei hohen Temperaturen gewinnt meist die Entropie, bei niedrigen die Enthalpie. Die molare Standardreaktionsenthalpie berechnet ihr wie bei der Enthalpie: Produkte minus Edukte.
Eselsbrücke: Gas hat mehr Entropie als Flüssigkeit, Flüssigkeit mehr als Festkörper - mehr Chaos = höhere Entropie!
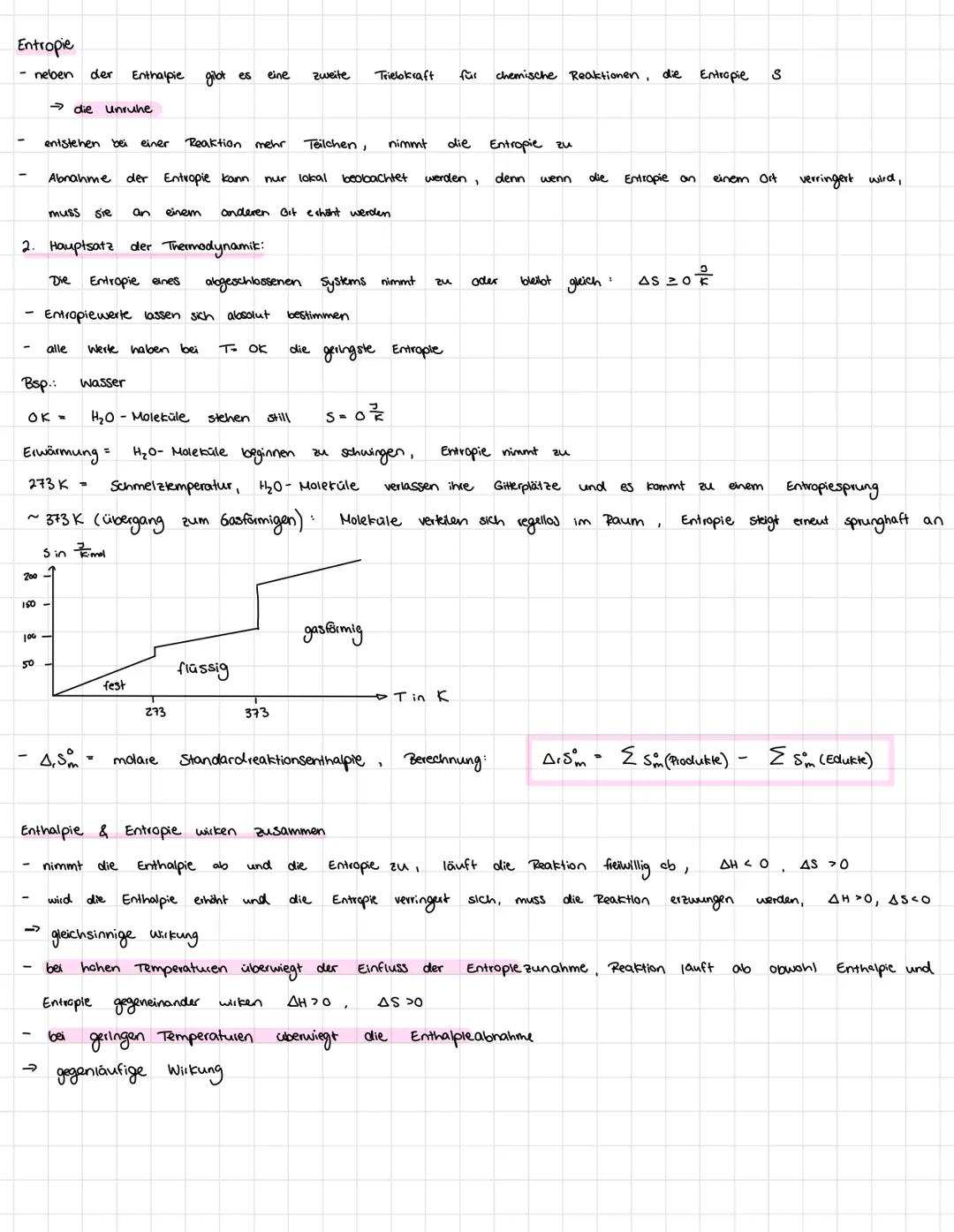
Die Gibbs-Helmholtz-Gleichung kombiniert Enthalpie und Entropie: ΔG = ΔH - T·ΔS. Sie sagt vorher, ob Reaktionen freiwillig ablaufen.
ΔG < 0 bedeutet exergonisch - die Reaktion läuft von selbst ab. ΔG > 0 bedeutet endergonisch - ihr müsst Energie zuführen, damit was passiert.
Auch wenn ΔG negativ ist, können manche Reaktionen trotzdem nicht ablaufen. Das liegt an metastabilen Systemen - die Aktivierungsenergie ist so hoch, dass praktisch nichts passiert. Die Reaktion wäre theoretisch möglich, aber viel zu langsam.
Realitätscheck: Diamant ist metastabil - er sollte zu Graphit werden, aber die Aktivierungsenergie ist viel zu hoch!

Benzin muss veredelt werden, bevor es in modernen Motoren funktioniert. Der Ottomotor arbeitet in vier Takten: Ansaugen von Benzin-Luft-Gemisch, Komprimieren, Zünden durch Zündkerze, Ausstoßen der Verbrennungsgase.
Das Problem: Klopfende Verbrennung entsteht, wenn sich das Gemisch unkontrolliert selbst entzündet, bevor die Flammenfront ankommt. Diese Sekundärzündungen erzeugen Druckstöße, die den Motor beschädigen können.
Die Oktanzahl misst die Klopffestigkeit. 2,2,4-Trimethylpentan hat Oktanzahl 100 (sehr klopffest), n-Heptan hat 0 (sehr klopffreudig). Je mehr Verzweigungen ein Alkan hat, desto klopffester ist es.
Tankstellen-Wissen: Super Plus (98 Oktan) ist klopffester als Super (95 Oktan) - aber nur Sportwagen brauchen das wirklich!

Der Dieselmotor funktioniert anders: Er saugt nur Luft an und komprimiert sie auf 900°C. Dann wird Diesel eingespritzt, der sich durch die Hitze selbst entzündet - keine Zündkerze nötig!
Dieselmotoren verbrauchen weniger Kraftstoff und sind umweltfreundlicher. Diesel enthält größere, unverzweigte Moleküle wie Hexadecan (C₁₆H₃₄).
Für CO₂-Berechnungen braucht ihr die Verbrennungsgleichung. Beispiel mit Heptan: C₇H₁₆ + 11 O₂ → 8 H₂O + 7 CO₂. Aus 1 Heptan-Molekül entstehen 7 CO₂-Moleküle. Mit Massenverhältnissen und Dichte könnt ihr dann berechnen: 8 Liter Heptan erzeugen etwa 16,8 kg CO₂.
Umwelt-Fakt: Ein Pkw stößt pro 100 km etwa das Doppelte seines Benzinverbrauchs an CO₂ aus - aus 8L Benzin werden ~16kg CO₂!

Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
kk
@zoldyckxc
Bei chemischen Reaktionen spielt Energie eine zentrale Rolle - mal wird sie freigesetzt, mal wird sie benötigt. Diese Energetik bestimmt nicht nur, ob Reaktionen von selbst ablaufen, sondern auch wie sie in praktischen Anwendungen wie Automotoren funktionieren.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Energie kann weder vernichtet noch aus dem Nichts entstehen - das ist der 1. Hauptsatz der Thermodynamik. Bei chemischen Reaktionen ändert sich nur die Art, wie Energie gespeichert ist.
Exotherme Reaktionen setzen Energie frei, weil die Produkte weniger Energie enthalten als die Ausgangsstoffe. Endotherme Reaktionen brauchen dagegen Energiezufuhr, da die Produkte energiereicher sind.
Die chemische Energie steckt in den Bindungen zwischen Atomen und der Bewegung aller Teilchen. Mit einem Kalorimeter könnt ihr messen, wie viel Wärme bei Reaktionen frei wird oder benötigt wird - das nennt man Reaktionswärme Qᵣ.
Merktipp: Exotherm = Energie raus (negatives Qᵣ), Endotherm = Energie rein (positives Qᵣ)

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Manchmal könnt ihr Reaktionsenthalpien nicht direkt messen - aber berechnen geht immer! Der Satz von Hess besagt: Es ist egal, welchen Reaktionsweg ihr nehmt, die Gesamtenergie-änderung bleibt gleich.
Die Formel dafür lautet: ΔᵣH°ₘ = Σ Δf H°ₘ (Produkte) - Σ Δf H°ₘ (Edukte). Die Bildungsenthalpie Δf H°ₘ zeigt, wie viel Energie nötig ist, um 1 Mol eines Stoffes aus seinen Elementen zu bilden.
Beim Lösen von Salzen wirken zwei Kräfte gegeneinander: Die Gitterenergie (endotherm, braucht Energie) und die Hydratationsenthalpie (exotherm, setzt Energie frei). Je nachdem was überwiegt, wird die Lösung warm oder kalt.
Praxistipp: Handwärmer werden warm (exotherm), Kältekompressen werden kalt (endotherm) - beides durch Löse-vorgänge!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Neben der Energie gibt es noch einen zweiten "Motor" für Reaktionen: die Entropie S - ein Maß für Unordnung. Der 2. Hauptsatz der Thermodynamik besagt: Die Entropie nimmt in abgeschlossenen Systemen immer zu.
Bei 0 K stehen alle Teilchen still . Mit steigender Temperatur bewegen sie sich mehr, die Entropie steigt. Beim Schmelzen und Verdampfen gibt es regelrechte Entropiesprünge, weil die Teilchen plötzlich viel mehr Bewegungsfreiheit haben.
Enthalpie und Entropie können zusammen oder gegeneinander wirken. Bei hohen Temperaturen gewinnt meist die Entropie, bei niedrigen die Enthalpie. Die molare Standardreaktionsenthalpie berechnet ihr wie bei der Enthalpie: Produkte minus Edukte.
Eselsbrücke: Gas hat mehr Entropie als Flüssigkeit, Flüssigkeit mehr als Festkörper - mehr Chaos = höhere Entropie!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Gibbs-Helmholtz-Gleichung kombiniert Enthalpie und Entropie: ΔG = ΔH - T·ΔS. Sie sagt vorher, ob Reaktionen freiwillig ablaufen.
ΔG < 0 bedeutet exergonisch - die Reaktion läuft von selbst ab. ΔG > 0 bedeutet endergonisch - ihr müsst Energie zuführen, damit was passiert.
Auch wenn ΔG negativ ist, können manche Reaktionen trotzdem nicht ablaufen. Das liegt an metastabilen Systemen - die Aktivierungsenergie ist so hoch, dass praktisch nichts passiert. Die Reaktion wäre theoretisch möglich, aber viel zu langsam.
Realitätscheck: Diamant ist metastabil - er sollte zu Graphit werden, aber die Aktivierungsenergie ist viel zu hoch!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Benzin muss veredelt werden, bevor es in modernen Motoren funktioniert. Der Ottomotor arbeitet in vier Takten: Ansaugen von Benzin-Luft-Gemisch, Komprimieren, Zünden durch Zündkerze, Ausstoßen der Verbrennungsgase.
Das Problem: Klopfende Verbrennung entsteht, wenn sich das Gemisch unkontrolliert selbst entzündet, bevor die Flammenfront ankommt. Diese Sekundärzündungen erzeugen Druckstöße, die den Motor beschädigen können.
Die Oktanzahl misst die Klopffestigkeit. 2,2,4-Trimethylpentan hat Oktanzahl 100 (sehr klopffest), n-Heptan hat 0 (sehr klopffreudig). Je mehr Verzweigungen ein Alkan hat, desto klopffester ist es.
Tankstellen-Wissen: Super Plus (98 Oktan) ist klopffester als Super (95 Oktan) - aber nur Sportwagen brauchen das wirklich!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Der Dieselmotor funktioniert anders: Er saugt nur Luft an und komprimiert sie auf 900°C. Dann wird Diesel eingespritzt, der sich durch die Hitze selbst entzündet - keine Zündkerze nötig!
Dieselmotoren verbrauchen weniger Kraftstoff und sind umweltfreundlicher. Diesel enthält größere, unverzweigte Moleküle wie Hexadecan (C₁₆H₃₄).
Für CO₂-Berechnungen braucht ihr die Verbrennungsgleichung. Beispiel mit Heptan: C₇H₁₆ + 11 O₂ → 8 H₂O + 7 CO₂. Aus 1 Heptan-Molekül entstehen 7 CO₂-Moleküle. Mit Massenverhältnissen und Dichte könnt ihr dann berechnen: 8 Liter Heptan erzeugen etwa 16,8 kg CO₂.
Umwelt-Fakt: Ein Pkw stößt pro 100 km etwa das Doppelte seines Benzinverbrauchs an CO₂ aus - aus 8L Benzin werden ~16kg CO₂!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
4
Smart Tools NEU
Verwandle diesen Lernzettel in: ✓ 50+ Übungsfragen ✓ Interaktive Karteikarten ✓ Komplette Probeklausur ✓ Aufsatzgliederungen
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer