Das Chemie-Abitur 2023 umfasst alle wichtigen Bereiche der organischen und... Mehr anzeigen
Effektive Lernzettel für dein Chemie Abitur im Leistungskurs








Abitur-Themen und chemische Gleichgewichte
Euer Chemie-Abitur deckt sechs Hauptbereiche ab: Kohlenwasserstoffe, Alkanole, Alkansäuren, Kohlenhydrate, Kunststoffe und chemische Gleichgewichte. Der Schwerpunkt liegt dabei auf praktischen Berechnungen und dem Verständnis von Reaktionsmechanismen.
Chemische Gleichgewichte sind dynamische Prozesse - Hin- und Rückreaktion laufen gleichzeitig ab. Typische Beispiele sind das Ester-Gleichgewicht oder die Ammoniak-Synthese nach Haber-Bosch. Das Massenwirkungsgesetz hilft euch bei der Berechnung von Gleichgewichtskonstanten.
Das Prinzip des kleinsten Zwangs erklärt, wie sich Gleichgewichte bei Änderung von Druck, Temperatur oder Konzentration verschieben. Katalysatoren beschleunigen nur die Einstellung des Gleichgewichts, ändern aber nicht dessen Lage.
Merkhilfe: Gleichgewichte sind wie eine Waage - sie reagieren auf jede Störung und suchen einen neuen Ausgleich!
Bei Protolyse-Gleichgewichten arbeitet ihr mit korrespondierenden Säure-Base-Paaren. Der pKs-Wert zeigt die Säurestärke an, während das Ionenprodukt des Wassers für pH-Berechnungen entscheidend ist.

Alkane und Isomerie
Alkane folgen der Summenformel CnH2n+2 und bilden eine homologe Reihe von Methan bis Decan. Diese gesättigten Kohlenwasserstoffe enthalten nur Einfachbindungen und sind relativ unreaktiv.
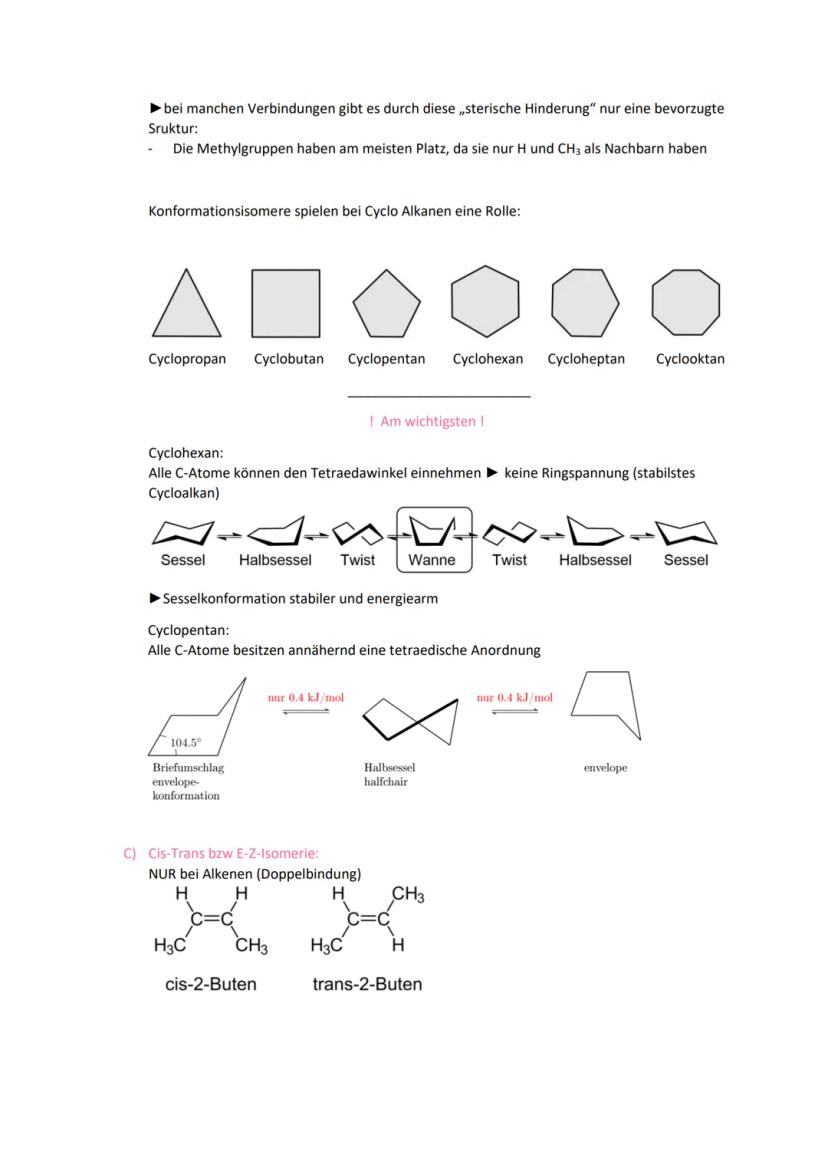
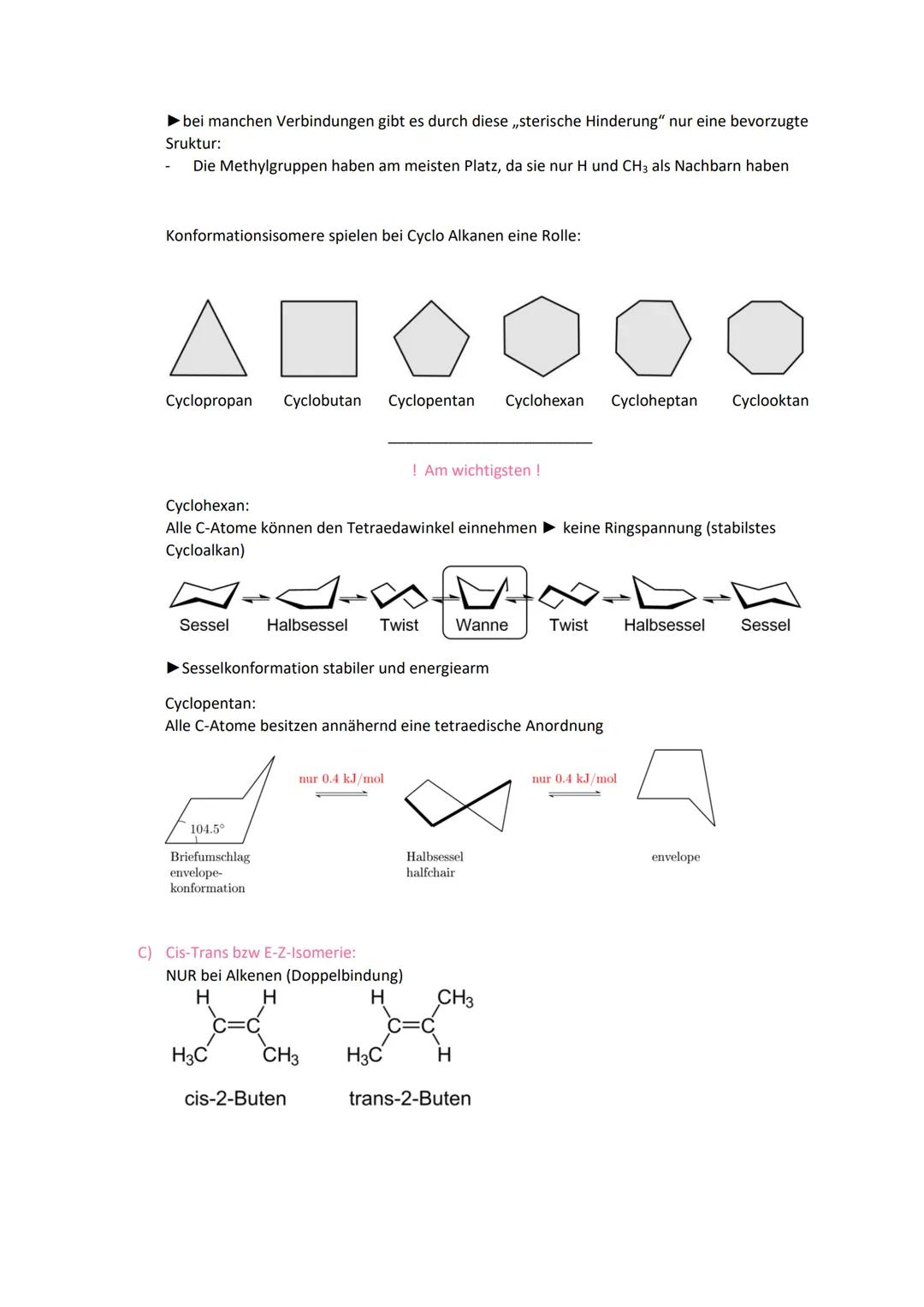
Isomere haben dieselbe Summenformel, aber unterschiedliche Strukturen. Bei der Konstitutionsisomerie unterscheidet sich die Verknüpfung der Atome - wie bei Butan und 2-Methylpropan. Die Konformationsisomerie entsteht durch Drehung um Einfachbindungen.
Ab fünf Kohlenstoffatomen wird Isomerie besonders wichtig, da die Anzahl möglicher Strukturen stark ansteigt. Die Newman-Projektion hilft euch, verschiedene Konformationen zu visualisieren - "eclipsed" (verdeckt) versus "staggered" (gestaffelt).
Tipp: Zeichnet Isomere systematisch auf - das verhindert, dass ihr welche überseht oder doppelt zählt!
Sterische Hinderung tritt auf, wenn Atomgruppen räumlich zu nah beieinander stehen. Das beeinflusst die Stabilität verschiedener Konformationen erheblich.
Nomenklatur und Eigenschaften
Die Nomenklatur organischer Verbindungen folgt klaren Regeln: Hauptkette bestimmen, nummerieren und Substituenten benennen. Die funktionelle Gruppe mit der höchsten Priorität bestimmt die Verbindungsklasse und bekommt die niedrigste Nummer.
Substituenten werden alphabetisch geordnet und mit griechischen Zahlwörtern bei mehrfachem Auftreten gekennzeichnet. Bindestriche trennen Zahlen von Buchstaben - nur der erste Buchstabe wird großgeschrieben.
Die Siede- und Schmelzpunkte der Alkane steigen mit der Kettenlänge. Längere Ketten haben mehr Elektronen, was stärkere Van-der-Waals-Kräfte ermöglicht. Deshalb braucht man mehr Energie für Phasenübergänge.
Eselsbrücke: Je länger die Kette, desto mehr "Klebkraft" zwischen den Molekülen!
Cycloalkane haben höhere Siedepunkte als ihre linearen Verwandten gleicher Kohlenstoffanzahl, da ihre kompakte Form stärkere intermolekulare Wechselwirkungen ermöglicht.

Verbrennungsanalyse und Elementarbestimmung
Die Verbrennungsanalyse ist ein klassisches Verfahren zur Elementarbestimmung organischer Verbindungen. Dabei wird die Probe vollständig verbrannt und die Verbrennungsprodukte CO₂ und H₂O quantitativ aufgefangen.
Das entstehende Wasser kondensiert in der Kühlfalle und wird gewogen. Kohlenstoffdioxid wird im Kaliapparat absorbiert und ebenfalls durch Wägung bestimmt. Kalkwasser dient als qualitativer Nachweis für CO₂.
Bei der Berechnung nutzt ihr die Stoffmengenkonzentration und Molmassen. Aus 44 g CO₂ stammen 12 g Kohlenstoff, aus 18 g H₂O stammen 2 g Wasserstoff. Der Sauerstoffanteil ergibt sich aus der Differenz zur Gesamtmasse.
Rechencheck: Die Summe aller Elementanteile muss immer die ursprüngliche Probenmasse ergeben!
Diese Methode funktioniert nur bei vollständiger Verbrennung und setzt voraus, dass außer C, H und O keine weiteren Elemente vorhanden sind.

Radikalische Substitution
Die radikalische Substitution läuft in drei Phasen ab: Startreaktion, Kettenreaktion und Abbruchreaktion. Radikale sind Teilchen mit ungepaarten Elektronen und damit sehr reaktionsfreudig.
Die Startreaktion erfolgt durch homolytische Spaltung eines Halogenmoleküls mit Lichtenergie. Dabei entstehen zwei Halogenradikale mit je einem ungepaarten Elektron. Diese sind der "Zündfunke" für die folgende Kettenreaktion.
In der Kettenreaktion reagiert das Halogenradikal mit dem Kohlenwasserstoff und bildet ein Alkylradikal plus Halogenwasserstoff. Das Alkylradikal reagiert dann mit einem weiteren Halogenmolekül zum substituierten Produkt und einem neuen Halogenradikal.
Wichtig: Die Kettenreaktion kann sich theoretisch unendlich wiederholen - deshalb reichen winzige Radikalmengen für große Umsätze!
Die Abbruchreaktion beendet die Kette, wenn zwei Radikale miteinander reagieren. Dabei können Halogen-Halogen-, Alkyl-Halogen- oder Alkyl-Alkyl-Bindungen entstehen.

Orbitalmodell und Elektronenverteilung
Das Orbitalmodell erweitert das Bohr'sche Atommodell und teilt Schalen in Orbitale auf. Ein Orbital ist der Raum, in dem ihr mit 90%iger Wahrscheinlichkeit ein Elektron findet. Die Energieniveaus steigen in der Reihenfolge s < p < d < f.
Jede Schale enthält maximal vier verschiedene Orbitaltypen: s-Orbitale (kugelförmig, 1×), p-Orbitale (hantelförmig, 3×), d-Orbitale (5×) und f-Orbitale (7×). Jedes Orbital kann maximal zwei Elektronen mit entgegengesetztem Spin aufnehmen.
Die Hund'sche Regel besagt, dass halbbesetzte und vollbesetzte Orbitale besonders stabil sind. Deshalb weicht Chrom vom erwarteten Elektronenaufbau ab: [Ar] 4s¹ 3d⁵ statt [Ar] 4s² 3d⁴.
Merkregel: Elektronen sind "Einzelgänger" - sie besetzen erst alle Orbitale einfach, bevor sie sich zu zweit niederlassen!
Die Elektronenverteilung bestimmt die chemischen Eigenschaften der Elemente und erklärt Besonderheiten im Periodensystem.

Hybridisierung bei Kohlenwasserstoffen
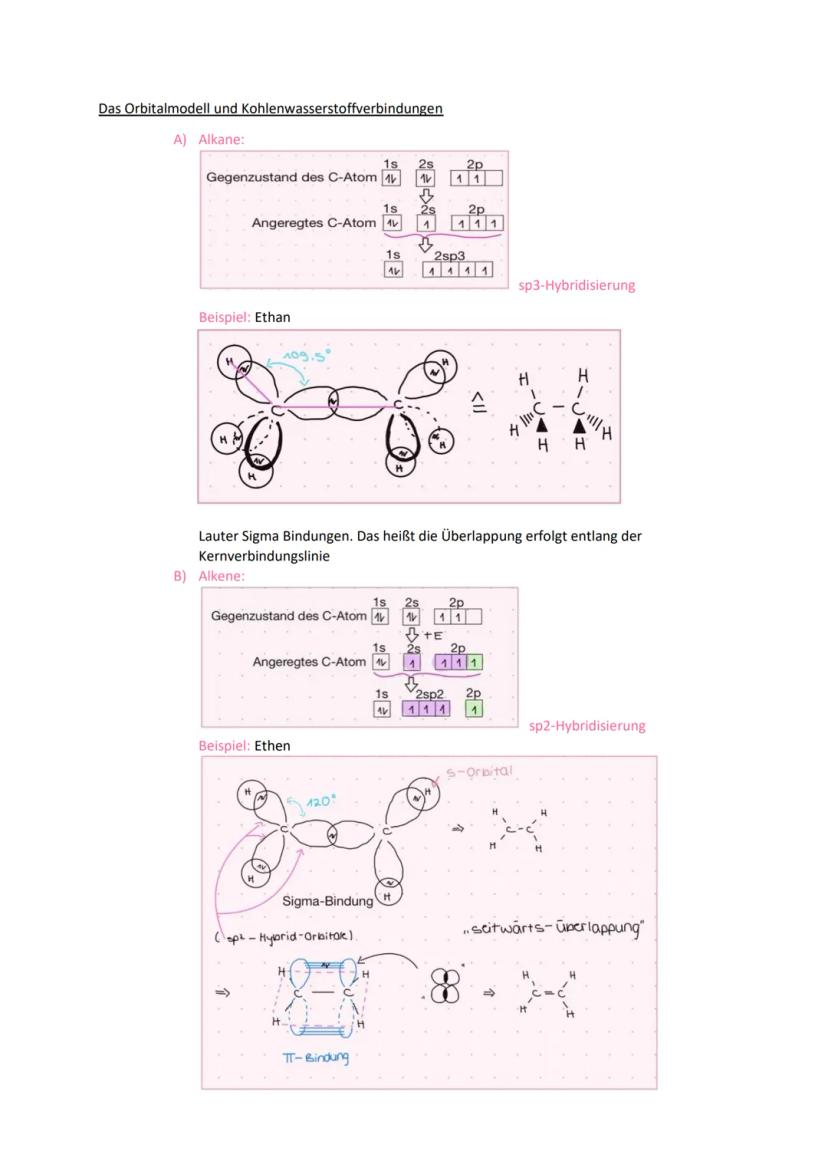
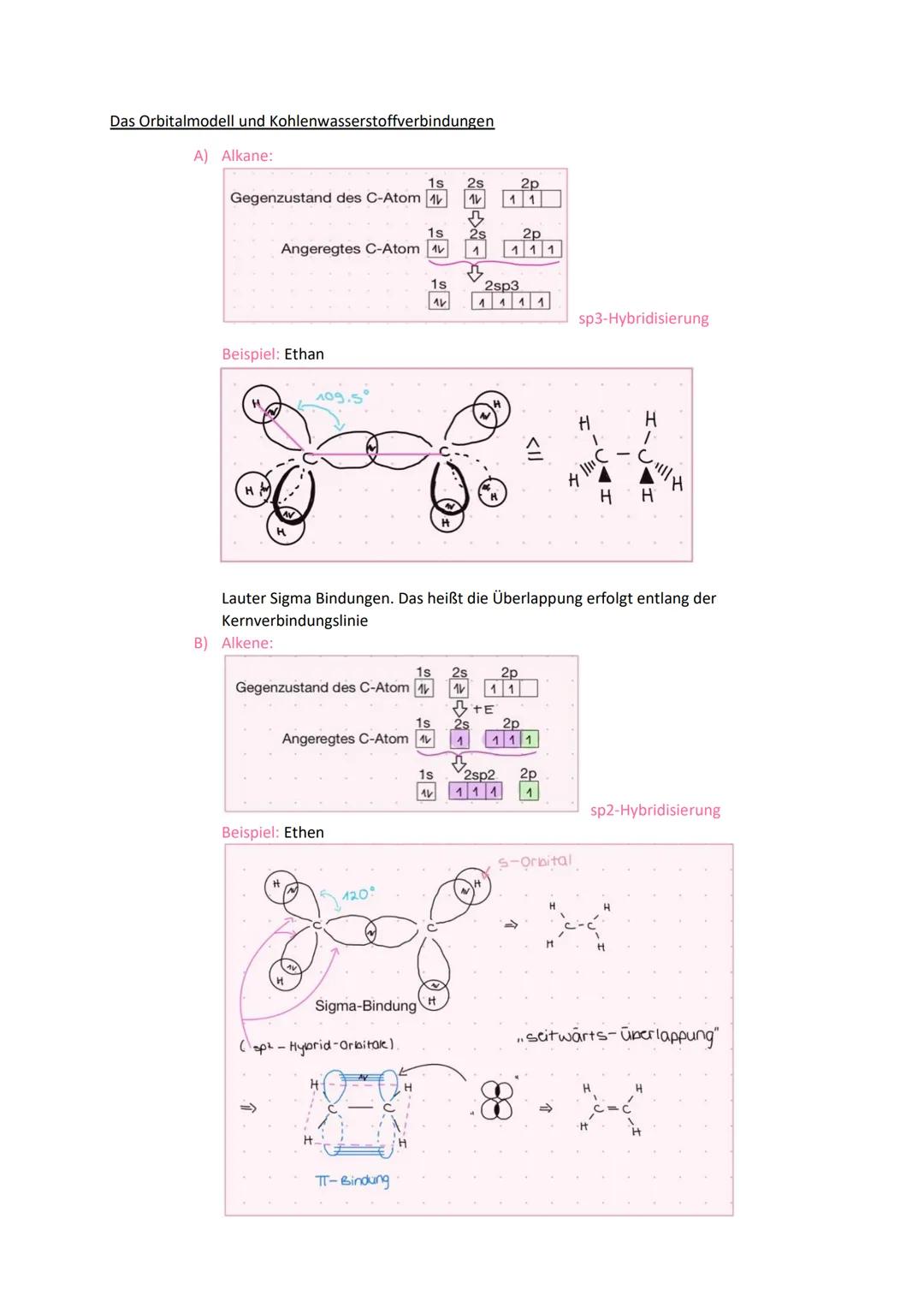
Hybridisierung erklärt, wie Kohlenstoff verschiedene Bindungsgeometrien eingehen kann. Bei sp³-Hybridisierung (Alkane) mischen sich ein s- und drei p-Orbitale zu vier gleichwertigen Hybridorbitalen mit tetraedrischem Winkel von 109,5°.
Bei sp²-Hybridisierung (Alkene) entstehen drei Hybridorbitale in einer Ebene mit 120° Winkeln. Das übrige p-Orbital steht senkrecht dazu und bildet π-Bindungen. Sigma-Bindungen entstehen durch Überlappung entlang der Kernverbindungslinie.
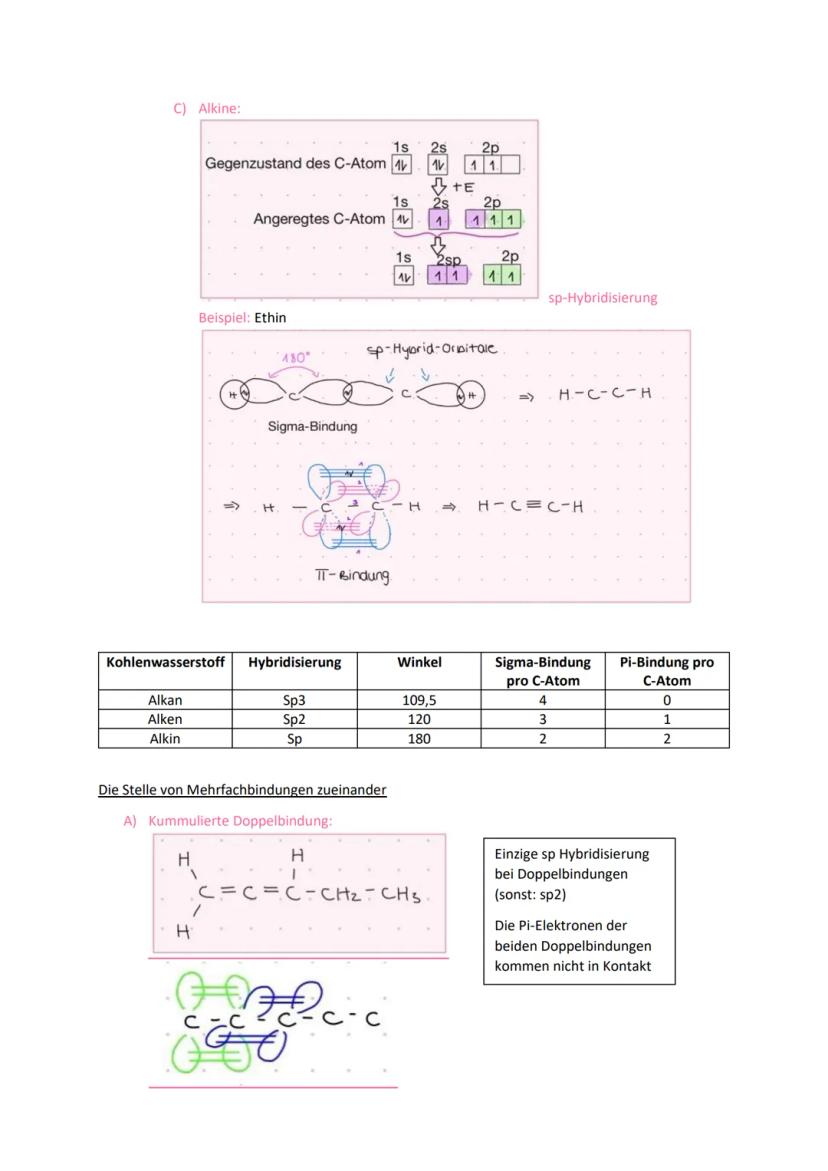
sp-Hybridisierung (Alkine) erzeugt zwei lineare Hybridorbitale mit 180° Winkel. Die beiden verbleibenden p-Orbitale bilden zwei π-Bindungen senkrecht zueinander. Dreifachbindungen bestehen aus einer Sigma- und zwei π-Bindungen.
Geometrie-Tipp: sp³ = Tetraeder, sp² = Dreieck, sp = Linie - die Hybridisierung bestimmt die Molekülform!
Die Hybridisierung erklärt auch, warum Alkane frei drehbare Einfachbindungen haben, während Doppel- und Dreifachbindungen die Rotation blockieren.
Doppelbindungen und ihre Anordnung
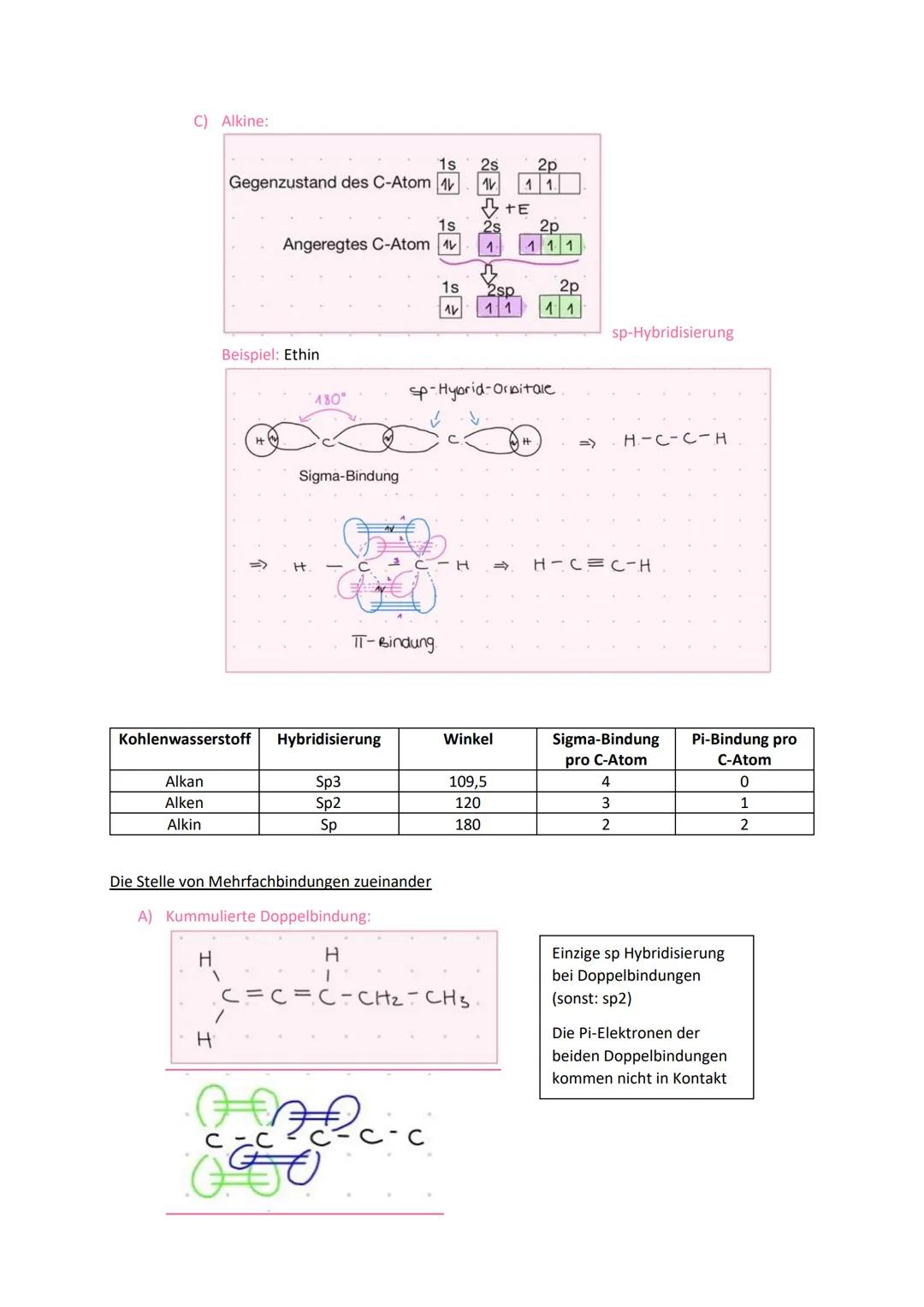
Die räumliche Anordnung von Doppelbindungen beeinflusst die Moleküleigenschaften erheblich. Bei kumulierten Doppelbindungen stehen zwei C=C-Bindungen direkt nebeneinander - die π-Elektronen können nicht miteinander wechselwirken.
Konjugierte Doppelbindungen sind durch eine Einfachbindung getrennt. Hier können die p-Orbitale überlappen und die π-Elektronen über einen größeren Raum "wandern". Das führt zu erhöhter Stabilität und ermöglicht Mesomerie (Ladungsverschiebung).
Bei isolierten Doppelbindungen verhindert der große Abstand (mindestens zwei Einfachbindungen) jede Wechselwirkung der π-Systeme. Jede Doppelbindung verhält sich unabhängig von den anderen.
Stabilität-Regel: Konjugierte Systeme sind stabiler als isolierte - die Elektronen können sich besser "verteilen"!
Induktive Effekte beschreiben die Elektronenverschiebung entlang von Bindungen. Alkylgruppen wirken elektronenschiebend , elektronegative Atome elektronenziehend . Diese Effekte nehmen mit der Entfernung exponentiell ab.

Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Säure-Base-Chemie
9Säure-Base-Theorie & Puffer
Entdecken Sie die Grundlagen der Säure-Base-Theorie, Pufferlösungen und Indikatoren. Diese Zusammenfassung behandelt wichtige Konzepte wie pH-Wert-Berechnungen, Titrationskurven und die Henderson-Hasselbalch-Gleichung. Ideal für Chemie-LK-Studierende, die sich auf Prüfungen vorbereiten.
Säure-Base-Gleichgewicht und Titration
Entdecken Sie die Grundlagen des chemischen Gleichgewichts und der Säure-Base-Reaktionen. Diese Zusammenfassung behandelt Le Chateliers Prinzip, Titrationskurven, pH-Wert-Berechnungen, Pufferlösungen und die Autoprotolyse von Wasser. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten. Enthält wichtige Formeln und Beispiele zur Veranschaulichung der Konzepte.
Chemie LK Abitur Zusammenfassung
Diese umfassende Zusammenfassung für den Chemie Leistungskurs (LK) in Baden-Württemberg deckt alle relevanten Themen ab, die für das Abitur 2022 wichtig sind. Sie enthält wichtige Konzepte wie Aromaten, chemische Gleichgewichte, Säuren und Basen, Elektrochemie, organische Chemie und mehr. Ideal zur Vorbereitung auf Prüfungen und zur Vertiefung des Verständnisses. Bei Interesse an der PDF-Version, kontaktieren Sie bitte [email protected].
Chemie Lernzettel Q1 - Aminosäuren/Enzyme/Proteine….
Lernzettel umfassend für die erste Klausur in der Oberstufe in Chemie- alles um Aminosäuren, Proteinen( mit Beispielen) als auch Enzymen (einfach erklärt und schlüssig )
Säure-Base-Gleichgewichte, Naturstoffe
1. Säure-Base-Gleichgewichte Säure-Base-Theorie nach Brønsted, Autoprotolyse und pH-Wert, Säure- & Basenstärke, pH-Werte berechnen, Säure-Base-Titration 2. Naturstoffe Chiralität, Optische Aktivität, Fischerprojektion, Kohlenhydrate, Ringform
Säure-Base-Reaktionen
Vertiefte Kenntnisse über Säure-Base-Chemie: Erfahren Sie alles über die Dissoziation von Säuren und Basen, pH-Wert-Berechnungen, Titrationskurven und Puffersysteme. Diese Zusammenfassung bietet eine klare Übersicht über die wichtigsten Konzepte, einschließlich der Henderson-Hasselbalch-Gleichung und der Neutralisationsreaktionen. Ideal für Chemie-Studierende und zur Vorbereitung auf Prüfungen.
Chemie Abitur 2024: Grundlagen
Umfassender Lernzettel für das Chemie-Abitur 2024 in Hessen. Behandelt zentrale Themen wie Enthalpie, Säure-Base-Gleichgewichte, chemische Reaktionen, Isomerie, und die Struktur von Proteinen und Kohlenhydraten. Ideal für die Prüfungsvorbereitung und das Verständnis chemischer Konzepte. Enthält wichtige Formeln, Reaktionsmechanismen und Nachweisreaktionen.
Säure-Base-Reaktionen verstehen
Entdecken Sie die Grundlagen der Säure-Base-Chemie, einschließlich pH-Wert-Berechnung, Pufferlösungen, und Titrationsmethoden. Diese Zusammenfassung bietet eine klare Übersicht über wichtige Konzepte wie das Ionenprodukt des Wassers, Brønsted-Theorie und die Rolle von Indikatoren in chemischen Reaktionen. Ideal für die Vorbereitung auf das Abitur 2024.
Säure-Base Grundlagen
Umfassende Zusammenfassung der Säure-Base-Theorie für das Abitur 2023. Behandelt pH-Wert-Berechnungen, Neutralisationsreaktionen, Indikatoren, Pufferlösungen, Titrationskurven und die Autoprotolyse von Wasser. Ideal für Chemie LK Schüler zur Prüfungsvorbereitung.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Effektive Lernzettel für dein Chemie Abitur im Leistungskurs
Das Chemie-Abitur 2023 umfasst alle wichtigen Bereiche der organischen und anorganischen Chemie. Von den Grundlagen der Kohlenwasserstoffe bis hin zu komplexen Gleichgewichten - hier findest du alle relevanten Themen kompakt zusammengefasst.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Abitur-Themen und chemische Gleichgewichte
Euer Chemie-Abitur deckt sechs Hauptbereiche ab: Kohlenwasserstoffe, Alkanole, Alkansäuren, Kohlenhydrate, Kunststoffe und chemische Gleichgewichte. Der Schwerpunkt liegt dabei auf praktischen Berechnungen und dem Verständnis von Reaktionsmechanismen.
Chemische Gleichgewichte sind dynamische Prozesse - Hin- und Rückreaktion laufen gleichzeitig ab. Typische Beispiele sind das Ester-Gleichgewicht oder die Ammoniak-Synthese nach Haber-Bosch. Das Massenwirkungsgesetz hilft euch bei der Berechnung von Gleichgewichtskonstanten.
Das Prinzip des kleinsten Zwangs erklärt, wie sich Gleichgewichte bei Änderung von Druck, Temperatur oder Konzentration verschieben. Katalysatoren beschleunigen nur die Einstellung des Gleichgewichts, ändern aber nicht dessen Lage.
Merkhilfe: Gleichgewichte sind wie eine Waage - sie reagieren auf jede Störung und suchen einen neuen Ausgleich!
Bei Protolyse-Gleichgewichten arbeitet ihr mit korrespondierenden Säure-Base-Paaren. Der pKs-Wert zeigt die Säurestärke an, während das Ionenprodukt des Wassers für pH-Berechnungen entscheidend ist.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Alkane und Isomerie
Alkane folgen der Summenformel CnH2n+2 und bilden eine homologe Reihe von Methan bis Decan. Diese gesättigten Kohlenwasserstoffe enthalten nur Einfachbindungen und sind relativ unreaktiv.
Isomere haben dieselbe Summenformel, aber unterschiedliche Strukturen. Bei der Konstitutionsisomerie unterscheidet sich die Verknüpfung der Atome - wie bei Butan und 2-Methylpropan. Die Konformationsisomerie entsteht durch Drehung um Einfachbindungen.
Ab fünf Kohlenstoffatomen wird Isomerie besonders wichtig, da die Anzahl möglicher Strukturen stark ansteigt. Die Newman-Projektion hilft euch, verschiedene Konformationen zu visualisieren - "eclipsed" (verdeckt) versus "staggered" (gestaffelt).
Tipp: Zeichnet Isomere systematisch auf - das verhindert, dass ihr welche überseht oder doppelt zählt!
Sterische Hinderung tritt auf, wenn Atomgruppen räumlich zu nah beieinander stehen. Das beeinflusst die Stabilität verschiedener Konformationen erheblich.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Nomenklatur und Eigenschaften
Die Nomenklatur organischer Verbindungen folgt klaren Regeln: Hauptkette bestimmen, nummerieren und Substituenten benennen. Die funktionelle Gruppe mit der höchsten Priorität bestimmt die Verbindungsklasse und bekommt die niedrigste Nummer.
Substituenten werden alphabetisch geordnet und mit griechischen Zahlwörtern bei mehrfachem Auftreten gekennzeichnet. Bindestriche trennen Zahlen von Buchstaben - nur der erste Buchstabe wird großgeschrieben.
Die Siede- und Schmelzpunkte der Alkane steigen mit der Kettenlänge. Längere Ketten haben mehr Elektronen, was stärkere Van-der-Waals-Kräfte ermöglicht. Deshalb braucht man mehr Energie für Phasenübergänge.
Eselsbrücke: Je länger die Kette, desto mehr "Klebkraft" zwischen den Molekülen!
Cycloalkane haben höhere Siedepunkte als ihre linearen Verwandten gleicher Kohlenstoffanzahl, da ihre kompakte Form stärkere intermolekulare Wechselwirkungen ermöglicht.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Verbrennungsanalyse und Elementarbestimmung
Die Verbrennungsanalyse ist ein klassisches Verfahren zur Elementarbestimmung organischer Verbindungen. Dabei wird die Probe vollständig verbrannt und die Verbrennungsprodukte CO₂ und H₂O quantitativ aufgefangen.
Das entstehende Wasser kondensiert in der Kühlfalle und wird gewogen. Kohlenstoffdioxid wird im Kaliapparat absorbiert und ebenfalls durch Wägung bestimmt. Kalkwasser dient als qualitativer Nachweis für CO₂.
Bei der Berechnung nutzt ihr die Stoffmengenkonzentration und Molmassen. Aus 44 g CO₂ stammen 12 g Kohlenstoff, aus 18 g H₂O stammen 2 g Wasserstoff. Der Sauerstoffanteil ergibt sich aus der Differenz zur Gesamtmasse.
Rechencheck: Die Summe aller Elementanteile muss immer die ursprüngliche Probenmasse ergeben!
Diese Methode funktioniert nur bei vollständiger Verbrennung und setzt voraus, dass außer C, H und O keine weiteren Elemente vorhanden sind.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Radikalische Substitution
Die radikalische Substitution läuft in drei Phasen ab: Startreaktion, Kettenreaktion und Abbruchreaktion. Radikale sind Teilchen mit ungepaarten Elektronen und damit sehr reaktionsfreudig.
Die Startreaktion erfolgt durch homolytische Spaltung eines Halogenmoleküls mit Lichtenergie. Dabei entstehen zwei Halogenradikale mit je einem ungepaarten Elektron. Diese sind der "Zündfunke" für die folgende Kettenreaktion.
In der Kettenreaktion reagiert das Halogenradikal mit dem Kohlenwasserstoff und bildet ein Alkylradikal plus Halogenwasserstoff. Das Alkylradikal reagiert dann mit einem weiteren Halogenmolekül zum substituierten Produkt und einem neuen Halogenradikal.
Wichtig: Die Kettenreaktion kann sich theoretisch unendlich wiederholen - deshalb reichen winzige Radikalmengen für große Umsätze!
Die Abbruchreaktion beendet die Kette, wenn zwei Radikale miteinander reagieren. Dabei können Halogen-Halogen-, Alkyl-Halogen- oder Alkyl-Alkyl-Bindungen entstehen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Orbitalmodell und Elektronenverteilung
Das Orbitalmodell erweitert das Bohr'sche Atommodell und teilt Schalen in Orbitale auf. Ein Orbital ist der Raum, in dem ihr mit 90%iger Wahrscheinlichkeit ein Elektron findet. Die Energieniveaus steigen in der Reihenfolge s < p < d < f.
Jede Schale enthält maximal vier verschiedene Orbitaltypen: s-Orbitale (kugelförmig, 1×), p-Orbitale (hantelförmig, 3×), d-Orbitale (5×) und f-Orbitale (7×). Jedes Orbital kann maximal zwei Elektronen mit entgegengesetztem Spin aufnehmen.
Die Hund'sche Regel besagt, dass halbbesetzte und vollbesetzte Orbitale besonders stabil sind. Deshalb weicht Chrom vom erwarteten Elektronenaufbau ab: [Ar] 4s¹ 3d⁵ statt [Ar] 4s² 3d⁴.
Merkregel: Elektronen sind "Einzelgänger" - sie besetzen erst alle Orbitale einfach, bevor sie sich zu zweit niederlassen!
Die Elektronenverteilung bestimmt die chemischen Eigenschaften der Elemente und erklärt Besonderheiten im Periodensystem.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Hybridisierung bei Kohlenwasserstoffen
Hybridisierung erklärt, wie Kohlenstoff verschiedene Bindungsgeometrien eingehen kann. Bei sp³-Hybridisierung (Alkane) mischen sich ein s- und drei p-Orbitale zu vier gleichwertigen Hybridorbitalen mit tetraedrischem Winkel von 109,5°.
Bei sp²-Hybridisierung (Alkene) entstehen drei Hybridorbitale in einer Ebene mit 120° Winkeln. Das übrige p-Orbital steht senkrecht dazu und bildet π-Bindungen. Sigma-Bindungen entstehen durch Überlappung entlang der Kernverbindungslinie.
sp-Hybridisierung (Alkine) erzeugt zwei lineare Hybridorbitale mit 180° Winkel. Die beiden verbleibenden p-Orbitale bilden zwei π-Bindungen senkrecht zueinander. Dreifachbindungen bestehen aus einer Sigma- und zwei π-Bindungen.
Geometrie-Tipp: sp³ = Tetraeder, sp² = Dreieck, sp = Linie - die Hybridisierung bestimmt die Molekülform!
Die Hybridisierung erklärt auch, warum Alkane frei drehbare Einfachbindungen haben, während Doppel- und Dreifachbindungen die Rotation blockieren.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Doppelbindungen und ihre Anordnung
Die räumliche Anordnung von Doppelbindungen beeinflusst die Moleküleigenschaften erheblich. Bei kumulierten Doppelbindungen stehen zwei C=C-Bindungen direkt nebeneinander - die π-Elektronen können nicht miteinander wechselwirken.
Konjugierte Doppelbindungen sind durch eine Einfachbindung getrennt. Hier können die p-Orbitale überlappen und die π-Elektronen über einen größeren Raum "wandern". Das führt zu erhöhter Stabilität und ermöglicht Mesomerie (Ladungsverschiebung).
Bei isolierten Doppelbindungen verhindert der große Abstand (mindestens zwei Einfachbindungen) jede Wechselwirkung der π-Systeme. Jede Doppelbindung verhält sich unabhängig von den anderen.
Stabilität-Regel: Konjugierte Systeme sind stabiler als isolierte - die Elektronen können sich besser "verteilen"!
Induktive Effekte beschreiben die Elektronenverschiebung entlang von Bindungen. Alkylgruppen wirken elektronenschiebend , elektronegative Atome elektronenziehend . Diese Effekte nehmen mit der Entfernung exponentiell ab.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Säure-Base-Chemie
9Säure-Base-Theorie & Puffer
Entdecken Sie die Grundlagen der Säure-Base-Theorie, Pufferlösungen und Indikatoren. Diese Zusammenfassung behandelt wichtige Konzepte wie pH-Wert-Berechnungen, Titrationskurven und die Henderson-Hasselbalch-Gleichung. Ideal für Chemie-LK-Studierende, die sich auf Prüfungen vorbereiten.
Säure-Base-Gleichgewicht und Titration
Entdecken Sie die Grundlagen des chemischen Gleichgewichts und der Säure-Base-Reaktionen. Diese Zusammenfassung behandelt Le Chateliers Prinzip, Titrationskurven, pH-Wert-Berechnungen, Pufferlösungen und die Autoprotolyse von Wasser. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten. Enthält wichtige Formeln und Beispiele zur Veranschaulichung der Konzepte.
Chemie LK Abitur Zusammenfassung
Diese umfassende Zusammenfassung für den Chemie Leistungskurs (LK) in Baden-Württemberg deckt alle relevanten Themen ab, die für das Abitur 2022 wichtig sind. Sie enthält wichtige Konzepte wie Aromaten, chemische Gleichgewichte, Säuren und Basen, Elektrochemie, organische Chemie und mehr. Ideal zur Vorbereitung auf Prüfungen und zur Vertiefung des Verständnisses. Bei Interesse an der PDF-Version, kontaktieren Sie bitte [email protected].
Chemie Lernzettel Q1 - Aminosäuren/Enzyme/Proteine….
Lernzettel umfassend für die erste Klausur in der Oberstufe in Chemie- alles um Aminosäuren, Proteinen( mit Beispielen) als auch Enzymen (einfach erklärt und schlüssig )
Säure-Base-Gleichgewichte, Naturstoffe
1. Säure-Base-Gleichgewichte Säure-Base-Theorie nach Brønsted, Autoprotolyse und pH-Wert, Säure- & Basenstärke, pH-Werte berechnen, Säure-Base-Titration 2. Naturstoffe Chiralität, Optische Aktivität, Fischerprojektion, Kohlenhydrate, Ringform
Säure-Base-Reaktionen
Vertiefte Kenntnisse über Säure-Base-Chemie: Erfahren Sie alles über die Dissoziation von Säuren und Basen, pH-Wert-Berechnungen, Titrationskurven und Puffersysteme. Diese Zusammenfassung bietet eine klare Übersicht über die wichtigsten Konzepte, einschließlich der Henderson-Hasselbalch-Gleichung und der Neutralisationsreaktionen. Ideal für Chemie-Studierende und zur Vorbereitung auf Prüfungen.
Chemie Abitur 2024: Grundlagen
Umfassender Lernzettel für das Chemie-Abitur 2024 in Hessen. Behandelt zentrale Themen wie Enthalpie, Säure-Base-Gleichgewichte, chemische Reaktionen, Isomerie, und die Struktur von Proteinen und Kohlenhydraten. Ideal für die Prüfungsvorbereitung und das Verständnis chemischer Konzepte. Enthält wichtige Formeln, Reaktionsmechanismen und Nachweisreaktionen.
Säure-Base-Reaktionen verstehen
Entdecken Sie die Grundlagen der Säure-Base-Chemie, einschließlich pH-Wert-Berechnung, Pufferlösungen, und Titrationsmethoden. Diese Zusammenfassung bietet eine klare Übersicht über wichtige Konzepte wie das Ionenprodukt des Wassers, Brønsted-Theorie und die Rolle von Indikatoren in chemischen Reaktionen. Ideal für die Vorbereitung auf das Abitur 2024.
Säure-Base Grundlagen
Umfassende Zusammenfassung der Säure-Base-Theorie für das Abitur 2023. Behandelt pH-Wert-Berechnungen, Neutralisationsreaktionen, Indikatoren, Pufferlösungen, Titrationskurven und die Autoprotolyse von Wasser. Ideal für Chemie LK Schüler zur Prüfungsvorbereitung.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.