Kohlenwasserstoffe, Alkohole und Carbonsäuren sind die Grundbausteine der organischen Chemie... Mehr anzeigen
Chemie Abitur Lernzettel 2024 - LK Hessen





Kohlenwasserstoffe - Die Grundlagen der organischen Chemie
Alkane sind eure ersten Verbündeten in der organischen Chemie. Die Namensfindung ist eigentlich simpel: Anzahl der C-Atome + Endung "-an". Bei verzweigten Ketten sucht ihr die längste Kette und nummeriert die Alkylreste alphabetisch durch.
Die homologe Reihe (Methan, Ethan, Propan...) solltet ihr im Schlaf können. Bei Konstitutionsisomeren habt ihr die gleiche Summenformel, aber unterschiedliche Verknüpfungen - Butan hat 2 Möglichkeiten, Pentan schon 3.
Van-der-Waals-Kräfte bestimmen die physikalischen Eigenschaften. Längere Ketten = stärkere VdWK = höhere Siedetemperatur. Verzweigte Alkane haben schwächere VdWK als lineare, daher niedrigere Siede- und Schmelztemperaturen.
Merksatz: Alkene haben Doppelbindungen , Alkine haben Dreifachbindungen . Je mehr Bindungen, desto schwächer die VdWK, desto niedriger die Siedetemperatur!
Alkene bilden durch ihre Doppelbindungen cis-trans-Isomere - die Substituenten können auf derselben oder gegenüberliegenden Seite stehen.
Oxidation und molekulare Effekte
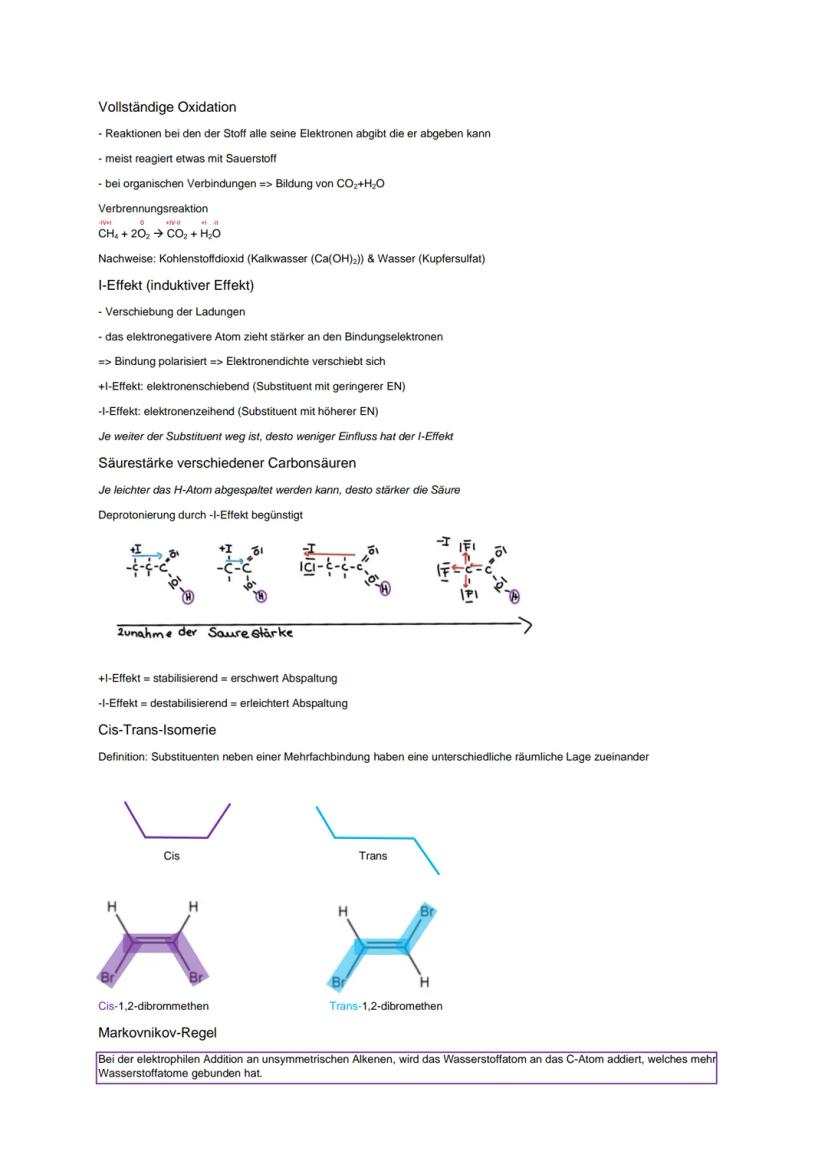
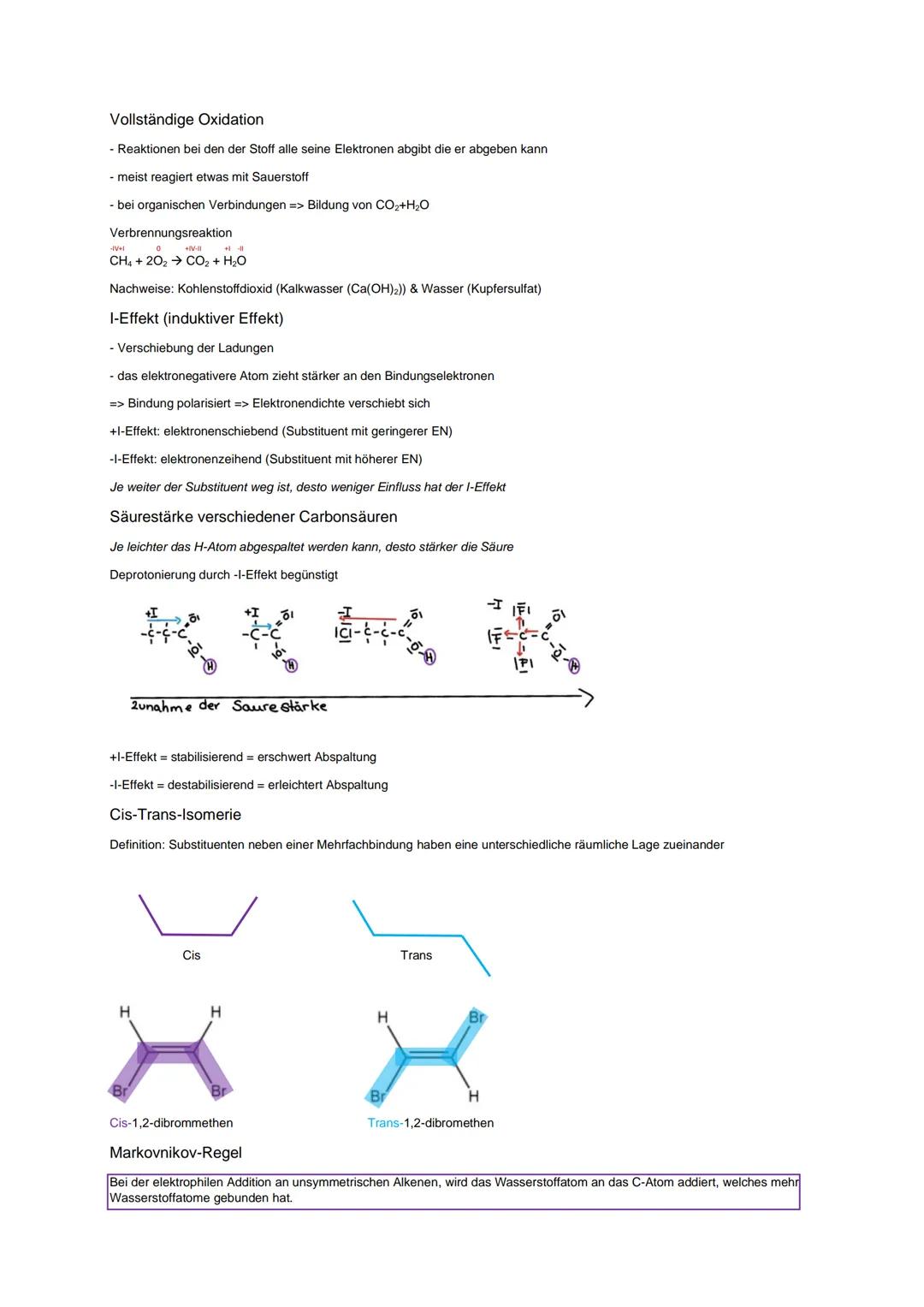
Vollständige Oxidation bedeutet Verbrennung zu CO₂ und H₂O. Den Nachweis macht ihr mit Kalkwasser für CO₂ und Kupfersulfat für Wasser - das kommt gerne in Experimenten dran.
Der I-Effekt (induktiver Effekt) beschreibt, wie sich Ladungen verschieben. Elektronegativere Atome ziehen Elektronen an , weniger elektronegative schieben sie weg . Das beeinflusst direkt die Säurestärke von Carbonsäuren.
Bei der Säurestärke gilt: Je leichter das H-Atom abgespalten wird, desto stärker die Säure. Der -I-Effekt erleichtert die Abspaltung, der +I-Effekt erschwert sie.
Klausur-Tipp: Die Markovnikov-Regel besagt, dass bei elektrophiler Addition das Wasserstoffatom an das C-Atom geht, das bereits mehr H-Atome hat!
Cis-trans-Isomerie entsteht bei Mehrfachbindungen, wenn die Substituenten unterschiedlich angeordnet sind.
Orbitalmodell - Die räumliche Struktur verstehen
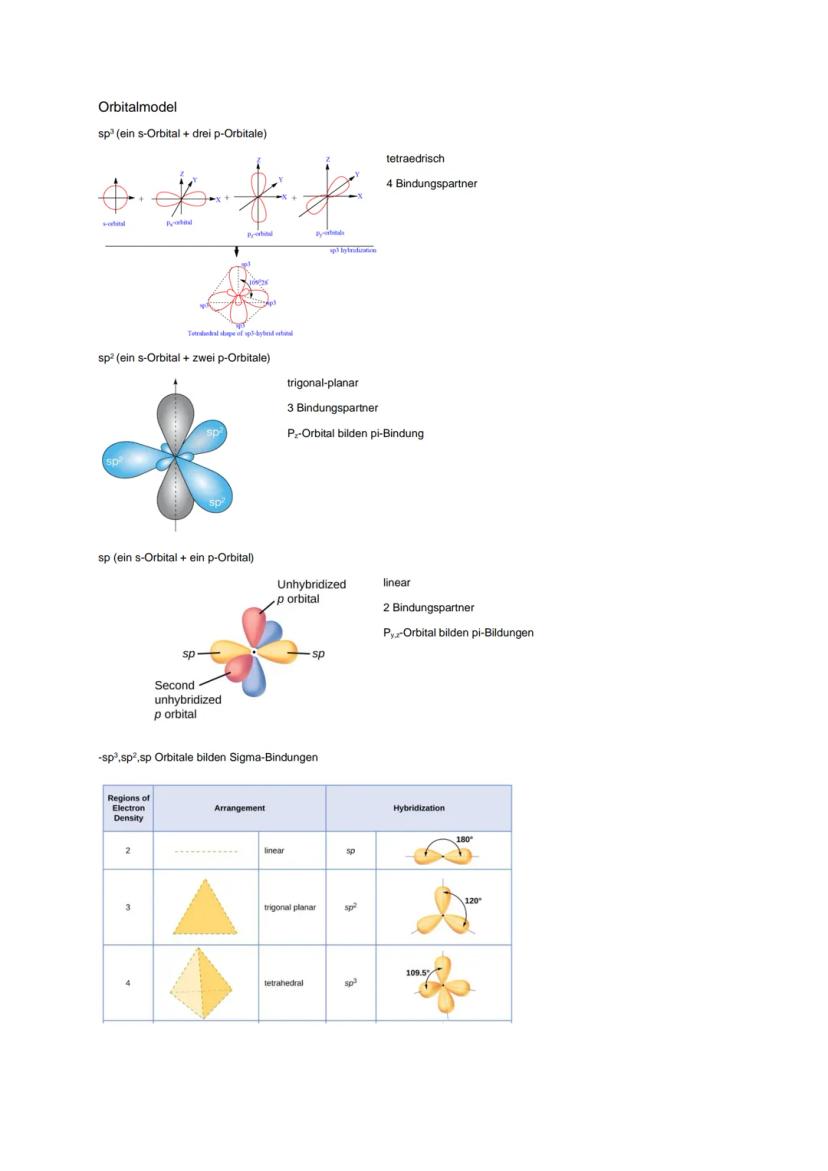
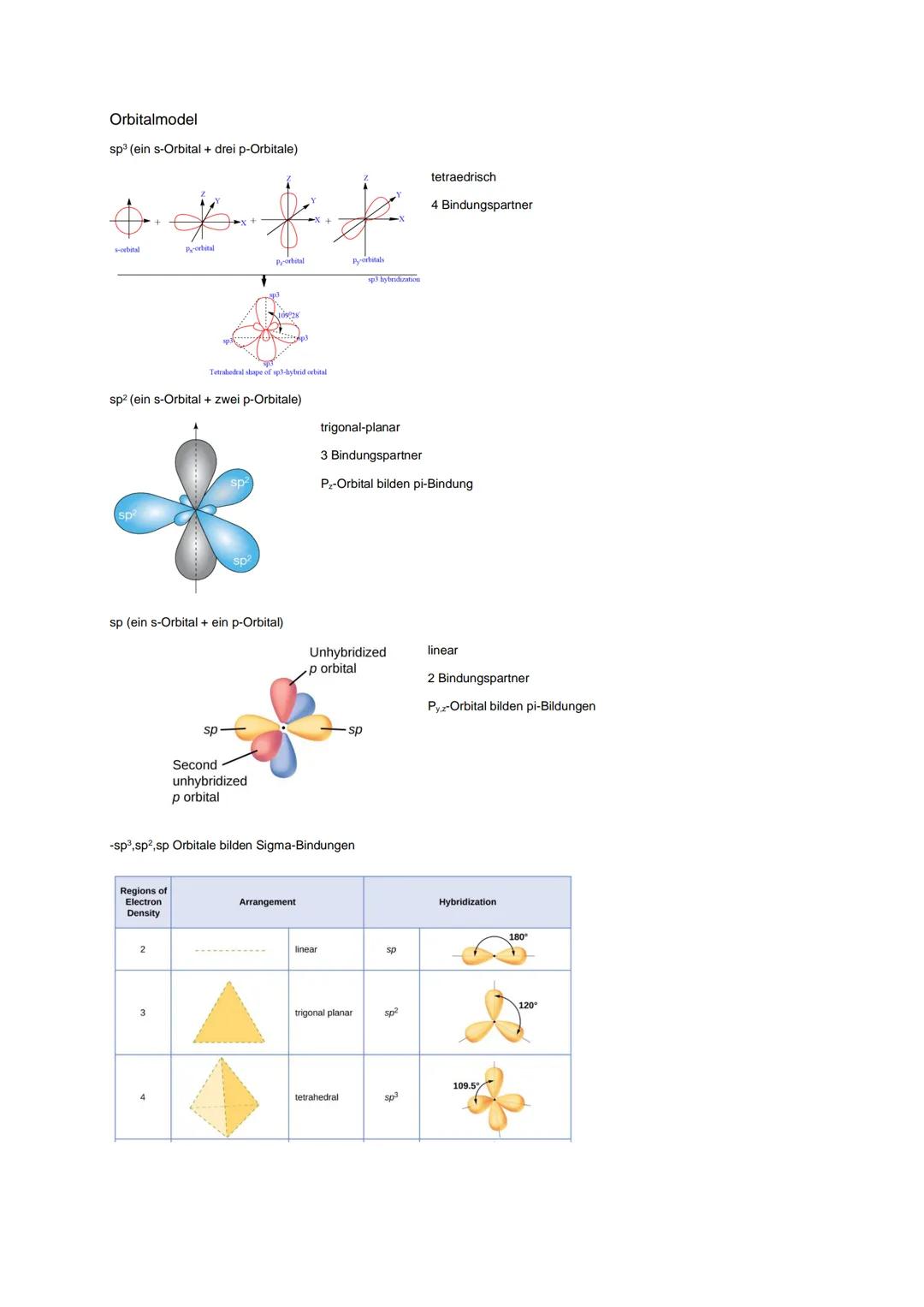
Hybridisierung erklärt, warum Moleküle bestimmte Formen haben. Das sp³-Orbital ist tetraedrisch mit 4 Bindungspartnern (109,5°), sp² ist trigonal-planar mit 3 Partnern (120°), sp ist linear mit 2 Partnern (180°).
Sigma-Bindungen entstehen durch Überlappung von Hybridorbitalen. Pi-Bindungen bilden sich aus unhybridisierten p-Orbitalen - das ist der "zweite Stock" bei Doppel- und Dreifachbindungen.
Die Anzahl der Elektronendichtebereiche bestimmt die Hybridisierung: 2 Bereiche = sp (linear), 3 Bereiche = sp² , 4 Bereiche = sp³ (tetraedrisch).
Verstehen statt auswendig lernen: Je mehr Bindungspartner ein C-Atom hat, desto "voller" wird der Raum um es herum!
Benzol und Mesomerie
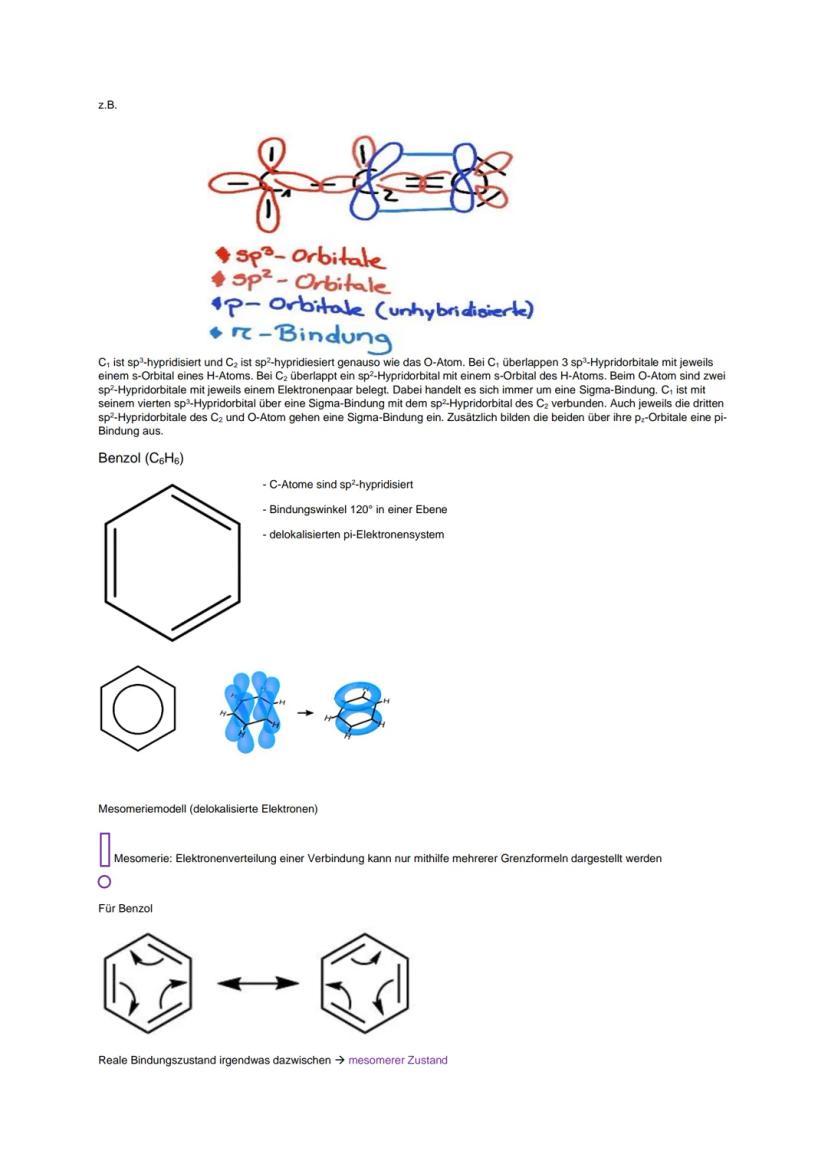
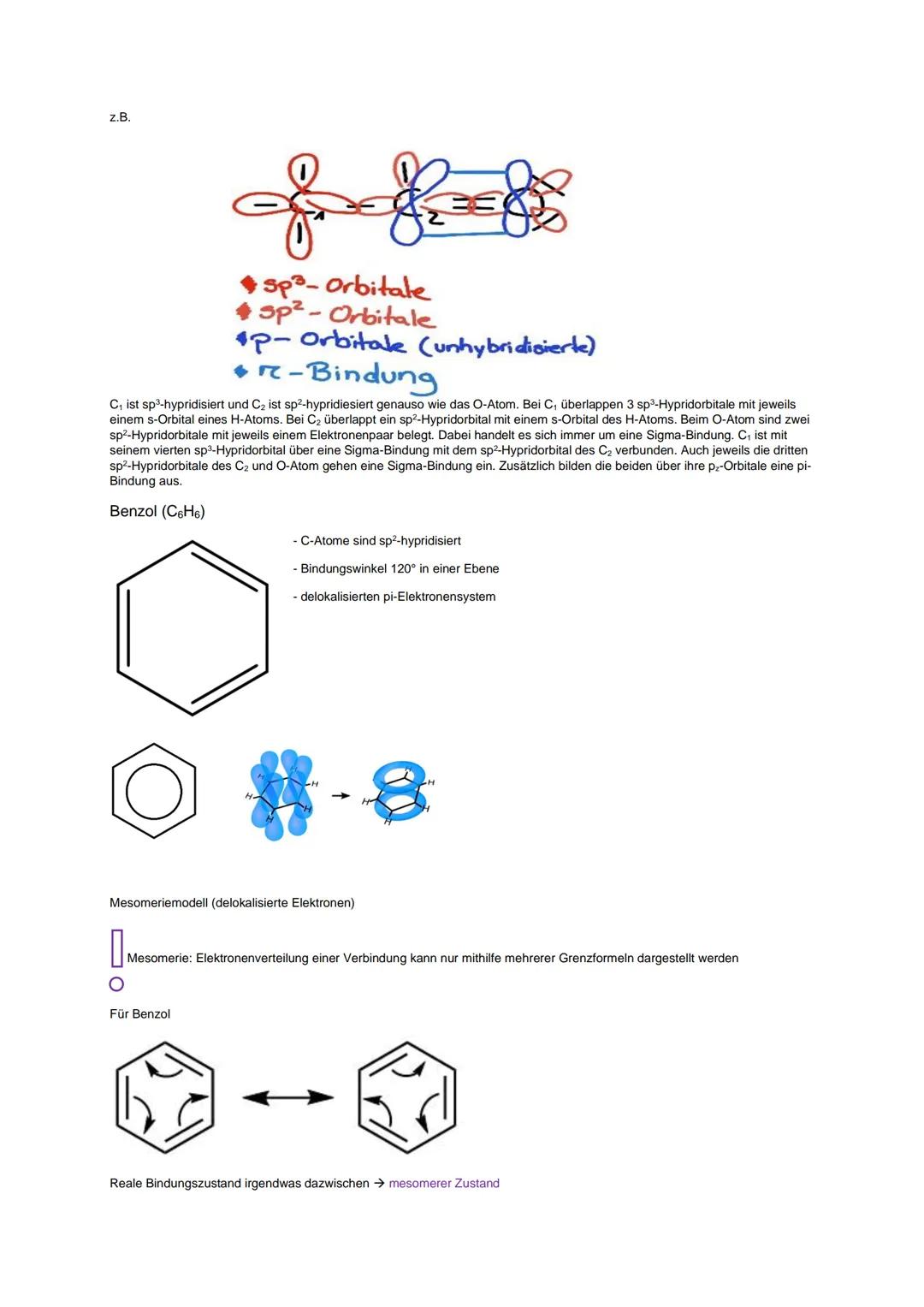
Benzol ist der Superstar der aromatischen Verbindungen. Alle C-Atome sind sp²-hybridisiert mit 120° Bindungswinkeln. Das Besondere: die delokalisierten π-Elektronen bewegen sich frei im Ring.
Mesomerie bedeutet, dass ihr mehrere Grenzformeln braucht, um eine Verbindung zu beschreiben. Der reale Zustand liegt irgendwo dazwischen. Je mehr Grenzformeln möglich sind, desto stabiler wird die Verbindung.
Für Benzol könnt ihr zwei klassische Grenzformeln zeichnen, aber die Realität ist ein mesomerer Zustand mit gleichmäßig verteilten Elektronen.
Aha-Moment: Mesomerie ist wie ein Durchschnitt - die Elektronen "entscheiden" sich nicht für eine Position, sondern sind überall gleichzeitig!
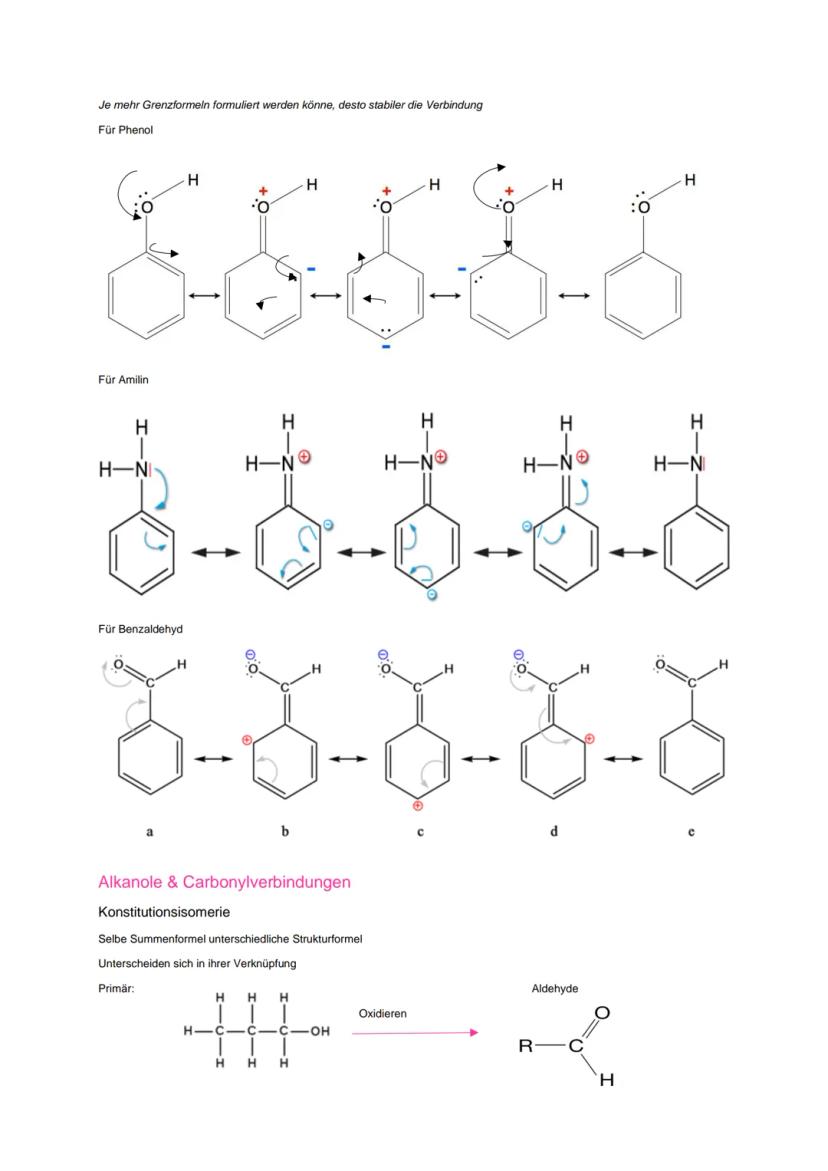
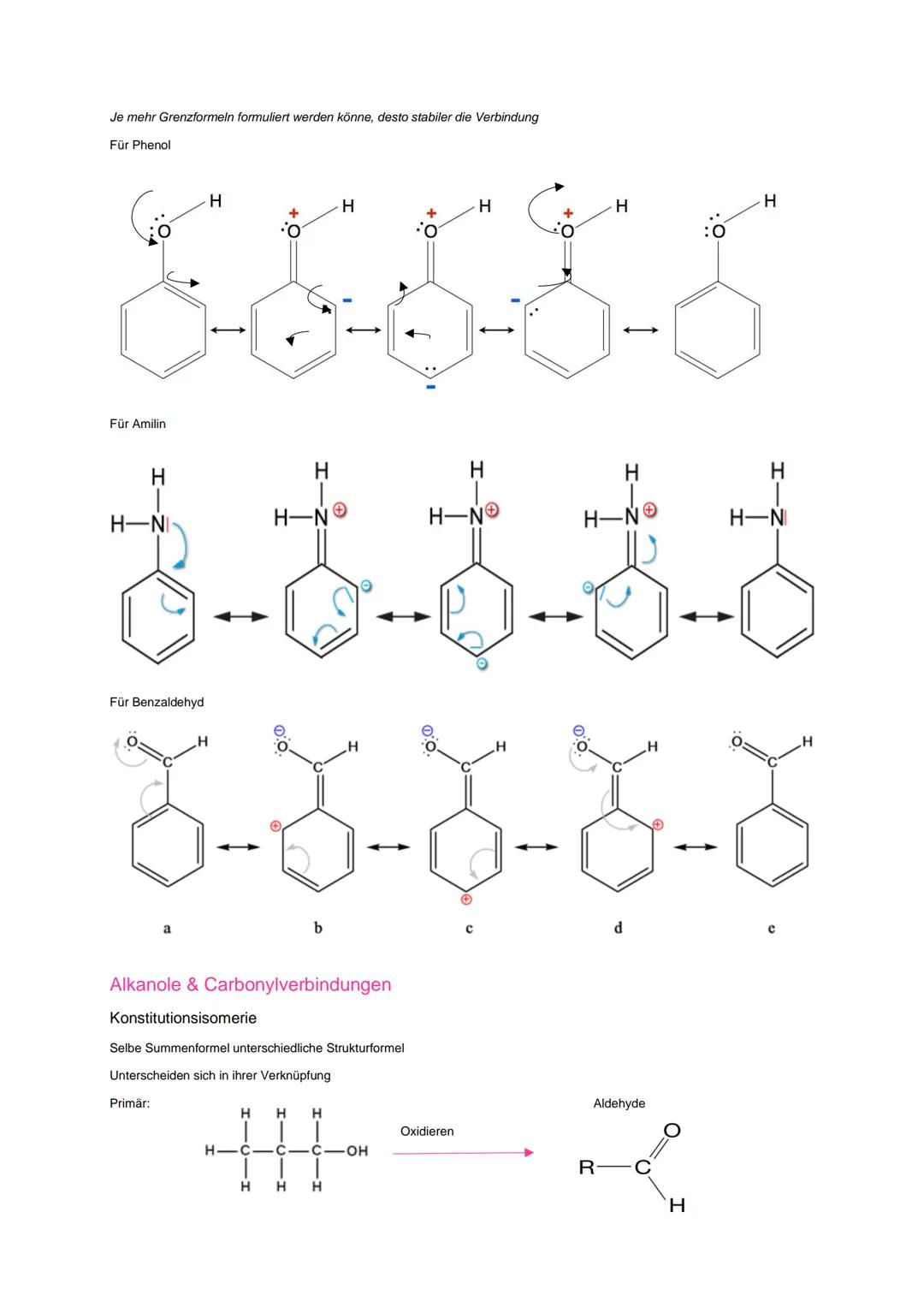
Bei Phenol, Anilin und Benzaldehyd könnt ihr jeweils mehrere Grenzformeln formulieren, was ihre Stabilität erklärt.
Alkohole - Primär, sekundär, tertiär
Konstitutionsisomere haben die gleiche Summenformel, aber unterschiedliche Strukturen. Bei Alkoholen unterscheidet ihr zwischen primären , sekundären und tertiären .
Primäre Alkohole oxidieren zu Aldehyden und dann zu Carbonsäuren. Sekundäre Alkohole werden zu Ketonen oxidiert.
Tertiäre Alkohole lassen sich nicht oxidieren, weil am C-Atom mit der OH-Gruppe kein H-Atom sitzt, das abgegeben werden könnte.
Oxidations-Regel: Nur da wo H-Atome sind, kann auch oxidiert werden!

Zwischenmolekulare Kräfte und Redoxreaktionen
Wasserstoffbrückenbindungen bei Alkoholen sind die stärksten zwischenmolekularen Kräfte. Deshalb haben Alkohole höhere Siedetemperaturen als Carbonyle, die nur Dipol-Dipol-Wechselwirkungen haben.
Bei der Löslichkeit sind kurzkette Alkohole hydrophil (wasserlöslich), ab 4 C-Atomen überwiegt der hydrophobe Teil.
Oxidationszahlen bestimmt ihr systematisch: Elemente haben 0, F hat -I, H hat +I, O meist -II. Die Summe im Molekül muss 0 ergeben.
Redox-Merksatz: Reduktionsmittel geben Elektronen ab (werden selbst oxidiert), Oxidationsmittel nehmen auf (werden selbst reduziert)!
Mehrwertige Alkohole wie Ethylenglykol oder Glycerin haben mehrere OH-Gruppen und sind daher besonders polar.

Aldehyde und Ketone - Carbonylverbindungen im Detail
Die Aldehydgruppe ist reaktiver als die Ketogruppe , weil sie reduzierend wirkt. Mit der Fehling-Probe (roter Niederschlag) oder Tollens-Probe (Silberspiegel) weist ihr Aldehyde nach.
Keto-Enol-Tautomerie beschreibt das Gleichgewicht zwischen Keton und Enol-Form. Meist liegt es auf der Keto-Seite, weil diese stabiler ist.
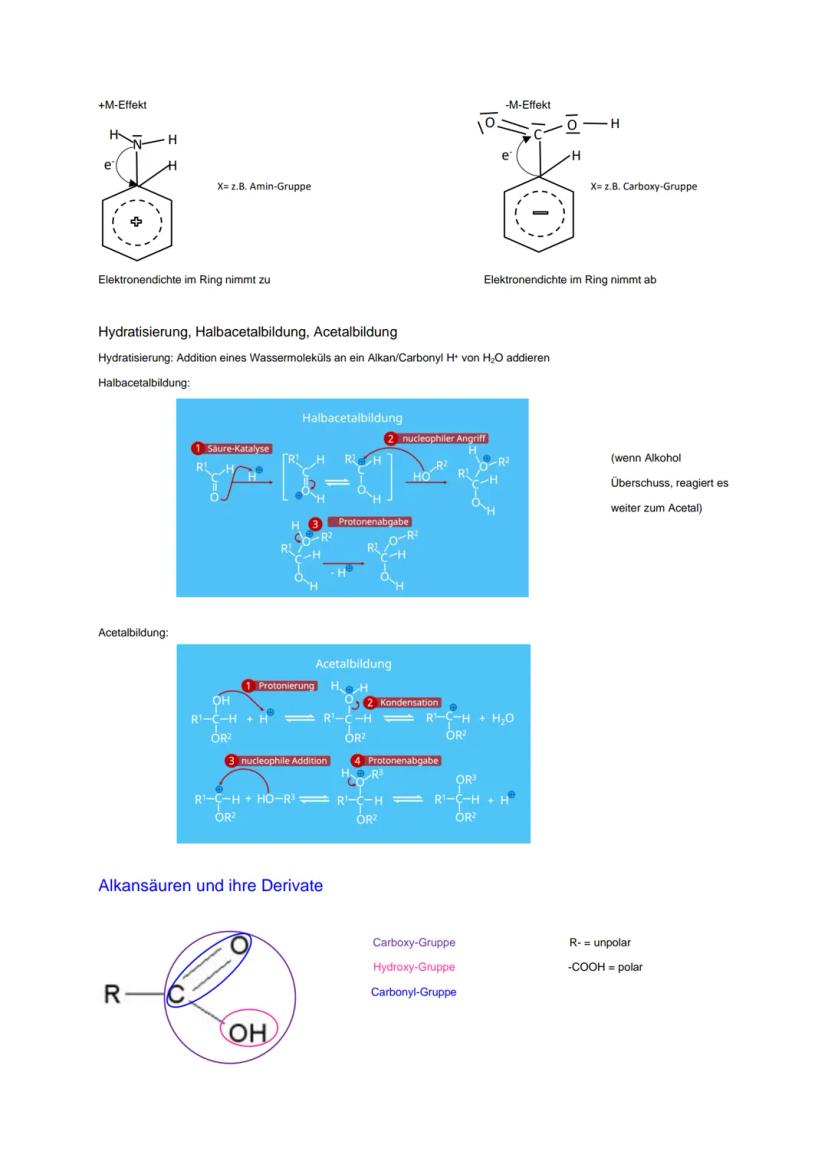
Der M-Effekt ist stärker als der I-Effekt. +M-Effekt erhöht die Elektronendichte , -M-Effekt verringert sie .
Nachweis-Trick: Nur Aldehyde geben positive Fehling- oder Tollens-Probe, Ketone bleiben negativ!
Tertiäre Alkohole haben am C-Atom mit der OH-Gruppe keine H-Atome mehr - deshalb können sie nicht oxidiert werden.

Reaktionsmechanismen - Addition und Bildung
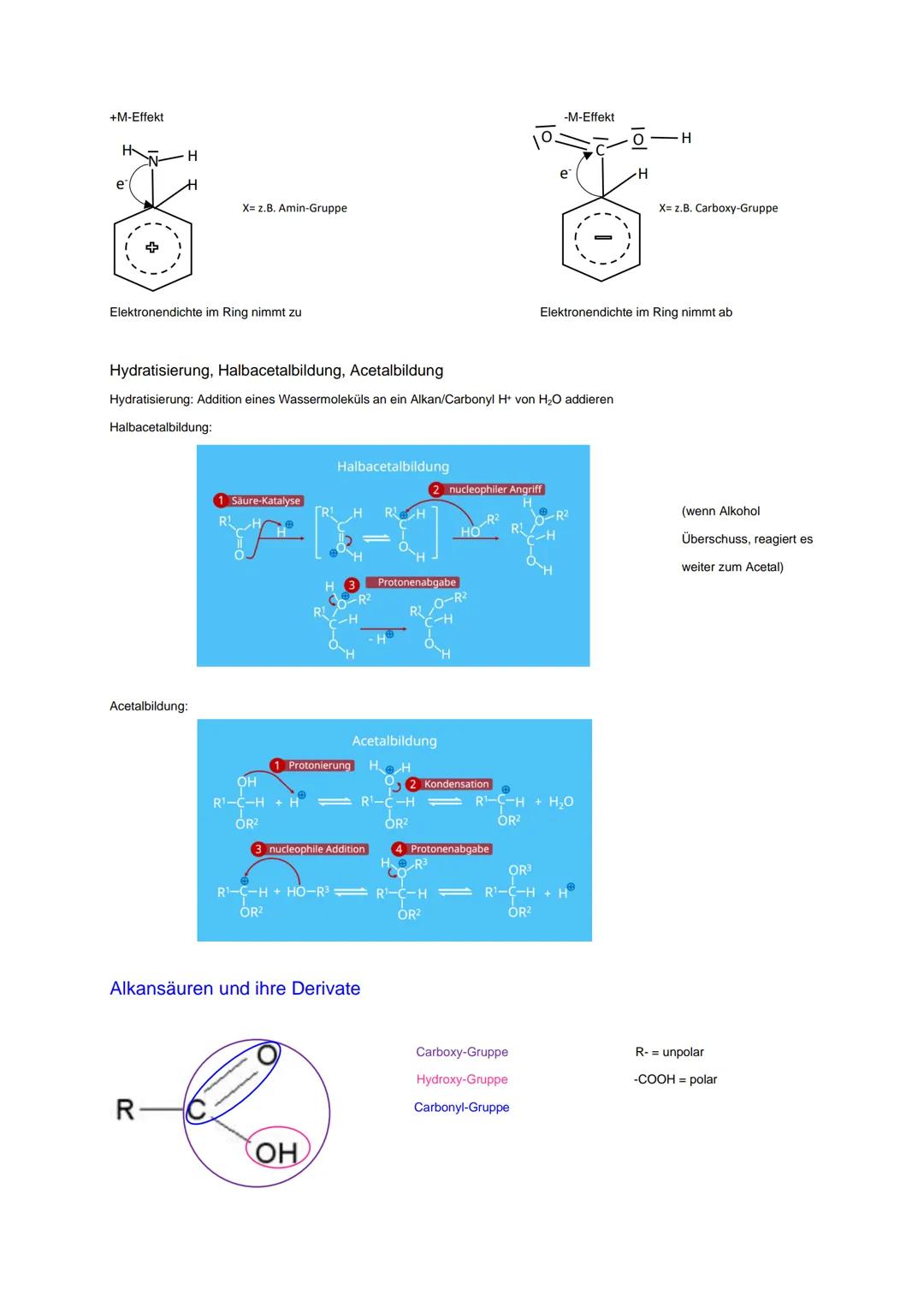
Hydratisierung bedeutet Wasseranlagerung an Carbonyle. Bei der Halbacetalbildung greift ein Alkohol nucleophil an, bei der Acetalbildung reagiert ein zweites Alkoholmolekül unter Wasserabspaltung.
Der Mechanismus läuft über Säurekatalyse: Protonierung macht das Carbonyl-C elektrophiler, dann folgt der nucleophile Angriff des Alkohols.
+M-Effekt bedeutet Elektronenschieben (z.B. Amingruppe), -M-Effekt bedeutet Elektronenziehen (z.B. Carboxygruppe). Das beeinflusst die Elektronendichte im Benzolring.
Mechanismus-Tipp: Säure protoniert zuerst, dann greift das Nucleophil an, am Ende wird wieder deprotoniert!
Die Reaktionsgeschwindigkeit hängt von der Elektronendichte ab: +M beschleunigt, -M verlangsamt.
Carbonsäuren und ihre Eigenschaften
Carbonsäuren haben eine Carboxygruppe aus Carbonyl- und Hydroxygruppe. Der unpolare Rest und die polare Carboxygruppe bestimmen die Eigenschaften.
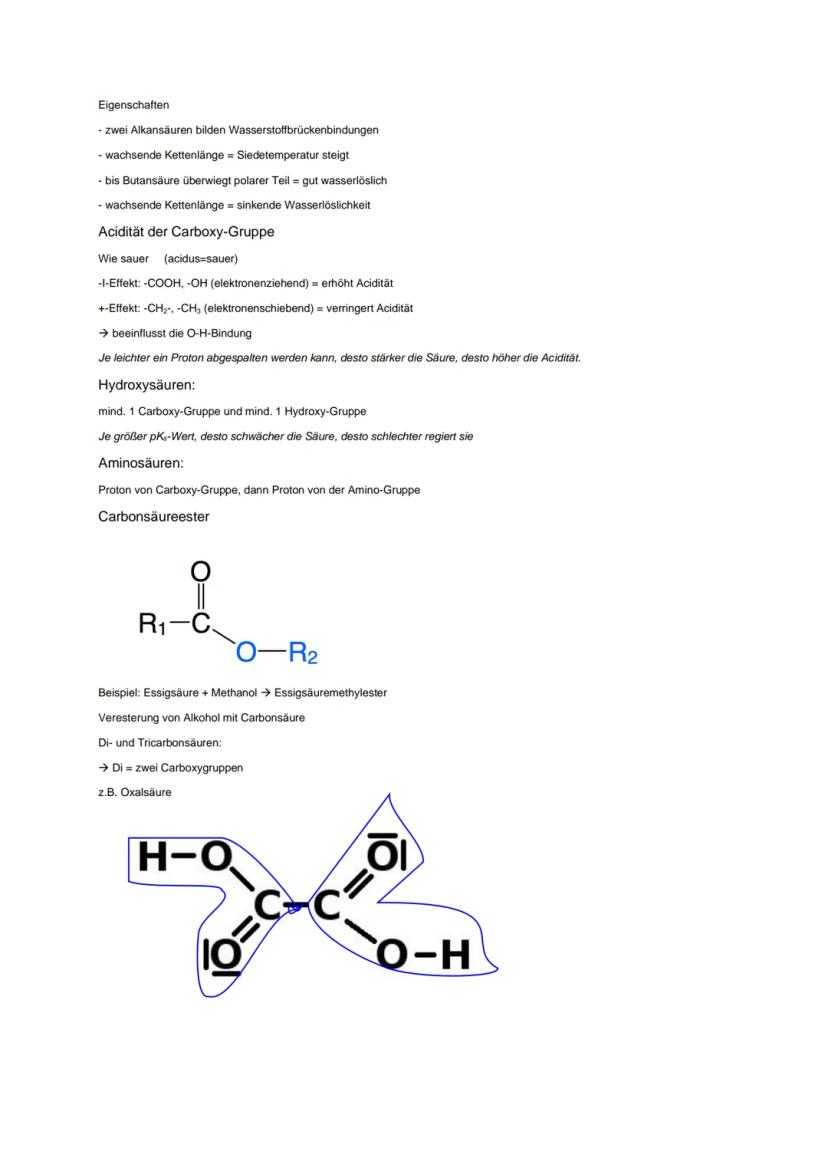
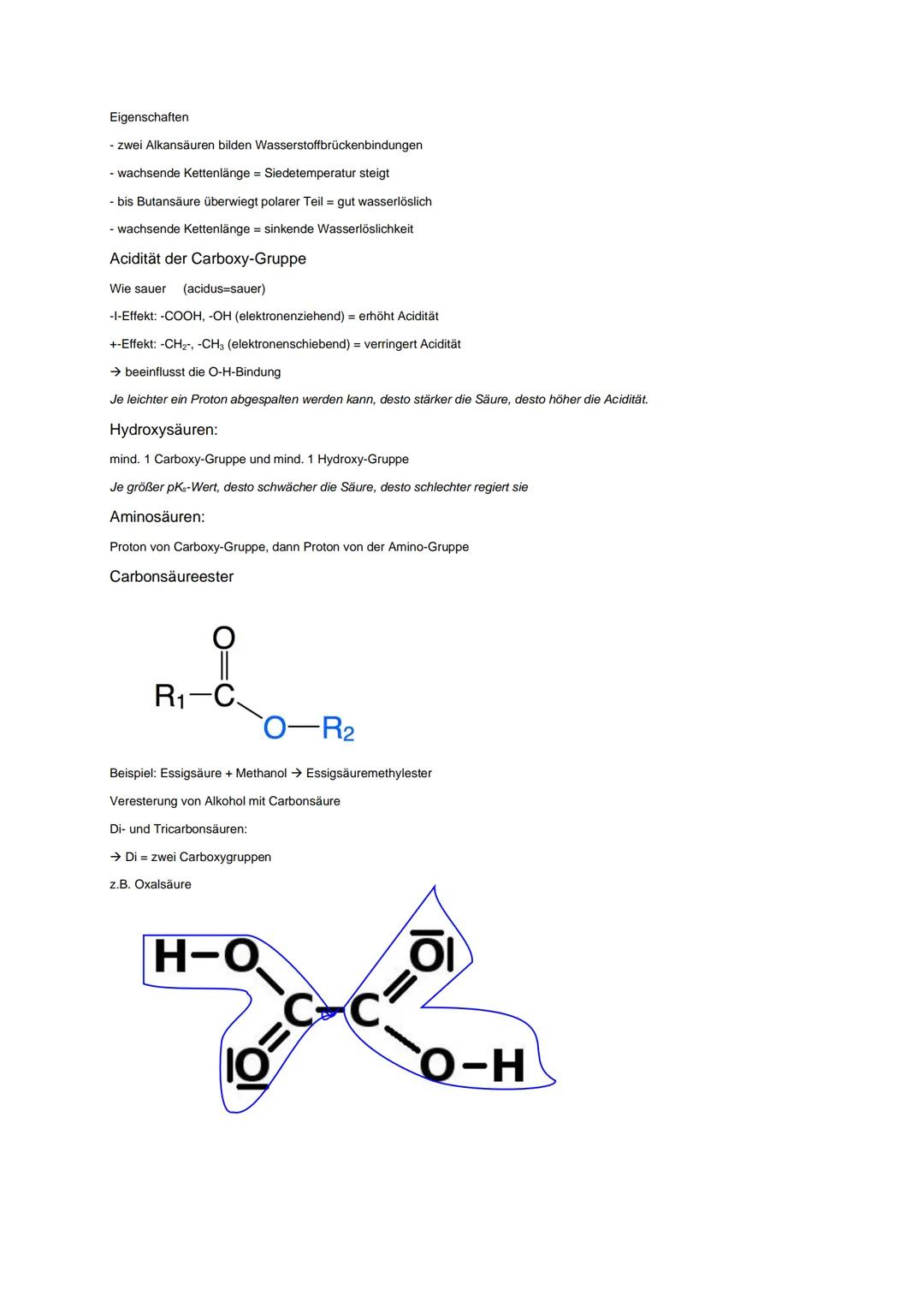
Wasserstoffbrückenbindungen zwischen zwei Carbonsäuren sind besonders stark. Mit wachsender Kettenlänge steigt die Siedetemperatur, aber die Wasserlöslichkeit sinkt (bis Butansäure gut löslich).
Die Acidität wird durch I-Effekte beeinflusst: -I-Effekt erhöht die Acidität, +I-Effekt verringert sie. Je größer der pKₛ-Wert, desto schwächer die Säure.
Säurestärke-Regel: Je leichter das Proton abgespalten wird, desto stärker die Säure!
Hydroxysäuren haben mindestens eine Carboxy- und eine Hydroxygruppe. Aminosäuren können beide Protonen abgeben - erst von der Carboxy-, dann von der Aminogruppe.
Carbonsäurederivate und Veresterung
Carbonsäureester entstehen durch Reaktion von Carbonsäure mit Alkohol. Die allgemeine Formel ist R₁-COO-R₂, wobei die Esterbindung zwischen Carbonyl-C und Sauerstoff liegt.
Veresterung ist eine Kondensationsreaktion: Carbonsäure + Alkohol → Ester + Wasser. Das klassische Beispiel ist Essigsäure + Methanol → Essigsäuremethylester.
Di- und Tricarbonsäuren haben mehrere Carboxygruppen. Oxalsäure ist die einfachste Dicarbonsäure mit zwei COOH-Gruppen.
Ester-Merkmal: Die Esterbindung -COO- ist das Erkennungszeichen - ein Sauerstoff "klebt" Säure und Alkohol zusammen!
Ester haben meist angenehme Gerüche und kommen in natürlichen Aromastoffen vor.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Säure-Base-Chemie
9Säure-Base-Theorie & Puffer
Entdecken Sie die Grundlagen der Säure-Base-Theorie, Pufferlösungen und Indikatoren. Diese Zusammenfassung behandelt wichtige Konzepte wie pH-Wert-Berechnungen, Titrationskurven und die Henderson-Hasselbalch-Gleichung. Ideal für Chemie-LK-Studierende, die sich auf Prüfungen vorbereiten.
Säure-Base-Gleichgewicht und Titration
Entdecken Sie die Grundlagen des chemischen Gleichgewichts und der Säure-Base-Reaktionen. Diese Zusammenfassung behandelt Le Chateliers Prinzip, Titrationskurven, pH-Wert-Berechnungen, Pufferlösungen und die Autoprotolyse von Wasser. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten. Enthält wichtige Formeln und Beispiele zur Veranschaulichung der Konzepte.
Chemie LK Abitur Zusammenfassung
Diese umfassende Zusammenfassung für den Chemie Leistungskurs (LK) in Baden-Württemberg deckt alle relevanten Themen ab, die für das Abitur 2022 wichtig sind. Sie enthält wichtige Konzepte wie Aromaten, chemische Gleichgewichte, Säuren und Basen, Elektrochemie, organische Chemie und mehr. Ideal zur Vorbereitung auf Prüfungen und zur Vertiefung des Verständnisses. Bei Interesse an der PDF-Version, kontaktieren Sie bitte [email protected].
Chemie Lernzettel Q1 - Aminosäuren/Enzyme/Proteine….
Lernzettel umfassend für die erste Klausur in der Oberstufe in Chemie- alles um Aminosäuren, Proteinen( mit Beispielen) als auch Enzymen (einfach erklärt und schlüssig )
Säure-Base-Gleichgewichte, Naturstoffe
1. Säure-Base-Gleichgewichte Säure-Base-Theorie nach Brønsted, Autoprotolyse und pH-Wert, Säure- & Basenstärke, pH-Werte berechnen, Säure-Base-Titration 2. Naturstoffe Chiralität, Optische Aktivität, Fischerprojektion, Kohlenhydrate, Ringform
Säure-Base-Reaktionen
Vertiefte Kenntnisse über Säure-Base-Chemie: Erfahren Sie alles über die Dissoziation von Säuren und Basen, pH-Wert-Berechnungen, Titrationskurven und Puffersysteme. Diese Zusammenfassung bietet eine klare Übersicht über die wichtigsten Konzepte, einschließlich der Henderson-Hasselbalch-Gleichung und der Neutralisationsreaktionen. Ideal für Chemie-Studierende und zur Vorbereitung auf Prüfungen.
Säure-Base-Reaktionen verstehen
Entdecken Sie die Grundlagen der Säure-Base-Chemie, einschließlich pH-Wert-Berechnung, Pufferlösungen, und Titrationsmethoden. Diese Zusammenfassung bietet eine klare Übersicht über wichtige Konzepte wie das Ionenprodukt des Wassers, Brønsted-Theorie und die Rolle von Indikatoren in chemischen Reaktionen. Ideal für die Vorbereitung auf das Abitur 2024.
Chemie Leistungskurs Abitur Lernzettel
Chemie Leistungskurs Abitur Lernzettel
Säure-Base Grundlagen
Umfassende Zusammenfassung der Säure-Base-Theorie für das Abitur 2023. Behandelt pH-Wert-Berechnungen, Neutralisationsreaktionen, Indikatoren, Pufferlösungen, Titrationskurven und die Autoprotolyse von Wasser. Ideal für Chemie LK Schüler zur Prüfungsvorbereitung.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Chemie Abitur Lernzettel 2024 - LK Hessen
Kohlenwasserstoffe, Alkohole und Carbonsäuren sind die Grundbausteine der organischen Chemie - und damit auch euer Schlüssel zum Abi-Erfolg. Hier bekommt ihr das komplette Paket: von der Nomenklatur bis zu den Reaktionsmechanismen, die garantiert in eurer Klausur drankommen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Kohlenwasserstoffe - Die Grundlagen der organischen Chemie
Alkane sind eure ersten Verbündeten in der organischen Chemie. Die Namensfindung ist eigentlich simpel: Anzahl der C-Atome + Endung "-an". Bei verzweigten Ketten sucht ihr die längste Kette und nummeriert die Alkylreste alphabetisch durch.
Die homologe Reihe (Methan, Ethan, Propan...) solltet ihr im Schlaf können. Bei Konstitutionsisomeren habt ihr die gleiche Summenformel, aber unterschiedliche Verknüpfungen - Butan hat 2 Möglichkeiten, Pentan schon 3.
Van-der-Waals-Kräfte bestimmen die physikalischen Eigenschaften. Längere Ketten = stärkere VdWK = höhere Siedetemperatur. Verzweigte Alkane haben schwächere VdWK als lineare, daher niedrigere Siede- und Schmelztemperaturen.
Merksatz: Alkene haben Doppelbindungen , Alkine haben Dreifachbindungen . Je mehr Bindungen, desto schwächer die VdWK, desto niedriger die Siedetemperatur!
Alkene bilden durch ihre Doppelbindungen cis-trans-Isomere - die Substituenten können auf derselben oder gegenüberliegenden Seite stehen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Oxidation und molekulare Effekte
Vollständige Oxidation bedeutet Verbrennung zu CO₂ und H₂O. Den Nachweis macht ihr mit Kalkwasser für CO₂ und Kupfersulfat für Wasser - das kommt gerne in Experimenten dran.
Der I-Effekt (induktiver Effekt) beschreibt, wie sich Ladungen verschieben. Elektronegativere Atome ziehen Elektronen an , weniger elektronegative schieben sie weg . Das beeinflusst direkt die Säurestärke von Carbonsäuren.
Bei der Säurestärke gilt: Je leichter das H-Atom abgespalten wird, desto stärker die Säure. Der -I-Effekt erleichtert die Abspaltung, der +I-Effekt erschwert sie.
Klausur-Tipp: Die Markovnikov-Regel besagt, dass bei elektrophiler Addition das Wasserstoffatom an das C-Atom geht, das bereits mehr H-Atome hat!
Cis-trans-Isomerie entsteht bei Mehrfachbindungen, wenn die Substituenten unterschiedlich angeordnet sind.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Orbitalmodell - Die räumliche Struktur verstehen
Hybridisierung erklärt, warum Moleküle bestimmte Formen haben. Das sp³-Orbital ist tetraedrisch mit 4 Bindungspartnern (109,5°), sp² ist trigonal-planar mit 3 Partnern (120°), sp ist linear mit 2 Partnern (180°).
Sigma-Bindungen entstehen durch Überlappung von Hybridorbitalen. Pi-Bindungen bilden sich aus unhybridisierten p-Orbitalen - das ist der "zweite Stock" bei Doppel- und Dreifachbindungen.
Die Anzahl der Elektronendichtebereiche bestimmt die Hybridisierung: 2 Bereiche = sp (linear), 3 Bereiche = sp² , 4 Bereiche = sp³ (tetraedrisch).
Verstehen statt auswendig lernen: Je mehr Bindungspartner ein C-Atom hat, desto "voller" wird der Raum um es herum!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Benzol und Mesomerie
Benzol ist der Superstar der aromatischen Verbindungen. Alle C-Atome sind sp²-hybridisiert mit 120° Bindungswinkeln. Das Besondere: die delokalisierten π-Elektronen bewegen sich frei im Ring.
Mesomerie bedeutet, dass ihr mehrere Grenzformeln braucht, um eine Verbindung zu beschreiben. Der reale Zustand liegt irgendwo dazwischen. Je mehr Grenzformeln möglich sind, desto stabiler wird die Verbindung.
Für Benzol könnt ihr zwei klassische Grenzformeln zeichnen, aber die Realität ist ein mesomerer Zustand mit gleichmäßig verteilten Elektronen.
Aha-Moment: Mesomerie ist wie ein Durchschnitt - die Elektronen "entscheiden" sich nicht für eine Position, sondern sind überall gleichzeitig!
Bei Phenol, Anilin und Benzaldehyd könnt ihr jeweils mehrere Grenzformeln formulieren, was ihre Stabilität erklärt.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Alkohole - Primär, sekundär, tertiär
Konstitutionsisomere haben die gleiche Summenformel, aber unterschiedliche Strukturen. Bei Alkoholen unterscheidet ihr zwischen primären , sekundären und tertiären .
Primäre Alkohole oxidieren zu Aldehyden und dann zu Carbonsäuren. Sekundäre Alkohole werden zu Ketonen oxidiert.
Tertiäre Alkohole lassen sich nicht oxidieren, weil am C-Atom mit der OH-Gruppe kein H-Atom sitzt, das abgegeben werden könnte.
Oxidations-Regel: Nur da wo H-Atome sind, kann auch oxidiert werden!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Zwischenmolekulare Kräfte und Redoxreaktionen
Wasserstoffbrückenbindungen bei Alkoholen sind die stärksten zwischenmolekularen Kräfte. Deshalb haben Alkohole höhere Siedetemperaturen als Carbonyle, die nur Dipol-Dipol-Wechselwirkungen haben.
Bei der Löslichkeit sind kurzkette Alkohole hydrophil (wasserlöslich), ab 4 C-Atomen überwiegt der hydrophobe Teil.
Oxidationszahlen bestimmt ihr systematisch: Elemente haben 0, F hat -I, H hat +I, O meist -II. Die Summe im Molekül muss 0 ergeben.
Redox-Merksatz: Reduktionsmittel geben Elektronen ab (werden selbst oxidiert), Oxidationsmittel nehmen auf (werden selbst reduziert)!
Mehrwertige Alkohole wie Ethylenglykol oder Glycerin haben mehrere OH-Gruppen und sind daher besonders polar.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Aldehyde und Ketone - Carbonylverbindungen im Detail
Die Aldehydgruppe ist reaktiver als die Ketogruppe , weil sie reduzierend wirkt. Mit der Fehling-Probe (roter Niederschlag) oder Tollens-Probe (Silberspiegel) weist ihr Aldehyde nach.
Keto-Enol-Tautomerie beschreibt das Gleichgewicht zwischen Keton und Enol-Form. Meist liegt es auf der Keto-Seite, weil diese stabiler ist.
Der M-Effekt ist stärker als der I-Effekt. +M-Effekt erhöht die Elektronendichte , -M-Effekt verringert sie .
Nachweis-Trick: Nur Aldehyde geben positive Fehling- oder Tollens-Probe, Ketone bleiben negativ!
Tertiäre Alkohole haben am C-Atom mit der OH-Gruppe keine H-Atome mehr - deshalb können sie nicht oxidiert werden.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Reaktionsmechanismen - Addition und Bildung
Hydratisierung bedeutet Wasseranlagerung an Carbonyle. Bei der Halbacetalbildung greift ein Alkohol nucleophil an, bei der Acetalbildung reagiert ein zweites Alkoholmolekül unter Wasserabspaltung.
Der Mechanismus läuft über Säurekatalyse: Protonierung macht das Carbonyl-C elektrophiler, dann folgt der nucleophile Angriff des Alkohols.
+M-Effekt bedeutet Elektronenschieben (z.B. Amingruppe), -M-Effekt bedeutet Elektronenziehen (z.B. Carboxygruppe). Das beeinflusst die Elektronendichte im Benzolring.
Mechanismus-Tipp: Säure protoniert zuerst, dann greift das Nucleophil an, am Ende wird wieder deprotoniert!
Die Reaktionsgeschwindigkeit hängt von der Elektronendichte ab: +M beschleunigt, -M verlangsamt.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Carbonsäuren und ihre Eigenschaften
Carbonsäuren haben eine Carboxygruppe aus Carbonyl- und Hydroxygruppe. Der unpolare Rest und die polare Carboxygruppe bestimmen die Eigenschaften.
Wasserstoffbrückenbindungen zwischen zwei Carbonsäuren sind besonders stark. Mit wachsender Kettenlänge steigt die Siedetemperatur, aber die Wasserlöslichkeit sinkt (bis Butansäure gut löslich).
Die Acidität wird durch I-Effekte beeinflusst: -I-Effekt erhöht die Acidität, +I-Effekt verringert sie. Je größer der pKₛ-Wert, desto schwächer die Säure.
Säurestärke-Regel: Je leichter das Proton abgespalten wird, desto stärker die Säure!
Hydroxysäuren haben mindestens eine Carboxy- und eine Hydroxygruppe. Aminosäuren können beide Protonen abgeben - erst von der Carboxy-, dann von der Aminogruppe.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Carbonsäurederivate und Veresterung
Carbonsäureester entstehen durch Reaktion von Carbonsäure mit Alkohol. Die allgemeine Formel ist R₁-COO-R₂, wobei die Esterbindung zwischen Carbonyl-C und Sauerstoff liegt.
Veresterung ist eine Kondensationsreaktion: Carbonsäure + Alkohol → Ester + Wasser. Das klassische Beispiel ist Essigsäure + Methanol → Essigsäuremethylester.
Di- und Tricarbonsäuren haben mehrere Carboxygruppen. Oxalsäure ist die einfachste Dicarbonsäure mit zwei COOH-Gruppen.
Ester-Merkmal: Die Esterbindung -COO- ist das Erkennungszeichen - ein Sauerstoff "klebt" Säure und Alkohol zusammen!
Ester haben meist angenehme Gerüche und kommen in natürlichen Aromastoffen vor.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Säure-Base-Chemie
9Säure-Base-Theorie & Puffer
Entdecken Sie die Grundlagen der Säure-Base-Theorie, Pufferlösungen und Indikatoren. Diese Zusammenfassung behandelt wichtige Konzepte wie pH-Wert-Berechnungen, Titrationskurven und die Henderson-Hasselbalch-Gleichung. Ideal für Chemie-LK-Studierende, die sich auf Prüfungen vorbereiten.
Säure-Base-Gleichgewicht und Titration
Entdecken Sie die Grundlagen des chemischen Gleichgewichts und der Säure-Base-Reaktionen. Diese Zusammenfassung behandelt Le Chateliers Prinzip, Titrationskurven, pH-Wert-Berechnungen, Pufferlösungen und die Autoprotolyse von Wasser. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten. Enthält wichtige Formeln und Beispiele zur Veranschaulichung der Konzepte.
Chemie LK Abitur Zusammenfassung
Diese umfassende Zusammenfassung für den Chemie Leistungskurs (LK) in Baden-Württemberg deckt alle relevanten Themen ab, die für das Abitur 2022 wichtig sind. Sie enthält wichtige Konzepte wie Aromaten, chemische Gleichgewichte, Säuren und Basen, Elektrochemie, organische Chemie und mehr. Ideal zur Vorbereitung auf Prüfungen und zur Vertiefung des Verständnisses. Bei Interesse an der PDF-Version, kontaktieren Sie bitte [email protected].
Chemie Lernzettel Q1 - Aminosäuren/Enzyme/Proteine….
Lernzettel umfassend für die erste Klausur in der Oberstufe in Chemie- alles um Aminosäuren, Proteinen( mit Beispielen) als auch Enzymen (einfach erklärt und schlüssig )
Säure-Base-Gleichgewichte, Naturstoffe
1. Säure-Base-Gleichgewichte Säure-Base-Theorie nach Brønsted, Autoprotolyse und pH-Wert, Säure- & Basenstärke, pH-Werte berechnen, Säure-Base-Titration 2. Naturstoffe Chiralität, Optische Aktivität, Fischerprojektion, Kohlenhydrate, Ringform
Säure-Base-Reaktionen
Vertiefte Kenntnisse über Säure-Base-Chemie: Erfahren Sie alles über die Dissoziation von Säuren und Basen, pH-Wert-Berechnungen, Titrationskurven und Puffersysteme. Diese Zusammenfassung bietet eine klare Übersicht über die wichtigsten Konzepte, einschließlich der Henderson-Hasselbalch-Gleichung und der Neutralisationsreaktionen. Ideal für Chemie-Studierende und zur Vorbereitung auf Prüfungen.
Säure-Base-Reaktionen verstehen
Entdecken Sie die Grundlagen der Säure-Base-Chemie, einschließlich pH-Wert-Berechnung, Pufferlösungen, und Titrationsmethoden. Diese Zusammenfassung bietet eine klare Übersicht über wichtige Konzepte wie das Ionenprodukt des Wassers, Brønsted-Theorie und die Rolle von Indikatoren in chemischen Reaktionen. Ideal für die Vorbereitung auf das Abitur 2024.
Chemie Leistungskurs Abitur Lernzettel
Chemie Leistungskurs Abitur Lernzettel
Säure-Base Grundlagen
Umfassende Zusammenfassung der Säure-Base-Theorie für das Abitur 2023. Behandelt pH-Wert-Berechnungen, Neutralisationsreaktionen, Indikatoren, Pufferlösungen, Titrationskurven und die Autoprotolyse von Wasser. Ideal für Chemie LK Schüler zur Prüfungsvorbereitung.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.