Du stehst vor Säuren, Basen und Redoxreaktionen - zwei der... Mehr anzeigen
Melde dich an, um den Inhalt zu sehenKostenlos!
Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Knowunity KI
Fächer
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Alle Themen anzeigen
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Alle Themen anzeigen
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Alle Themen anzeigen
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Alle Themen anzeigen
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Alle Themen anzeigen
3,011
•
Aktualisiert May 8, 2026
•
Michaela Kerner
@michaela.ek
Du stehst vor Säuren, Basen und Redoxreaktionen - zwei der... Mehr anzeigen







Starke vs. schwache Säuren - das ist der Schlüssel zum Verständnis! Starke Säuren (pKs < 3,75) geben ihre Protonen komplett ab, während schwache Säuren (pKs > 3,75) nur teilweise dissoziieren.
Der pH-Wert zeigt dir, wie sauer eine Lösung ist: pH = -lg(c(H₃O⁺)). Bei starken Säuren rechnest du einfach mit der Konzentration, bei schwachen brauchst du die Wurzelformel: pH = ½.
Brønsted-Säure-Base-Theory macht alles verständlich: Säuren sind Protonendonatoren, Basen sind Protonenakzeptoren. Ampholyte wie Wasser können beides - je nach Reaktionspartner!
Merktrick: pH + pOH = 14 - das gilt immer bei 25°C!
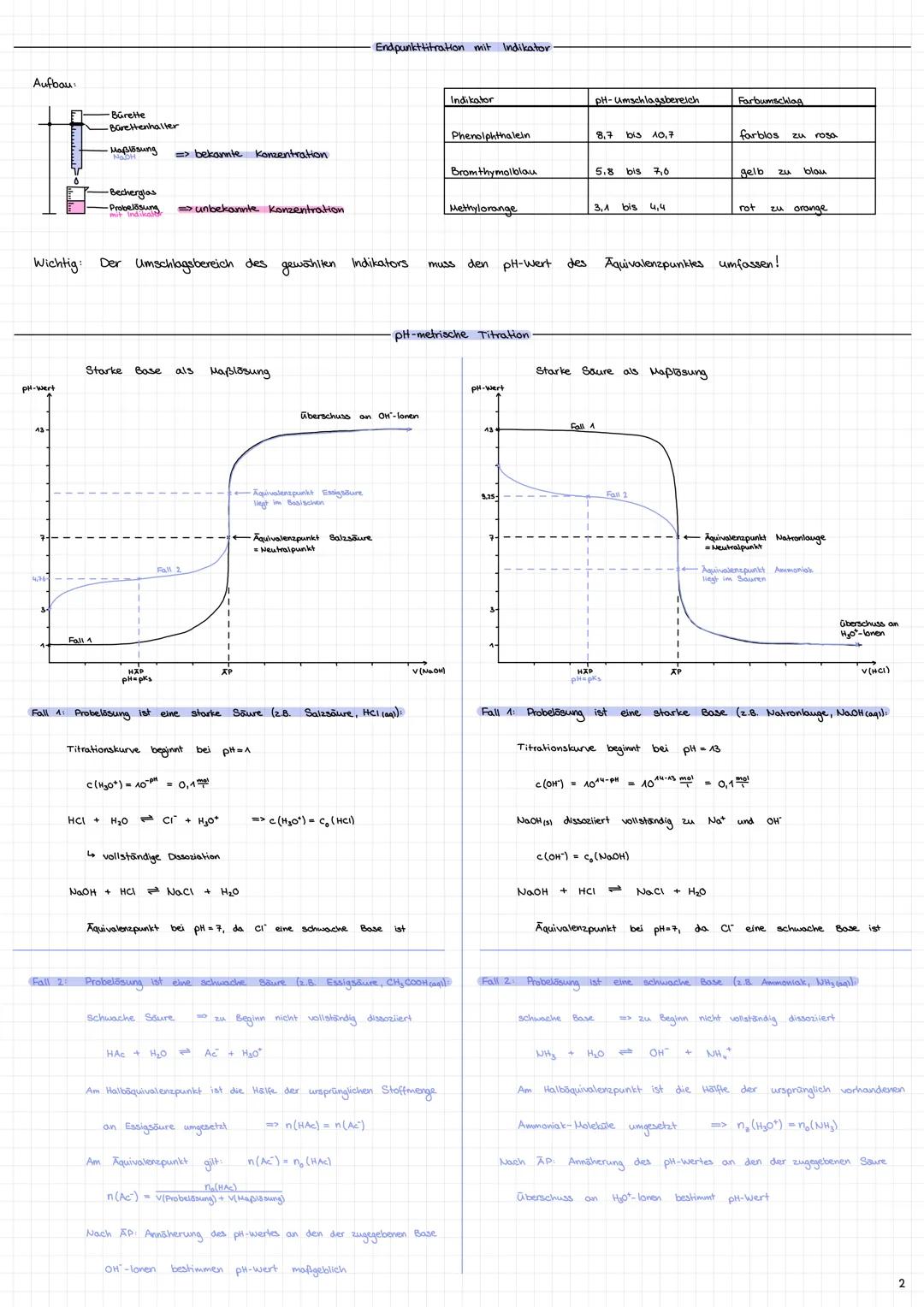
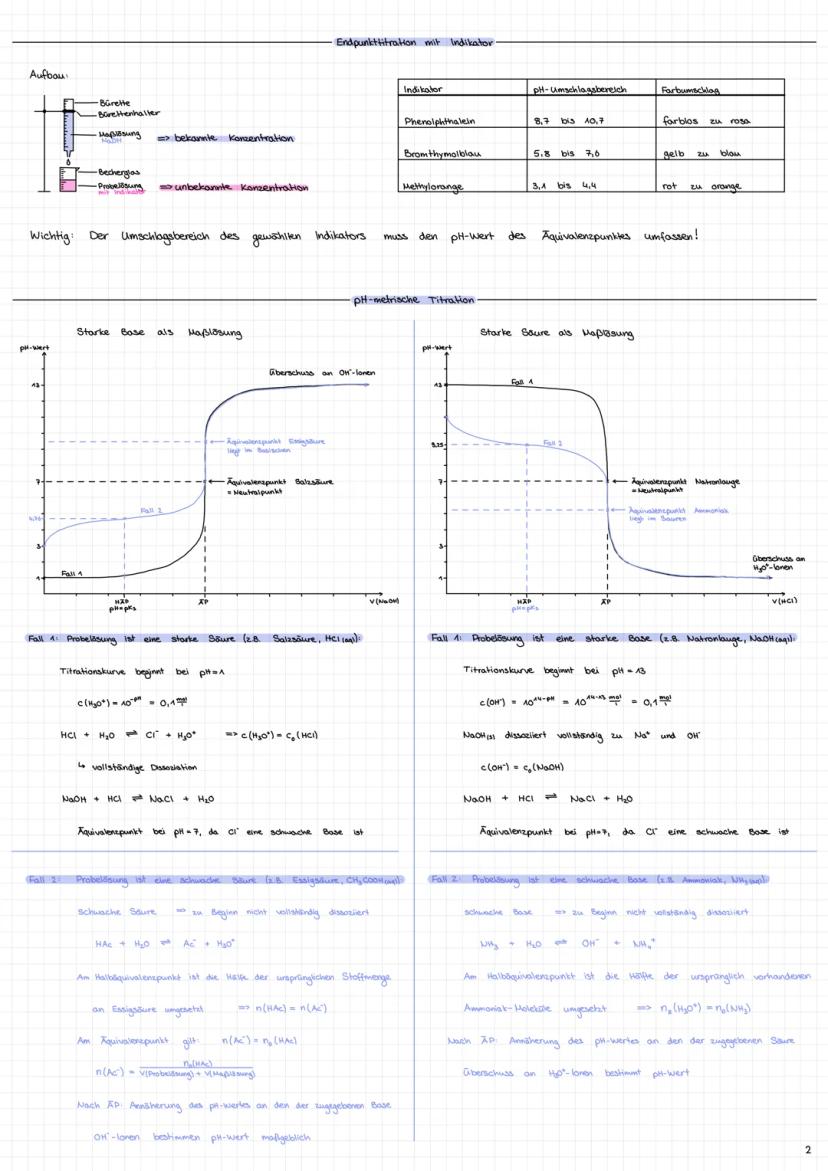
Titration ist deine Methode, um unbekannte Konzentrationen herauszufinden. Du gibst tropfenweise eine Maßlösung (bekannte Konzentration) zu deiner Probelösung bis zum Äquivalenzpunkt.
Bei der pH-metrischen Titration siehst du verschiedene Kurvenverläufe: Starke Säuren gegen starke Basen ergeben einen Äquivalenzpunkt bei pH = 7. Schwache Säuren gegen starke Basen landen im basischen Bereich (pH > 7).
Der Halbäquivalenzpunkt ist besonders clever - hier gilt pH = pKs! Das nutzt du zur Bestimmung der Säurekonstante.
Indikatorauswahl ist entscheidend: Der Umschlagsbereich muss den Äquivalenzpunkt umfassen. Phenolphthalein (8,7-10,7) für schwache Säuren, Methylorange (3,1-4,4) für schwache Basen.
Rechentrick: c(Probelösung) = c(Maßlösung) × V(Maßlösung) / V(Probelösung)
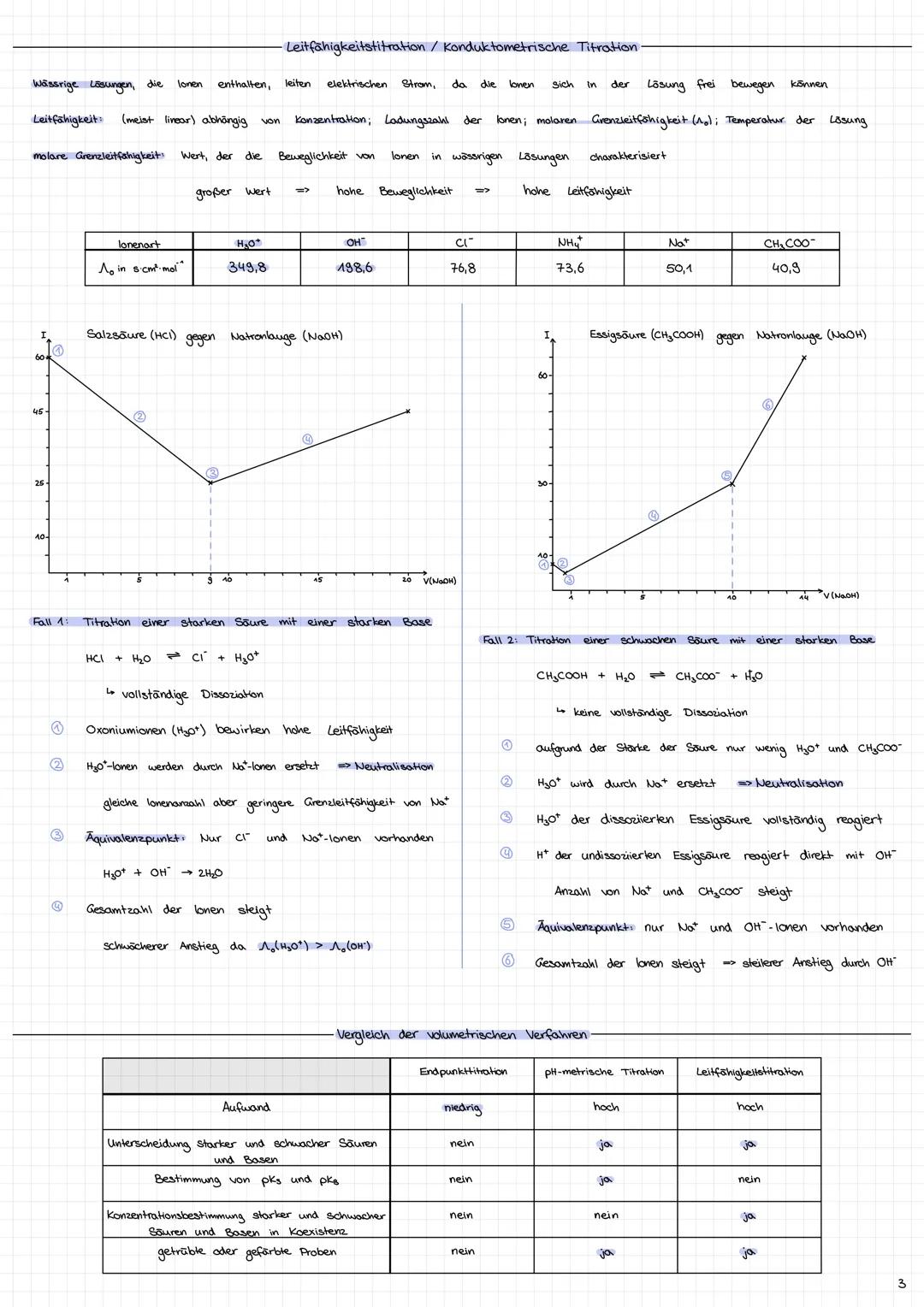
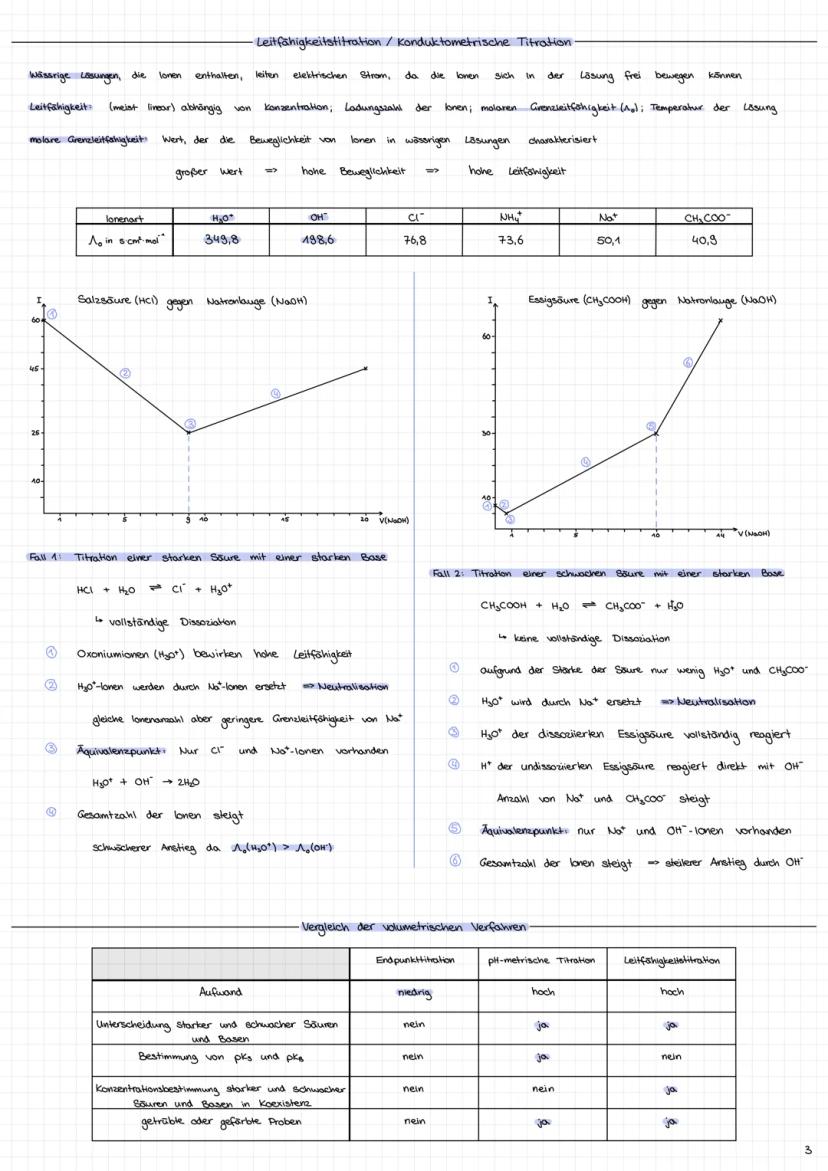
Leitfähigkeitstitration nutzt die Tatsache, dass Ionen elektrischen Strom leiten. Die molare Grenzleitfähigkeit zeigt dir, wie beweglich verschiedene Ionen sind: H₃O⁺ (349,8) ist champion, OH⁻ (198,6) auf Platz zwei!
Bei starken Säuren gegen starke Basen siehst du erst einen Abfall (H₃O⁺ wird durch Na⁺ ersetzt), dann einen steilen Anstieg . Bei schwachen Säuren startest du mit niedriger Leitfähigkeit und steigst dann stark an.
Vorteile der Leitfähigkeitstitration: Du kannst trübe oder gefärbte Proben messen und starke von schwachen Säuren unterscheiden. Der Aufwand ist allerdings höher als bei einfachen Endpunkttitrationen.
Praktischer Tipp: Äquivalenzpunkt = Schnittpunkt der beiden Geraden im Leitfähigkeits-Diagramm!

Redoxreaktionen sind überall: Rost, Batterien, Atmung! Das Donator-Akzeptor-Prinzip erklärt alles: Oxidation bedeutet Elektronenabgabe, Reduktion bedeutet Elektronenaufnahme - und beides läuft immer gleichzeitig ab.
Oxidationszahlen bestimmen ist dein Werkzeug: Einzelne Atome haben immer 0, Metallionen sind positiv, in Molekülen ergibt die Summe null. Wasserstoff meist +I, Sauerstoff meist -II, Fluor immer -I.
Redoxgleichungen aufstellen: Erst Oxidationszahlen bestimmen, dann Teilgleichungen für Oxidation und Reduktion aufstellen, Ladungen mit H⁺/OH⁻ ausgleichen, Atombilanz mit H₂O, multiplizieren und addieren.
Oxidationsmittel werden selbst reduziert (Oxidationszahl sinkt), Reduktionsmittel werden selbst oxidiert (Oxidationszahl steigt).
Eselsbrücke: "OIL RIG" - Oxidation Is Loss, Reduction Is Gain (of electrons)!
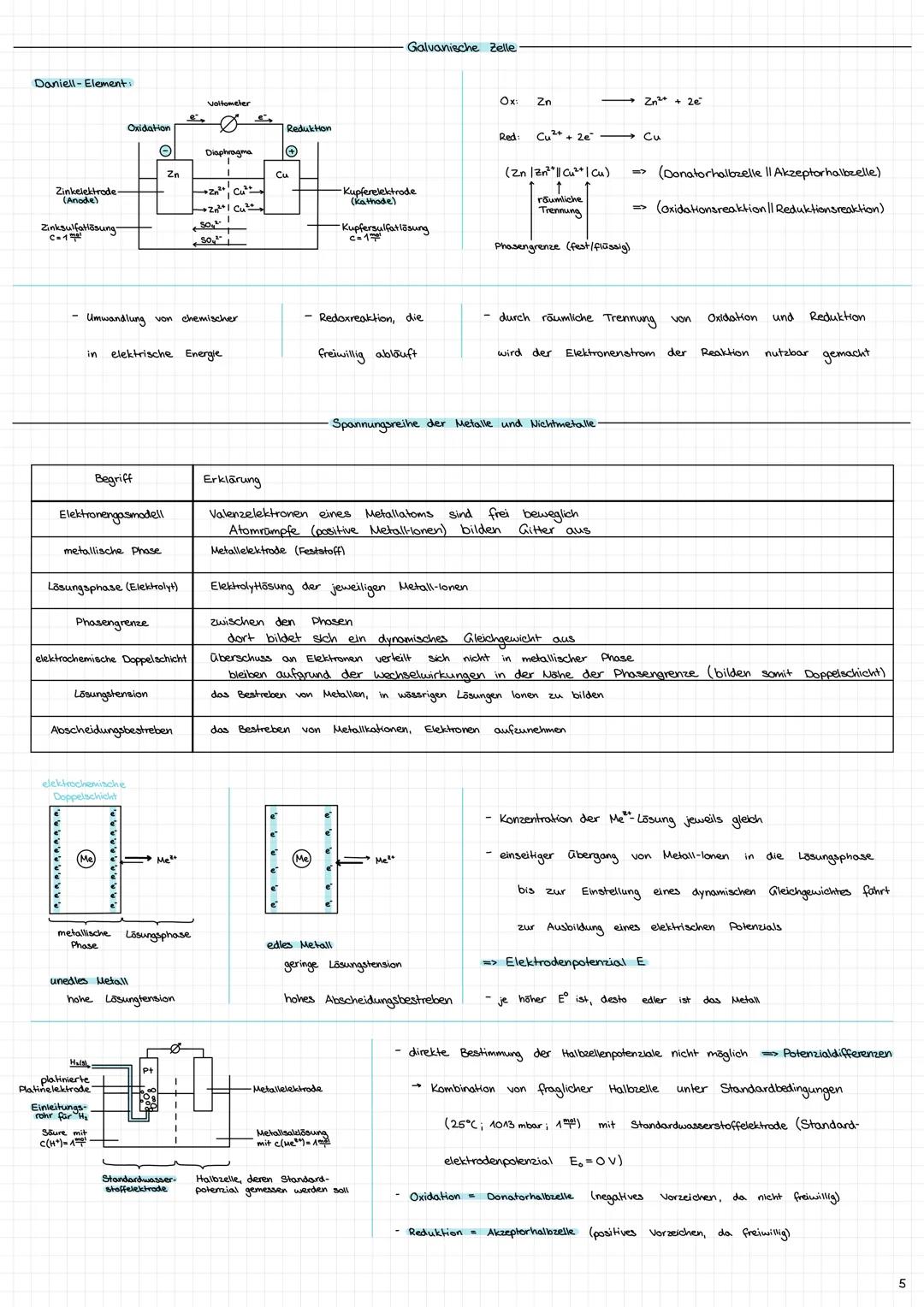
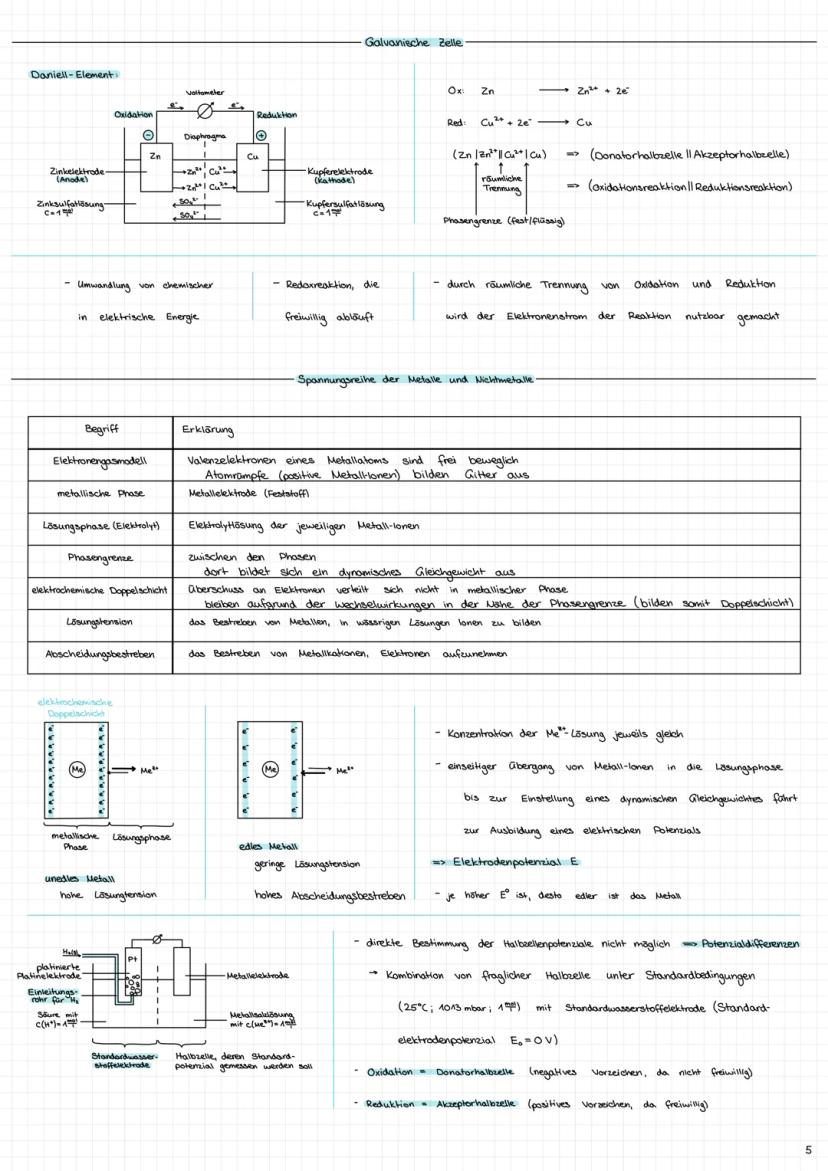
Das Daniell-Element zeigt dir das Prinzip: Räumliche Trennung von Oxidation und Reduktion macht den Elektronenstrom nutzbar! Anode (Oxidation) und Kathode (Reduktion) sind durch einen äußeren Stromkreis verbunden.
Die Spannungsreihe ordnet Metalle nach ihrer Lösungstension - dem Bestreben, Ionen zu bilden. Unedle Metalle wollen Elektronen abgeben, edle Metalle nehmen sie gern auf.
Elektrodenpotentiale entstehen durch die elektrochemische Doppelschicht an der Phasengrenze. Das Standardelektrodenpotential wird gegen die Wasserstoffelektrode gemessen.
Zellspannung berechnen: U = E(Kathode) - E(Anode). Die Halbzelle mit dem höheren E⁰-Wert wird zur Kathode!
Merkregel: "Edle Metalle sind faule Metalle" - sie geben ungern Elektronen ab!

Die Nernst-Gleichung zeigt dir, wie sich Konzentrationen auf das Elektrodenpotential auswirken: E = E⁰ + × lg. Höhere Ionenkonzentration macht eine Elektrode "edler"!
Praktische Anwendung: Mit E = E⁰ - 0,059V × pH kannst du pH-abhängige Potentiale berechnen. Das gilt für H₂-Elektroden und O₂-Elektroden - super wichtig für Brennstoffzellen!
Konzentrationszellen entstehen, wenn gleiche Elektroden in verschiedene Konzentrationen eintauchen. Der Konzentrationsunterschied treibt die Reaktion an, bis sich die Konzentrationen angleichen.
Bei der Berechnung beachtest du nur Teilchen in Lösung - feste, flüssige oder gasförmige Stoffe haben die "Konzentration" 1. Oxidationsmittel stehen im Zähler, Reduktionsmittel im Nenner!
Faustregel: Pro 10-fache Konzentrationserhöhung steigt das Potential um etwa 60 mV!

Elektrolyse dreht galvanische Zellen um: Du zwingst mit äußerer Spannung nicht-freiwillige Reaktionen ab! Die Zersetzungsspannung ist die Mindestspannung, die du brauchst - sie entspricht der umgekehrten Zellspannung.
Überspannung entsteht durch praktische Probleme: andere Elektrodenmaterialien, langsamere Reaktionen, Gasblasenbildung. Deshalb brauchst du oft mehr Spannung als theoretisch berechnet.
Das Faraday-Gesetz verbindet Strom und Stoffumsatz: n = I × t / (z × F). Mit 96.485 As/mol kannst du berechnen, wie viel Stoff bei gegebenem Strom umgesetzt wird.
Brennstoffzellen sind das Gegenteil - sie wandeln kontinuierlich zugeführte Brennstoffe in Strom um. Die Wasserstoff-Sauerstoff-Brennstoffzelle spaltet die explosive Knallgasreaktion in zwei kontrollierte Teilreaktionen auf.
Merkhilfe Elektrolyse: "OPA muss überredet werden" - Oxidation, Plus, Anode!

Batterien (Primärelemente) kannst du nur einmal nutzen, Akkus (Sekundärelemente) lassen sich wieder aufladen. Der Unterschied liegt in der Reversibilität der elektrochemischen Reaktionen.
Leclanché-Batterien nutzen Zink und Mangandioxid, Alkali-Mangan-Batterien arbeiten im alkalischen Milieu. Lithium-Batterien haben die höchste Energiedichte - deshalb stecken sie in deinem Handy!
Blei-Akkus in Autos wandeln Blei und Bleioxid mit Schwefelsäure um - beide Elektroden werden zu Bleisulfat! Nickel-Metallhydrid-Akkus brauchen alkalisches Milieu und sind umweltfreundlicher.
Korrosion zerstört Metalle durch Oxidation. Sauerstoffkorrosion braucht O₂ und Wasser, Säurekorrosion läuft mit H₃O⁺-Ionen ab. Beide folgen dem Redoxprinzip!
Alltagstipp: Batterien nie mischen - verschiedene Typen haben unterschiedliche Spannungen und Eigenschaften!

Korrosionsschutz verhindert die Zerstörung von Metallen. Passiver Schutz trennt räumlich: Lackieren, Galvanisieren oder Passivieren bilden eine Schutzschicht zwischen Metall und Oxidationsmittel.
Kathodischer Schutz nutzt Opferanoden - unedlere Metalle, die sich opfern und das wertvollere Metall schützen. Zink schützt Eisen, weil es unedler ist und sich zuerst auflöst.
Feuerverzinken kombiniert beide Prinzipien: Der Zinküberzug wirkt erst passiv als Barriere. Bei Beschädigungen schützt Zink aktiv als Opferanode das freigelegte Eisen.
Lokalelemente entstehen, wenn verschiedene Metalle sich in einem Elektrolyt berühren. Das unedlere Metall wird zur Lokalanode und korrodiert verstärkt - deshalb keine unterschiedlichen Metalle verschrauben!
Praktischer Tipp: Zinkopferanoden an Schiffen müssen regelmäßig erneuert werden!
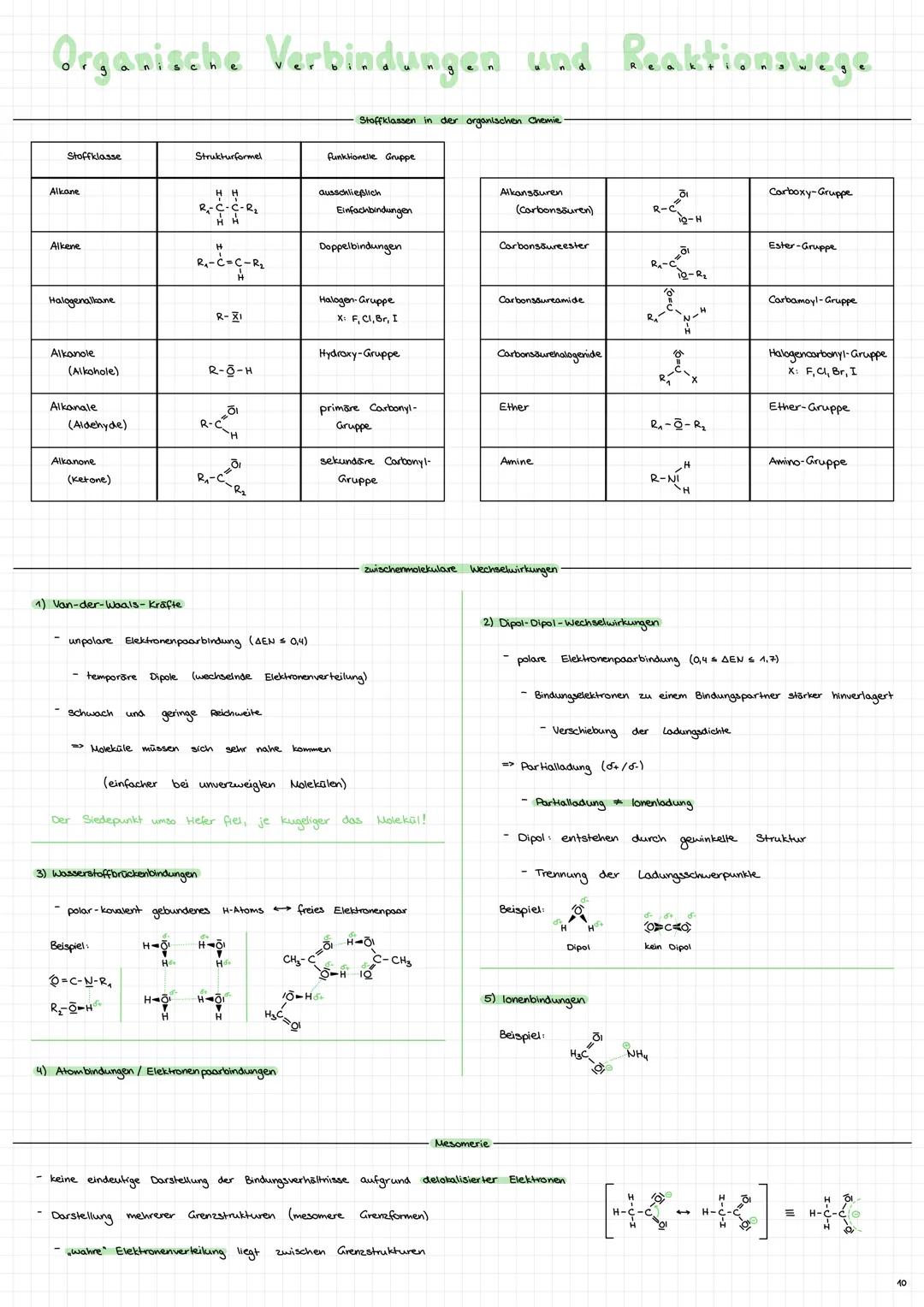
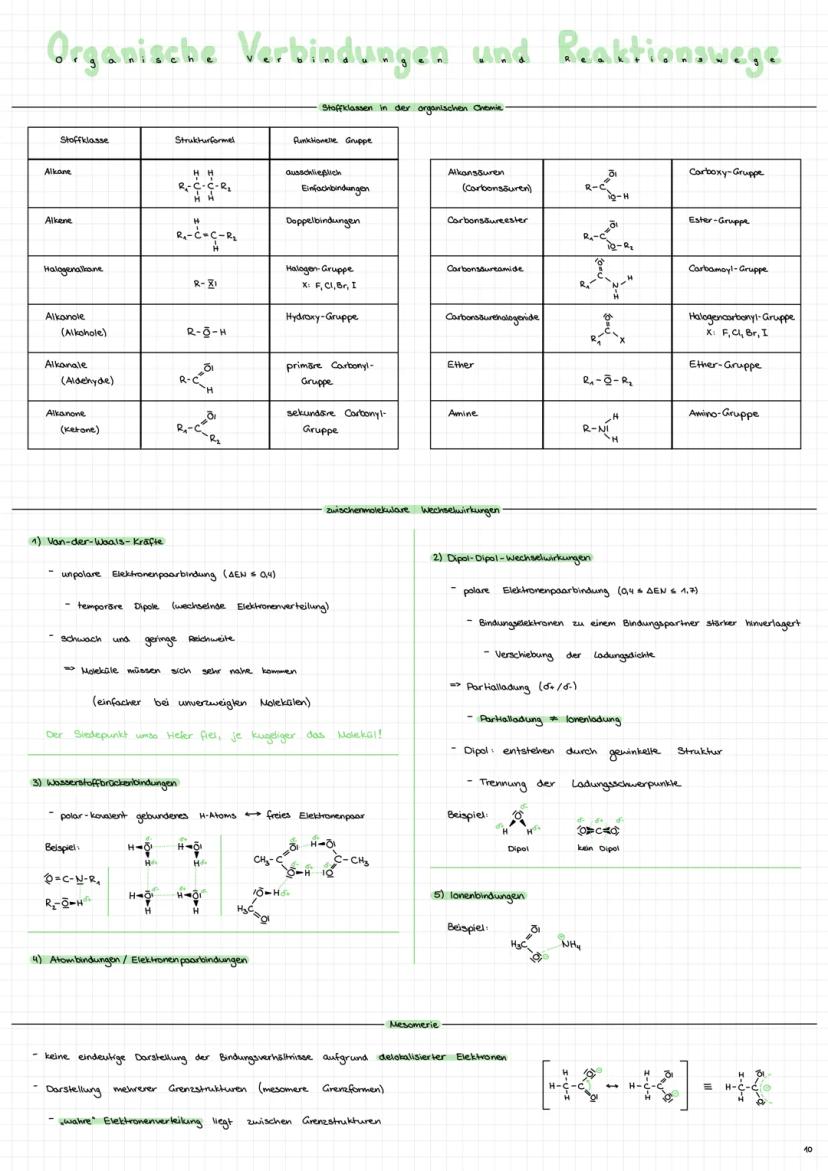
Funktionelle Gruppen bestimmen die Eigenschaften organischer Moleküle! Alkohole , Carbonsäuren , Ester , Amine - jede Gruppe hat typische Reaktionen.
Zwischenmolekulare Kräfte erklären Siede- und Schmelzpunkte: Van-der-Waals-Kräfte bei unpolaren Molekülen, Dipol-Dipol-Kräfte bei polaren, Wasserstoffbrücken bei -OH, -NH und -FH-Gruppen.
Wasserstoffbrücken sind besonders stark - deshalb hat Wasser so ungewöhnliche Eigenschaften! Ein polar gebundenes H-Atom wird von einem freien Elektronenpaar angezogen.
Mesomerie tritt auf, wenn Elektronen delokalisiert sind - die "wahre" Struktur liegt zwischen mehreren Grenzformen. Das stabilisiert Moleküle wie Benzol oder Carboxylat-Ionen.
Strukturtrick: Je mehr Wasserstoffbrücken möglich sind, desto höher der Siedepunkt!
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Michaela Kerner
@michaela.ek
Du stehst vor Säuren, Basen und Redoxreaktionen - zwei der wichtigsten Themen in der Chemie! Diese Konzepte begegnen dir überall: vom pH-Wert deines Shampoos bis zur Batterie in deinem Handy.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Starke vs. schwache Säuren - das ist der Schlüssel zum Verständnis! Starke Säuren (pKs < 3,75) geben ihre Protonen komplett ab, während schwache Säuren (pKs > 3,75) nur teilweise dissoziieren.
Der pH-Wert zeigt dir, wie sauer eine Lösung ist: pH = -lg(c(H₃O⁺)). Bei starken Säuren rechnest du einfach mit der Konzentration, bei schwachen brauchst du die Wurzelformel: pH = ½.
Brønsted-Säure-Base-Theory macht alles verständlich: Säuren sind Protonendonatoren, Basen sind Protonenakzeptoren. Ampholyte wie Wasser können beides - je nach Reaktionspartner!
Merktrick: pH + pOH = 14 - das gilt immer bei 25°C!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Titration ist deine Methode, um unbekannte Konzentrationen herauszufinden. Du gibst tropfenweise eine Maßlösung (bekannte Konzentration) zu deiner Probelösung bis zum Äquivalenzpunkt.
Bei der pH-metrischen Titration siehst du verschiedene Kurvenverläufe: Starke Säuren gegen starke Basen ergeben einen Äquivalenzpunkt bei pH = 7. Schwache Säuren gegen starke Basen landen im basischen Bereich (pH > 7).
Der Halbäquivalenzpunkt ist besonders clever - hier gilt pH = pKs! Das nutzt du zur Bestimmung der Säurekonstante.
Indikatorauswahl ist entscheidend: Der Umschlagsbereich muss den Äquivalenzpunkt umfassen. Phenolphthalein (8,7-10,7) für schwache Säuren, Methylorange (3,1-4,4) für schwache Basen.
Rechentrick: c(Probelösung) = c(Maßlösung) × V(Maßlösung) / V(Probelösung)

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Leitfähigkeitstitration nutzt die Tatsache, dass Ionen elektrischen Strom leiten. Die molare Grenzleitfähigkeit zeigt dir, wie beweglich verschiedene Ionen sind: H₃O⁺ (349,8) ist champion, OH⁻ (198,6) auf Platz zwei!
Bei starken Säuren gegen starke Basen siehst du erst einen Abfall (H₃O⁺ wird durch Na⁺ ersetzt), dann einen steilen Anstieg . Bei schwachen Säuren startest du mit niedriger Leitfähigkeit und steigst dann stark an.
Vorteile der Leitfähigkeitstitration: Du kannst trübe oder gefärbte Proben messen und starke von schwachen Säuren unterscheiden. Der Aufwand ist allerdings höher als bei einfachen Endpunkttitrationen.
Praktischer Tipp: Äquivalenzpunkt = Schnittpunkt der beiden Geraden im Leitfähigkeits-Diagramm!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Redoxreaktionen sind überall: Rost, Batterien, Atmung! Das Donator-Akzeptor-Prinzip erklärt alles: Oxidation bedeutet Elektronenabgabe, Reduktion bedeutet Elektronenaufnahme - und beides läuft immer gleichzeitig ab.
Oxidationszahlen bestimmen ist dein Werkzeug: Einzelne Atome haben immer 0, Metallionen sind positiv, in Molekülen ergibt die Summe null. Wasserstoff meist +I, Sauerstoff meist -II, Fluor immer -I.
Redoxgleichungen aufstellen: Erst Oxidationszahlen bestimmen, dann Teilgleichungen für Oxidation und Reduktion aufstellen, Ladungen mit H⁺/OH⁻ ausgleichen, Atombilanz mit H₂O, multiplizieren und addieren.
Oxidationsmittel werden selbst reduziert (Oxidationszahl sinkt), Reduktionsmittel werden selbst oxidiert (Oxidationszahl steigt).
Eselsbrücke: "OIL RIG" - Oxidation Is Loss, Reduction Is Gain (of electrons)!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Das Daniell-Element zeigt dir das Prinzip: Räumliche Trennung von Oxidation und Reduktion macht den Elektronenstrom nutzbar! Anode (Oxidation) und Kathode (Reduktion) sind durch einen äußeren Stromkreis verbunden.
Die Spannungsreihe ordnet Metalle nach ihrer Lösungstension - dem Bestreben, Ionen zu bilden. Unedle Metalle wollen Elektronen abgeben, edle Metalle nehmen sie gern auf.
Elektrodenpotentiale entstehen durch die elektrochemische Doppelschicht an der Phasengrenze. Das Standardelektrodenpotential wird gegen die Wasserstoffelektrode gemessen.
Zellspannung berechnen: U = E(Kathode) - E(Anode). Die Halbzelle mit dem höheren E⁰-Wert wird zur Kathode!
Merkregel: "Edle Metalle sind faule Metalle" - sie geben ungern Elektronen ab!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Nernst-Gleichung zeigt dir, wie sich Konzentrationen auf das Elektrodenpotential auswirken: E = E⁰ + × lg. Höhere Ionenkonzentration macht eine Elektrode "edler"!
Praktische Anwendung: Mit E = E⁰ - 0,059V × pH kannst du pH-abhängige Potentiale berechnen. Das gilt für H₂-Elektroden und O₂-Elektroden - super wichtig für Brennstoffzellen!
Konzentrationszellen entstehen, wenn gleiche Elektroden in verschiedene Konzentrationen eintauchen. Der Konzentrationsunterschied treibt die Reaktion an, bis sich die Konzentrationen angleichen.
Bei der Berechnung beachtest du nur Teilchen in Lösung - feste, flüssige oder gasförmige Stoffe haben die "Konzentration" 1. Oxidationsmittel stehen im Zähler, Reduktionsmittel im Nenner!
Faustregel: Pro 10-fache Konzentrationserhöhung steigt das Potential um etwa 60 mV!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Elektrolyse dreht galvanische Zellen um: Du zwingst mit äußerer Spannung nicht-freiwillige Reaktionen ab! Die Zersetzungsspannung ist die Mindestspannung, die du brauchst - sie entspricht der umgekehrten Zellspannung.
Überspannung entsteht durch praktische Probleme: andere Elektrodenmaterialien, langsamere Reaktionen, Gasblasenbildung. Deshalb brauchst du oft mehr Spannung als theoretisch berechnet.
Das Faraday-Gesetz verbindet Strom und Stoffumsatz: n = I × t / (z × F). Mit 96.485 As/mol kannst du berechnen, wie viel Stoff bei gegebenem Strom umgesetzt wird.
Brennstoffzellen sind das Gegenteil - sie wandeln kontinuierlich zugeführte Brennstoffe in Strom um. Die Wasserstoff-Sauerstoff-Brennstoffzelle spaltet die explosive Knallgasreaktion in zwei kontrollierte Teilreaktionen auf.
Merkhilfe Elektrolyse: "OPA muss überredet werden" - Oxidation, Plus, Anode!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Batterien (Primärelemente) kannst du nur einmal nutzen, Akkus (Sekundärelemente) lassen sich wieder aufladen. Der Unterschied liegt in der Reversibilität der elektrochemischen Reaktionen.
Leclanché-Batterien nutzen Zink und Mangandioxid, Alkali-Mangan-Batterien arbeiten im alkalischen Milieu. Lithium-Batterien haben die höchste Energiedichte - deshalb stecken sie in deinem Handy!
Blei-Akkus in Autos wandeln Blei und Bleioxid mit Schwefelsäure um - beide Elektroden werden zu Bleisulfat! Nickel-Metallhydrid-Akkus brauchen alkalisches Milieu und sind umweltfreundlicher.
Korrosion zerstört Metalle durch Oxidation. Sauerstoffkorrosion braucht O₂ und Wasser, Säurekorrosion läuft mit H₃O⁺-Ionen ab. Beide folgen dem Redoxprinzip!
Alltagstipp: Batterien nie mischen - verschiedene Typen haben unterschiedliche Spannungen und Eigenschaften!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Korrosionsschutz verhindert die Zerstörung von Metallen. Passiver Schutz trennt räumlich: Lackieren, Galvanisieren oder Passivieren bilden eine Schutzschicht zwischen Metall und Oxidationsmittel.
Kathodischer Schutz nutzt Opferanoden - unedlere Metalle, die sich opfern und das wertvollere Metall schützen. Zink schützt Eisen, weil es unedler ist und sich zuerst auflöst.
Feuerverzinken kombiniert beide Prinzipien: Der Zinküberzug wirkt erst passiv als Barriere. Bei Beschädigungen schützt Zink aktiv als Opferanode das freigelegte Eisen.
Lokalelemente entstehen, wenn verschiedene Metalle sich in einem Elektrolyt berühren. Das unedlere Metall wird zur Lokalanode und korrodiert verstärkt - deshalb keine unterschiedlichen Metalle verschrauben!
Praktischer Tipp: Zinkopferanoden an Schiffen müssen regelmäßig erneuert werden!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Funktionelle Gruppen bestimmen die Eigenschaften organischer Moleküle! Alkohole , Carbonsäuren , Ester , Amine - jede Gruppe hat typische Reaktionen.
Zwischenmolekulare Kräfte erklären Siede- und Schmelzpunkte: Van-der-Waals-Kräfte bei unpolaren Molekülen, Dipol-Dipol-Kräfte bei polaren, Wasserstoffbrücken bei -OH, -NH und -FH-Gruppen.
Wasserstoffbrücken sind besonders stark - deshalb hat Wasser so ungewöhnliche Eigenschaften! Ein polar gebundenes H-Atom wird von einem freien Elektronenpaar angezogen.
Mesomerie tritt auf, wenn Elektronen delokalisiert sind - die "wahre" Struktur liegt zwischen mehreren Grenzformen. Das stabilisiert Moleküle wie Benzol oder Carboxylat-Ionen.
Strukturtrick: Je mehr Wasserstoffbrücken möglich sind, desto höher der Siedepunkt!
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
58
Smart Tools NEU
Verwandle diesen Lernzettel in: ✓ 50+ Übungsfragen ✓ Interaktive Karteikarten ✓ Komplette Probeklausur ✓ Aufsatzgliederungen
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer