Bindungsarten sind das Fundament der Chemie - sie erklären, warum... Mehr anzeigen
Chemie Lernzettel: Überblick der Bindungsarten



Ionenbindung - Wenn Atome Elektronen tauschen
Stell dir vor, ein Atom ist so großzügig, dass es seine Elektronen verschenkt, während ein anderes gierig welche sammelt. Genau das passiert bei der Ionenbindung zwischen Metallen und Nichtmetallen!
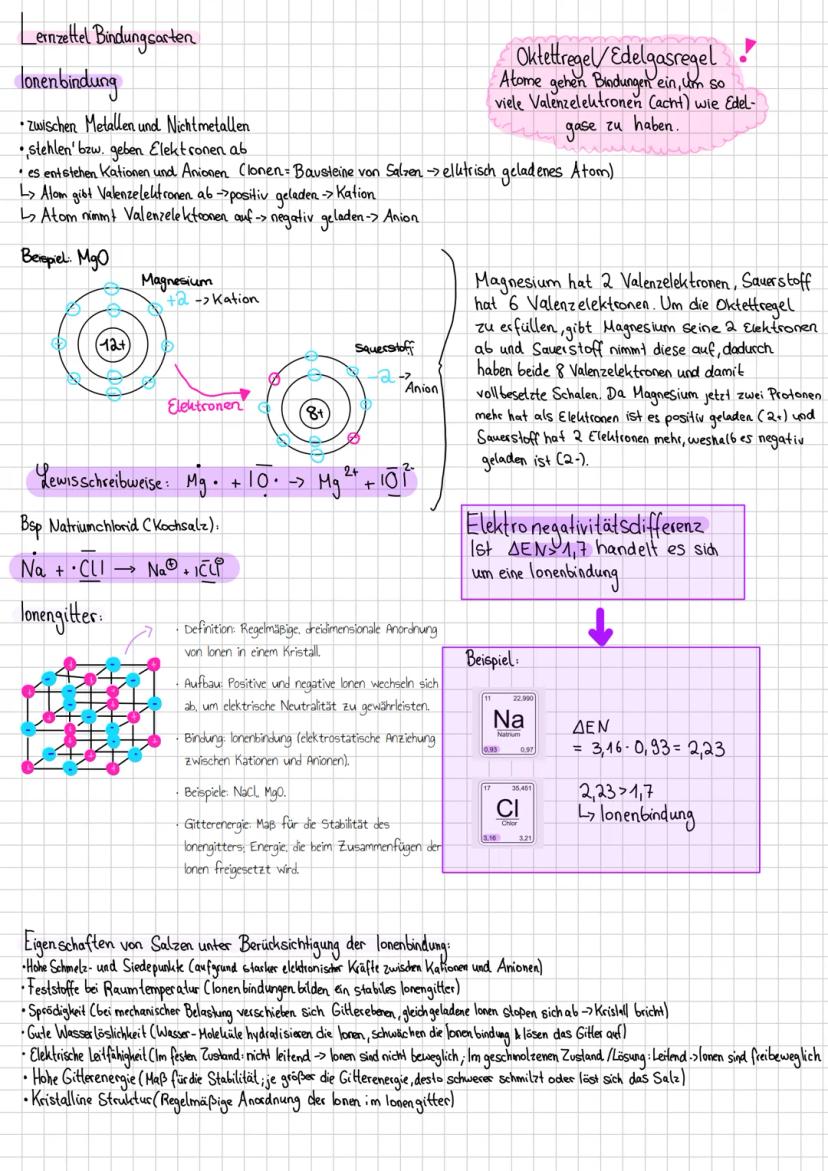
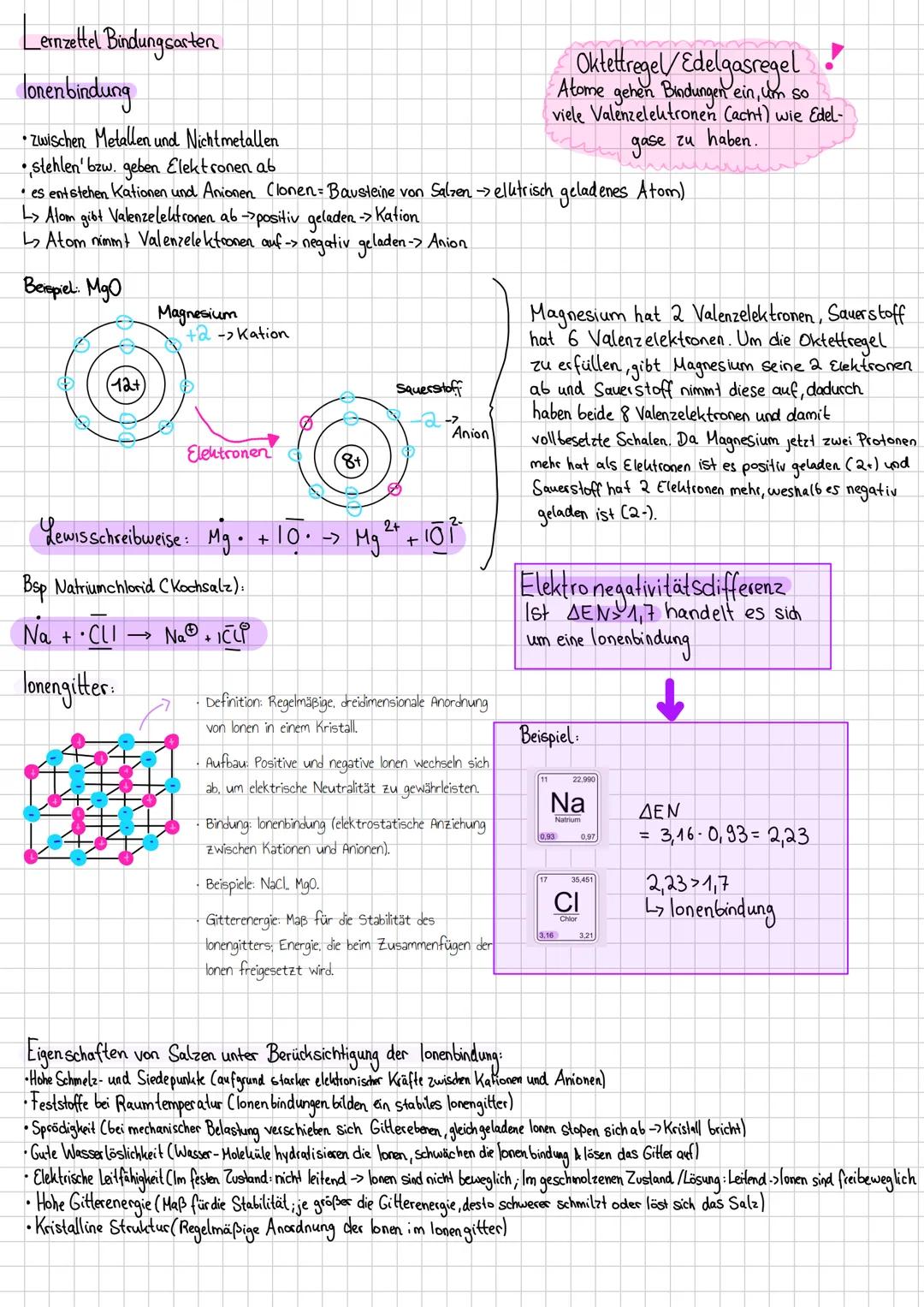
Das Ganze funktioniert nach der Oktettregel: Alle Atome wollen acht Valenzelektronen haben, wie die coolen Edelgase. Metalle wie Magnesium geben ihre Elektronen ab und werden zu positiv geladenen Kationen (Mg²⁺). Nichtmetalle wie Sauerstoff nehmen diese auf und werden zu negativ geladenen Anionen (O²⁻).
Die entstandenen Ionen ordnen sich in einem Ionengitter an - einer perfekt organisierten 3D-Struktur, wo sich positive und negative Ladungen abwechseln. Diese Anordnung ist extrem stabil und erklärt, warum Salze so hart sind und hohe Schmelzpunkte haben.
Merkhilfe: Ist die Elektronegativitätsdifferenz ΔEN ≥ 1,7, liegt eine Ionenbindung vor. Bei NaCl: ΔEN = 3,16 - 0,93 = 2,23 → eindeutig ionisch!
Typische Eigenschaften von Salzen: Hohe Schmelzpunkte, spröde, wasserlöslich, leiten Strom nur geschmolzen oder gelöst (dann können sich die Ionen frei bewegen).
Metallbindung - Das Elektronengas hält alles zusammen
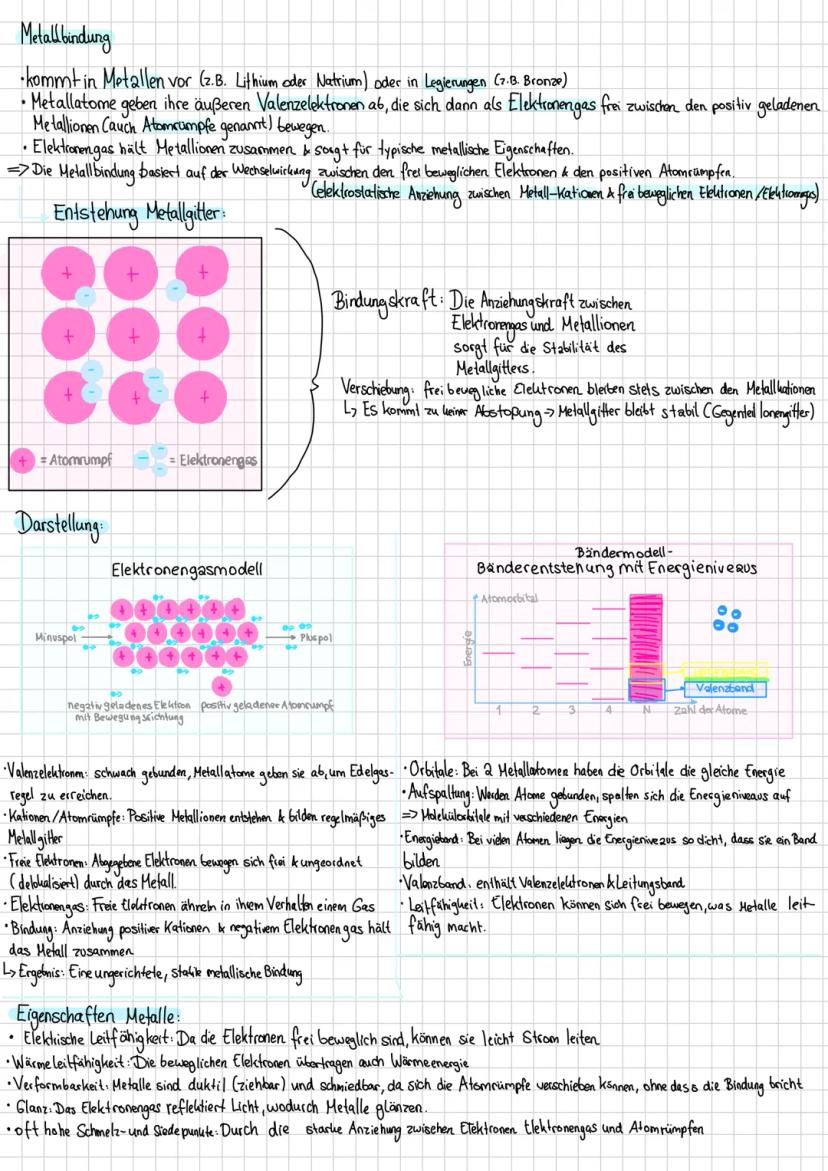
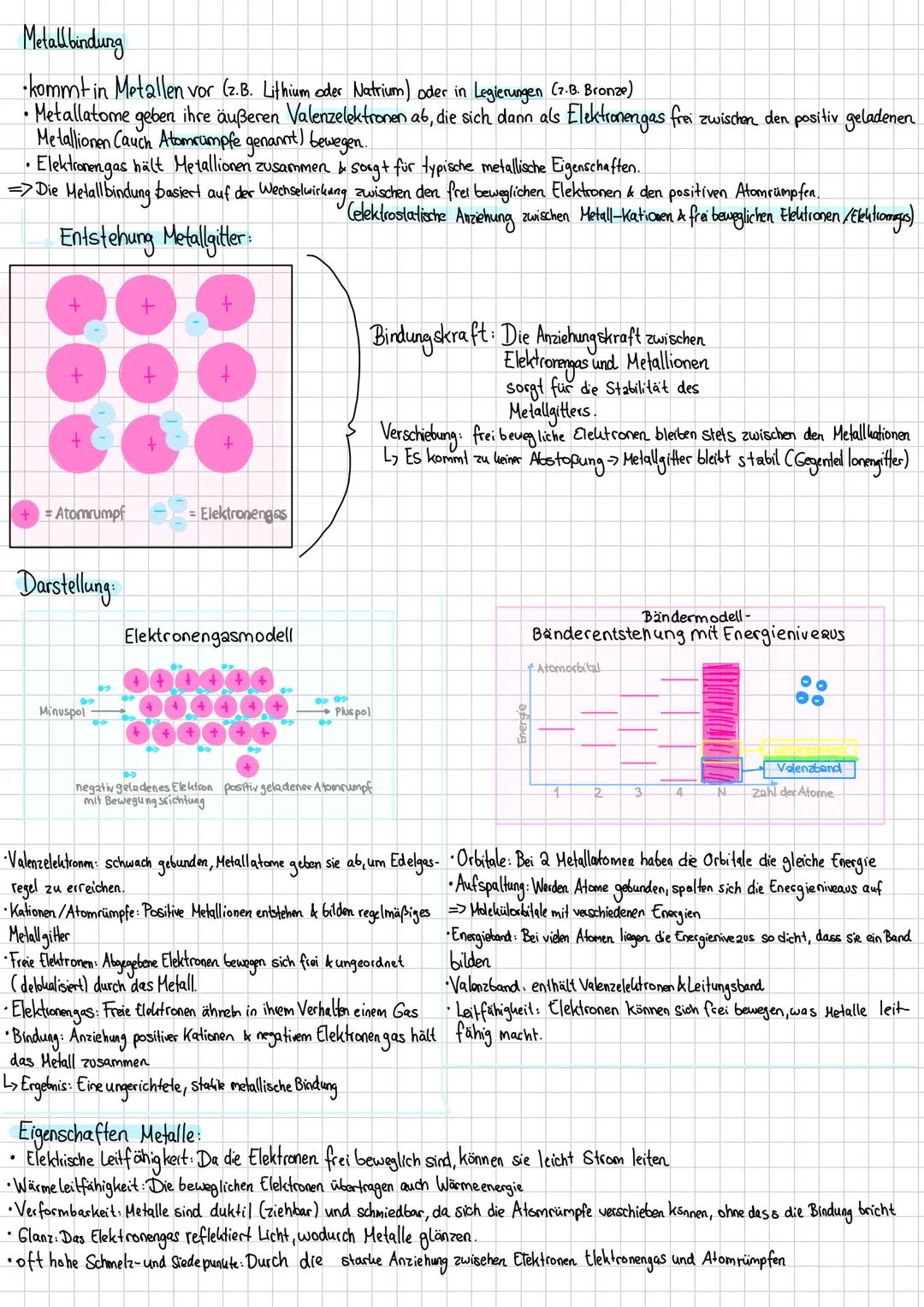
Metalle sind die Teamplayer unter den Elementen! Alle Metallatome werfen ihre Valenzelektronen in einen gemeinsamen Topf und bilden ein Elektronengas, das frei zwischen den positiv geladenen Atomrümpfen umherschwirrt.
Dieses Elektronengasmodell erklärt perfekt, warum Metalle so besondere Eigenschaften haben. Die frei beweglichen Elektronen können leicht Strom und Wärme leiten - deshalb sind Kupferkabel so effektiv und Metallpfannen heizen schnell auf.
Das Beste: Wenn du ein Metall verformst, verschieben sich zwar die Atomrümpfe, aber das Elektronengas passt sich flexibel an. Die Bindung bricht nicht! Deshalb kannst du Gold zu hauchdünnen Folien schlagen oder Kupfer zu Drähten ziehen.
Fun Fact: Der metallische Glanz entsteht, weil das Elektronengas Licht reflektiert - Metalle sind quasi natürliche Spiegel!
Die Metallbindung ist ungerichtet und stark, was zu den typisch hohen Schmelzpunkten führt. Je mehr Valenzelektronen, desto stärker die Bindung - deshalb schmilzt Aluminium (3 Valenzelektronen) erst bei 660°C.

Atombindung - Teilen macht stark
Bei der Atombindung (auch kovalente Bindung) sind Nichtmetallatome echte Teamplayer: Sie teilen ihre Valenzelektronen miteinander, statt sie zu klauen oder zu verschenken. So entstehen Moleküle wie H₂O oder CO₂.
Es gibt zwei Varianten: Unpolare Atombindungen entstehen zwischen gleichen Atomen . Hier werden die Elektronen fair geteilt, weil beide gleich stark ziehen (ΔEN ≤ 0,5). Bei polaren Atombindungen wie H-Cl zieht ein Partner stärker - das elektronegativere Atom wird leicht negativ (δ⁻), das andere leicht positiv (δ⁺).
Die Keilschreibweise hilft dir, die 3D-Struktur von Molekülen zu verstehen. Normale Striche liegen in der Papierebene, dicke Keile kommen nach vorne, gestrichelte Linien gehen nach hinten. Bei Methan (CH₄) erkennst du so die tetraedrische Anordnung.
Praxis-Tipp: Die Lewis-Schreibweise zeigt dir schnell, wie viele Elektronenpaare geteilt werden. H₂O: Sauerstoff teilt je ein Elektronenpaar mit zwei Wasserstoffatomen.
Diese räumliche Anordnung ist entscheidend für Eigenschaften und Reaktionen - besonders wichtig in der Biochemie!

Dipole und zwischenmolekulare Kräfte
Ein Dipol ist wie ein winziger Magnet mit Plus- und Minuspol. Entstehen tut er, wenn polare Bindungen in unsymmetrischen Molekülen die Elektronen ungleichmäßig verteilen - eine Seite wird δ⁻, die andere δ⁺.
Der Trick liegt in der Geometrie: CO₂ hat zwar polare C=O-Bindungen, aber durch die lineare, symmetrische Form heben sich die Ladungen auf - kein Dipol. Wasser dagegen ist gewinkelt gebaut, deshalb bleibt es polar und wird zum Dipol.
Hier wird's wichtig: Chemische Bindungen halten die Atome innerhalb von Molekülen zusammen - sie sind stark! Zwischenmolekulare Kräfte dagegen wirken zwischen verschiedenen Molekülen und sind deutlich schwächer.
Eselsbrücke: Chemische Bindungen = Binnen-Bindungen (innerhalb), zwischenmolekulare Kräfte = Zwischen-Bindungen (zwischen Molekülen).
Diese zwischenmolekularen Kräfte bestimmen physikalische Eigenschaften wie Siedepunkt oder Löslichkeit. Wasser hat wegen seiner starken Wasserstoffbrücken einen hohen Siedepunkt von 100°C, während Methan mit schwachen Van-der-Waals-Kräften schon bei -162°C siedet.

Zwischenmolekulare Kräfte im Detail
Dipol-Dipol-Kräfte entstehen zwischen polaren Molekülen, die sich wie winzige Magnete anziehen. Der positive Pol eines Moleküls zieht den negativen Pol des Nachbarn an - so halten Methanol-Moleküle zusammen.
Wasserstoffbrückenbindungen sind die Superstars unter den zwischenmolekularen Kräften! Sie entstehen nur, wenn Wasserstoff an sehr elektronegative Atome wie O, N oder F gebunden ist. Das H-Atom wird dann von den freien Elektronenpaaren benachbarter Moleküle angezogen.
Deshalb hat Wasser so ungewöhnliche Eigenschaften: Hoher Siedepunkt, Oberflächenspannung, und es löst polare Stoffe super. Ohne Wasserstoffbrücken gäbe es kein Leben - sie halten sogar die DNA-Stränge zusammen!
Van-der-Waals-Kräfte wirken auch zwischen unpolaren Molekülen. Durch die ständige Elektronenbewegung entstehen kurzzeitige "momentane Dipole", die in Nachbarmolekülen "induzierte Dipole" auslösen. Diese schwachen Anziehungen erklären, warum sogar Edelgase bei sehr tiefen Temperaturen flüssig werden.
Stärke-Ranking: Wasserstoffbrücken > Dipol-Dipol-Kräfte > Van-der-Waals-Kräfte. Je stärker die Kräfte, desto höher Schmelz- und Siedepunkt!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: London-Dispersionskräfte (LDK)
1Beliebtester Inhalt in Chemie
9Beliebtester Inhalt
9Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Chemie Lernzettel: Überblick der Bindungsarten
Bindungsarten sind das Fundament der Chemie - sie erklären, warum Atome zusammenhalten und wie Moleküle entstehen. In dieser Übersicht lernst du die drei wichtigsten Bindungstypen kennen: Ionenbindung, Metallbindung und Atombindung, plus die schwächeren Kräfte zwischen Molekülen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Ionenbindung - Wenn Atome Elektronen tauschen
Stell dir vor, ein Atom ist so großzügig, dass es seine Elektronen verschenkt, während ein anderes gierig welche sammelt. Genau das passiert bei der Ionenbindung zwischen Metallen und Nichtmetallen!
Das Ganze funktioniert nach der Oktettregel: Alle Atome wollen acht Valenzelektronen haben, wie die coolen Edelgase. Metalle wie Magnesium geben ihre Elektronen ab und werden zu positiv geladenen Kationen (Mg²⁺). Nichtmetalle wie Sauerstoff nehmen diese auf und werden zu negativ geladenen Anionen (O²⁻).
Die entstandenen Ionen ordnen sich in einem Ionengitter an - einer perfekt organisierten 3D-Struktur, wo sich positive und negative Ladungen abwechseln. Diese Anordnung ist extrem stabil und erklärt, warum Salze so hart sind und hohe Schmelzpunkte haben.
Merkhilfe: Ist die Elektronegativitätsdifferenz ΔEN ≥ 1,7, liegt eine Ionenbindung vor. Bei NaCl: ΔEN = 3,16 - 0,93 = 2,23 → eindeutig ionisch!
Typische Eigenschaften von Salzen: Hohe Schmelzpunkte, spröde, wasserlöslich, leiten Strom nur geschmolzen oder gelöst (dann können sich die Ionen frei bewegen).

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Metallbindung - Das Elektronengas hält alles zusammen
Metalle sind die Teamplayer unter den Elementen! Alle Metallatome werfen ihre Valenzelektronen in einen gemeinsamen Topf und bilden ein Elektronengas, das frei zwischen den positiv geladenen Atomrümpfen umherschwirrt.
Dieses Elektronengasmodell erklärt perfekt, warum Metalle so besondere Eigenschaften haben. Die frei beweglichen Elektronen können leicht Strom und Wärme leiten - deshalb sind Kupferkabel so effektiv und Metallpfannen heizen schnell auf.
Das Beste: Wenn du ein Metall verformst, verschieben sich zwar die Atomrümpfe, aber das Elektronengas passt sich flexibel an. Die Bindung bricht nicht! Deshalb kannst du Gold zu hauchdünnen Folien schlagen oder Kupfer zu Drähten ziehen.
Fun Fact: Der metallische Glanz entsteht, weil das Elektronengas Licht reflektiert - Metalle sind quasi natürliche Spiegel!
Die Metallbindung ist ungerichtet und stark, was zu den typisch hohen Schmelzpunkten führt. Je mehr Valenzelektronen, desto stärker die Bindung - deshalb schmilzt Aluminium (3 Valenzelektronen) erst bei 660°C.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Atombindung - Teilen macht stark
Bei der Atombindung (auch kovalente Bindung) sind Nichtmetallatome echte Teamplayer: Sie teilen ihre Valenzelektronen miteinander, statt sie zu klauen oder zu verschenken. So entstehen Moleküle wie H₂O oder CO₂.
Es gibt zwei Varianten: Unpolare Atombindungen entstehen zwischen gleichen Atomen . Hier werden die Elektronen fair geteilt, weil beide gleich stark ziehen (ΔEN ≤ 0,5). Bei polaren Atombindungen wie H-Cl zieht ein Partner stärker - das elektronegativere Atom wird leicht negativ (δ⁻), das andere leicht positiv (δ⁺).
Die Keilschreibweise hilft dir, die 3D-Struktur von Molekülen zu verstehen. Normale Striche liegen in der Papierebene, dicke Keile kommen nach vorne, gestrichelte Linien gehen nach hinten. Bei Methan (CH₄) erkennst du so die tetraedrische Anordnung.
Praxis-Tipp: Die Lewis-Schreibweise zeigt dir schnell, wie viele Elektronenpaare geteilt werden. H₂O: Sauerstoff teilt je ein Elektronenpaar mit zwei Wasserstoffatomen.
Diese räumliche Anordnung ist entscheidend für Eigenschaften und Reaktionen - besonders wichtig in der Biochemie!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Dipole und zwischenmolekulare Kräfte
Ein Dipol ist wie ein winziger Magnet mit Plus- und Minuspol. Entstehen tut er, wenn polare Bindungen in unsymmetrischen Molekülen die Elektronen ungleichmäßig verteilen - eine Seite wird δ⁻, die andere δ⁺.
Der Trick liegt in der Geometrie: CO₂ hat zwar polare C=O-Bindungen, aber durch die lineare, symmetrische Form heben sich die Ladungen auf - kein Dipol. Wasser dagegen ist gewinkelt gebaut, deshalb bleibt es polar und wird zum Dipol.
Hier wird's wichtig: Chemische Bindungen halten die Atome innerhalb von Molekülen zusammen - sie sind stark! Zwischenmolekulare Kräfte dagegen wirken zwischen verschiedenen Molekülen und sind deutlich schwächer.
Eselsbrücke: Chemische Bindungen = Binnen-Bindungen (innerhalb), zwischenmolekulare Kräfte = Zwischen-Bindungen (zwischen Molekülen).
Diese zwischenmolekularen Kräfte bestimmen physikalische Eigenschaften wie Siedepunkt oder Löslichkeit. Wasser hat wegen seiner starken Wasserstoffbrücken einen hohen Siedepunkt von 100°C, während Methan mit schwachen Van-der-Waals-Kräften schon bei -162°C siedet.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Zwischenmolekulare Kräfte im Detail
Dipol-Dipol-Kräfte entstehen zwischen polaren Molekülen, die sich wie winzige Magnete anziehen. Der positive Pol eines Moleküls zieht den negativen Pol des Nachbarn an - so halten Methanol-Moleküle zusammen.
Wasserstoffbrückenbindungen sind die Superstars unter den zwischenmolekularen Kräften! Sie entstehen nur, wenn Wasserstoff an sehr elektronegative Atome wie O, N oder F gebunden ist. Das H-Atom wird dann von den freien Elektronenpaaren benachbarter Moleküle angezogen.
Deshalb hat Wasser so ungewöhnliche Eigenschaften: Hoher Siedepunkt, Oberflächenspannung, und es löst polare Stoffe super. Ohne Wasserstoffbrücken gäbe es kein Leben - sie halten sogar die DNA-Stränge zusammen!
Van-der-Waals-Kräfte wirken auch zwischen unpolaren Molekülen. Durch die ständige Elektronenbewegung entstehen kurzzeitige "momentane Dipole", die in Nachbarmolekülen "induzierte Dipole" auslösen. Diese schwachen Anziehungen erklären, warum sogar Edelgase bei sehr tiefen Temperaturen flüssig werden.
Stärke-Ranking: Wasserstoffbrücken > Dipol-Dipol-Kräfte > Van-der-Waals-Kräfte. Je stärker die Kräfte, desto höher Schmelz- und Siedepunkt!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: London-Dispersionskräfte (LDK)
1Beliebtester Inhalt in Chemie
9Beliebtester Inhalt
9Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.