Die organische Chemie ist das Gebiet der Chemie, das sich... Mehr anzeigen
Organische Chemie – Notizen für die 11. Klasse






Grundlagen der organischen Chemie
Stell dir vor, du müsstest alle chemischen Stoffe in zwei große Gruppen einteilen - das ist genau das, was Chemiker getan haben! Anorganische Stoffe wie Salzsäure oder Natronlauge stehen den organischen Stoffen wie Alkohol oder Methan gegenüber.
Organische Chemie ist die Chemie der Kohlenwasserstoffverbindungen, mit wenigen Ausnahmen wie Kohlendioxid oder Kohlensäure. Der Grund für diese Trennung wird schnell klar, wenn du dir die typischen Eigenschaften anschaust: Organische Stoffe sind meist brennbar, riechen charakteristisch und lösen sich schlecht in Wasser.
Das Geheimnis liegt im Kohlenstoff. Mit seinen vier Außenelektronen kann er vier Bindungen eingehen und beliebig lange, stabile Ketten bilden. Das macht ihn zum perfekten Baustein für komplexe Moleküle. Meist kommen noch Wasserstoff, Sauerstoff oder Stickstoff dazu.
Merktipp: Stoffe, die nur aus Kohlenstoff und Wasserstoff bestehen, heißen Kohlenwasserstoffe - sie sind die einfachsten organischen Verbindungen.
Chemische Bindungen verstehen
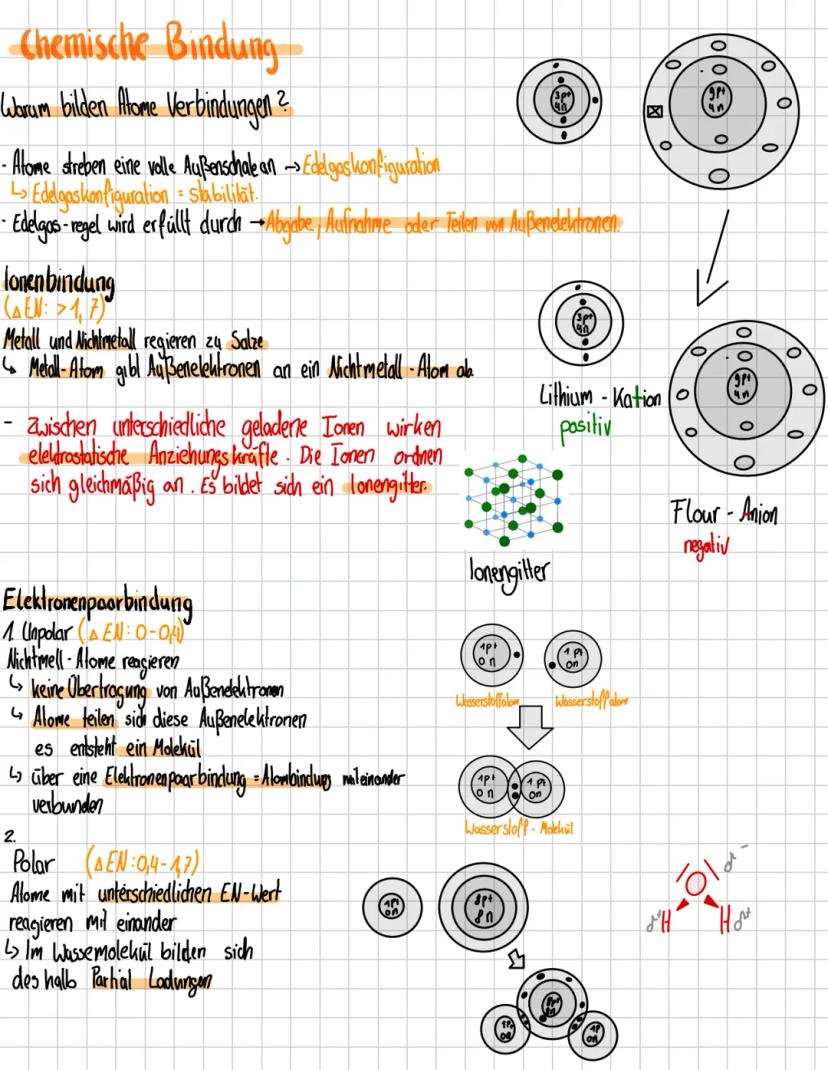
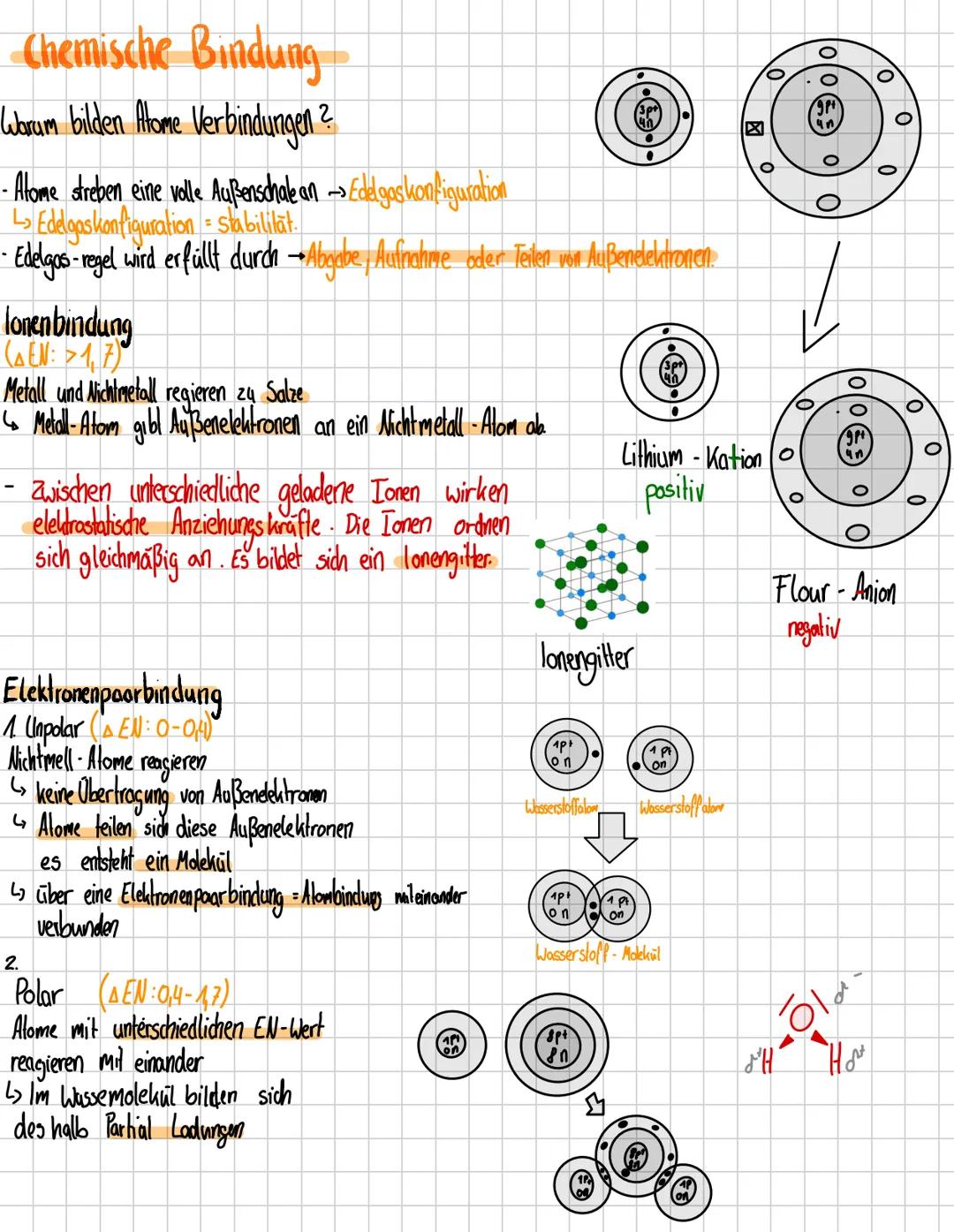
Warum halten Atome überhaupt zusammen? Ganz einfach: Sie wollen alle eine volle Außenschale haben, genau wie die Edelgase. Dafür geben sie Elektronen ab, nehmen welche auf oder teilen sie sich.
Bei der Ionenbindung (ΔEN ≥ 1,7) tauschen Metalle und Nichtmetalle Elektronen komplett aus. Das Metall wird positiv geladen, das Nichtmetall negativ - und Gegensätze ziehen sich bekanntlich an.
Die Elektronenpaarbindung funktioniert anders: Hier teilen sich Atome die Elektronen. Bei unpolaren Bindungen teilen beide Atome fair, bei polaren Bindungen zieht ein Partner stärker an den Elektronen.
Eselsbrücke: Die Elektronegativitätsdifferenz (ΔEN) verrät dir sofort, welche Bindung vorliegt - je größer der Unterschied, desto ungleicher wird geteilt.

Alkane - die Grundbausteine
Alkane sind die einfachsten organischen Verbindungen und folgen der Formel CₙH₂ₙ₊₂. Du startest mit Methan (CH₄), dann kommt Ethan (C₂H₆), Propan (C₃H₈) und so weiter - das nennt man eine homologe Reihe.
Jedes Kohlenstoffatom hat vier Bindungen, und alle Bindungen sind Einfachbindungen. Die Atome stehen immer in einem Winkel von 109,5° zueinander - das ergibt eine tetraedrische Form.
Für die Darstellung gibt es verschiedene Möglichkeiten: Die Summenformel zeigt nur, wie viele Atome da sind. Die Strukturformel zeigt alle Bindungen. Die Halbstrukturformel ist ein guter Kompromiss. Die Skelettformel zeigt nur die Kohlenstoffkette als Zickzacklinie.
Praxistipp: Lerne die ersten zehn Alkane auswendig - ihre Namen tauchen in fast jeder Chemie-Klausur auf!

Elektronegativität und zwischenmolekulare Kräfte
Die Elektronegativität ist wie ein Maß für die "Gier" eines Atoms nach Elektronen. Im Periodensystem steigt sie von links nach rechts und von unten nach oben. Mit der Elektronegativitätsdifferenz (ΔEN) erkennst du sofort, welche Bindung vorliegt.
Bei unpolaren Atombindungen ziehen beide Atome gleich stark - wie bei Chlorgas (Cl₂). Bei polaren Atombindungen entsteht eine ungleiche Ladungsverteilung - das Wassermolekül ist ein perfektes Beispiel.
Zwischen Molekülen wirken zwischenmolekulare Kräfte: Van-der-Waals-Kräfte sind die schwächsten und wirken zwischen unpolaren Molekülen. Wasserstoffbrücken sind die stärksten und entstehen zwischen polar gebundenem Wasserstoff und stark elektronegativen Atomen.
Wichtig: Diese Kräfte bestimmen, ob ein Stoff bei Raumtemperatur fest, flüssig oder gasförmig ist!

Eigenschaften und Isomerie der Alkane
Je länger die Kohlenstoffkette wird, desto höher werden Schmelz- und Siedetemperatur. Das liegt daran, dass längere Moleküle eine größere Oberfläche haben und sich daher stärker über Van-der-Waals-Kräfte anziehen.
Stell dir vor, du versuchst zwei Schnüre zu trennen: Kurze Schnüre lassen sich leicht voneinander lösen, lange hingegen haften viel stärker aneinander. Genau so ist es bei Molekülen auch.
Isomere sind besonders spannend: Das sind Moleküle mit derselben Summenformel, aber unterschiedlicher Struktur. Bei Butan (C₄H₁₀) gibt es zwei Möglichkeiten - eine gerade Kette und eine verzweigte .
Kohlenstoffatome werden nach ihrer Nachbarschaft klassifiziert: Primäre C-Atome haben einen C-Nachbarn, sekundäre haben zwei, tertiäre haben drei.
Faustregel: Je verzweigter ein Alkan ist, desto niedriger ist sein Siedepunkt - verzweigte Moleküle können sich nicht so gut aneinander anlagern.

Physikalische Eigenschaften der Alkane
Alkane sind hydrophob - sie mischen sich nicht mit Wasser. Das liegt daran, dass Wassermoleküle über starke Wasserstoffbrücken zusammenhalten, während Alkane nur schwache Van-der-Waals-Kräfte haben. Die Alkane können diese starken Wasserbindungen nicht aufbrechen.
Die Chemiker-Regel lautet: "Ähnliches löst Ähnliches." Polare Stoffe lösen sich in polaren Stoffen, unpolare in unpolaren. Deshalb löst sich Öl nicht in Wasser, aber sehr gut in Benzin.
Die Viskosität (Zähflüssigkeit) nimmt mit der Kettenlänge zu. Kurze Alkane wie Methan sind gasförmig, mittlere wie Hexan sind dünnflüssig, lange wie Vaseline sind zähflüssig. Beim Fließen müssen die Moleküle aneinander vorbeigleiten - je stärker sie sich anziehen, desto schwieriger wird das.
Van-der-Waals-Kräfte entstehen durch kurzzeitige Ladungsverschiebungen in den Molekülen. Diese "spontanen Dipole" ziehen benachbarte Moleküle an - allerdings nur schwach und nur kurz.
Alltags-Beispiel: Honig fließt langsamer als Wasser, weil seine Moleküle stärker aneinander haften - genau wie bei langen Alkanen!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Bindungspolarität
4Molekulare Polarität verstehen
Erfahren Sie alles über die Polarität von Molekülen, einschließlich der Elektronegativität, Bindungspolarität und Dipole. Diese Zusammenfassung behandelt die Unterschiede zwischen polaren und unpolaren Molekülen sowie Beispiele wie HCl und CF4. Ideal für Schüler, die sich auf Prüfungen vorbereiten oder ihr Wissen über chemische Bindungen vertiefen möchten.
Chemische Bindungen und Polarität
Entdecken Sie die verschiedenen Arten chemischer Bindungen, einschließlich Ionenbindung, Atombindung und Wasserstoffbrückenbindung. Erfahren Sie mehr über die Polarität von Molekülen, Elektronegativität und die Eigenschaften von Salzen. Diese Zusammenfassung bietet eine klare Übersicht über die Grundlagen der chemischen Bindungen und deren Bedeutung in der Chemie.
Wasserstoffbrücken und Molekülpolarität
Dieser Lernzettel behandelt die Grundlagen von Wasserstoffbrücken, Dipol-Molekülen und Atombindungen. Er erklärt die Eigenschaften von Wasser, die Oberflächenspannung, die Struktur von Eis und die Unterschiede zwischen polaren und unpolaren Bindungen. Ideal für Chemie-Studierende, die ein tieferes Verständnis der Molekülinteraktionen und deren Auswirkungen auf physikalische Eigenschaften suchen.
Elektronegativität und Bindungstypen
Dieser handschriftliche Lernzettel erklärt die Konzepte der Elektronegativität und die Polarität von chemischen Bindungen. Er behandelt die Unterschiede zwischen polaren und unpolaren Bindungen sowie die Bedeutung der Elektronegativität in der Molekülstruktur. Ideal für Chemie-Studierende, die ein besseres Verständnis für chemische Bindungen entwickeln möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Charaktere aus Heimsuchung von Jenny Erpenbeck
Mindmap, Allgemeines, Verlauf
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Organische Chemie – Notizen für die 11. Klasse
Die organische Chemie ist das Gebiet der Chemie, das sich mit Kohlenwasserstoffverbindungen beschäftigt - also den Stoffen, die hauptsächlich aus Kohlenstoff und Wasserstoff bestehen. Du kennst viele davon bereits aus dem Alltag: Alkohol, Benzin oder Methan. Diese Stoffe haben besondere... Mehr anzeigen

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Grundlagen der organischen Chemie
Stell dir vor, du müsstest alle chemischen Stoffe in zwei große Gruppen einteilen - das ist genau das, was Chemiker getan haben! Anorganische Stoffe wie Salzsäure oder Natronlauge stehen den organischen Stoffen wie Alkohol oder Methan gegenüber.
Organische Chemie ist die Chemie der Kohlenwasserstoffverbindungen, mit wenigen Ausnahmen wie Kohlendioxid oder Kohlensäure. Der Grund für diese Trennung wird schnell klar, wenn du dir die typischen Eigenschaften anschaust: Organische Stoffe sind meist brennbar, riechen charakteristisch und lösen sich schlecht in Wasser.
Das Geheimnis liegt im Kohlenstoff. Mit seinen vier Außenelektronen kann er vier Bindungen eingehen und beliebig lange, stabile Ketten bilden. Das macht ihn zum perfekten Baustein für komplexe Moleküle. Meist kommen noch Wasserstoff, Sauerstoff oder Stickstoff dazu.
Merktipp: Stoffe, die nur aus Kohlenstoff und Wasserstoff bestehen, heißen Kohlenwasserstoffe - sie sind die einfachsten organischen Verbindungen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Chemische Bindungen verstehen
Warum halten Atome überhaupt zusammen? Ganz einfach: Sie wollen alle eine volle Außenschale haben, genau wie die Edelgase. Dafür geben sie Elektronen ab, nehmen welche auf oder teilen sie sich.
Bei der Ionenbindung (ΔEN ≥ 1,7) tauschen Metalle und Nichtmetalle Elektronen komplett aus. Das Metall wird positiv geladen, das Nichtmetall negativ - und Gegensätze ziehen sich bekanntlich an.
Die Elektronenpaarbindung funktioniert anders: Hier teilen sich Atome die Elektronen. Bei unpolaren Bindungen teilen beide Atome fair, bei polaren Bindungen zieht ein Partner stärker an den Elektronen.
Eselsbrücke: Die Elektronegativitätsdifferenz (ΔEN) verrät dir sofort, welche Bindung vorliegt - je größer der Unterschied, desto ungleicher wird geteilt.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Alkane - die Grundbausteine
Alkane sind die einfachsten organischen Verbindungen und folgen der Formel CₙH₂ₙ₊₂. Du startest mit Methan (CH₄), dann kommt Ethan (C₂H₆), Propan (C₃H₈) und so weiter - das nennt man eine homologe Reihe.
Jedes Kohlenstoffatom hat vier Bindungen, und alle Bindungen sind Einfachbindungen. Die Atome stehen immer in einem Winkel von 109,5° zueinander - das ergibt eine tetraedrische Form.
Für die Darstellung gibt es verschiedene Möglichkeiten: Die Summenformel zeigt nur, wie viele Atome da sind. Die Strukturformel zeigt alle Bindungen. Die Halbstrukturformel ist ein guter Kompromiss. Die Skelettformel zeigt nur die Kohlenstoffkette als Zickzacklinie.
Praxistipp: Lerne die ersten zehn Alkane auswendig - ihre Namen tauchen in fast jeder Chemie-Klausur auf!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Elektronegativität und zwischenmolekulare Kräfte
Die Elektronegativität ist wie ein Maß für die "Gier" eines Atoms nach Elektronen. Im Periodensystem steigt sie von links nach rechts und von unten nach oben. Mit der Elektronegativitätsdifferenz (ΔEN) erkennst du sofort, welche Bindung vorliegt.
Bei unpolaren Atombindungen ziehen beide Atome gleich stark - wie bei Chlorgas (Cl₂). Bei polaren Atombindungen entsteht eine ungleiche Ladungsverteilung - das Wassermolekül ist ein perfektes Beispiel.
Zwischen Molekülen wirken zwischenmolekulare Kräfte: Van-der-Waals-Kräfte sind die schwächsten und wirken zwischen unpolaren Molekülen. Wasserstoffbrücken sind die stärksten und entstehen zwischen polar gebundenem Wasserstoff und stark elektronegativen Atomen.
Wichtig: Diese Kräfte bestimmen, ob ein Stoff bei Raumtemperatur fest, flüssig oder gasförmig ist!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Eigenschaften und Isomerie der Alkane
Je länger die Kohlenstoffkette wird, desto höher werden Schmelz- und Siedetemperatur. Das liegt daran, dass längere Moleküle eine größere Oberfläche haben und sich daher stärker über Van-der-Waals-Kräfte anziehen.
Stell dir vor, du versuchst zwei Schnüre zu trennen: Kurze Schnüre lassen sich leicht voneinander lösen, lange hingegen haften viel stärker aneinander. Genau so ist es bei Molekülen auch.
Isomere sind besonders spannend: Das sind Moleküle mit derselben Summenformel, aber unterschiedlicher Struktur. Bei Butan (C₄H₁₀) gibt es zwei Möglichkeiten - eine gerade Kette und eine verzweigte .
Kohlenstoffatome werden nach ihrer Nachbarschaft klassifiziert: Primäre C-Atome haben einen C-Nachbarn, sekundäre haben zwei, tertiäre haben drei.
Faustregel: Je verzweigter ein Alkan ist, desto niedriger ist sein Siedepunkt - verzweigte Moleküle können sich nicht so gut aneinander anlagern.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Physikalische Eigenschaften der Alkane
Alkane sind hydrophob - sie mischen sich nicht mit Wasser. Das liegt daran, dass Wassermoleküle über starke Wasserstoffbrücken zusammenhalten, während Alkane nur schwache Van-der-Waals-Kräfte haben. Die Alkane können diese starken Wasserbindungen nicht aufbrechen.
Die Chemiker-Regel lautet: "Ähnliches löst Ähnliches." Polare Stoffe lösen sich in polaren Stoffen, unpolare in unpolaren. Deshalb löst sich Öl nicht in Wasser, aber sehr gut in Benzin.
Die Viskosität (Zähflüssigkeit) nimmt mit der Kettenlänge zu. Kurze Alkane wie Methan sind gasförmig, mittlere wie Hexan sind dünnflüssig, lange wie Vaseline sind zähflüssig. Beim Fließen müssen die Moleküle aneinander vorbeigleiten - je stärker sie sich anziehen, desto schwieriger wird das.
Van-der-Waals-Kräfte entstehen durch kurzzeitige Ladungsverschiebungen in den Molekülen. Diese "spontanen Dipole" ziehen benachbarte Moleküle an - allerdings nur schwach und nur kurz.
Alltags-Beispiel: Honig fließt langsamer als Wasser, weil seine Moleküle stärker aneinander haften - genau wie bei langen Alkanen!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Bindungspolarität
4Molekulare Polarität verstehen
Erfahren Sie alles über die Polarität von Molekülen, einschließlich der Elektronegativität, Bindungspolarität und Dipole. Diese Zusammenfassung behandelt die Unterschiede zwischen polaren und unpolaren Molekülen sowie Beispiele wie HCl und CF4. Ideal für Schüler, die sich auf Prüfungen vorbereiten oder ihr Wissen über chemische Bindungen vertiefen möchten.
Chemische Bindungen und Polarität
Entdecken Sie die verschiedenen Arten chemischer Bindungen, einschließlich Ionenbindung, Atombindung und Wasserstoffbrückenbindung. Erfahren Sie mehr über die Polarität von Molekülen, Elektronegativität und die Eigenschaften von Salzen. Diese Zusammenfassung bietet eine klare Übersicht über die Grundlagen der chemischen Bindungen und deren Bedeutung in der Chemie.
Wasserstoffbrücken und Molekülpolarität
Dieser Lernzettel behandelt die Grundlagen von Wasserstoffbrücken, Dipol-Molekülen und Atombindungen. Er erklärt die Eigenschaften von Wasser, die Oberflächenspannung, die Struktur von Eis und die Unterschiede zwischen polaren und unpolaren Bindungen. Ideal für Chemie-Studierende, die ein tieferes Verständnis der Molekülinteraktionen und deren Auswirkungen auf physikalische Eigenschaften suchen.
Elektronegativität und Bindungstypen
Dieser handschriftliche Lernzettel erklärt die Konzepte der Elektronegativität und die Polarität von chemischen Bindungen. Er behandelt die Unterschiede zwischen polaren und unpolaren Bindungen sowie die Bedeutung der Elektronegativität in der Molekülstruktur. Ideal für Chemie-Studierende, die ein besseres Verständnis für chemische Bindungen entwickeln möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Charaktere aus Heimsuchung von Jenny Erpenbeck
Mindmap, Allgemeines, Verlauf
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.