Redoxreaktionen sind überall um uns herum - von der Atmung... Mehr anzeigen
Redoxreaktionen in der Chemie leicht erklärt






Grundbegriffe der Redoxreaktionen
Stell dir vor, Elektronen sind wie Geschenke, die zwischen Atomen ausgetauscht werden. Bei einer Redoxreaktion passiert genau das - es ist eine Elektronenübergangsreaktion, bei der immer zwei Prozesse gleichzeitig ablaufen.
Die Oxidation ist der Prozess, bei dem ein Stoff Elektronen abgibt (seine Oxidationszahl steigt). Die Reduktion läuft parallel ab - hier nimmt ein anderer Stoff die Elektronen auf (seine Oxidationszahl sinkt). Ohne Oxidation keine Reduktion und umgekehrt!
Oxidationsmittel sind die "Elektronenräuber" - sie sorgen dafür, dass andere Stoffe oxidiert werden, werden dabei aber selbst reduziert. Reduktionsmittel machen das Gegenteil: Sie reduzieren andere Stoffe und werden selbst oxidiert.
💡 Merkhilfe: OIL RIG - Oxidation Is Loss (of electrons), Reduction Is Gain (of electrons)
Korrespondierende Redoxpaare sind wie Tanzpartner - sie gehören zusammen und können durch Elektronenaufnahme oder -abgabe ineinander umgewandelt werden. Oxidationszahlen helfen dir dabei, den Überblick zu behalten - sie zeigen die fiktive Ladung jedes Atoms in einer Verbindung.

Besondere Redoxreaktionen und Grundformen
Manche Elemente sind echte Verwandlungskünstler und können sowohl als Oxidations- als auch als Reduktionsmittel auftreten - je nach Reaktionsbedingungen. Das nennt sich Donator-Akzeptor-Konzept: Reduktionsmittel sind Elektronendonatoren, Oxidationsmittel sind Elektronenakzeptoren.
Bei der Synproportionierung treffen sich Atome desselben Elements aus verschiedenen Oxidationsstufen in der Mitte - wie bei einem Kompromiss. Bei der Disproportionierung passiert das Gegenteil: Ein Element "spaltet sich" in höhere und niedrigere Oxidationsstufen auf.
Redoxtitration ist dein Werkzeug für quantitative Analysen. Damit bestimmst du die Stoffmenge einer unbekannten Substanz mithilfe einer bekannten Maßlösung - perfekt für Laborarbeiten!
💡 Praxis-Tipp: Lerne die wichtigsten Ionen auswendig - Sulfat (SO₄²⁻), Nitrat (NO₃⁻), Permanganat (MnO₄⁻) und Co. begegnen dir ständig!
Die Mangan-Verbindungen sind besonders interessant: Kaliumpermanganat kann je nach pH-Wert zu farblosem Mn²⁺ (sauer) oder braunem MnO₂ (neutral) reduziert werden.

Oxidationszahlen bestimmen - die 8 goldenen Regeln
Oxidationszahlen zu bestimmen ist wie ein Puzzle - mit den richtigen Regeln wird's zum Kinderspiel. Elementare Atome haben immer die Oxidationszahl 0 (wie C oder Fe). Metalle folgen ihrer Hauptgruppennummer, Ionen entsprechen ihrer Ladung.
Bei mehratomigen Verbindungen ohne Ladung muss die Summe aller Oxidationszahlen 0 ergeben. Bei mehratomigen Ionen muss die Summe der Ionenladung entsprechen. Wasserstoff hat fast immer +1 (Ausnahme: Metallhydride wie LiH), Sauerstoff fast immer -2 (Ausnahme: Peroxide wie H₂O₂).
Bei organischen Verbindungen betrachtest du jedes Kohlenstoffatom einzeln mit seinen direkten Nachbarn - auch hier muss die Summe stimmen.
💡 Übungs-Tipp: Übe mit einfachen Verbindungen wie H₂O, CO₂ oder NH₃, bevor du zu komplexeren Molekülen übergehst!
Redoxreaktionen in der Natur findest du überall: Photosynthese und Zellatmung sind die wichtigsten Lebensprozesse. In der Industrie ermöglichen sie Ammoniaksynthese und Metallgewinnung aus Erzen.

Anwendungen: Metallherstellung und Hochofen
In deinem Haushalt begegnest du Redoxreaktionen bei Bleichmitteln, Reinigungsmitteln und sogar bei Feuerwerken (Pyrotechnik). Die Metallherstellung funktioniert in zwei Schritten: Erst werden sulfidische oder carbonatische Erze durch Luftzufuhr in Oxide umgewandelt, dann werden diese Oxide mit Kohlenstoff, Wasserstoff oder unedlen Metallen zu reinen Metallen reduziert.
Der Hochofen arbeitet nach dem cleveren Gegenstromprinzip: Gase steigen nach oben, Feststoffe sinken nach unten. Das sorgt für bessere Trennung und optimale Reaktionsbedingungen. Allerdings ist dieser Prozess nicht nachhaltig wegen der CO₂-Produktion.
Nachhaltige Alternativen setzen auf Wasserstoff statt Kohlenstoff oder verwenden Elektrolichtöfen, die mit erneuerbarer Energie betrieben werden.
💡 Zukunft der Industrie: Die Stahlindustrie forscht intensiv an wasserstoffbasierten Verfahren, um klimaneutral zu werden!
Beim aluminothermischen Schweißen (Thermitschweißen) reagieren Aluminium und Eisen(III)-oxid so heftig exotherm, dass dabei Temperaturen von über 2000°C entstehen - perfekt zum Schweißen von Schienen.
Redoxtitration und Eisenverbindungen
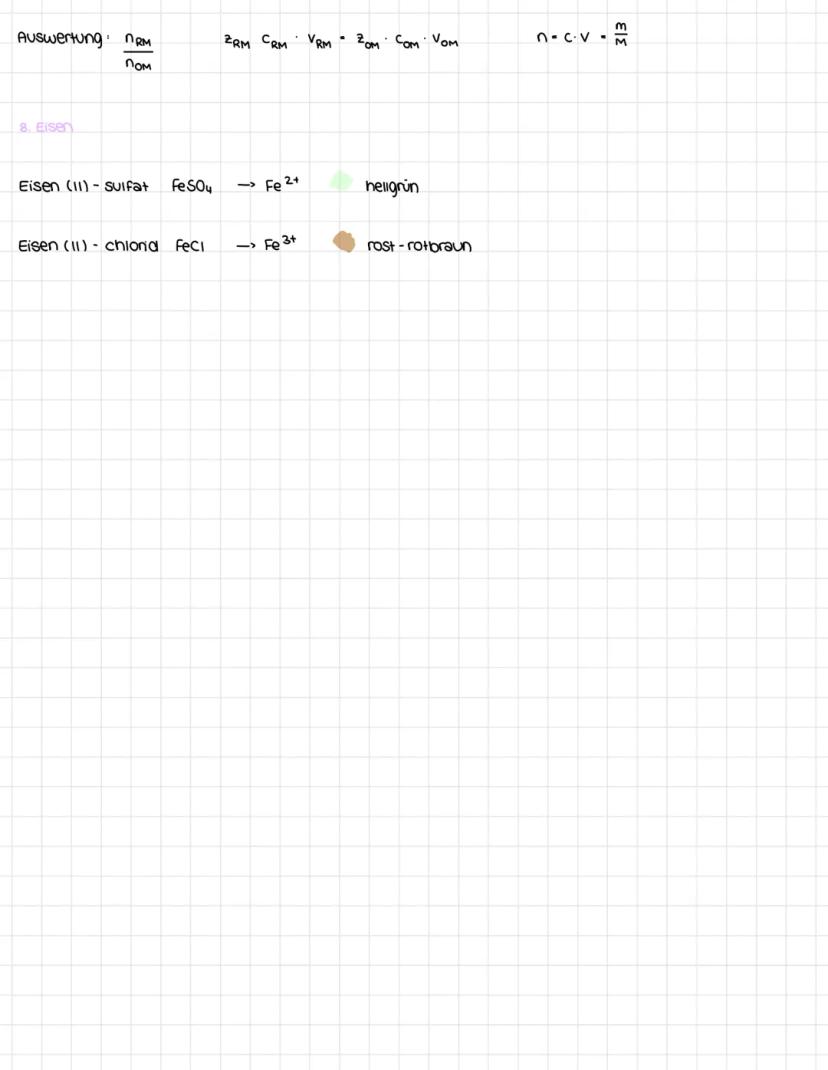
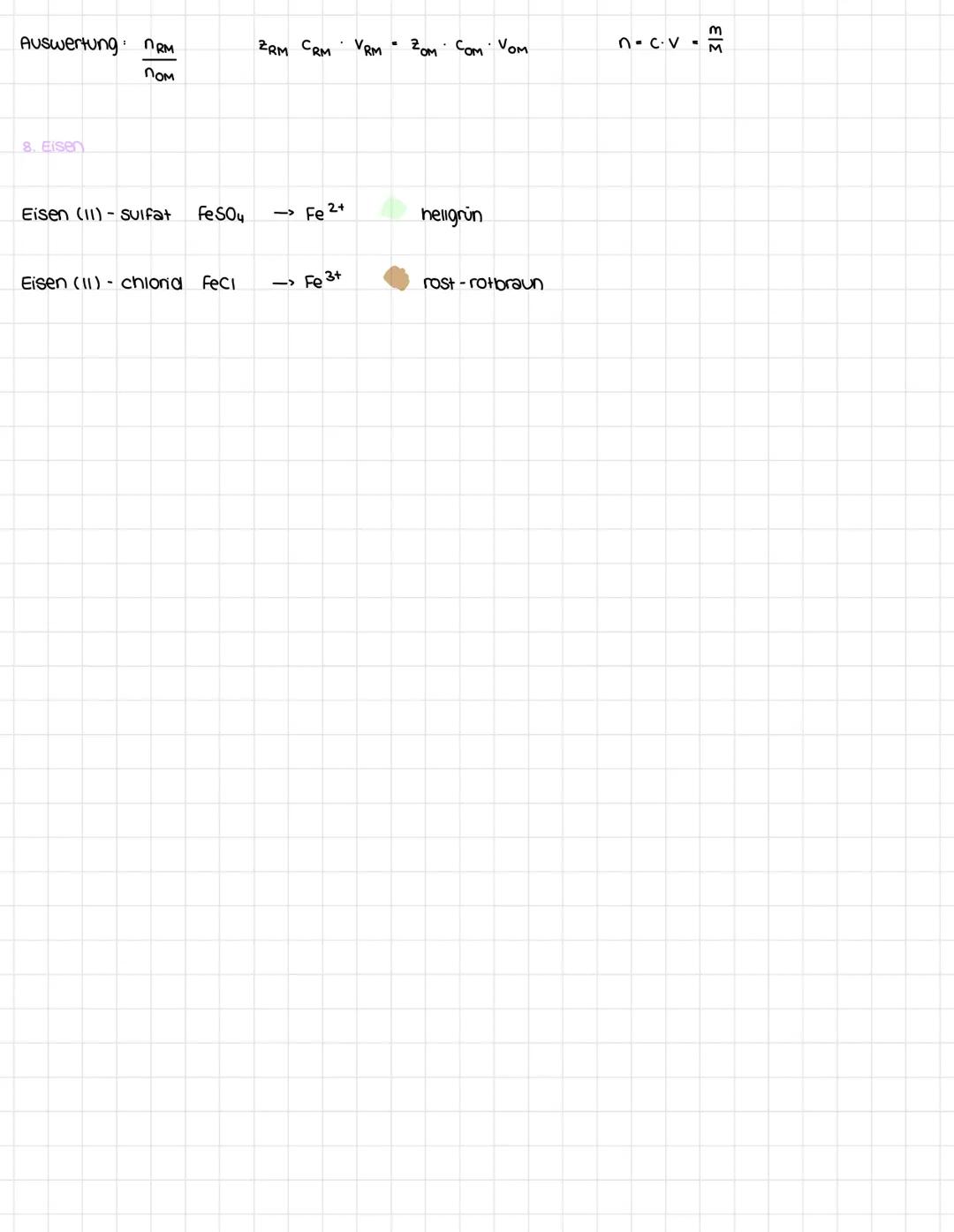
Bei der Redoxtitration erkennst du den Äquivalenzpunkt am Farbumschlag eines Indikators oder misst ihn mit pH-Metern bzw. Leitfähigkeitsmessgeräten. Die Auswertung erfolgt über die Formel mit Stoffmengen, Konzentrationen und Volumina der beteiligten Lösungen.
Eisenverbindungen haben charakteristische Farben: Eisen(II)-sulfat (FeSO₄) erscheint hellgrün mit Fe²⁺-Ionen, während Eisen(III)-chlorid (FeCl₃) rostrotbraun mit Fe³⁺-Ionen aussieht. Diese Farbunterschiede helfen dir bei der Identifikation in Experimenten.
Die mathematische Auswertung nutzt das Verhältnis der Elektronenübergänge: n(RM)/n(OM) = z(OM)/z(RM), wobei z die Anzahl der übertragenen Elektronen pro Molekül angibt.
💡 Labor-Tipp: Achte auf die charakteristischen Farben - sie verraten dir oft schon vor der Berechnung, welche Ionen vorliegen!
Bei komplexeren Reaktionsgleichungen musst du die Teilreaktionen erst ausgleichen und dann sinnvoll kombinieren, damit die Elektronenbilanz stimmt.

Reaktionsgleichungen aufstellen - Schritt für Schritt
Das Aufstellen von Redoxgleichungen ist wie ein Puzzle: Du identifizierst zuerst die korrespondierenden Redoxpaare, dann stellst du die Teilgleichungen für Oxidation und Reduktion auf. Wichtig ist, dass die Anzahl der übertragenen Elektronen in beiden Teilreaktionen gleich ist.
Bei der Reaktion von H₂O₂ mit Permanganat bilden sich die Paare H₂O₂|O₂ und MnO₄⁻|MnO₄²⁻. Du gleichst jede Teilreaktion einzeln aus und multiplizierst dann mit geeigneten Faktoren, damit die Elektronenbilanz stimmt.
Komplexere Beispiele wie die Reaktion von Ameisensäure mit Permanganat erfordern mehr Aufmerksamkeit: Hier werden 5 Elektronen übertragen, also brauchst du das 2-fache der Permanganat-Gleichung und das 5-fache der Ameisensäure-Gleichung.
💡 Erfolgs-Strategie: Übe das schrittweise Vorgehen - erst Oxidationszahlen bestimmen, dann Redoxpaare finden, Teilgleichungen aufstellen und zum Schluss ausgleichen!
Bei Disproportionierungsreaktionen wie beim Zerfall von KMnO₄ entstehen mehrere Produkte mit unterschiedlichen Oxidationsstufen desselben Elements - hier ist besondere Sorgfalt beim Ausgleichen gefragt.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Redoxreaktionen
9Redoxreaktionen und Oxidationszahlen
Entdecken Sie die Grundlagen der Redoxreaktionen, einschließlich der Definitionen von Oxidation und Reduktion, Elektronendonatoren und -akzeptoren sowie der Redoxreihe. Diese Zusammenfassung bietet eine klare Erklärung der Oxidationszahlen und deren Bestimmung. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Redoxreaktionen: Grundlagen und Gleichungen
Entdecken Sie die wesentlichen Konzepte der Redoxreaktionen, einschließlich Oxidation, Reduktion und Oxidationszahlen. Diese Zusammenfassung bietet eine klare Anleitung zur Entwicklung von Redoxgleichungen in sauren und alkalischen Lösungen, ideal für Chemie GK Schüler in Baden-Württemberg. Lernen Sie die Schritte zur Bestimmung von Redoxpaaren und das Ausgleichen von Gleichungen.
Redoxreaktionen & Elektrochemie
Entdecken Sie die Grundlagen der Redoxreaktionen und Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Batterietypen wie Zink-Kohle- und Nickel-Metallhydrid-Akkus sowie die Bedeutung von Oxidation und Reduktion. Diese Zusammenfassung bietet eine klare Übersicht über die wichtigsten Konzepte und Reaktionen, die für das Abitur 2022 relevant sind.
Chemie Abitur 2024: Grundlagen
Dieser Lernzettel bietet eine umfassende Übersicht über die wichtigsten Themen für das Chemie-Abitur 2024, einschließlich Reaktionskinetik, chemische Gleichgewichte, Redoxreaktionen, Titration, und die Eigenschaften von Stoffklassen. Ideal für die Prüfungsvorbereitung und das Verständnis grundlegender chemischer Konzepte.
Chemie Abitur Zusammenfassung
Umfassende Übersicht über alle relevanten Themen für das Chemie-Abitur in Niedersachsen 2022. Behandelt werden unter anderem Reaktionskinetik, Redoxreaktionen, organische Chemie, chemische Gleichgewichte, Enthalpieänderungen und Polymerchemie. Ideal für die Prüfungsvorbereitung.
Redoxreaktionen und Oxidationszahlen
Erfahre alles über Redoxreaktionen, Oxidation und Reduktion sowie die Bedeutung von Oxidationszahlen. Diese Zusammenfassung bietet klare Definitionen, Regeln und Beispiele, um das Verständnis von Elektronenübertragungen in chemischen Reaktionen zu vertiefen. Ideal für Chemie-Studierende und zur Prüfungsvorbereitung.
Oxidationszahlen & Redoxreaktionen
Erfahren Sie, wie man Oxidationszahlen bestimmt und Redoxreaktionen aufstellt. Diese Zusammenfassung behandelt die Schritte zur Zuordnung von Oxidationszahlen, die Berechnung von Teil- und Gesamtgleichungen sowie die Konzepte von Oxidation und Reduktion. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie: Elemente & Reaktionen
Entdecken Sie die Grundlagen der Chemie mit diesem Lernmaterial. Erfahren Sie mehr über Atome, Moleküle, chemische Bindungen, Reaktionen (Redox, Säure-Base) und zwischenmolekulare Wechselwirkungen. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Redoxreaktionen und Elektrochemie
Detaillierte Zusammenfassung zu Redoxreaktionen und elektrochemischen Prozessen, einschließlich der Nernst-Gleichung, galvanischen Zellen und Elektrolyse. Ideal für Chemie-LK-Studierende, die sich auf Prüfungen vorbereiten. Behandelt wichtige Konzepte wie Oxidationsmittel, Reduktionsmittel, Standardpotentiale und Brennstoffzellen.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Redoxreaktionen in der Chemie leicht erklärt
Redoxreaktionen sind überall um uns herum - von der Atmung in deinen Zellen bis zum Rosten von Metall. Diese Elektronenübergangsreaktionen bestehen immer aus zwei Teilen: Oxidation (Elektronenabgabe) und Reduktion (Elektronenaufnahme), die gleichzeitig ablaufen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Grundbegriffe der Redoxreaktionen
Stell dir vor, Elektronen sind wie Geschenke, die zwischen Atomen ausgetauscht werden. Bei einer Redoxreaktion passiert genau das - es ist eine Elektronenübergangsreaktion, bei der immer zwei Prozesse gleichzeitig ablaufen.
Die Oxidation ist der Prozess, bei dem ein Stoff Elektronen abgibt (seine Oxidationszahl steigt). Die Reduktion läuft parallel ab - hier nimmt ein anderer Stoff die Elektronen auf (seine Oxidationszahl sinkt). Ohne Oxidation keine Reduktion und umgekehrt!
Oxidationsmittel sind die "Elektronenräuber" - sie sorgen dafür, dass andere Stoffe oxidiert werden, werden dabei aber selbst reduziert. Reduktionsmittel machen das Gegenteil: Sie reduzieren andere Stoffe und werden selbst oxidiert.
💡 Merkhilfe: OIL RIG - Oxidation Is Loss (of electrons), Reduction Is Gain (of electrons)
Korrespondierende Redoxpaare sind wie Tanzpartner - sie gehören zusammen und können durch Elektronenaufnahme oder -abgabe ineinander umgewandelt werden. Oxidationszahlen helfen dir dabei, den Überblick zu behalten - sie zeigen die fiktive Ladung jedes Atoms in einer Verbindung.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Besondere Redoxreaktionen und Grundformen
Manche Elemente sind echte Verwandlungskünstler und können sowohl als Oxidations- als auch als Reduktionsmittel auftreten - je nach Reaktionsbedingungen. Das nennt sich Donator-Akzeptor-Konzept: Reduktionsmittel sind Elektronendonatoren, Oxidationsmittel sind Elektronenakzeptoren.
Bei der Synproportionierung treffen sich Atome desselben Elements aus verschiedenen Oxidationsstufen in der Mitte - wie bei einem Kompromiss. Bei der Disproportionierung passiert das Gegenteil: Ein Element "spaltet sich" in höhere und niedrigere Oxidationsstufen auf.
Redoxtitration ist dein Werkzeug für quantitative Analysen. Damit bestimmst du die Stoffmenge einer unbekannten Substanz mithilfe einer bekannten Maßlösung - perfekt für Laborarbeiten!
💡 Praxis-Tipp: Lerne die wichtigsten Ionen auswendig - Sulfat (SO₄²⁻), Nitrat (NO₃⁻), Permanganat (MnO₄⁻) und Co. begegnen dir ständig!
Die Mangan-Verbindungen sind besonders interessant: Kaliumpermanganat kann je nach pH-Wert zu farblosem Mn²⁺ (sauer) oder braunem MnO₂ (neutral) reduziert werden.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Oxidationszahlen bestimmen - die 8 goldenen Regeln
Oxidationszahlen zu bestimmen ist wie ein Puzzle - mit den richtigen Regeln wird's zum Kinderspiel. Elementare Atome haben immer die Oxidationszahl 0 (wie C oder Fe). Metalle folgen ihrer Hauptgruppennummer, Ionen entsprechen ihrer Ladung.
Bei mehratomigen Verbindungen ohne Ladung muss die Summe aller Oxidationszahlen 0 ergeben. Bei mehratomigen Ionen muss die Summe der Ionenladung entsprechen. Wasserstoff hat fast immer +1 (Ausnahme: Metallhydride wie LiH), Sauerstoff fast immer -2 (Ausnahme: Peroxide wie H₂O₂).
Bei organischen Verbindungen betrachtest du jedes Kohlenstoffatom einzeln mit seinen direkten Nachbarn - auch hier muss die Summe stimmen.
💡 Übungs-Tipp: Übe mit einfachen Verbindungen wie H₂O, CO₂ oder NH₃, bevor du zu komplexeren Molekülen übergehst!
Redoxreaktionen in der Natur findest du überall: Photosynthese und Zellatmung sind die wichtigsten Lebensprozesse. In der Industrie ermöglichen sie Ammoniaksynthese und Metallgewinnung aus Erzen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Anwendungen: Metallherstellung und Hochofen
In deinem Haushalt begegnest du Redoxreaktionen bei Bleichmitteln, Reinigungsmitteln und sogar bei Feuerwerken (Pyrotechnik). Die Metallherstellung funktioniert in zwei Schritten: Erst werden sulfidische oder carbonatische Erze durch Luftzufuhr in Oxide umgewandelt, dann werden diese Oxide mit Kohlenstoff, Wasserstoff oder unedlen Metallen zu reinen Metallen reduziert.
Der Hochofen arbeitet nach dem cleveren Gegenstromprinzip: Gase steigen nach oben, Feststoffe sinken nach unten. Das sorgt für bessere Trennung und optimale Reaktionsbedingungen. Allerdings ist dieser Prozess nicht nachhaltig wegen der CO₂-Produktion.
Nachhaltige Alternativen setzen auf Wasserstoff statt Kohlenstoff oder verwenden Elektrolichtöfen, die mit erneuerbarer Energie betrieben werden.
💡 Zukunft der Industrie: Die Stahlindustrie forscht intensiv an wasserstoffbasierten Verfahren, um klimaneutral zu werden!
Beim aluminothermischen Schweißen (Thermitschweißen) reagieren Aluminium und Eisen(III)-oxid so heftig exotherm, dass dabei Temperaturen von über 2000°C entstehen - perfekt zum Schweißen von Schienen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Redoxtitration und Eisenverbindungen
Bei der Redoxtitration erkennst du den Äquivalenzpunkt am Farbumschlag eines Indikators oder misst ihn mit pH-Metern bzw. Leitfähigkeitsmessgeräten. Die Auswertung erfolgt über die Formel mit Stoffmengen, Konzentrationen und Volumina der beteiligten Lösungen.
Eisenverbindungen haben charakteristische Farben: Eisen(II)-sulfat (FeSO₄) erscheint hellgrün mit Fe²⁺-Ionen, während Eisen(III)-chlorid (FeCl₃) rostrotbraun mit Fe³⁺-Ionen aussieht. Diese Farbunterschiede helfen dir bei der Identifikation in Experimenten.
Die mathematische Auswertung nutzt das Verhältnis der Elektronenübergänge: n(RM)/n(OM) = z(OM)/z(RM), wobei z die Anzahl der übertragenen Elektronen pro Molekül angibt.
💡 Labor-Tipp: Achte auf die charakteristischen Farben - sie verraten dir oft schon vor der Berechnung, welche Ionen vorliegen!
Bei komplexeren Reaktionsgleichungen musst du die Teilreaktionen erst ausgleichen und dann sinnvoll kombinieren, damit die Elektronenbilanz stimmt.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Reaktionsgleichungen aufstellen - Schritt für Schritt
Das Aufstellen von Redoxgleichungen ist wie ein Puzzle: Du identifizierst zuerst die korrespondierenden Redoxpaare, dann stellst du die Teilgleichungen für Oxidation und Reduktion auf. Wichtig ist, dass die Anzahl der übertragenen Elektronen in beiden Teilreaktionen gleich ist.
Bei der Reaktion von H₂O₂ mit Permanganat bilden sich die Paare H₂O₂|O₂ und MnO₄⁻|MnO₄²⁻. Du gleichst jede Teilreaktion einzeln aus und multiplizierst dann mit geeigneten Faktoren, damit die Elektronenbilanz stimmt.
Komplexere Beispiele wie die Reaktion von Ameisensäure mit Permanganat erfordern mehr Aufmerksamkeit: Hier werden 5 Elektronen übertragen, also brauchst du das 2-fache der Permanganat-Gleichung und das 5-fache der Ameisensäure-Gleichung.
💡 Erfolgs-Strategie: Übe das schrittweise Vorgehen - erst Oxidationszahlen bestimmen, dann Redoxpaare finden, Teilgleichungen aufstellen und zum Schluss ausgleichen!
Bei Disproportionierungsreaktionen wie beim Zerfall von KMnO₄ entstehen mehrere Produkte mit unterschiedlichen Oxidationsstufen desselben Elements - hier ist besondere Sorgfalt beim Ausgleichen gefragt.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Redoxreaktionen
9Redoxreaktionen und Oxidationszahlen
Entdecken Sie die Grundlagen der Redoxreaktionen, einschließlich der Definitionen von Oxidation und Reduktion, Elektronendonatoren und -akzeptoren sowie der Redoxreihe. Diese Zusammenfassung bietet eine klare Erklärung der Oxidationszahlen und deren Bestimmung. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Redoxreaktionen: Grundlagen und Gleichungen
Entdecken Sie die wesentlichen Konzepte der Redoxreaktionen, einschließlich Oxidation, Reduktion und Oxidationszahlen. Diese Zusammenfassung bietet eine klare Anleitung zur Entwicklung von Redoxgleichungen in sauren und alkalischen Lösungen, ideal für Chemie GK Schüler in Baden-Württemberg. Lernen Sie die Schritte zur Bestimmung von Redoxpaaren und das Ausgleichen von Gleichungen.
Redoxreaktionen & Elektrochemie
Entdecken Sie die Grundlagen der Redoxreaktionen und Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Batterietypen wie Zink-Kohle- und Nickel-Metallhydrid-Akkus sowie die Bedeutung von Oxidation und Reduktion. Diese Zusammenfassung bietet eine klare Übersicht über die wichtigsten Konzepte und Reaktionen, die für das Abitur 2022 relevant sind.
Chemie Abitur 2024: Grundlagen
Dieser Lernzettel bietet eine umfassende Übersicht über die wichtigsten Themen für das Chemie-Abitur 2024, einschließlich Reaktionskinetik, chemische Gleichgewichte, Redoxreaktionen, Titration, und die Eigenschaften von Stoffklassen. Ideal für die Prüfungsvorbereitung und das Verständnis grundlegender chemischer Konzepte.
Chemie Abitur Zusammenfassung
Umfassende Übersicht über alle relevanten Themen für das Chemie-Abitur in Niedersachsen 2022. Behandelt werden unter anderem Reaktionskinetik, Redoxreaktionen, organische Chemie, chemische Gleichgewichte, Enthalpieänderungen und Polymerchemie. Ideal für die Prüfungsvorbereitung.
Redoxreaktionen und Oxidationszahlen
Erfahre alles über Redoxreaktionen, Oxidation und Reduktion sowie die Bedeutung von Oxidationszahlen. Diese Zusammenfassung bietet klare Definitionen, Regeln und Beispiele, um das Verständnis von Elektronenübertragungen in chemischen Reaktionen zu vertiefen. Ideal für Chemie-Studierende und zur Prüfungsvorbereitung.
Oxidationszahlen & Redoxreaktionen
Erfahren Sie, wie man Oxidationszahlen bestimmt und Redoxreaktionen aufstellt. Diese Zusammenfassung behandelt die Schritte zur Zuordnung von Oxidationszahlen, die Berechnung von Teil- und Gesamtgleichungen sowie die Konzepte von Oxidation und Reduktion. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie: Elemente & Reaktionen
Entdecken Sie die Grundlagen der Chemie mit diesem Lernmaterial. Erfahren Sie mehr über Atome, Moleküle, chemische Bindungen, Reaktionen (Redox, Säure-Base) und zwischenmolekulare Wechselwirkungen. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Redoxreaktionen und Elektrochemie
Detaillierte Zusammenfassung zu Redoxreaktionen und elektrochemischen Prozessen, einschließlich der Nernst-Gleichung, galvanischen Zellen und Elektrolyse. Ideal für Chemie-LK-Studierende, die sich auf Prüfungen vorbereiten. Behandelt wichtige Konzepte wie Oxidationsmittel, Reduktionsmittel, Standardpotentiale und Brennstoffzellen.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.