Die Welt der Atommodelle und chemischen Bindungen wird viel klarer,... Mehr anzeigen
Melde dich an, um den Inhalt zu sehenKostenlos!
Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Knowunity KI
Fächer
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Alle Themen anzeigen
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Alle Themen anzeigen
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Alle Themen anzeigen
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Alle Themen anzeigen
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Alle Themen anzeigen
494
•
Aktualisiert May 13, 2026
•
Anna
@anna_299423
Die Welt der Atommodelle und chemischen Bindungen wird viel klarer,... Mehr anzeigen




Das Schalenmodell zeigt dir, wo sich Elektronen aufhalten. Die Formel 2n² verrät dir, wie viele Elektronen maximal in eine Schale passen: K-Schale (2 Elektronen), L-Schale (8 Elektronen), M-Schale (18 Elektronen) und so weiter. Das ist wie ein Apartment-Gebäude mit verschiedenen Stockwerken.
Beim Energiestufenmodell haben Elektronen verschiedene Energielevel. Je weiter außen, desto mehr Energie besitzen sie. Das erklärt, warum äußere Elektronen leichter abgegeben werden können.
Die Elektronenbesetzung folgt einer bestimmten Reihenfolge: erst s-Orbitale, dann p-, d- und f-Orbitale. Chlor schreibst du als 1s² 2s² 2p⁶ 3s² 3p⁵. Das sieht kompliziert aus, folgt aber einfachen Regeln.
Merktipp: Die Kastchenschreibweise hilft dir dabei, die Orbital-Reihenfolge zu visualisieren und Elektronenkonfigurationen schnell zu bestimmen.
Bei Lewisformeln zeichnest du Bindungen als Striche und freie Elektronenpaare als Punkte. Partialladungen entstehen, wenn Atome unterschiedlich stark an Elektronen ziehen.
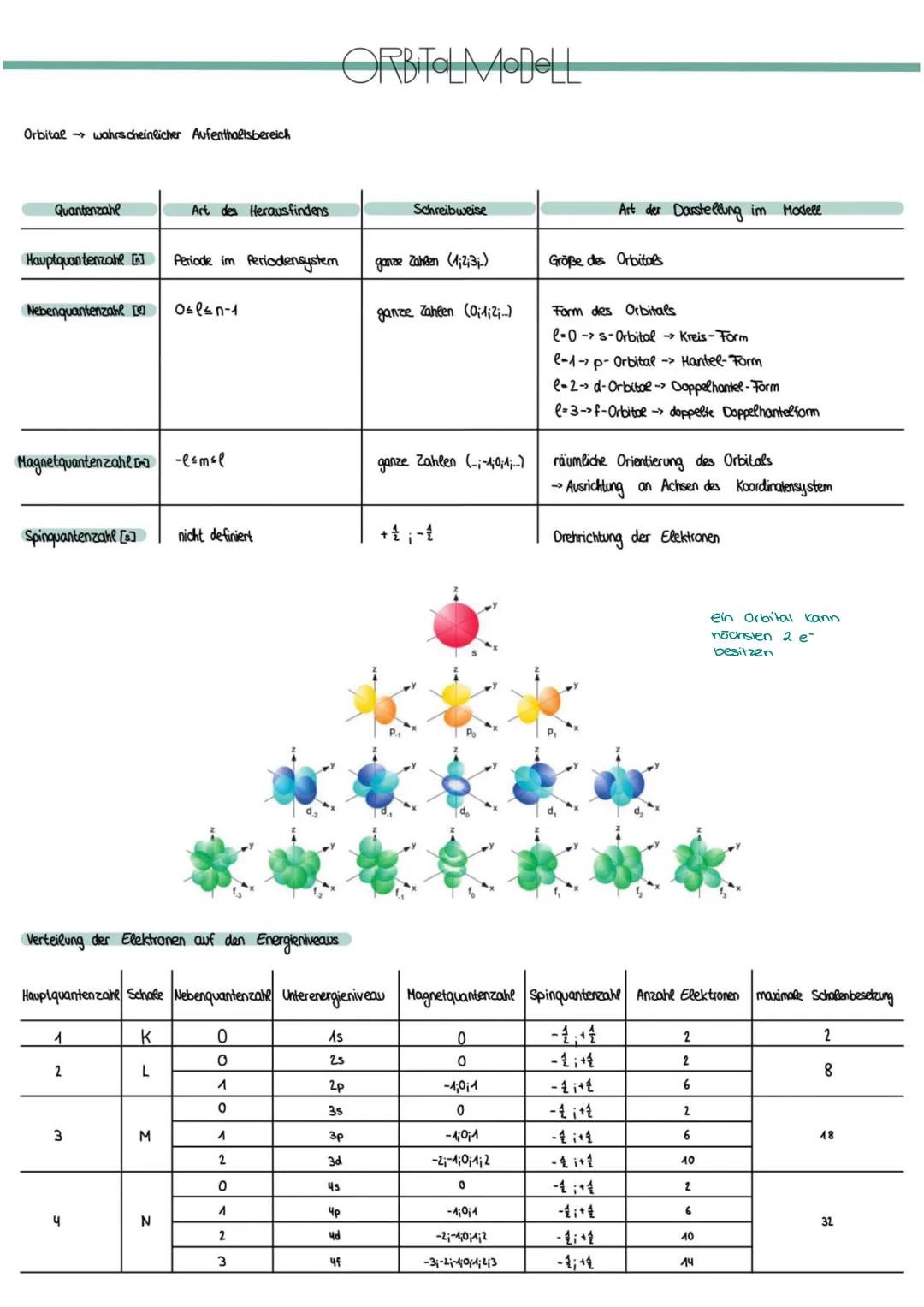
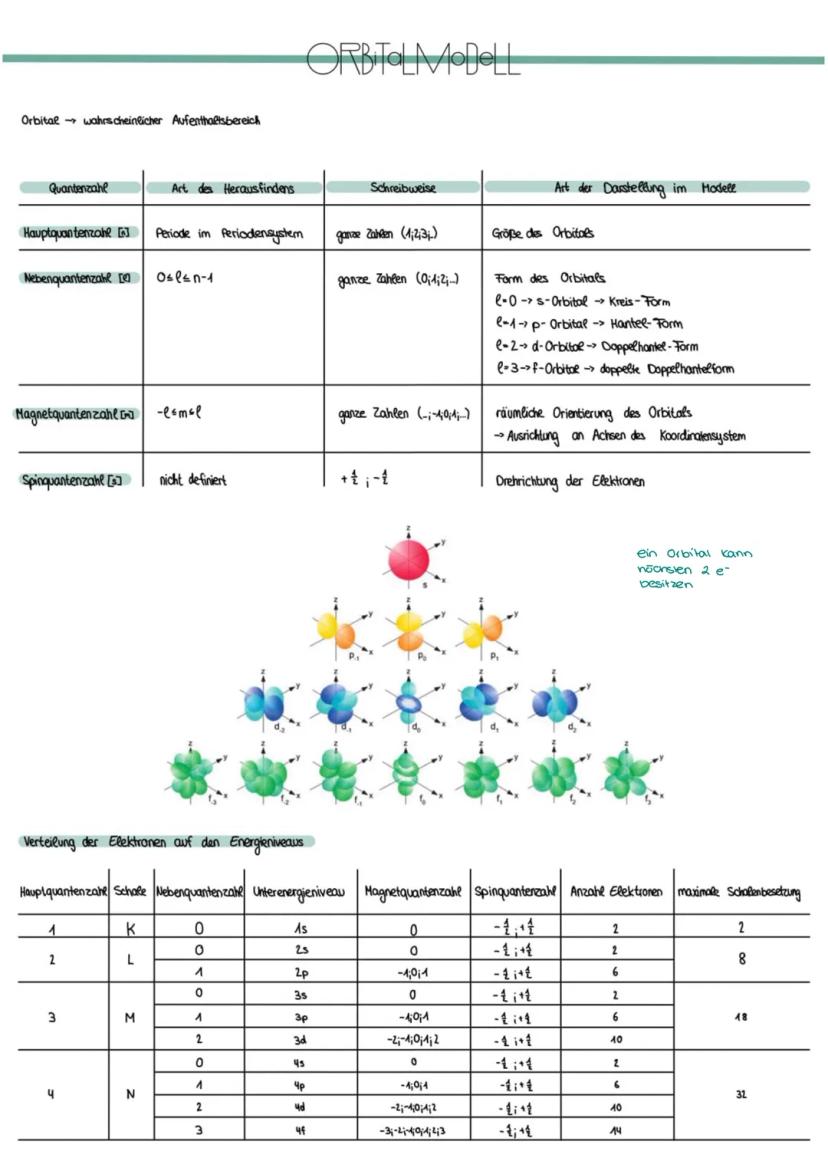
Das Orbitalmodell beschreibt Elektronen nicht als Teilchen auf festen Bahnen, sondern als Wolken mit bestimmten Aufenthaltswahrscheinlichkeiten. Vier Quantenzahlen charakterisieren jeden Elektronenplatz komplett.
Die Hauptquantenzahl n entspricht der Periode im Periodensystem und bestimmt die Orbitalgröße. Die Nebenquantenzahl l definiert die Orbitalform: s-Orbitale sind kugelförmig, p-Orbitale hantelförmig, d-Orbitale doppelhantelförmig.
Die Magnetquantenzahl ml zeigt die räumliche Orientierung an. p-Orbitale gibt es dreimal (px, py, pz), d-Orbitale fünfmal. Die Spinquantenzahl s beschreibt die Drehrichtung der Elektronen .
Wichtig: Pro Orbital passen maximal 2 Elektronen mit entgegengesetztem Spin - das ist das Pauli-Prinzip!
Die Tabelle zeigt dir die maximale Elektronenanzahl pro Schale: K-Schale (2e⁻), L-Schale (8e⁻), M-Schale (18e⁻), N-Schale (32e⁻). Diese Zahlen ergeben sich aus der Anzahl verfügbarer Orbitale.

Ionenbindungen entstehen zwischen Metallen und Nichtmetallen. Metalle geben Elektronen ab (werden zu Kationen), Nichtmetalle nehmen sie auf (werden zu Anionen). Die entstehenden Salzgitter sind spröde, haben hohe Schmelzpunkte und leiten nur gelöst den Strom.
Bei metallischen Bindungen schwimmen Atomrümpfe in einem "Elektronensee". Diese frei beweglichen Elektronen erklären typische Metalleigenschaften: Glanz, elektrische Leitfähigkeit, Wärmeleitfähigkeit und Verformbarkeit.
Interessant ist die Temperaturabhängigkeit der Leitfähigkeit: Beim Abkühlen schwingen die Atomrümpfe weniger, stören die Elektronen weniger - der Widerstand sinkt, die Leitfähigkeit steigt.
Merkregel: Ionenbindungen = spröde Salze, Metallbindungen = verformbare Leiter, Elektronenpaarbindungen = Moleküle!
Die Gitterenergie bestimmt die Stabilität von Ionenverbindungen. Je größer diese Energie, desto höher sind Schmelz- und Siedepunkt der entstehenden Salze.
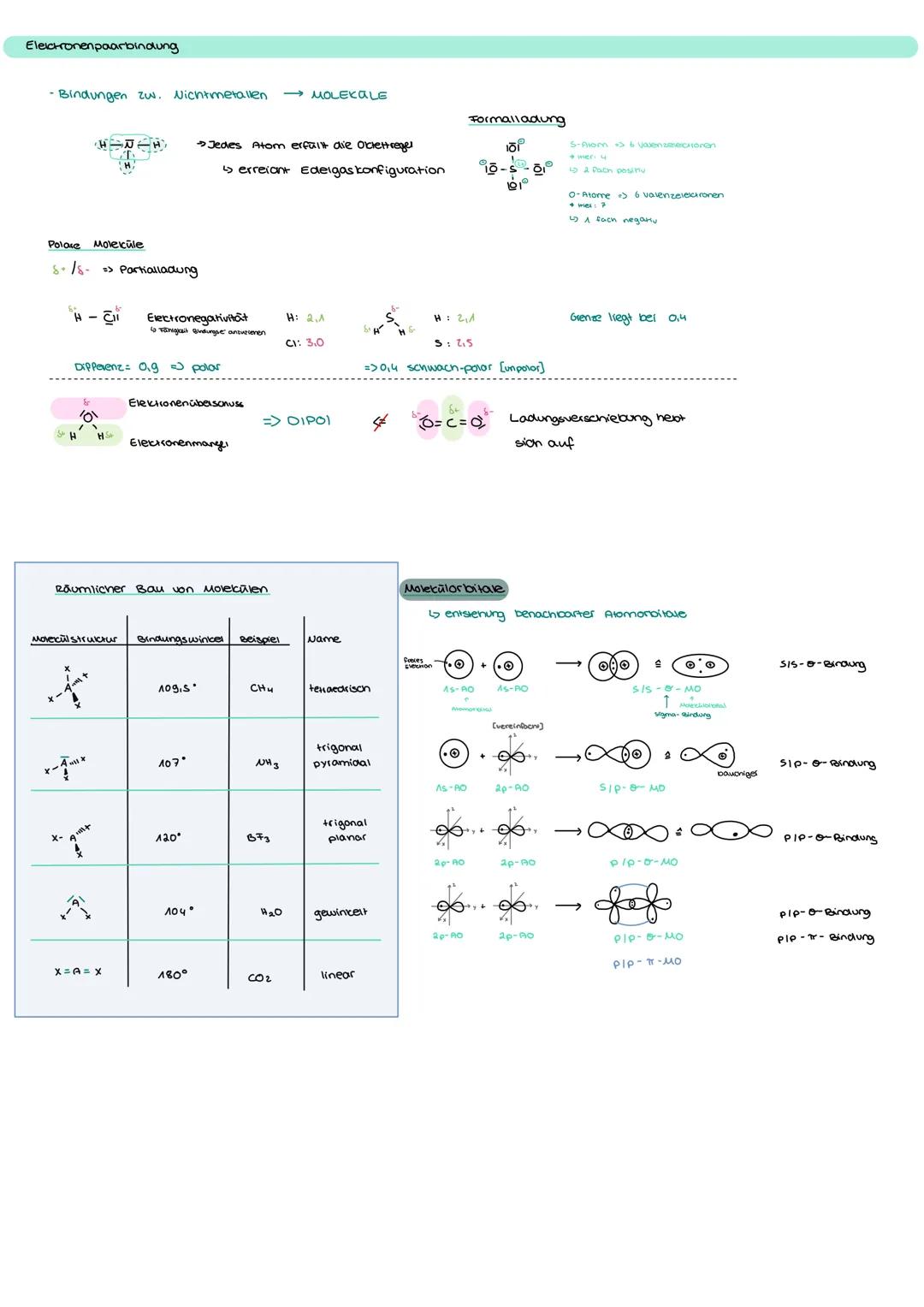
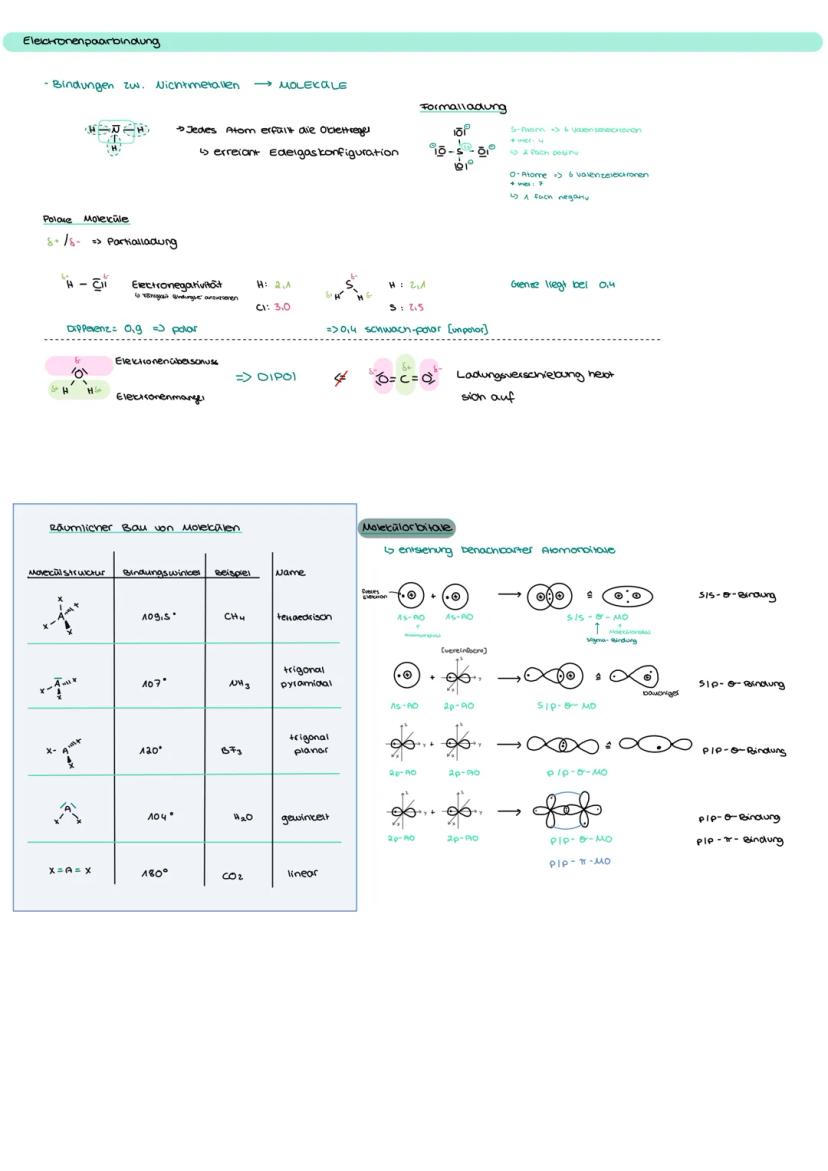
Elektronenpaarbindungen verbinden Nichtmetalle zu Molekülen. Dabei teilen sich Atome Elektronenpaare, um die Oktettregel zu erfüllen - jedes Atom möchte acht Außenelektronen haben wie die Edelgase.
Polare Moleküle entstehen durch unterschiedliche Elektronegativitäten. HCl ist polar , während H₂ unpolar ist . Der Dipol zeigt von δ+ zu δ-.
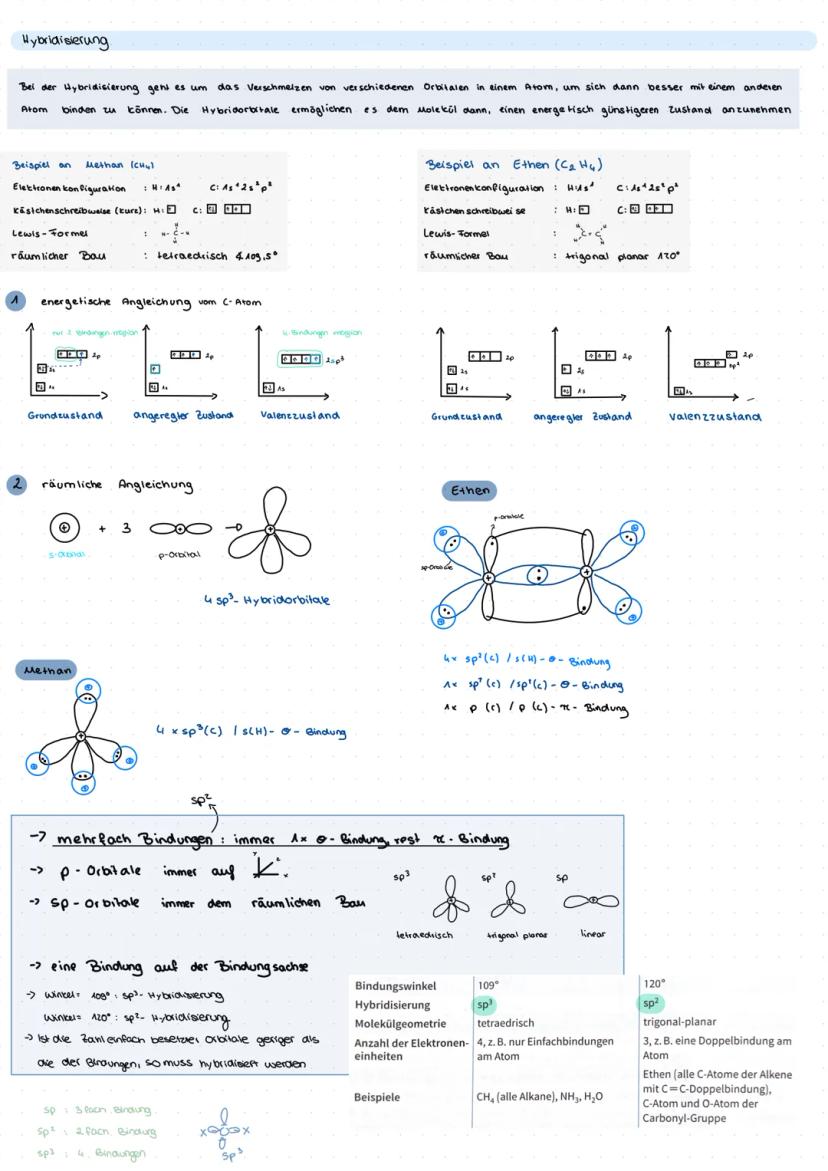
Die Molekülgeometrie hängt von bindenden und freien Elektronenpaaren ab. CH₄ ist tetraedrisch (109,5°), NH₃ trigonal pyramidal (107°), H₂O gewinkelt (104°). Diese Winkel sind prüfungsrelevant!
Praxistipp: CO₂ ist linear und unpolar, obwohl C=O-Bindungen polar sind - die Ladungsverschiebungen heben sich auf!
Molekülorbitale entstehen durch Überlappung von Atomorbitalen. σ-Bindungen sind stärker als π-Bindungen, was die Reaktivität von Doppel- und Dreifachbindungen erklärt.
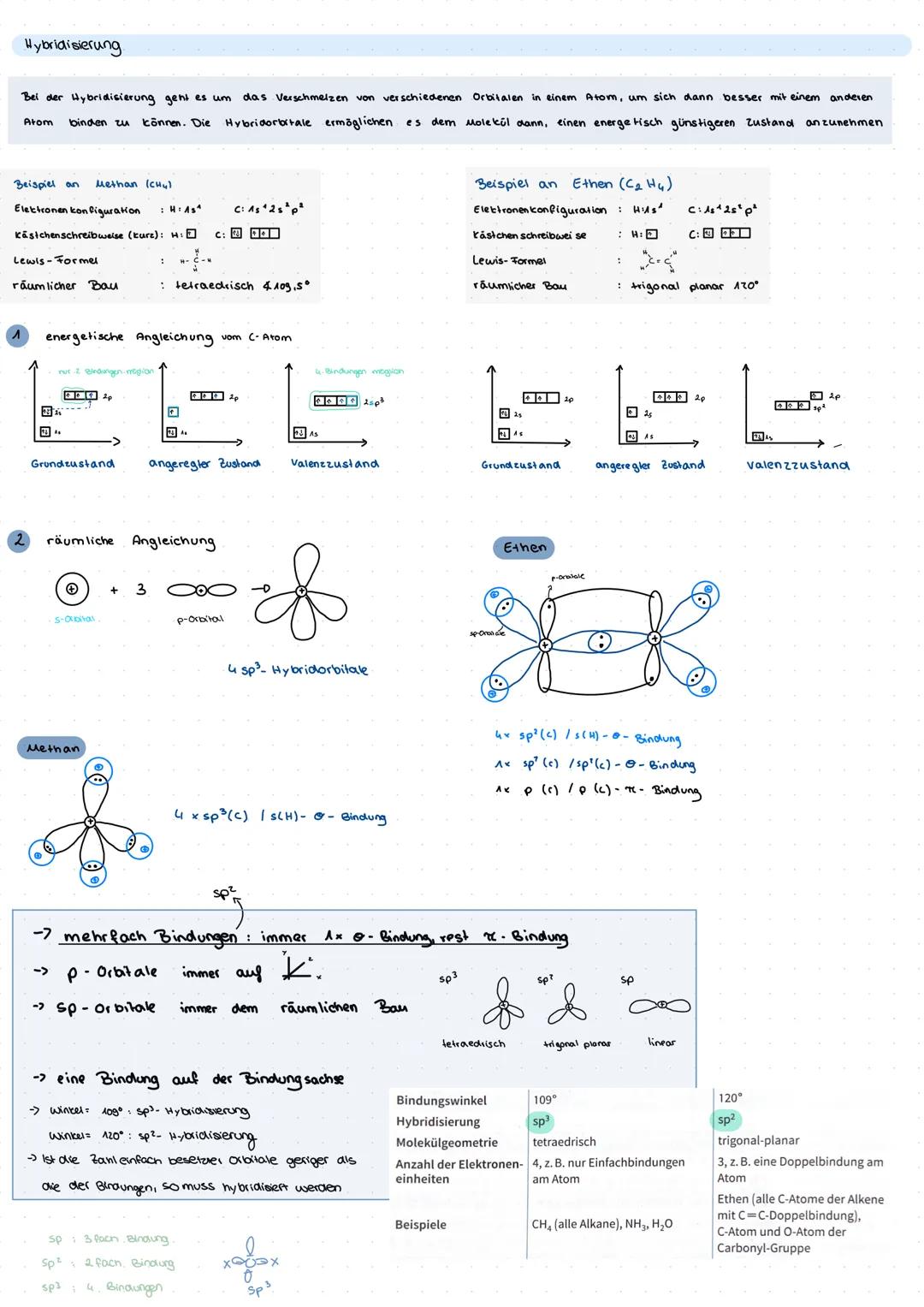
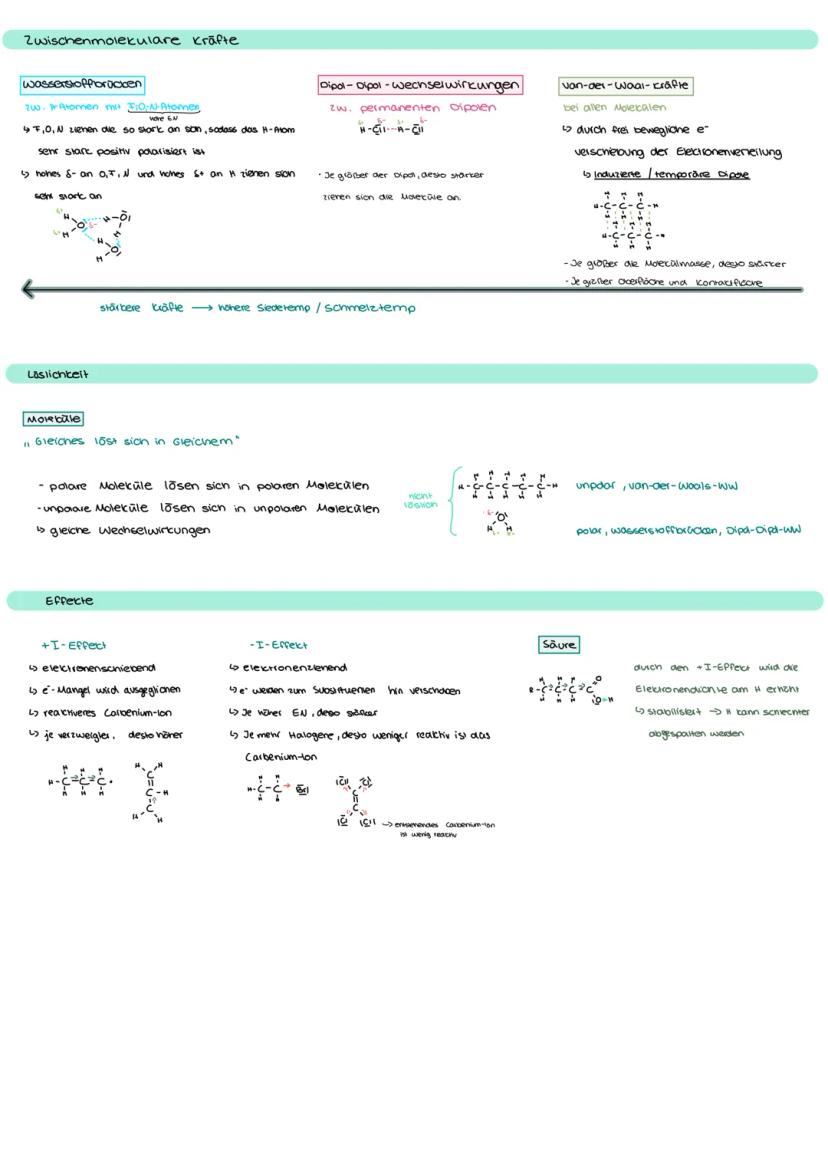
Wasserstoffbrücken sind die stärksten zwischenmolekularen Kräfte. Sie entstehen zwischen H-Atomen und stark elektronegativen Atomen (F, O, N). Das erklärt, warum Wasser trotz geringer Molmasse einen hohen Siedepunkt hat.
Dipol-Dipol-Wechselwirkungen wirken zwischen polaren Molekülen wie HCl. Van-der-Waals-Kräfte gibt es bei allen Molekülen - sie entstehen durch temporäre Elektronenverschiebungen und werden stärker mit zunehmender Molekülgröße.
Die Faustregel für Löslichkeit: "Gleiches löst sich in Gleichem!" Polare Stoffe lösen sich in polaren Lösungsmitteln, unpolare in unpolaren. Ethanol mischt sich mit Wasser (beide polar), Fette nicht.
Klausurtipp: Je stärker die zwischenmolekularen Kräfte, desto höher Siede- und Schmelztemperatur!
Induktive Effekte beeinflussen die Elektronendichte. Der +I-Effekt schiebt Elektronen, der -I-Effekt zieht sie an. Das beeinflusst die Reaktivität von Carbenium-Ionen erheblich.
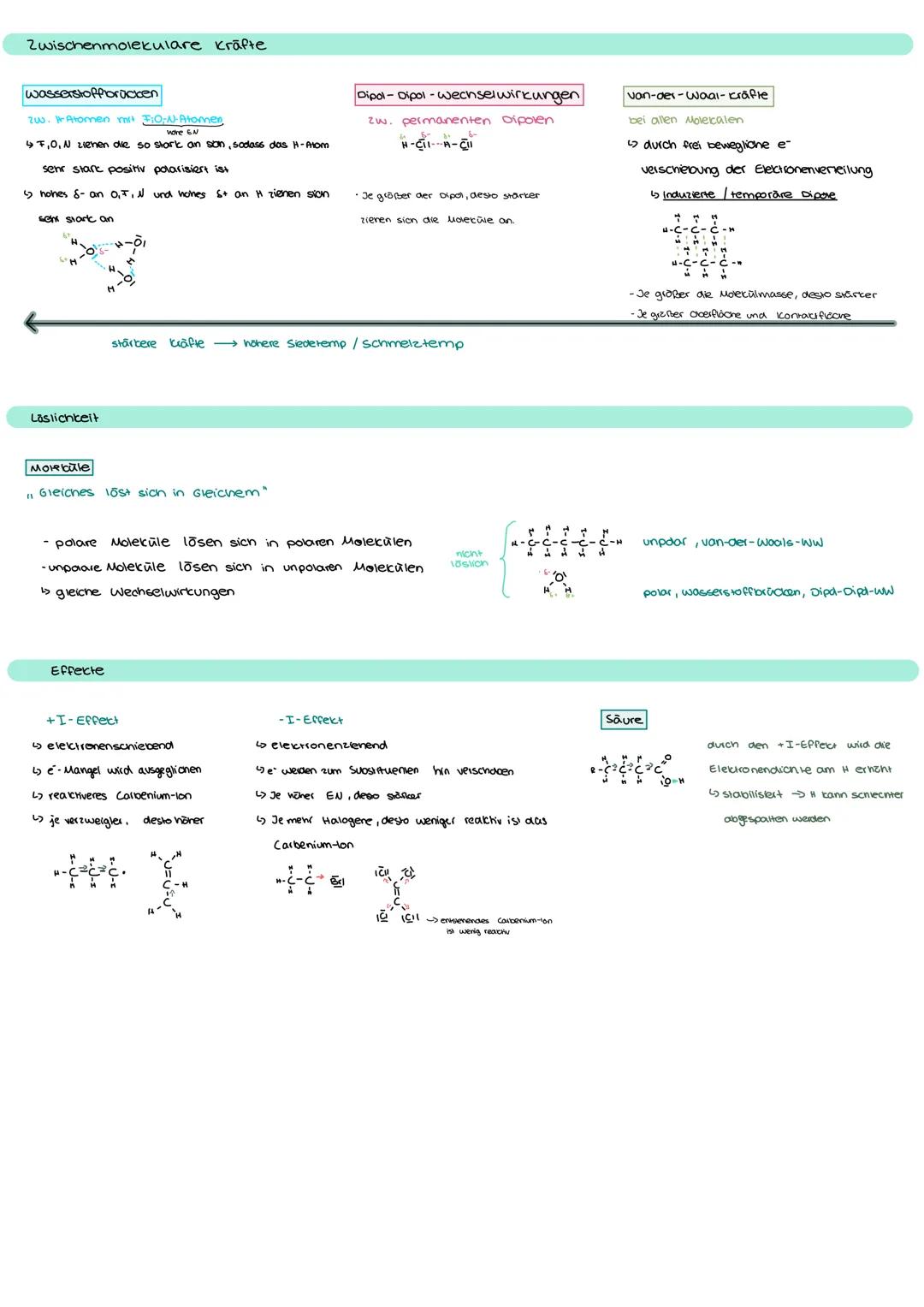
Radikalstabilität steigt mit der Anzahl der Alkylgruppen durch den +I-Effekt. Tertiäre Radikale sind stabiler als sekundäre, diese stabiler als primäre. Das erklärt, warum manche Reaktionen bevorzugt ablaufen.
Die Markovnikov-Regel besagt: Bei der Addition an unsymmetrische Doppelbindungen lagert sich das H-Atom an das C-Atom mit den meisten H-Atomen an. So entsteht das stabilste Carbenium-Ion.
Reaktivität hängt von der Elektronendichte an reaktiven Zentren ab. Elektronenziehende Gruppen erhöhen die Reaktivität von Carbonsäuren, während elektronenschiebende Gruppen sie verringern.
Wichtig: Die Stabilität von Carbenium-Ionen folgt der Reihenfolge: tertiär > sekundär > primär!
Carboxylationen sind wenig reaktiv, da die negative Ladung durch Resonanz stabilisiert wird. Je mehr elektronenziehende Gruppen, desto stärker die entsprechende Säure.

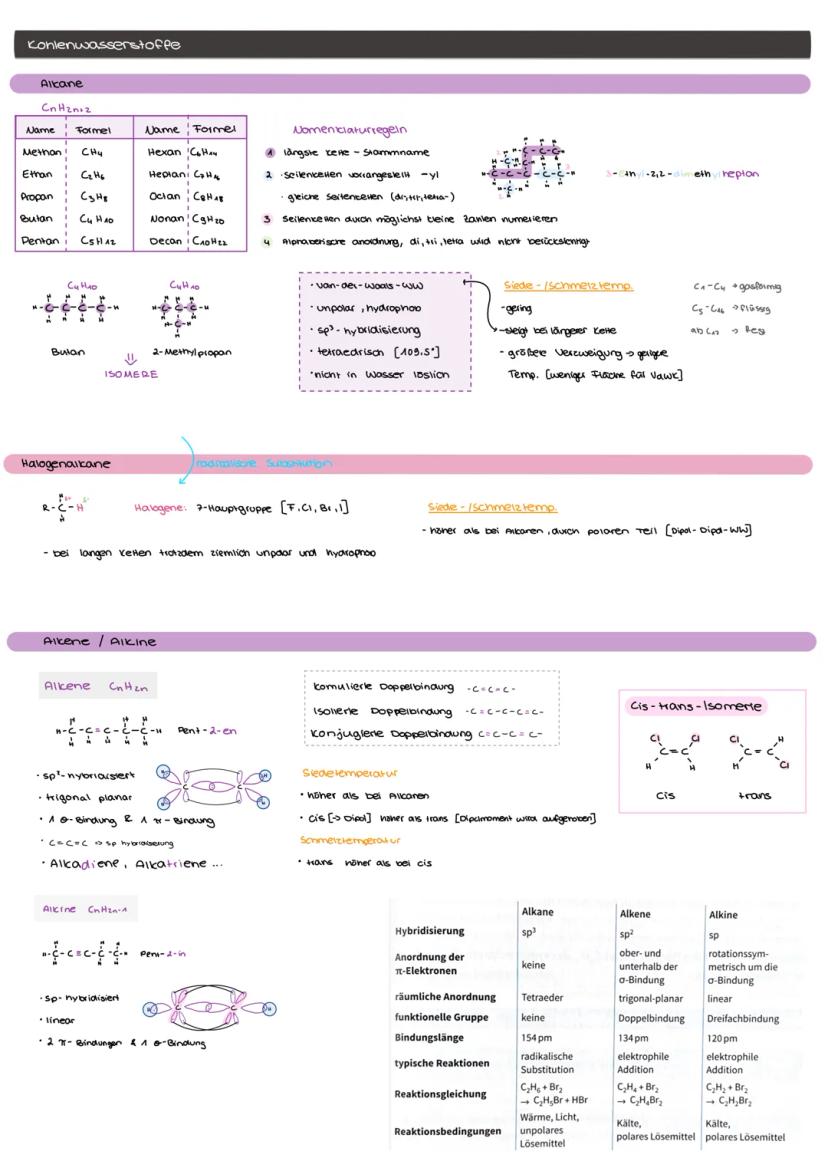
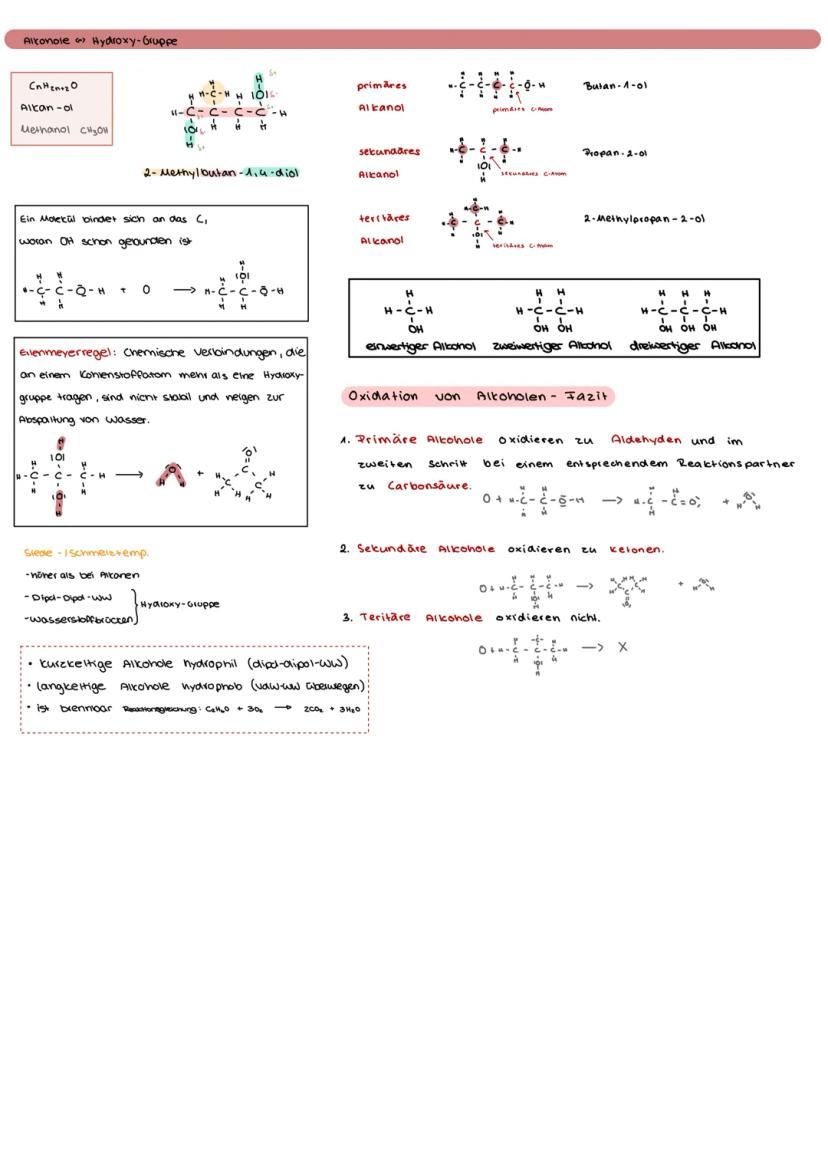
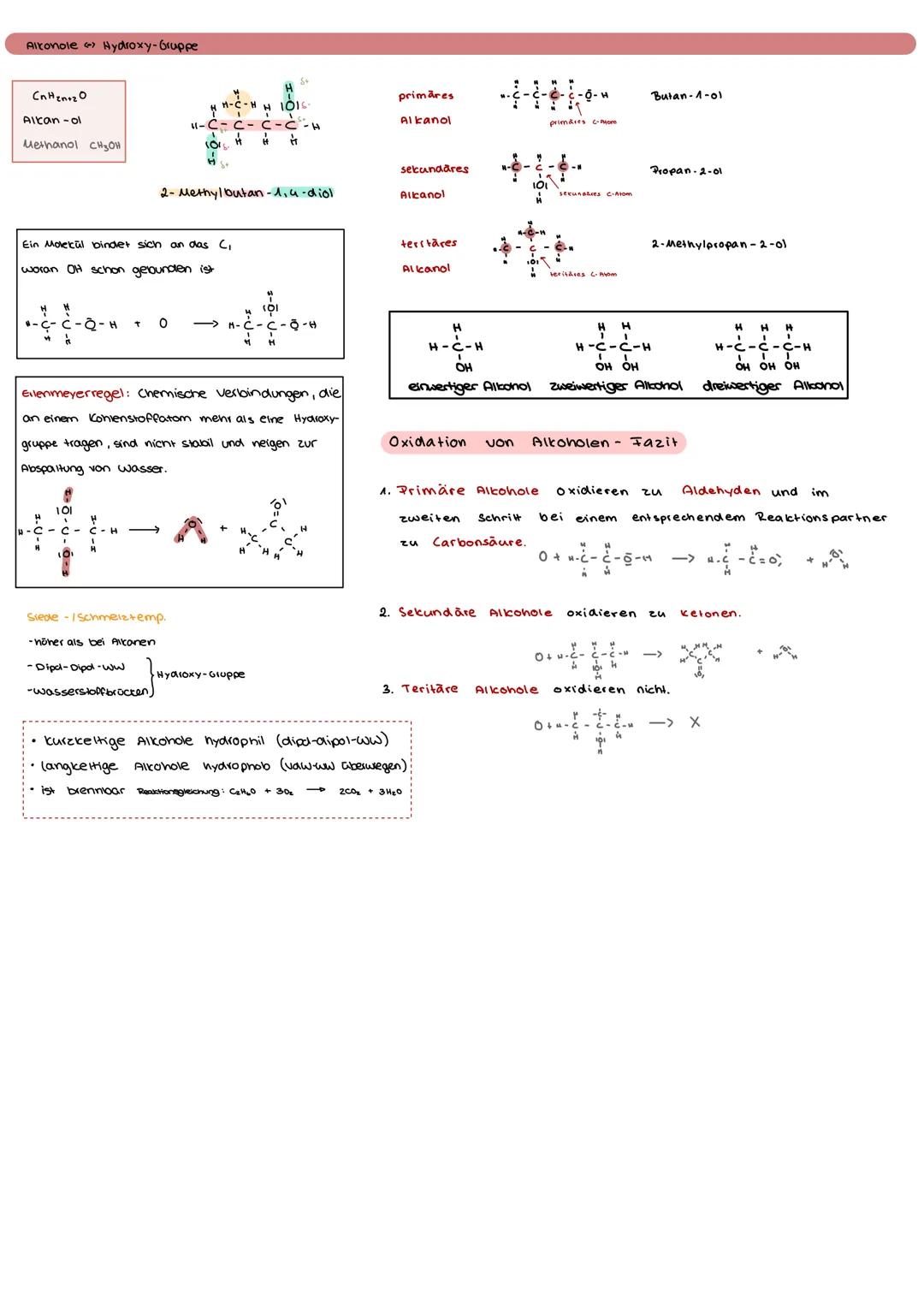
Alkohole enthalten die Hydroxy-Gruppe und folgen der Formel CₙH₂ₙ₊₁OH. Die Benennung erfolgt mit der Endung "-ol", wobei die OH-Gruppe die niedrigste Nummer erhält.
Die Erlenmeyer-Regel besagt: Verbindungen mit zwei OH-Gruppen am selben C-Atom sind instabil und spalten Wasser ab. Das erklärt, warum bestimmte Moleküle nicht existieren.
Siede- und Schmelztemperaturen von Alkoholen liegen höher als bei entsprechenden Alkanen wegen der Wasserstoffbrücken. Kurze Alkohole sind hydrophil (wasserlöslich), lange hydrophob (fettlöslich).
Oxidationsregel: Primäre Alkohole → Aldehyde → Carbonsäuren, sekundäre Alkohole → Ketone, tertiäre Alkohole oxidieren nicht!
Die Alkohol-Oxidation ist ein wichtiger Mechanismus. Primäre Alkohole bilden erst Aldehyde, dann Carbonsäuren. Sekundäre Alkohole werden zu Ketonen oxidiert.

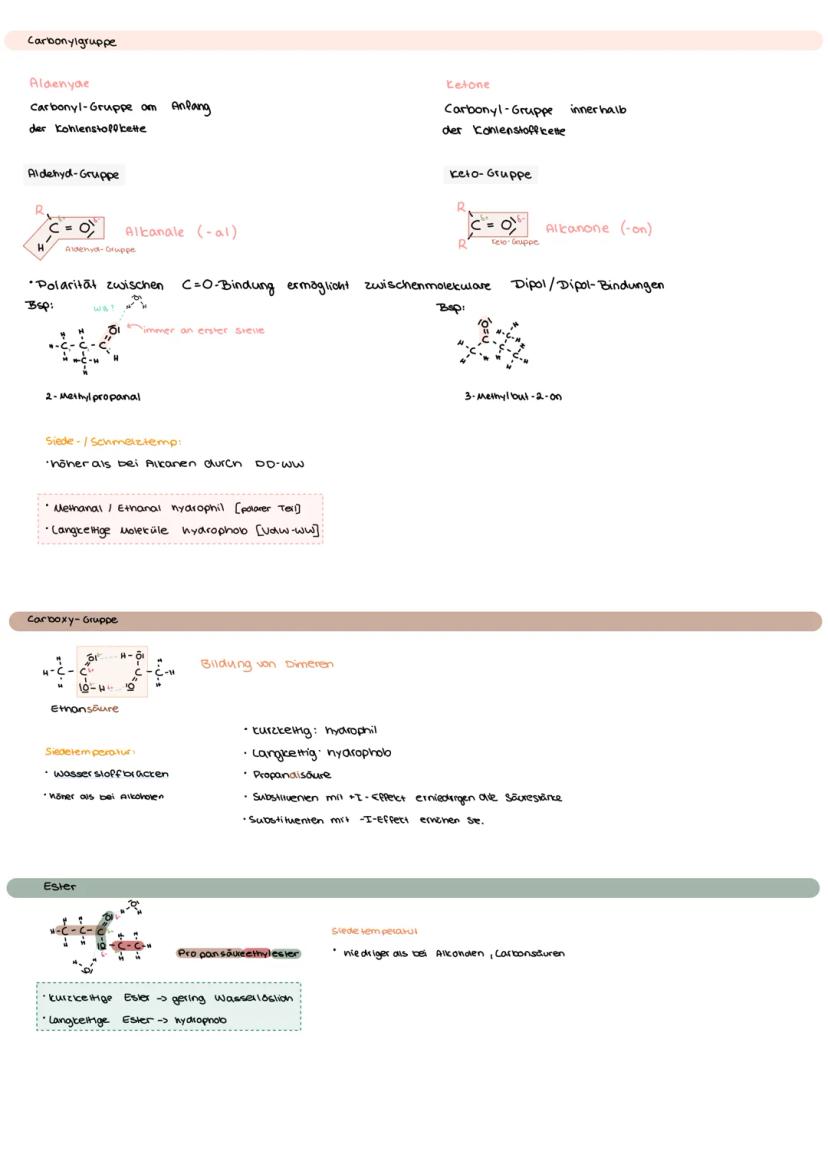
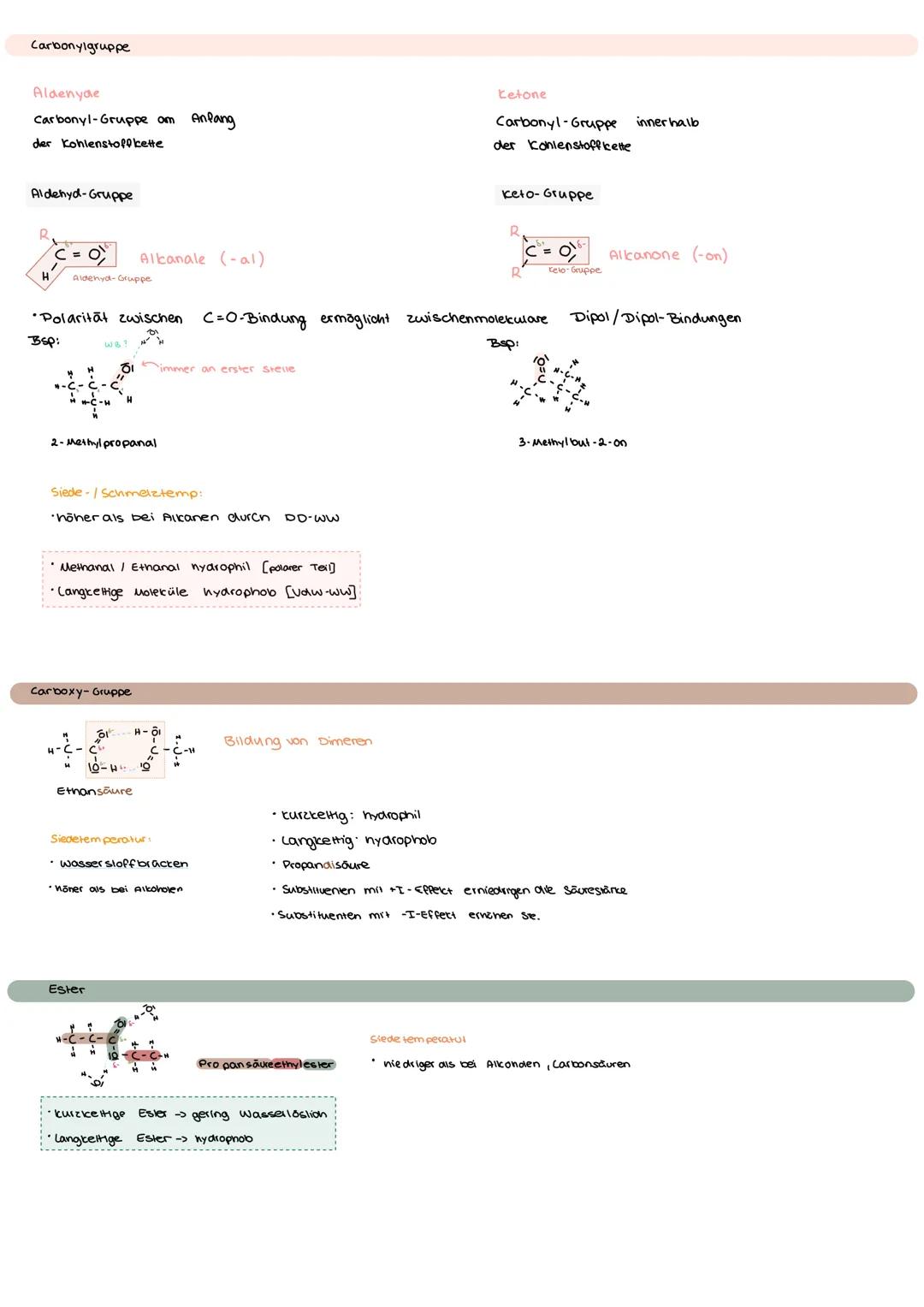
Aldehyde haben die Carbonyl-Gruppe am Kettenende , Ketone in der Kette . Die C=O-Bindung ist polar und ermöglicht Dipol-Dipol-Wechselwirkungen.
Carbonsäuren bilden durch Wasserstoffbrücken Dimere, was ihre hohen Siedetemperaturen erklärt. Substituenten mit -I-Effekt erhöhen die Säurestärke, solche mit +I-Effekt verringern sie.
Ester entstehen aus Carbonsäuren und Alkoholen. Sie haben niedrigere Siedetemperaturen als die entsprechenden Carbonsäuren, da keine Wasserstoffbrücken möglich sind.
Löslichkeitsregel: Kurze Carbonylverbindungen sind hydrophil durch die polare C=O-Gruppe, lange werden hydrophob durch die Alkylkette!
Die Polarität der Carbonyl-Gruppe macht das C-Atom partiell positiv (δ+) und das O-Atom partiell negativ (δ-). Das erklärt die typischen Additionsreaktionen.
Fette sind Triglyceride aus einem Glycerin-Molekül und drei Fettsäuren. Die Verknüpfung erfolgt über Esterbindungen zwischen den OH-Gruppen des Glycerins und den Carboxyl-Gruppen der Fettsäuren.
Gesättigte Fettsäuren ohne Doppelbindungen sind bei Raumtemperatur fest, ungesättigte mit Doppelbindungen flüssig. Der Grund: Gesättigte Ketten passen besser zusammen, haben mehr van-der-Waals-Wechselwirkungen.
Die Nomenklatur der Fettsäuren: C18:2 (9,12) bedeutet 18 C-Atome, 2 Doppelbindungen an Position 9 und 12. Die Zählung beginnt bei der Carboxyl-Gruppe.
Gesundheitstipp: Ungesättigte Fette sind gesünder - ihre unregelmäßige Struktur macht sie bei Körpertemperatur flüssiger!
ω-Fettsäuren werden vom Methylende her nummeriert. ω-3-Fettsäuren haben die erste Doppelbindung am 3. C-Atom vom Methylende - sie sind essentiell für den Menschen.
Alkane reagieren über radikalische Substitution (Sₙ), da sie nur C-H und C-C-Bindungen haben. UV-Licht spaltet Halogenmoleküle zu Radikalen, die dann H-Atome ersetzen.
Alkene mit ihrer C=C-Doppelbindung reagieren über elektrophile Addition (Aₑ). Elektrophile greifen die elektronenreiche Doppelbindung an. Die Umkehrreaktion ist die Eliminierung .
Alkohole können eliminiert oder oxidiert werden. Bei der Eliminierung entstehen Alkene und Wasser, bei der Oxidation Aldehyde, Ketone oder Carbonsäuren - je nach Alkohol-Typ.
Mechanismus-Merkhilfe: Gesättigte Verbindungen = Substitution, ungesättigte = Addition, funktionelle Gruppen = spezifische Reaktionen!
Ester bilden sich über Addition-Eliminierung zwischen Carbonsäuren und Alkoholen. Carbonylverbindungen entstehen durch Oxidation entsprechender Alkohole - ein wichtiger Syntheseweg in der organischen Chemie.
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Anna
@anna_299423
Die Welt der Atommodelle und chemischen Bindungen wird viel klarer, wenn du die Grundlagen verstehst. Von der Art, wie Elektronen um den Atomkern tanzen, bis hin zu den verschiedenen Bindungstypen – das alles bestimmt, wie sich Stoffe verhalten und warum... Mehr anzeigen

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Das Schalenmodell zeigt dir, wo sich Elektronen aufhalten. Die Formel 2n² verrät dir, wie viele Elektronen maximal in eine Schale passen: K-Schale (2 Elektronen), L-Schale (8 Elektronen), M-Schale (18 Elektronen) und so weiter. Das ist wie ein Apartment-Gebäude mit verschiedenen Stockwerken.
Beim Energiestufenmodell haben Elektronen verschiedene Energielevel. Je weiter außen, desto mehr Energie besitzen sie. Das erklärt, warum äußere Elektronen leichter abgegeben werden können.
Die Elektronenbesetzung folgt einer bestimmten Reihenfolge: erst s-Orbitale, dann p-, d- und f-Orbitale. Chlor schreibst du als 1s² 2s² 2p⁶ 3s² 3p⁵. Das sieht kompliziert aus, folgt aber einfachen Regeln.
Merktipp: Die Kastchenschreibweise hilft dir dabei, die Orbital-Reihenfolge zu visualisieren und Elektronenkonfigurationen schnell zu bestimmen.
Bei Lewisformeln zeichnest du Bindungen als Striche und freie Elektronenpaare als Punkte. Partialladungen entstehen, wenn Atome unterschiedlich stark an Elektronen ziehen.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Das Orbitalmodell beschreibt Elektronen nicht als Teilchen auf festen Bahnen, sondern als Wolken mit bestimmten Aufenthaltswahrscheinlichkeiten. Vier Quantenzahlen charakterisieren jeden Elektronenplatz komplett.
Die Hauptquantenzahl n entspricht der Periode im Periodensystem und bestimmt die Orbitalgröße. Die Nebenquantenzahl l definiert die Orbitalform: s-Orbitale sind kugelförmig, p-Orbitale hantelförmig, d-Orbitale doppelhantelförmig.
Die Magnetquantenzahl ml zeigt die räumliche Orientierung an. p-Orbitale gibt es dreimal (px, py, pz), d-Orbitale fünfmal. Die Spinquantenzahl s beschreibt die Drehrichtung der Elektronen .
Wichtig: Pro Orbital passen maximal 2 Elektronen mit entgegengesetztem Spin - das ist das Pauli-Prinzip!
Die Tabelle zeigt dir die maximale Elektronenanzahl pro Schale: K-Schale (2e⁻), L-Schale (8e⁻), M-Schale (18e⁻), N-Schale (32e⁻). Diese Zahlen ergeben sich aus der Anzahl verfügbarer Orbitale.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Ionenbindungen entstehen zwischen Metallen und Nichtmetallen. Metalle geben Elektronen ab (werden zu Kationen), Nichtmetalle nehmen sie auf (werden zu Anionen). Die entstehenden Salzgitter sind spröde, haben hohe Schmelzpunkte und leiten nur gelöst den Strom.
Bei metallischen Bindungen schwimmen Atomrümpfe in einem "Elektronensee". Diese frei beweglichen Elektronen erklären typische Metalleigenschaften: Glanz, elektrische Leitfähigkeit, Wärmeleitfähigkeit und Verformbarkeit.
Interessant ist die Temperaturabhängigkeit der Leitfähigkeit: Beim Abkühlen schwingen die Atomrümpfe weniger, stören die Elektronen weniger - der Widerstand sinkt, die Leitfähigkeit steigt.
Merkregel: Ionenbindungen = spröde Salze, Metallbindungen = verformbare Leiter, Elektronenpaarbindungen = Moleküle!
Die Gitterenergie bestimmt die Stabilität von Ionenverbindungen. Je größer diese Energie, desto höher sind Schmelz- und Siedepunkt der entstehenden Salze.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Elektronenpaarbindungen verbinden Nichtmetalle zu Molekülen. Dabei teilen sich Atome Elektronenpaare, um die Oktettregel zu erfüllen - jedes Atom möchte acht Außenelektronen haben wie die Edelgase.
Polare Moleküle entstehen durch unterschiedliche Elektronegativitäten. HCl ist polar , während H₂ unpolar ist . Der Dipol zeigt von δ+ zu δ-.
Die Molekülgeometrie hängt von bindenden und freien Elektronenpaaren ab. CH₄ ist tetraedrisch (109,5°), NH₃ trigonal pyramidal (107°), H₂O gewinkelt (104°). Diese Winkel sind prüfungsrelevant!
Praxistipp: CO₂ ist linear und unpolar, obwohl C=O-Bindungen polar sind - die Ladungsverschiebungen heben sich auf!
Molekülorbitale entstehen durch Überlappung von Atomorbitalen. σ-Bindungen sind stärker als π-Bindungen, was die Reaktivität von Doppel- und Dreifachbindungen erklärt.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Wasserstoffbrücken sind die stärksten zwischenmolekularen Kräfte. Sie entstehen zwischen H-Atomen und stark elektronegativen Atomen (F, O, N). Das erklärt, warum Wasser trotz geringer Molmasse einen hohen Siedepunkt hat.
Dipol-Dipol-Wechselwirkungen wirken zwischen polaren Molekülen wie HCl. Van-der-Waals-Kräfte gibt es bei allen Molekülen - sie entstehen durch temporäre Elektronenverschiebungen und werden stärker mit zunehmender Molekülgröße.
Die Faustregel für Löslichkeit: "Gleiches löst sich in Gleichem!" Polare Stoffe lösen sich in polaren Lösungsmitteln, unpolare in unpolaren. Ethanol mischt sich mit Wasser (beide polar), Fette nicht.
Klausurtipp: Je stärker die zwischenmolekularen Kräfte, desto höher Siede- und Schmelztemperatur!
Induktive Effekte beeinflussen die Elektronendichte. Der +I-Effekt schiebt Elektronen, der -I-Effekt zieht sie an. Das beeinflusst die Reaktivität von Carbenium-Ionen erheblich.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Radikalstabilität steigt mit der Anzahl der Alkylgruppen durch den +I-Effekt. Tertiäre Radikale sind stabiler als sekundäre, diese stabiler als primäre. Das erklärt, warum manche Reaktionen bevorzugt ablaufen.
Die Markovnikov-Regel besagt: Bei der Addition an unsymmetrische Doppelbindungen lagert sich das H-Atom an das C-Atom mit den meisten H-Atomen an. So entsteht das stabilste Carbenium-Ion.
Reaktivität hängt von der Elektronendichte an reaktiven Zentren ab. Elektronenziehende Gruppen erhöhen die Reaktivität von Carbonsäuren, während elektronenschiebende Gruppen sie verringern.
Wichtig: Die Stabilität von Carbenium-Ionen folgt der Reihenfolge: tertiär > sekundär > primär!
Carboxylationen sind wenig reaktiv, da die negative Ladung durch Resonanz stabilisiert wird. Je mehr elektronenziehende Gruppen, desto stärker die entsprechende Säure.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Alkohole enthalten die Hydroxy-Gruppe und folgen der Formel CₙH₂ₙ₊₁OH. Die Benennung erfolgt mit der Endung "-ol", wobei die OH-Gruppe die niedrigste Nummer erhält.
Die Erlenmeyer-Regel besagt: Verbindungen mit zwei OH-Gruppen am selben C-Atom sind instabil und spalten Wasser ab. Das erklärt, warum bestimmte Moleküle nicht existieren.
Siede- und Schmelztemperaturen von Alkoholen liegen höher als bei entsprechenden Alkanen wegen der Wasserstoffbrücken. Kurze Alkohole sind hydrophil (wasserlöslich), lange hydrophob (fettlöslich).
Oxidationsregel: Primäre Alkohole → Aldehyde → Carbonsäuren, sekundäre Alkohole → Ketone, tertiäre Alkohole oxidieren nicht!
Die Alkohol-Oxidation ist ein wichtiger Mechanismus. Primäre Alkohole bilden erst Aldehyde, dann Carbonsäuren. Sekundäre Alkohole werden zu Ketonen oxidiert.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Aldehyde haben die Carbonyl-Gruppe am Kettenende , Ketone in der Kette . Die C=O-Bindung ist polar und ermöglicht Dipol-Dipol-Wechselwirkungen.
Carbonsäuren bilden durch Wasserstoffbrücken Dimere, was ihre hohen Siedetemperaturen erklärt. Substituenten mit -I-Effekt erhöhen die Säurestärke, solche mit +I-Effekt verringern sie.
Ester entstehen aus Carbonsäuren und Alkoholen. Sie haben niedrigere Siedetemperaturen als die entsprechenden Carbonsäuren, da keine Wasserstoffbrücken möglich sind.
Löslichkeitsregel: Kurze Carbonylverbindungen sind hydrophil durch die polare C=O-Gruppe, lange werden hydrophob durch die Alkylkette!
Die Polarität der Carbonyl-Gruppe macht das C-Atom partiell positiv (δ+) und das O-Atom partiell negativ (δ-). Das erklärt die typischen Additionsreaktionen.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Fette sind Triglyceride aus einem Glycerin-Molekül und drei Fettsäuren. Die Verknüpfung erfolgt über Esterbindungen zwischen den OH-Gruppen des Glycerins und den Carboxyl-Gruppen der Fettsäuren.
Gesättigte Fettsäuren ohne Doppelbindungen sind bei Raumtemperatur fest, ungesättigte mit Doppelbindungen flüssig. Der Grund: Gesättigte Ketten passen besser zusammen, haben mehr van-der-Waals-Wechselwirkungen.
Die Nomenklatur der Fettsäuren: C18:2 (9,12) bedeutet 18 C-Atome, 2 Doppelbindungen an Position 9 und 12. Die Zählung beginnt bei der Carboxyl-Gruppe.
Gesundheitstipp: Ungesättigte Fette sind gesünder - ihre unregelmäßige Struktur macht sie bei Körpertemperatur flüssiger!
ω-Fettsäuren werden vom Methylende her nummeriert. ω-3-Fettsäuren haben die erste Doppelbindung am 3. C-Atom vom Methylende - sie sind essentiell für den Menschen.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Alkane reagieren über radikalische Substitution (Sₙ), da sie nur C-H und C-C-Bindungen haben. UV-Licht spaltet Halogenmoleküle zu Radikalen, die dann H-Atome ersetzen.
Alkene mit ihrer C=C-Doppelbindung reagieren über elektrophile Addition (Aₑ). Elektrophile greifen die elektronenreiche Doppelbindung an. Die Umkehrreaktion ist die Eliminierung .
Alkohole können eliminiert oder oxidiert werden. Bei der Eliminierung entstehen Alkene und Wasser, bei der Oxidation Aldehyde, Ketone oder Carbonsäuren - je nach Alkohol-Typ.
Mechanismus-Merkhilfe: Gesättigte Verbindungen = Substitution, ungesättigte = Addition, funktionelle Gruppen = spezifische Reaktionen!
Ester bilden sich über Addition-Eliminierung zwischen Carbonsäuren und Alkoholen. Carbonylverbindungen entstehen durch Oxidation entsprechender Alkohole - ein wichtiger Syntheseweg in der organischen Chemie.
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
10
Smart Tools NEU
Verwandle diesen Lernzettel in: ✓ 50+ Übungsfragen ✓ Interaktive Karteikarten ✓ Komplette Probeklausur ✓ Aufsatzgliederungen
Entdecken Sie die Grundlagen der Chemie mit diesem Lernmaterial. Erfahren Sie mehr über Atome, Moleküle, chemische Bindungen, Reaktionen (Redox, Säure-Base) und zwischenmolekulare Wechselwirkungen. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Entdecken Sie die Reaktionen von Säuren mit Wasser und unedlen Metallen sowie die Eigenschaften alkalischer Lösungen. Diese Zusammenfassung enthält wichtige Reaktionsgleichungen, Definitionen und Beispiele für Säuren wie HCl, H2SO4 und NaOH. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Erforschen Sie den Mechanismus der elektrophilen Substitution bei der Bromierung von Benzol. Diese Zusammenfassung behandelt die Bildung des π-Komplexes, den elektrophilen Angriff, die Mesomerie des Zwischenprodukts und die Rückbildung des Katalysators. Ideal für Chemie-Studierende, die die Reaktionsmechanismen verstehen möchten.
Dieser Lernzettel bietet eine umfassende Übersicht über Alkene, einschließlich ihrer homologen Reihe, Benennungsregeln, Isomerie (cis/trans) und der elektrophilen Addition. Erfahren Sie mehr über die Reaktionsmechanismen und die Struktur-Eigenschafts-Beziehungen von Alkenen. Ideal für die Vorbereitung auf Klausuren.
Entdecken Sie die Nachweisverfahren für Chlorid-, Sulfat-, Wasserstoff- und Hydroxid-Ionen in wässrigen Lösungen. Diese Zusammenfassung behandelt die chemischen Reaktionen mit Silbernitrat, Bariumchlorid und Universalindikatoren, die zur Identifizierung dieser Ionen verwendet werden. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Dieser Lernzettel bietet eine umfassende Erklärung der BRINCLHOF Regel, die die Bildung von zweiatomigen Molekülen für bestimmte Elemente wie Brom, Iod, Stickstoff, Chlor, Wasserstoff, Sauerstoff und Fluor beschreibt. Ideal für Chemie-Studierende, die die Grundlagen der Molekülstruktur und Bindungstypen verstehen möchten.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer