Chemie in der 13. Klasse - hier geht's ans Eingemachte!... Mehr anzeigen
Chemie LK Abitur Lernzettel Q1 2024: Wichtige Themen







Orbitalmodell und Quantenzahlen
Stell dir vor, Elektronen sind wie Wellen in einem Kasten - genau das beschreibt das Orbitalmodell. Es zeigt dir, wo sich Elektronen mit welcher Wahrscheinlichkeit aufhalten.
Die Quantenzahlen sind wie die Adresse jedes Elektrons. Die Hauptquantenzahl n gibt das Energieniveau an , während die Nebenquantenzahl l die Form bestimmt: s-Orbitale sind kugelförmig , p-Orbitale hantelförmig .
Elektronenverteilung folgt klaren Regeln: Erst werden energieärmere Orbitale gefüllt, pro Orbital passen maximal zwei Elektronen mit unterschiedlichem Spin. Die Hund'sche Regel besagt, dass entartete Orbitale erst einzeln, dann paarweise besetzt werden.
Merktipp: Die Reihenfolge 1s, 2s, 2p, 3s, 3p, 4s, 3d... bestimmt die Elektronenkonfiguration aller Atome!
Molekülorbitalmodell und Hybridisierung
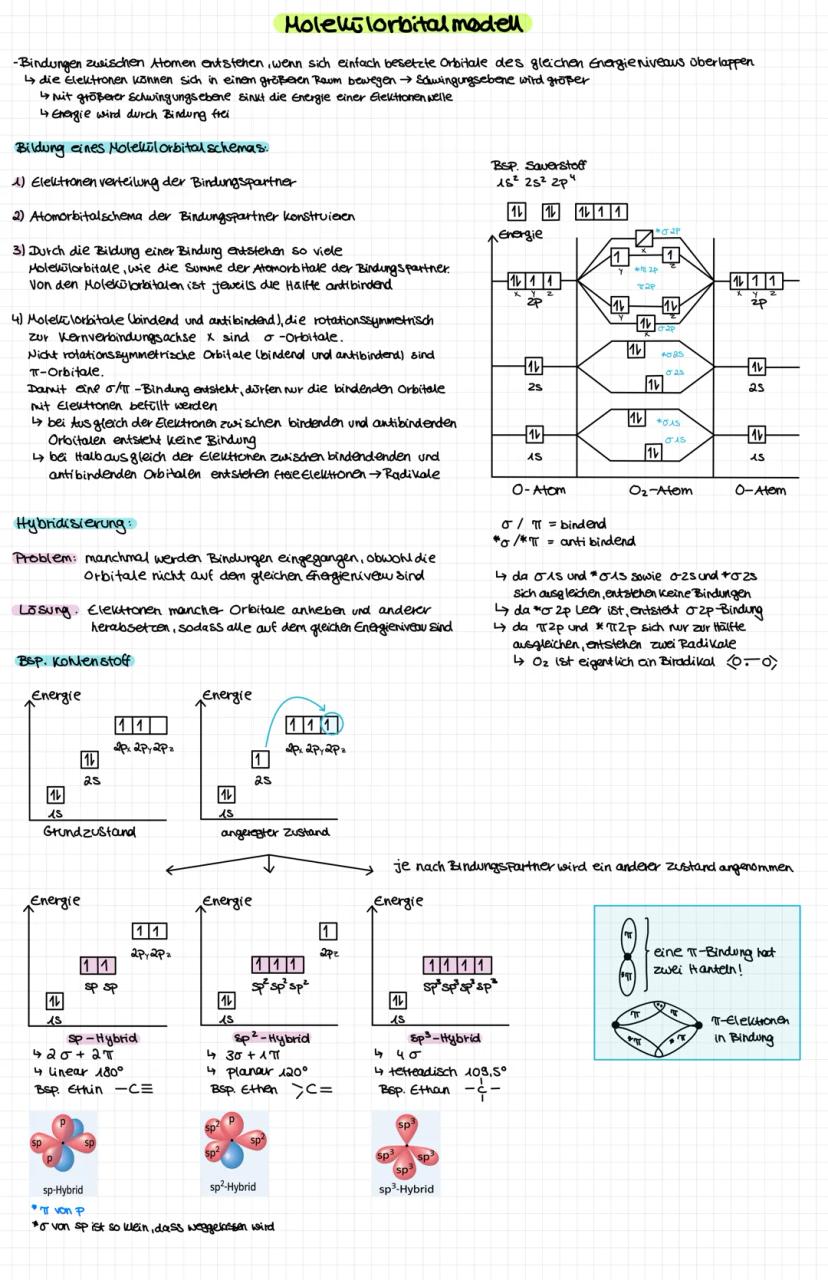
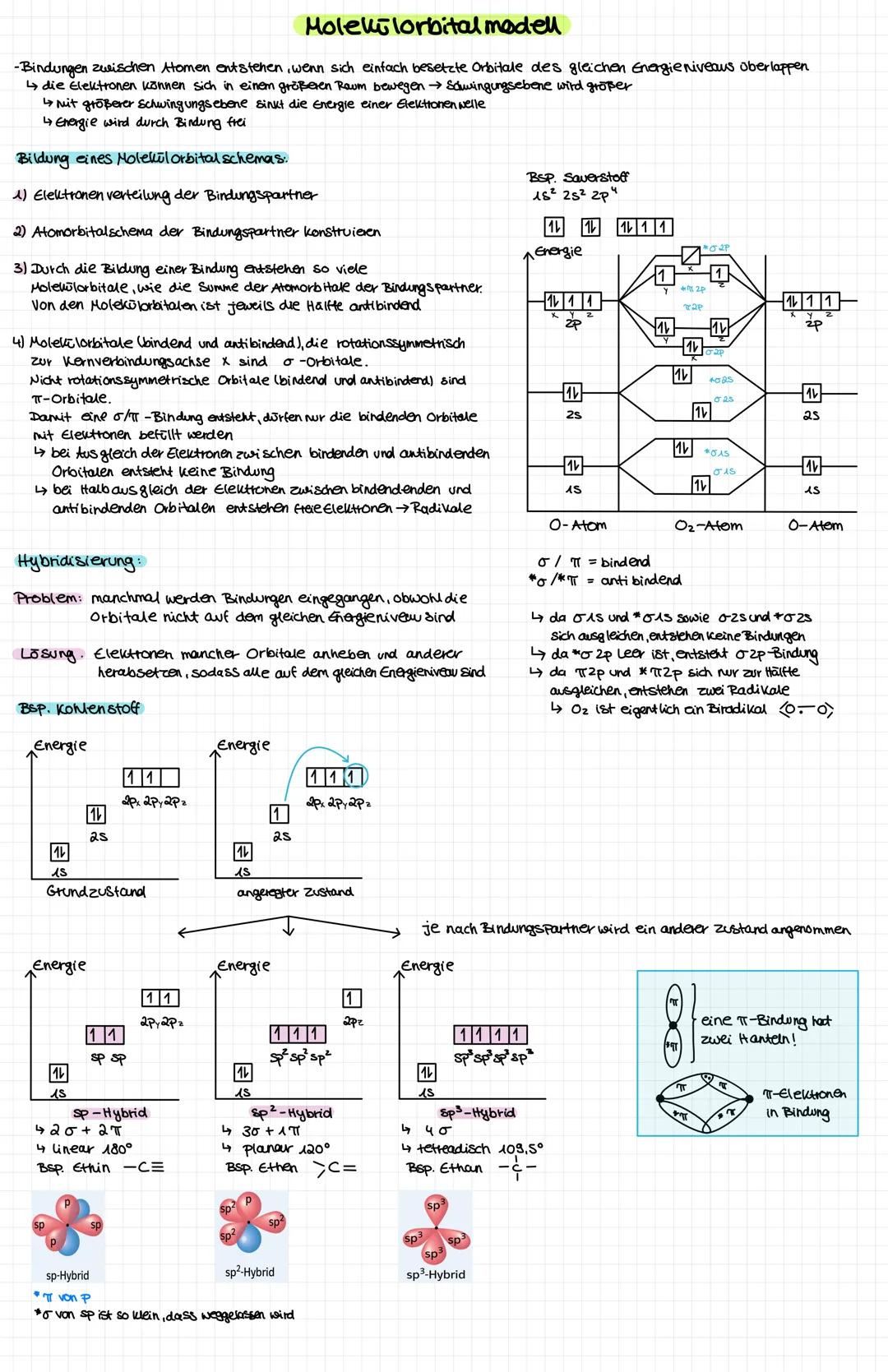
Wenn Atome Bindungen eingehen, entstehen Molekülorbitale - das ist wie Zimmer teilen, nur energetisch günstiger! Aus zwei Atomorbitalen werden immer ein bindendes und ein antibindendes Molekülorbital.
Hybridisierung erklärt, warum Kohlenstoff vier gleichwertige Bindungen eingehen kann. Bei sp³-Hybridisierung entstehen tetraedrische Winkel (109,5°), bei sp² planare Strukturen (120°) und bei sp lineare Anordnungen (180°).
σ-Bindungen sind rotationssymmetrisch zur Kernverbindungsachse, π-Bindungen haben zwei "Hanteln" ober- und unterhalb. Doppelbindungen bestehen aus einer σ- und einer π-Bindung.
Praxistipp: Die Hybridisierung bestimmt die Molekülgeometrie - wichtig für alle organischen Verbindungen!
Alkane und Alkene - die Grundbausteine
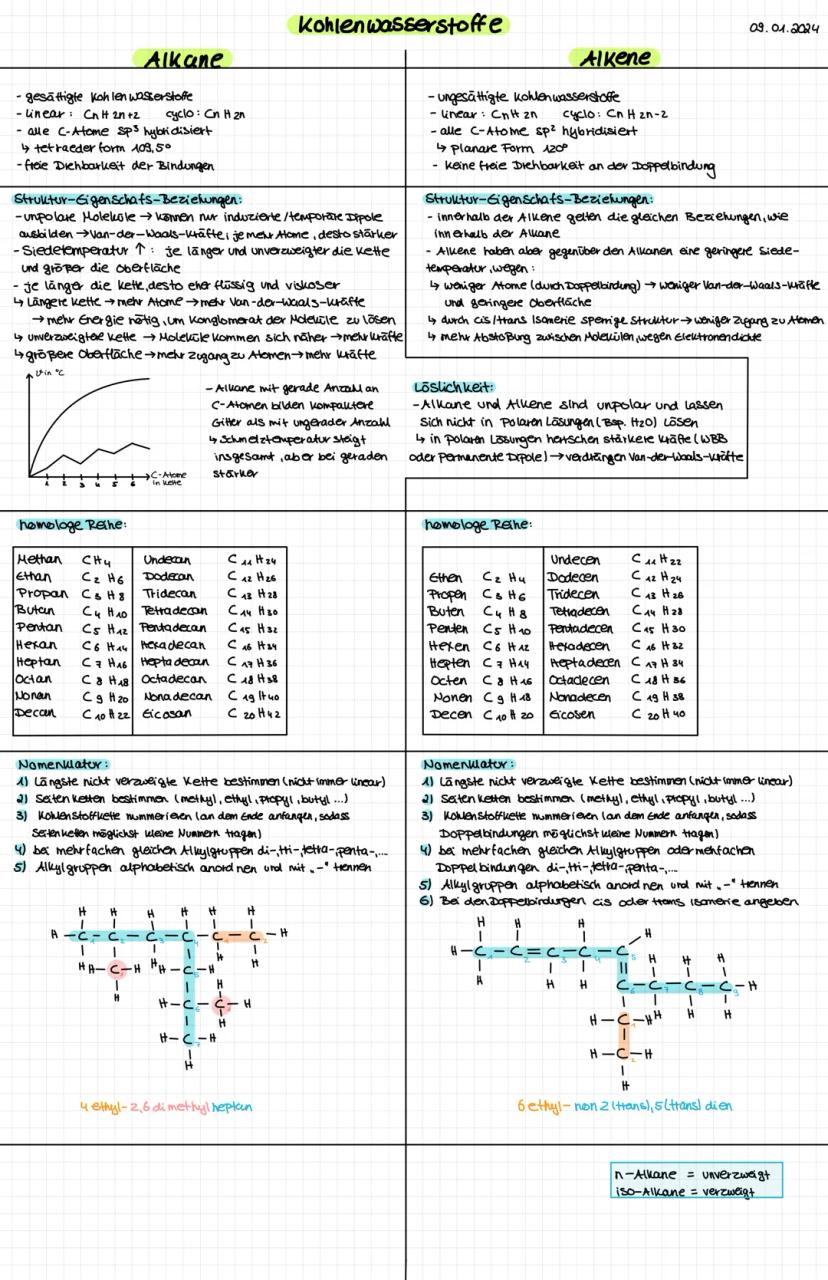
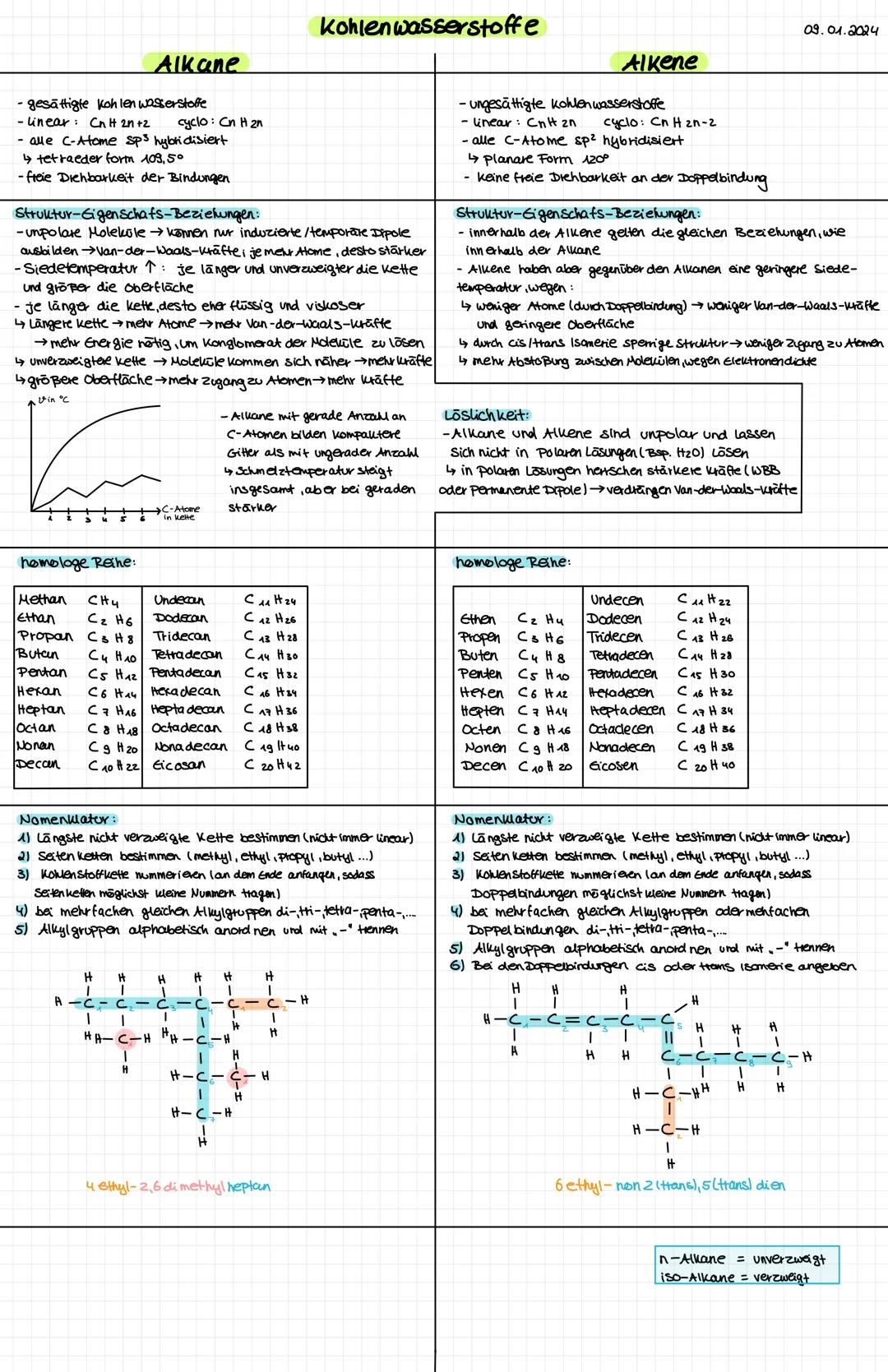
Alkane sind gesättigte Kohlenwasserstoffe mit der Formel CₙH₂ₙ₊₂. Sie haben nur Einfachbindungen und sind daher relativ reaktionsträge. Alle C-Atome sind sp³-hybridisiert mit 109,5° Bindungswinkeln.
Alkene enthalten mindestens eine Doppelbindung (CₙH₂ₙ) und sind deutlich reaktiver. Die cis/trans-Isomerie spielt eine wichtige Rolle - cis bedeutet "auf derselben Seite", trans "auf gegenüberliegenden Seiten".
Die Siedetemperaturen steigen mit der Kettenlänge durch stärkere Van-der-Waals-Kräfte. Verzweigungen senken die Siedetemperatur, da sich die Moleküle schlechter anlagern können.
Klausurtipp: Nomenklatur systematisch angehen - längste Kette finden, nummerieren, Substituenten alphabetisch ordnen!

Reaktionsmechanismen verstehen
Radikalische Substitution bei Alkanen läuft in drei Stufen ab: Start (Radikalbildung durch UV), Kettenfortpflanzung und Kettenabbruch (Radikale reagieren miteinander).
Elektrophile Addition bei Alkenen erfolgt über einen π-Komplex, dann σ-Komplex als Zwischenstufe und schließlich Rückseitenangriff. Der Bromentest nutzt diese Reaktion - Bromlösung wird entfärbt.
Induktive Effekte bestimmen die Reaktivität: +I-Effekte (Alkylgruppen) schieben Elektronen, -I-Effekte (Halogene) ziehen sie ab. Das beeinflusst die Stabilität von Zwischenstufen erheblich.
Verstehenstipp: Zeichne immer die Elektronenbewegung mit Pfeilen - so wird der Mechanismus klar!

Regioselektivität und Eliminierung
Die Markovnikov-Regel sagt vorher, welches Produkt bei HX-Addition hauptsächlich entsteht: Das Proton lagert sich an das C-Atom mit mehr H-Atomen an, weil das entstehende Carbokation durch +I-Effekte stabilisiert wird.
Carbokationen haben eine Stabilitätsreihe: tertiär > sekundär > primär. Je mehr Alkylreste, desto stabiler durch Elektronendelokalisierung.
Eliminierungsreaktionen sind das Gegenteil von Additionen - aus Halogenalkanen entstehen wieder Alkene. Die Reaktion läuft bevorzugt über stabilere Carbokationen.
Eselsbrücke: "Gleiches gesellt sich zu Gleichem" - H⁺ geht zu vielen H-Atomen (Markovnikov)!

Oxidationszahlen und Verbrennungsreaktionen
Oxidationszahlen zeigen den "Elektronenzustand" eines Atoms im Vergleich zum neutralen Atom. In organischen Molekülen: Außenelektronen minus Bindungselektronen (je nach Elektronegativität).
Verbrennung von Kohlenwasserstoffen ist stark exotherm und läuft nach dem Schema: CₓHᵧ + O₂ → CO₂ + H₂O. Je ungesättigter, desto höher die Aktivierungsenergie.
Nachweisreaktionen: H₂O mit weißem Kupfersulfat (wird blau), CO₂ mit Kalkwasser (wird trüb). Diese Reaktionen nutzt du im Labor ständig.
Laborpraxis: Immer beide Verbrennungsprodukte nachweisen - nur so bist du sicher!
Aromaten - die besonderen Ringsysteme
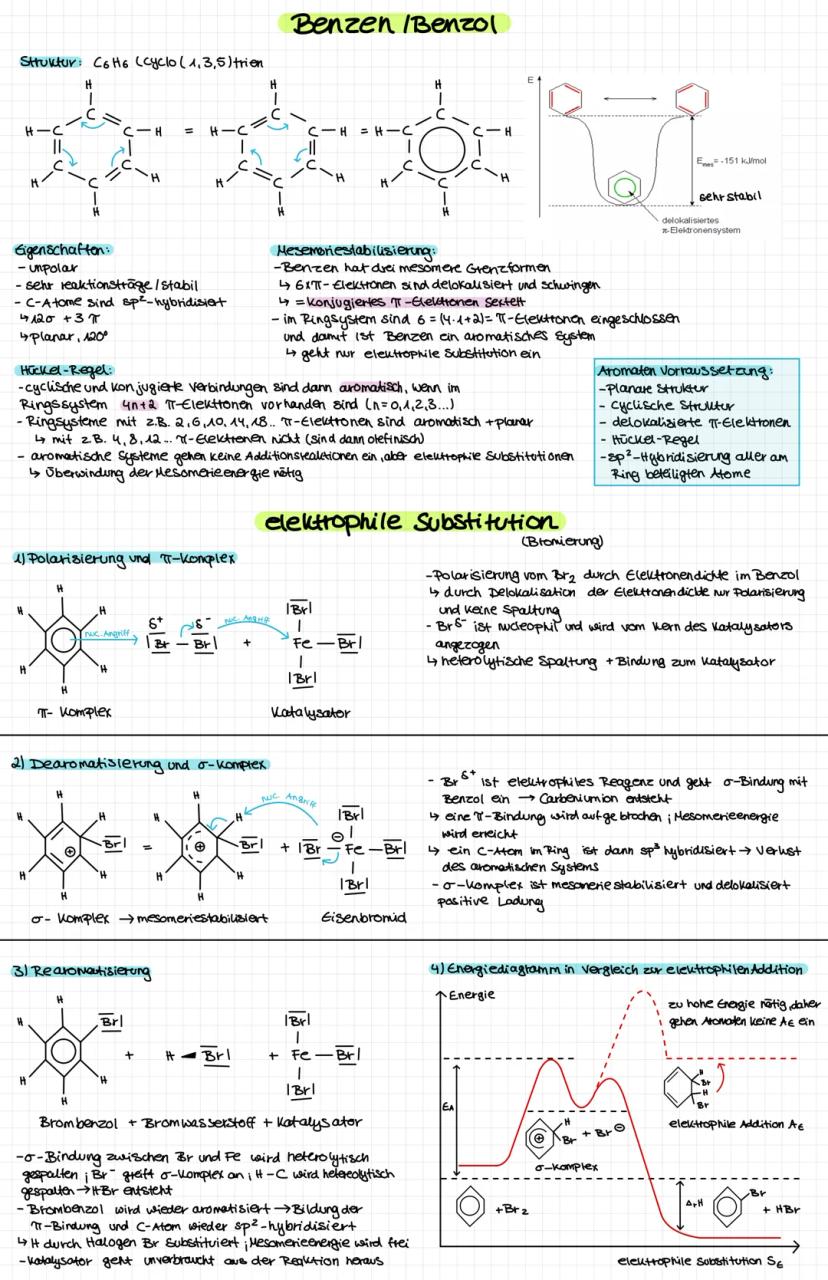
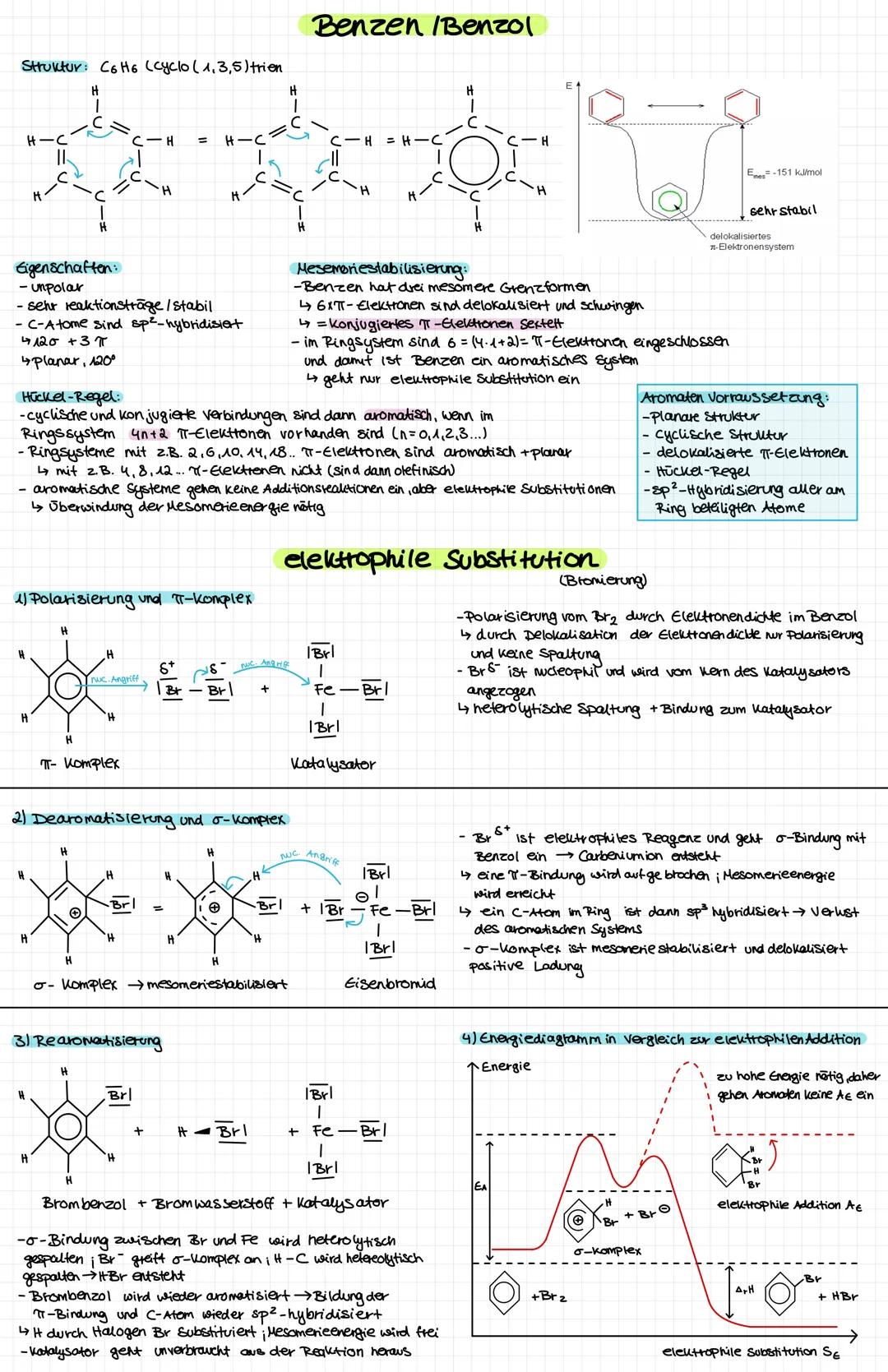
Benzol (C₆H₆) ist der Prototyp aromatischer Verbindungen. Die Hückel-Regel erklärt seine besondere Stabilität durch Mesomerie.
Elektrophile Substitution ist die typische Reaktion von Aromaten. Der Mechanismus läuft über π-Komplex, σ-Komplex (Dearomatisierung) und Rearomatisierung. Die Mesomerieenergie muss überwunden werden.
Aromaten sind sehr reaktionsträge, weil das delokalisierte π-Elektronensystem energetisch günstig ist. Additionsreaktionen würden dieses System zerstören.
Wichtig für Klausuren: Aromaten = planar, cyclisch, konjugiert, 4n+2 π-Elektronen!

Alkanole - die vielseitigen Alkohole
Alkanole entstehen, wenn H-Atome in Alkanen durch OH-Gruppen ersetzt werden. Die Hydroxylgruppe macht sie polar und wasserlöslich durch Wasserstoffbrückenbindungen.
Struktur-Eigenschafts-Beziehungen: Je länger die Kohlenstoffkette, desto lipophiler. Je mehr OH-Gruppen, desto hydrophiler. Das beeinflusst Löslichkeit und Siedetemperatur drastisch.
Konstitutionsisomerie unterscheidet primäre (OH am Kettenende), sekundäre (OH in der Mitte) und tertiäre Alkohole (OH am verzweigten C). Das bestimmt ihre Reaktivität.
Alltagsbezug: Ethanol, Glycerin, Methanol - Alkohole begegnen dir überall!

Oxidationsreaktionen der Alkohole
Partielle Oxidation mit Kupferoxid oder Kaliumpermanganat folgt klaren Regeln: Primäre Alkohole werden zu Aldehyden, dann zu Carbonsäuren. Sekundäre werden zu Ketonen, tertiäre oxidieren nicht.
Die Redoxgleichungen musst du systematisch aufstellen: Oxidationsstufen bestimmen, Teilreaktionen formulieren, Elektronen ausgleichen. In saurer Lösung entstehen andere Produkte als in basischer.
Permanganatreaktionen erkennst du an den Farbwechseln: violett (MnO₄⁻) → grün (MnO₄²⁻) → braun (MnO₂). Das ist gleichzeitig ein Nachweis für die Oxidation.
Übungstipp: Oxidationsreaktionen Schritt für Schritt durchgehen - dann wird's routine!
Carbonylverbindungen - Aldehyde und Ketone
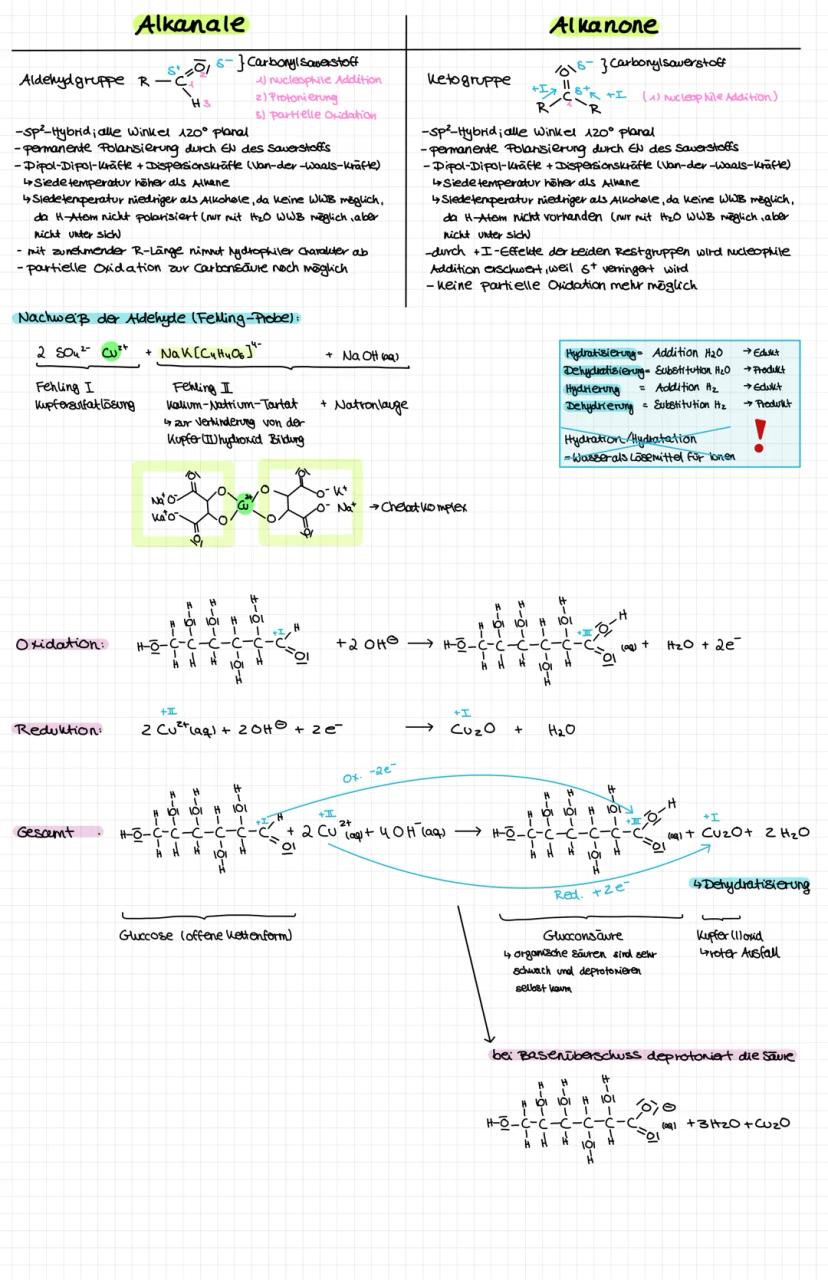
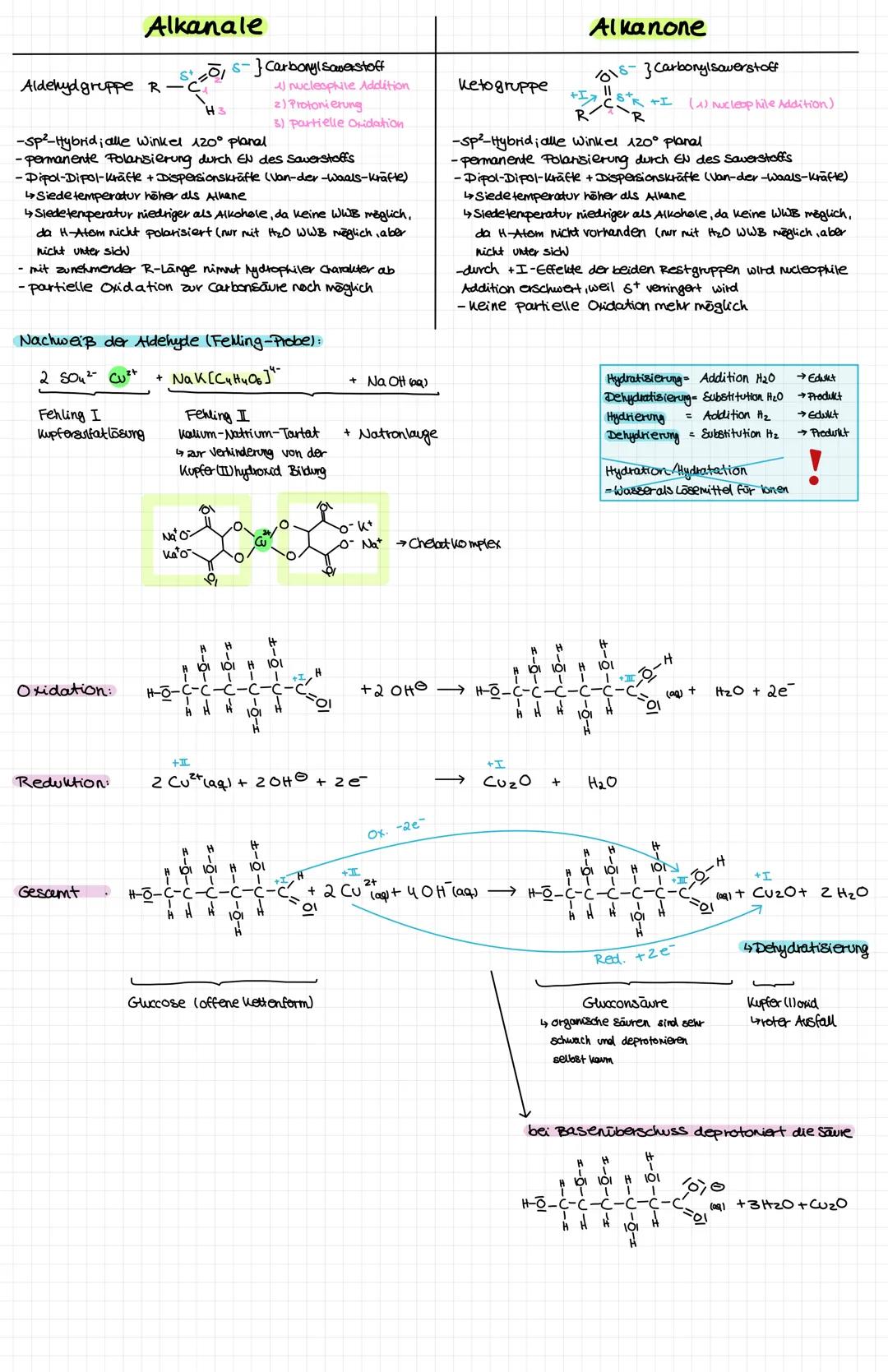
Alkanale (Aldehyde) haben die Carbonylgruppe am Kettenende , Alkanone (Ketone) in der Kette . Die Carbonylgruppe ist stark polar durch den Elektronegativitätsunterschied.
Nucleophile Addition ist die typische Reaktion - Nucleophile greifen am positiv polarisierten Kohlenstoff an. Bei Ketonen ist das schwieriger wegen der +I-Effekte beider Alkylreste.
Fehling-Probe weist Aldehyde nach: Cu²⁺ (blau) wird zu Cu₂O (rotbraun) reduziert, während der Aldehyd zur Carbonsäure oxidiert wird. Ketone reagieren nicht.
Mechanismus-Tipp: Immer erst die Polarität der Carbonylgruppe erkennen, dann den nucleophilen Angriff!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Alcohols
9Oxidation und Alkanole
Entdecken Sie die Grundlagen der Oxidation von Alkoholen, die Nomenklatur von Alkanolen, Alkanalen und Alkanonen sowie die Siedetemperatur und Löslichkeit in organischer Chemie. Diese Zusammenfassung bietet einen klaren Überblick über wichtige Konzepte wie Oxidationszahlen, nucleophile Substitution und die Eigenschaften von Carbonsäuren. Ideal für Studierende der organischen Chemie.
Alkohole und ihre Derivate
Entdecken Sie die Eigenschaften und Unterschiede zwischen Alkoholen, Aldehyden und Ketonen. Diese Zusammenfassung behandelt die Nomenklatur, Nachweisreaktionen wie die Fehling-Probe, Oxidationsprozesse und die Löslichkeit in Wasser. Ideal für Chemie-Studierende, die ein tiefes Verständnis für organische Verbindungen entwickeln möchten.
Alkanole: Struktur und Eigenschaften
Entdecken Sie die Welt der Alkanole! Diese Zusammenfassung behandelt die homologe Reihe, funktionelle Gruppen, Nomenklatur, sowie primäre, sekundäre und tertiäre Alkohole. Erfahren Sie mehr über mehrwertige Alkohole und deren Löslichkeit in Wasser. Ideal für Chemie-Studierende, die ein tieferes Verständnis für organische Verbindungen entwickeln möchten.
Oxidationszahlen und Organische Chemie
Entdecken Sie die Regeln zur Ermittlung von Oxidationszahlen und die Grundlagen der organischen Chemie, einschließlich Alkane, Alkanole, Alkanale, Alkanone und Carbonsäuren. Lernen Sie die funktionellen Gruppen, Isomere, Redoxreaktionen und die Bedeutung von Siedepunkten und Löslichkeit. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemische Verbindungen: Alkane & Aldehyde
Entdecken Sie die Eigenschaften, Benennung und Löslichkeit von Alkanen, Alkoholen, Aldehyden und Ketonen. Dieser Lernzettel bietet eine umfassende Übersicht über Polarität, intermolekulare Kräfte und Siedepunkte, ideal für die Klausurvorbereitung in Chemie.
Nukleophile Substitution & Alkanole
Entdecken Sie die Grundlagen der nukleophilen Substitution, die Eigenschaften und Nomenklatur von Alkanolen sowie die Reaktionen von Aldehyden und Ketonen. Diese Zusammenfassung behandelt wichtige Konzepte wie die Fehling-Probe, mehrwertige Alkohole, Dipol-Wechselwirkungen und Wasserstoffbrückenbindungen. Ideal für Chemie-Abiturienten.
Alkanole: Eigenschaften & Struktur
Entdecken Sie die Welt der Alkanole, einschließlich ihrer homologen Reihe, Isomerie, alkoholischer Gärung und Destillation. Erfahren Sie mehr über die funktionelle Hydroxylgruppe, die Unterschiede zwischen lipophilen und hydrophoben Stoffen sowie die Eigenschaften mehrwertiger Alkohole. Ideal für Chemie-Studierende, die sich mit der Struktur und den Eigenschaften von Alkanolen vertraut machen möchten.
Eigenschaften organischer Verbindungen
Entdecken Sie die Eigenschaften und Reaktionen von organischen Stoffklassen wie Alkoholen, Aldehyden, Ketonen, Carbonsäuren und Estern. Diese Zusammenfassung bietet einen Überblick über ihre Struktur, Löslichkeit, Siedepunkte und charakteristische Reaktionen, einschließlich Veresterung und Oxidation. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Homologe Reihe der Alkanole
Entdecken Sie die homologe Reihe der Alkanole, einschließlich Methanol und Ethanol. Lernen Sie die Struktur, Eigenschaften, Herstellung und Nomenklatur von Alkanolen kennen. Diese Zusammenfassung bietet einen klaren Überblick über die verschiedenen Alkanole, ihre Siedepunkte und die Unterschiede zwischen primären, sekundären und tertiären Alkanolen. Ideal für Studierende der organischen Chemie.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Chemie LK Abitur Lernzettel Q1 2024: Wichtige Themen
Chemie in der 13. Klasse - hier geht's ans Eingemachte! Du wirst das Orbitalmodell verstehen, komplexe Moleküle bauen und Reaktionsmechanismen durchschauen. Das klingt komplizierter als es ist - mit den richtigen Konzepten wird's richtig spannend.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Orbitalmodell und Quantenzahlen
Stell dir vor, Elektronen sind wie Wellen in einem Kasten - genau das beschreibt das Orbitalmodell. Es zeigt dir, wo sich Elektronen mit welcher Wahrscheinlichkeit aufhalten.
Die Quantenzahlen sind wie die Adresse jedes Elektrons. Die Hauptquantenzahl n gibt das Energieniveau an , während die Nebenquantenzahl l die Form bestimmt: s-Orbitale sind kugelförmig , p-Orbitale hantelförmig .
Elektronenverteilung folgt klaren Regeln: Erst werden energieärmere Orbitale gefüllt, pro Orbital passen maximal zwei Elektronen mit unterschiedlichem Spin. Die Hund'sche Regel besagt, dass entartete Orbitale erst einzeln, dann paarweise besetzt werden.
Merktipp: Die Reihenfolge 1s, 2s, 2p, 3s, 3p, 4s, 3d... bestimmt die Elektronenkonfiguration aller Atome!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Molekülorbitalmodell und Hybridisierung
Wenn Atome Bindungen eingehen, entstehen Molekülorbitale - das ist wie Zimmer teilen, nur energetisch günstiger! Aus zwei Atomorbitalen werden immer ein bindendes und ein antibindendes Molekülorbital.
Hybridisierung erklärt, warum Kohlenstoff vier gleichwertige Bindungen eingehen kann. Bei sp³-Hybridisierung entstehen tetraedrische Winkel (109,5°), bei sp² planare Strukturen (120°) und bei sp lineare Anordnungen (180°).
σ-Bindungen sind rotationssymmetrisch zur Kernverbindungsachse, π-Bindungen haben zwei "Hanteln" ober- und unterhalb. Doppelbindungen bestehen aus einer σ- und einer π-Bindung.
Praxistipp: Die Hybridisierung bestimmt die Molekülgeometrie - wichtig für alle organischen Verbindungen!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Alkane und Alkene - die Grundbausteine
Alkane sind gesättigte Kohlenwasserstoffe mit der Formel CₙH₂ₙ₊₂. Sie haben nur Einfachbindungen und sind daher relativ reaktionsträge. Alle C-Atome sind sp³-hybridisiert mit 109,5° Bindungswinkeln.
Alkene enthalten mindestens eine Doppelbindung (CₙH₂ₙ) und sind deutlich reaktiver. Die cis/trans-Isomerie spielt eine wichtige Rolle - cis bedeutet "auf derselben Seite", trans "auf gegenüberliegenden Seiten".
Die Siedetemperaturen steigen mit der Kettenlänge durch stärkere Van-der-Waals-Kräfte. Verzweigungen senken die Siedetemperatur, da sich die Moleküle schlechter anlagern können.
Klausurtipp: Nomenklatur systematisch angehen - längste Kette finden, nummerieren, Substituenten alphabetisch ordnen!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Reaktionsmechanismen verstehen
Radikalische Substitution bei Alkanen läuft in drei Stufen ab: Start (Radikalbildung durch UV), Kettenfortpflanzung und Kettenabbruch (Radikale reagieren miteinander).
Elektrophile Addition bei Alkenen erfolgt über einen π-Komplex, dann σ-Komplex als Zwischenstufe und schließlich Rückseitenangriff. Der Bromentest nutzt diese Reaktion - Bromlösung wird entfärbt.
Induktive Effekte bestimmen die Reaktivität: +I-Effekte (Alkylgruppen) schieben Elektronen, -I-Effekte (Halogene) ziehen sie ab. Das beeinflusst die Stabilität von Zwischenstufen erheblich.
Verstehenstipp: Zeichne immer die Elektronenbewegung mit Pfeilen - so wird der Mechanismus klar!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Regioselektivität und Eliminierung
Die Markovnikov-Regel sagt vorher, welches Produkt bei HX-Addition hauptsächlich entsteht: Das Proton lagert sich an das C-Atom mit mehr H-Atomen an, weil das entstehende Carbokation durch +I-Effekte stabilisiert wird.
Carbokationen haben eine Stabilitätsreihe: tertiär > sekundär > primär. Je mehr Alkylreste, desto stabiler durch Elektronendelokalisierung.
Eliminierungsreaktionen sind das Gegenteil von Additionen - aus Halogenalkanen entstehen wieder Alkene. Die Reaktion läuft bevorzugt über stabilere Carbokationen.
Eselsbrücke: "Gleiches gesellt sich zu Gleichem" - H⁺ geht zu vielen H-Atomen (Markovnikov)!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Oxidationszahlen und Verbrennungsreaktionen
Oxidationszahlen zeigen den "Elektronenzustand" eines Atoms im Vergleich zum neutralen Atom. In organischen Molekülen: Außenelektronen minus Bindungselektronen (je nach Elektronegativität).
Verbrennung von Kohlenwasserstoffen ist stark exotherm und läuft nach dem Schema: CₓHᵧ + O₂ → CO₂ + H₂O. Je ungesättigter, desto höher die Aktivierungsenergie.
Nachweisreaktionen: H₂O mit weißem Kupfersulfat (wird blau), CO₂ mit Kalkwasser (wird trüb). Diese Reaktionen nutzt du im Labor ständig.
Laborpraxis: Immer beide Verbrennungsprodukte nachweisen - nur so bist du sicher!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Aromaten - die besonderen Ringsysteme
Benzol (C₆H₆) ist der Prototyp aromatischer Verbindungen. Die Hückel-Regel erklärt seine besondere Stabilität durch Mesomerie.
Elektrophile Substitution ist die typische Reaktion von Aromaten. Der Mechanismus läuft über π-Komplex, σ-Komplex (Dearomatisierung) und Rearomatisierung. Die Mesomerieenergie muss überwunden werden.
Aromaten sind sehr reaktionsträge, weil das delokalisierte π-Elektronensystem energetisch günstig ist. Additionsreaktionen würden dieses System zerstören.
Wichtig für Klausuren: Aromaten = planar, cyclisch, konjugiert, 4n+2 π-Elektronen!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Alkanole - die vielseitigen Alkohole
Alkanole entstehen, wenn H-Atome in Alkanen durch OH-Gruppen ersetzt werden. Die Hydroxylgruppe macht sie polar und wasserlöslich durch Wasserstoffbrückenbindungen.
Struktur-Eigenschafts-Beziehungen: Je länger die Kohlenstoffkette, desto lipophiler. Je mehr OH-Gruppen, desto hydrophiler. Das beeinflusst Löslichkeit und Siedetemperatur drastisch.
Konstitutionsisomerie unterscheidet primäre (OH am Kettenende), sekundäre (OH in der Mitte) und tertiäre Alkohole (OH am verzweigten C). Das bestimmt ihre Reaktivität.
Alltagsbezug: Ethanol, Glycerin, Methanol - Alkohole begegnen dir überall!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Oxidationsreaktionen der Alkohole
Partielle Oxidation mit Kupferoxid oder Kaliumpermanganat folgt klaren Regeln: Primäre Alkohole werden zu Aldehyden, dann zu Carbonsäuren. Sekundäre werden zu Ketonen, tertiäre oxidieren nicht.
Die Redoxgleichungen musst du systematisch aufstellen: Oxidationsstufen bestimmen, Teilreaktionen formulieren, Elektronen ausgleichen. In saurer Lösung entstehen andere Produkte als in basischer.
Permanganatreaktionen erkennst du an den Farbwechseln: violett (MnO₄⁻) → grün (MnO₄²⁻) → braun (MnO₂). Das ist gleichzeitig ein Nachweis für die Oxidation.
Übungstipp: Oxidationsreaktionen Schritt für Schritt durchgehen - dann wird's routine!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Carbonylverbindungen - Aldehyde und Ketone
Alkanale (Aldehyde) haben die Carbonylgruppe am Kettenende , Alkanone (Ketone) in der Kette . Die Carbonylgruppe ist stark polar durch den Elektronegativitätsunterschied.
Nucleophile Addition ist die typische Reaktion - Nucleophile greifen am positiv polarisierten Kohlenstoff an. Bei Ketonen ist das schwieriger wegen der +I-Effekte beider Alkylreste.
Fehling-Probe weist Aldehyde nach: Cu²⁺ (blau) wird zu Cu₂O (rotbraun) reduziert, während der Aldehyd zur Carbonsäure oxidiert wird. Ketone reagieren nicht.
Mechanismus-Tipp: Immer erst die Polarität der Carbonylgruppe erkennen, dann den nucleophilen Angriff!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Alcohols
9Oxidation und Alkanole
Entdecken Sie die Grundlagen der Oxidation von Alkoholen, die Nomenklatur von Alkanolen, Alkanalen und Alkanonen sowie die Siedetemperatur und Löslichkeit in organischer Chemie. Diese Zusammenfassung bietet einen klaren Überblick über wichtige Konzepte wie Oxidationszahlen, nucleophile Substitution und die Eigenschaften von Carbonsäuren. Ideal für Studierende der organischen Chemie.
Alkohole und ihre Derivate
Entdecken Sie die Eigenschaften und Unterschiede zwischen Alkoholen, Aldehyden und Ketonen. Diese Zusammenfassung behandelt die Nomenklatur, Nachweisreaktionen wie die Fehling-Probe, Oxidationsprozesse und die Löslichkeit in Wasser. Ideal für Chemie-Studierende, die ein tiefes Verständnis für organische Verbindungen entwickeln möchten.
Alkanole: Struktur und Eigenschaften
Entdecken Sie die Welt der Alkanole! Diese Zusammenfassung behandelt die homologe Reihe, funktionelle Gruppen, Nomenklatur, sowie primäre, sekundäre und tertiäre Alkohole. Erfahren Sie mehr über mehrwertige Alkohole und deren Löslichkeit in Wasser. Ideal für Chemie-Studierende, die ein tieferes Verständnis für organische Verbindungen entwickeln möchten.
Oxidationszahlen und Organische Chemie
Entdecken Sie die Regeln zur Ermittlung von Oxidationszahlen und die Grundlagen der organischen Chemie, einschließlich Alkane, Alkanole, Alkanale, Alkanone und Carbonsäuren. Lernen Sie die funktionellen Gruppen, Isomere, Redoxreaktionen und die Bedeutung von Siedepunkten und Löslichkeit. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemische Verbindungen: Alkane & Aldehyde
Entdecken Sie die Eigenschaften, Benennung und Löslichkeit von Alkanen, Alkoholen, Aldehyden und Ketonen. Dieser Lernzettel bietet eine umfassende Übersicht über Polarität, intermolekulare Kräfte und Siedepunkte, ideal für die Klausurvorbereitung in Chemie.
Nukleophile Substitution & Alkanole
Entdecken Sie die Grundlagen der nukleophilen Substitution, die Eigenschaften und Nomenklatur von Alkanolen sowie die Reaktionen von Aldehyden und Ketonen. Diese Zusammenfassung behandelt wichtige Konzepte wie die Fehling-Probe, mehrwertige Alkohole, Dipol-Wechselwirkungen und Wasserstoffbrückenbindungen. Ideal für Chemie-Abiturienten.
Alkanole: Eigenschaften & Struktur
Entdecken Sie die Welt der Alkanole, einschließlich ihrer homologen Reihe, Isomerie, alkoholischer Gärung und Destillation. Erfahren Sie mehr über die funktionelle Hydroxylgruppe, die Unterschiede zwischen lipophilen und hydrophoben Stoffen sowie die Eigenschaften mehrwertiger Alkohole. Ideal für Chemie-Studierende, die sich mit der Struktur und den Eigenschaften von Alkanolen vertraut machen möchten.
Eigenschaften organischer Verbindungen
Entdecken Sie die Eigenschaften und Reaktionen von organischen Stoffklassen wie Alkoholen, Aldehyden, Ketonen, Carbonsäuren und Estern. Diese Zusammenfassung bietet einen Überblick über ihre Struktur, Löslichkeit, Siedepunkte und charakteristische Reaktionen, einschließlich Veresterung und Oxidation. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Homologe Reihe der Alkanole
Entdecken Sie die homologe Reihe der Alkanole, einschließlich Methanol und Ethanol. Lernen Sie die Struktur, Eigenschaften, Herstellung und Nomenklatur von Alkanolen kennen. Diese Zusammenfassung bietet einen klaren Überblick über die verschiedenen Alkanole, ihre Siedepunkte und die Unterschiede zwischen primären, sekundären und tertiären Alkanolen. Ideal für Studierende der organischen Chemie.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.