Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen und anorganischen... Mehr anzeigen
Melde dich an, um den Inhalt zu sehenKostenlos!
Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Knowunity KI
Fächer
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Alle Themen anzeigen
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Alle Themen anzeigen
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Alle Themen anzeigen
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Alle Themen anzeigen
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Alle Themen anzeigen
1,282
•
Aktualisiert Mar 18, 2026
•
jule
@jule_k4tr9
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen und anorganischen... Mehr anzeigen








Diese Seite enthält keine spezifischen Inhalte und dient als Übersichtsseite für die folgenden chemischen Konzepte.

Atombindungen sind der Schlüssel zum Verständnis der Chemie - sie entstehen durch gemeinsame Elektronenpaare zwischen Atomen. Diese kovalenten Bindungen halten Moleküle zusammen und sind eine der drei Hauptbindungsarten.
Bei Ionenbindungen ziehen sich gegensätzlich geladene Ionen elektrostatisch an. Die Elektronegativitätsdifferenz ΔEN verrät dir, welche Bindungsart vorliegt: 0-0,5 = unpolare kovalente Bindung, 0,5-1,7 = polare kovalente Bindung, >1,7 = Ionenbindung.
Zwischenmolekulare Kräfte bestimmen Eigenschaften wie Siedetemperatur. Van-der-Waals-Kräfte sind schwach, Dipol-Dipol-Wechselwirkungen entstehen bei polaren Molekülen, und Wasserstoffbrückenbindungen sind besonders stark (H mit N, O oder F).
Merktipp: Die Elektronegativitätsdifferenz ist dein Kompass für Bindungstypen!
Die wichtigsten Reaktionstypen sind: SR (radikalische Substitution), AE (elektrophile Addition), E (Eliminierung), SN (nucleophile Substitution), AN (nucleophile Addition), Kondensation und Hydrolyse.
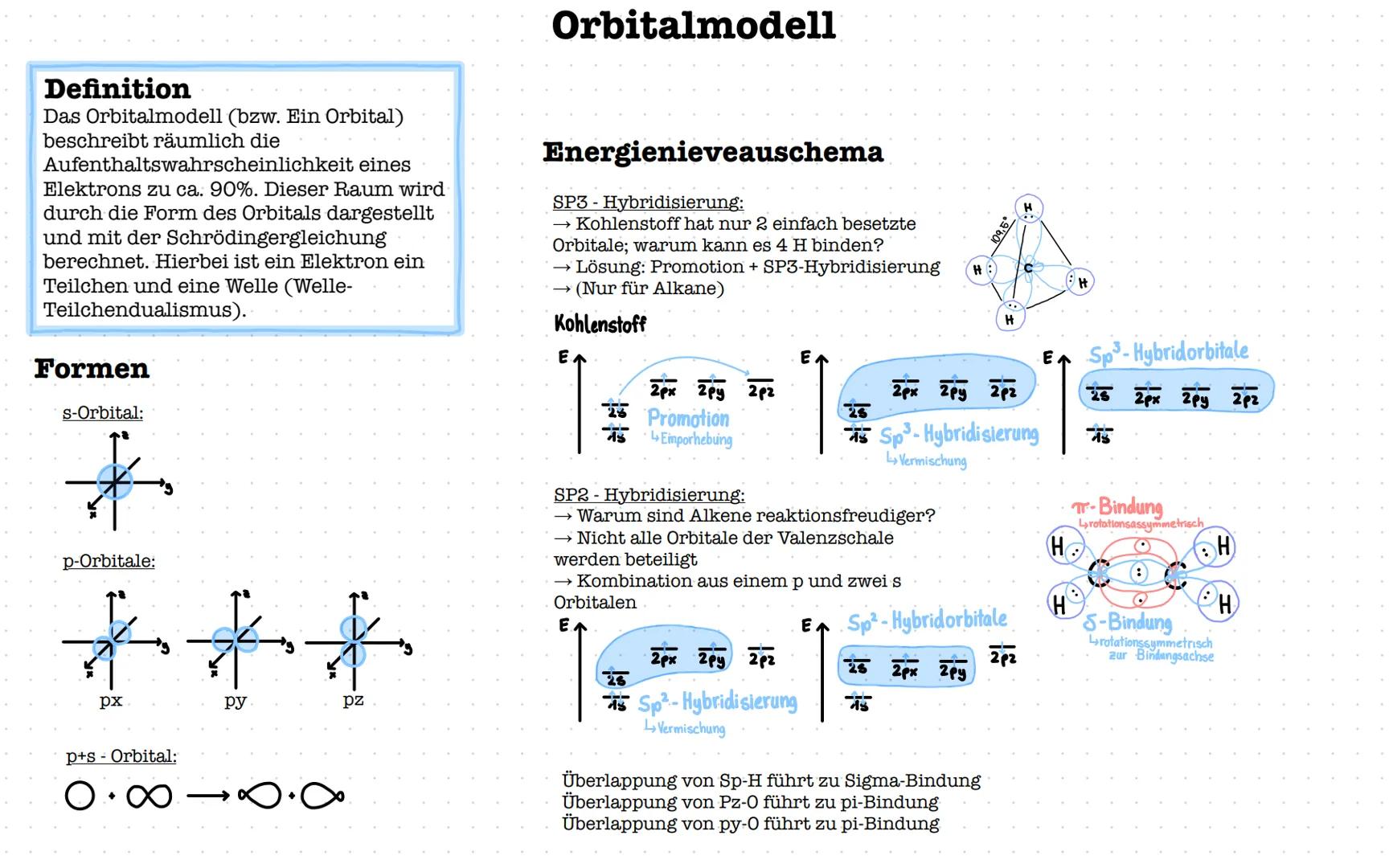
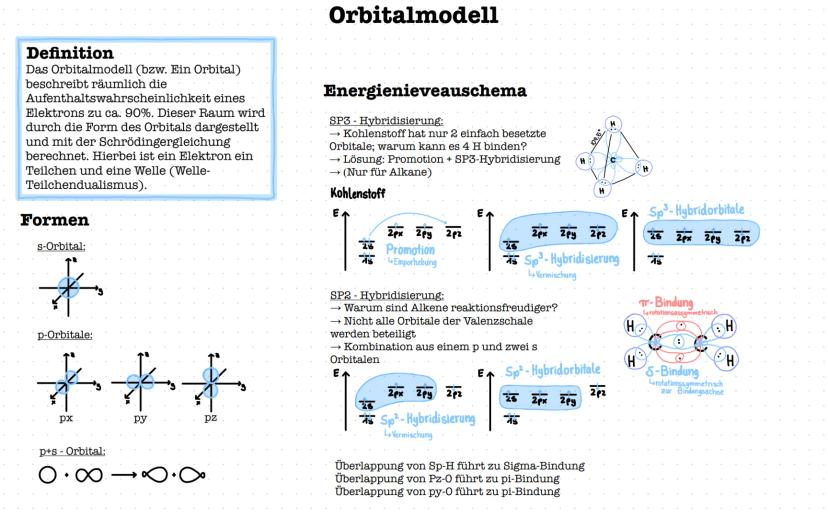
Das Orbitalmodell zeigt dir, wo sich Elektronen mit 90%iger Wahrscheinlichkeit aufhalten. Stell dir Orbitale als "Elektronenwolken" vor - s-Orbitale sind kugelförmig, p-Orbitale hantelförmig.
SP³-Hybridisierung erklärt, warum Kohlenstoff vier Bindungen eingehen kann, obwohl er nur zwei ungepaarte Elektronen hat. Durch "Promotion" wird ein Elektron angeregt, dann verschmelzen s- und p-Orbitale zu vier gleichwertigen sp³-Orbitalen.
SP²-Hybridisierung findest du bei Alkenen. Hier entstehen drei sp²-Orbitale für σ-Bindungen und ein p-Orbital bleibt für die π-Bindung der Doppelbindung übrig.
Praxistipp: SP³ = Einfachbindungen (Alkane), SP² = Doppelbindungen (Alkene)
Die Überlappung von Orbitalen bestimmt die Bindungsart: σ-Bindungen entstehen durch frontale Überlappung, π-Bindungen durch seitliche Überlappung von p-Orbitalen.

Oxidationszahlen sind deine Hilfsmittel zum Aufstellen von Formeln und Verstehen von Redoxreaktionen. Sie funktionieren wie Wertigkeiten mit Vorzeichen.
Die wichtigsten Regeln: Elementarsubstanzen haben die Oxidationszahl 0, Alkalimetalle immer +I, Erdalkalimetalle +II, Fluor immer -I, Wasserstoff +I, Sauerstoff -II. Die Summe aller Oxidationszahlen in neutralen Verbindungen ist null.
Bei Oxidationen steigt die Oxidationszahl, bei Reduktionen sinkt sie. Das merkst du dir mit "OIL RIG": Oxidation Is Loss (of electrons), Reduction Is Gain.
Eselsbrücke: Metalle sind immer positiv, Nichtmetalle meist negativ!
Mit diesen Regeln kannst du Formeln ableiten und Redoxgleichungen aufstellen - essentiell für Elektrochemie und viele andere Bereiche.

Die Siedetemperatur hängt von zwei Faktoren ab: der Molekülmasse und den zwischenmolekularen Kräften. Wasserstoffbrücken > Dipol-Dipol > Van-der-Waals-Kräfte in der Stärke.
I-Effekte beschreiben Elektronenverschiebungen: Der +I-Effekt (elektronenschiebend) tritt bei Alkylgruppen auf, der -I-Effekt (elektronenziehend) bei Halogenen. Für die Löslichkeit gilt: "Gleiches löst sich in Gleichem" - polar löst polar, unpolar löst unpolar.
Mesomerie stabilisiert Moleküle durch Elektronenverschiebung. Der +M-Effekt ist elektronenschiebend (NH₂, OH), der -M-Effekt elektronenziehend (NO₂, COOH).
Merkhilfe: Hydrophil = wasserlöslich, lipophil = fettlöslich!
Bei Konkurrenzreaktionen (SN1 vs. SN2, S vs. E) entscheiden Struktur, Lösungsmittel, Nucleophil und Abgangsgruppe über den Reaktionsweg. Säuren sind Protonendonatoren, Basen Protonenakzeptoren.
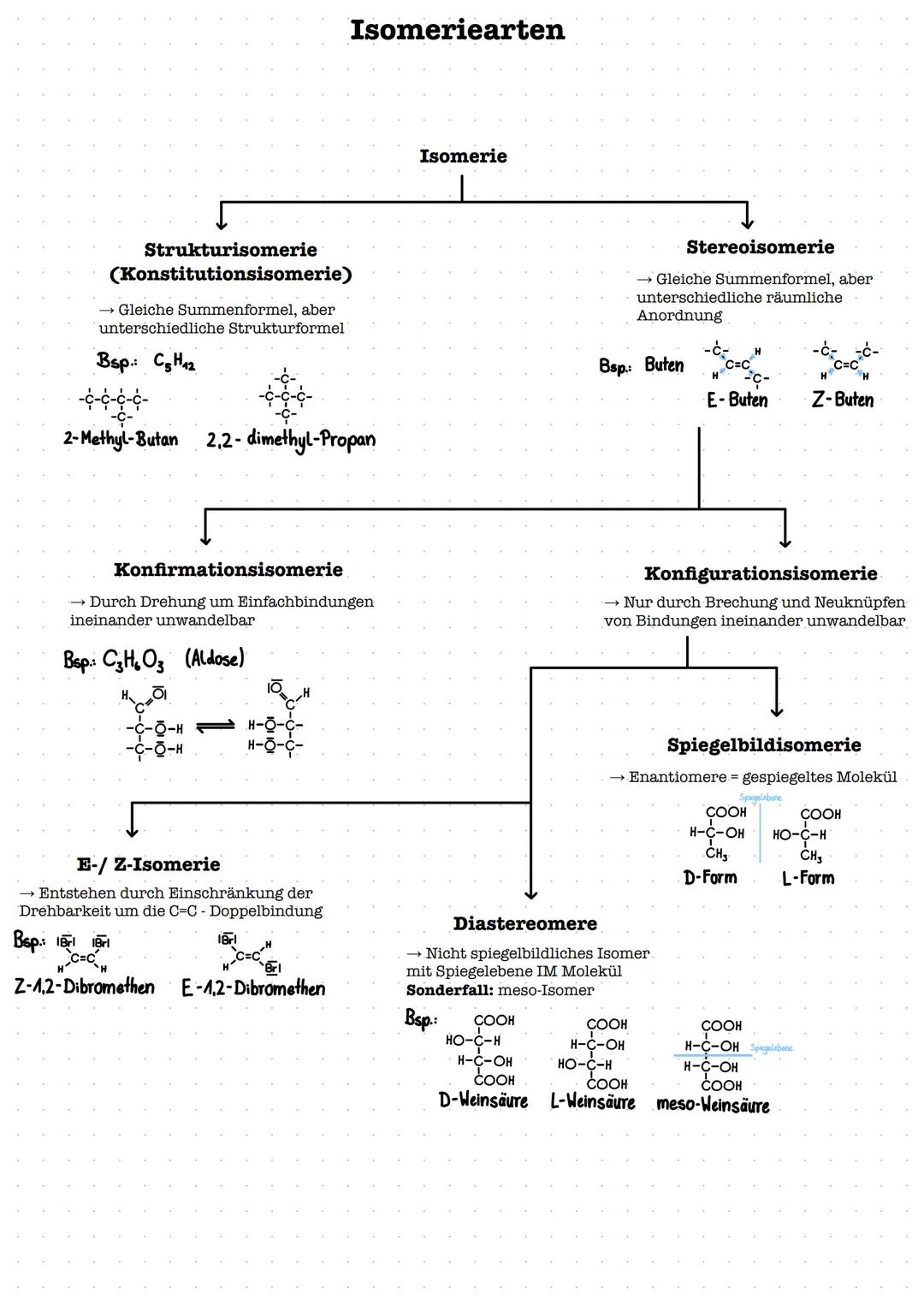
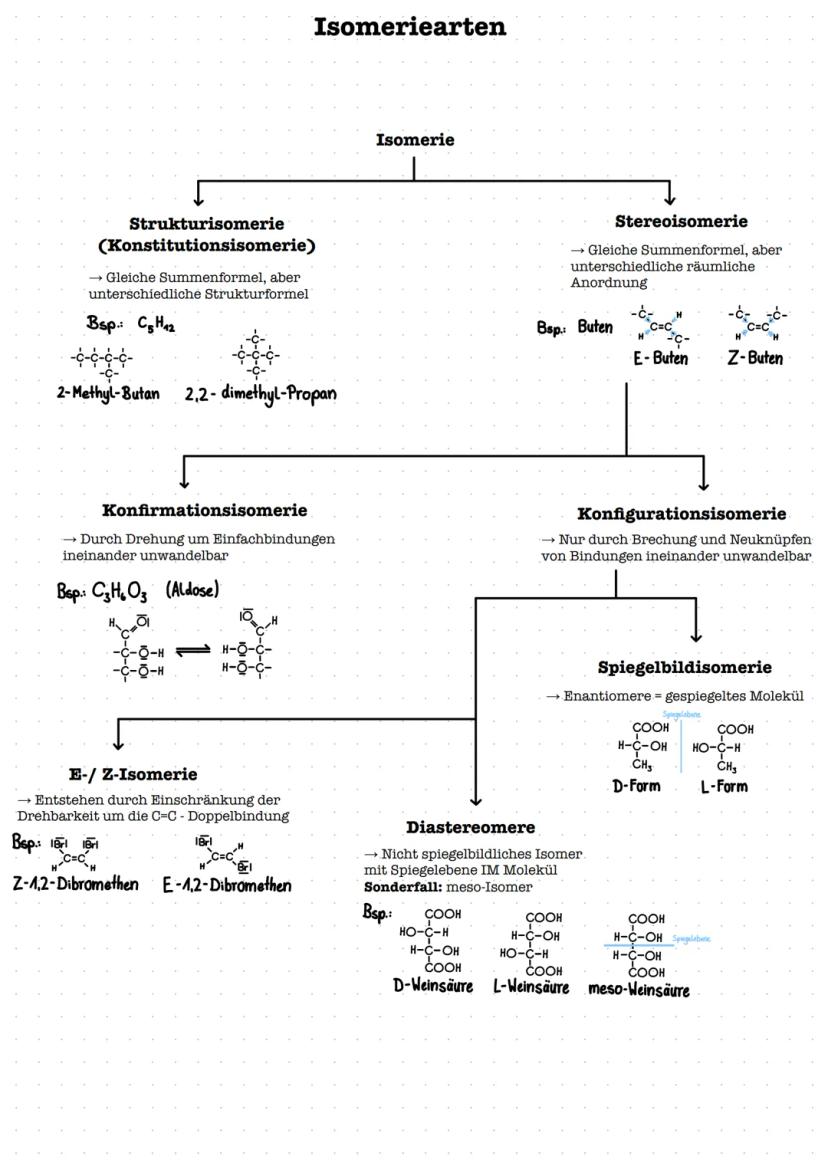
Isomere haben dieselbe Summenformel, aber unterschiedliche Struktur oder räumliche Anordnung. Das macht sie zu völlig verschiedenen Verbindungen mit anderen Eigenschaften.
Strukturisomerie bedeutet unterschiedliche Verknüpfung der Atome - wie bei den verschiedenen Pentanen .
Stereoisomerie teilt sich in Konformations- und Konfigurationsisomerie. E/Z-Isomerie entsteht bei Doppelbindungen durch eingeschränkte Drehbarkeit - E bedeutet "entgegen", Z "zusammen".
Visualisierungstipp: Baue Moleküle mit einem Modellbausatz - dann verstehst du Isomerie sofort!
Enantiomere sind Spiegelbilder , Diastereomere sind nicht spiegelbildliche Stereoisomere. Das meso-Isomer ist ein Spezialfall mit interner Spiegelebene.

Gasnachweise sind klassische Experimente: Knallgasprobe für H₂, Glimmspanprobe für O₂ (entflammt) und N₂ (erlischt). CO₂ trübt Kalkwasser durch CaCO₃-Bildung.
Ionnachweise funktionieren über charakteristische Reaktionen: Silbernitrat für Halogenide (weiße bis gelbe Niederschläge), Bariumchlorid für Sulfat (weißer Niederschlag).
Für organische Stoffklassen gibt's spezielle Tests: Bromwasser-Entfärbung für C=C-Bindungen, Fehling-Probe für Aldehyde (ziegelroter Niederschlag), Silberspiegelprobe nur für Aldehyde.
Prüfungstipp: Lerne die Farben der Nachweise auswendig - das bringt sichere Punkte!
Beilsteinprobe (grüne Flamme) für Halogenverbindungen, Ninhydrin (blau) für Aminosäuren, Iod-Stärke-Reaktion (tiefblau) für Stärke sind weitere wichtige Nachweise.

Keto-Gruppen reagieren nicht auf Fehling, Silberspiegel oder Schiff - das unterscheidet sie von Aldehyden. Carbonsäuren erkennst du an sauren Lösungen mit rotem pH-Papier.
Peptide weist du mit der Biuret-Probe nach . Aromatische Peptide reagieren mit der Xanthoprotein-Reaktion (gelb mit Salpetersäure).
Die Iod-Stärke-Reaktion mit Lugol'scher Lösung erzeugt die charakteristische Blaufärbung und ist ein zuverlässiger Stärke-Nachweis.
Abiturtipp: Übe die Nachweise praktisch - viele Schulen haben entsprechende Experimente in der mündlichen Prüfung!

Diese Seite dient als Übergang zu den organischen Stoffklassen und deren charakteristischen Reaktionen.
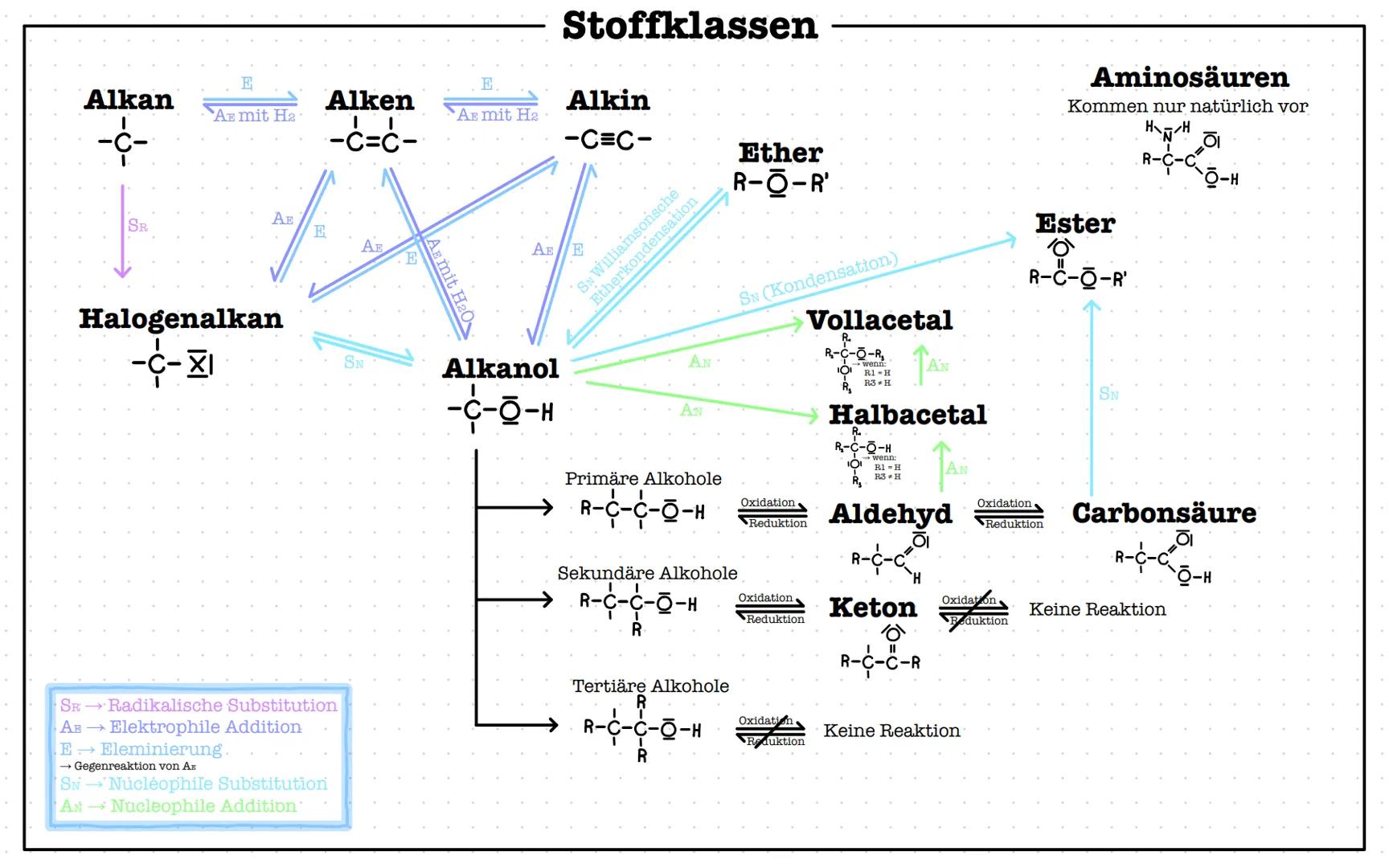
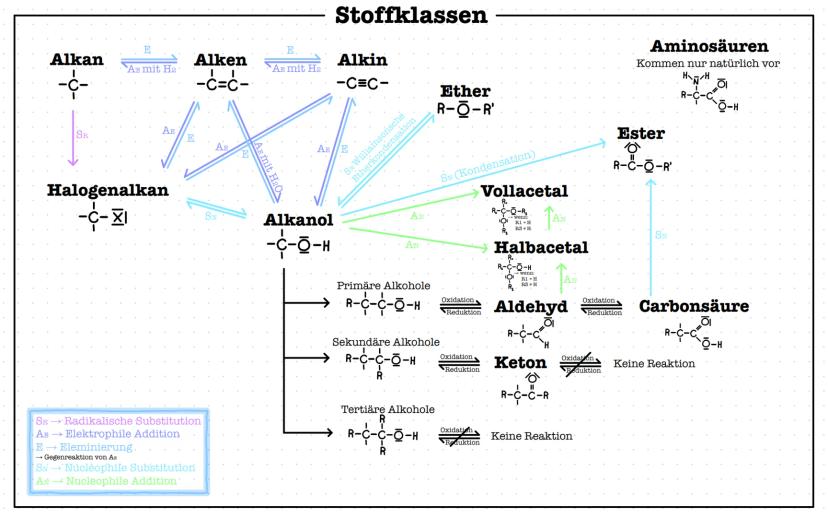
Diese Reaktionsübersicht zeigt dir alle wichtigen Umwandlungen zwischen organischen Stoffklassen. Alkane reagieren über SR zu Halogenalkanen, Alkene über AE mit verschiedenen Reagenzien.
Alkohole lassen sich durch Oxidation zu Aldehyden (primäre Alkohole) oder Ketonen (sekundäre Alkohole) umwandeln. Tertiäre Alkohole oxidieren nicht.
Aldehyde oxidieren weiter zu Carbonsäuren, beide lassen sich zu Alkoholen reduzieren. Ester entstehen aus Carbonsäuren und Alkoholen durch Kondensation.
Lernstrategie: Präge dir diese Reaktionswege als "chemische Landkarte" ein!
Ether entstehen durch Williamson'sche Ethersynthese, Acetale durch Addition von Alkoholen an Carbonylverbindungen. Aminosäuren kommen nur natürlich vor und haben besondere Eigenschaften.
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
jule
@jule_k4tr9
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen und anorganischen Chemie für dein Abitur. Du lernst hier alles über chemische Bindungen, Reaktionstypen und organische Stoffklassen - genau das, was du für Klausuren brauchst!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Diese Seite enthält keine spezifischen Inhalte und dient als Übersichtsseite für die folgenden chemischen Konzepte.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Atombindungen sind der Schlüssel zum Verständnis der Chemie - sie entstehen durch gemeinsame Elektronenpaare zwischen Atomen. Diese kovalenten Bindungen halten Moleküle zusammen und sind eine der drei Hauptbindungsarten.
Bei Ionenbindungen ziehen sich gegensätzlich geladene Ionen elektrostatisch an. Die Elektronegativitätsdifferenz ΔEN verrät dir, welche Bindungsart vorliegt: 0-0,5 = unpolare kovalente Bindung, 0,5-1,7 = polare kovalente Bindung, >1,7 = Ionenbindung.
Zwischenmolekulare Kräfte bestimmen Eigenschaften wie Siedetemperatur. Van-der-Waals-Kräfte sind schwach, Dipol-Dipol-Wechselwirkungen entstehen bei polaren Molekülen, und Wasserstoffbrückenbindungen sind besonders stark (H mit N, O oder F).
Merktipp: Die Elektronegativitätsdifferenz ist dein Kompass für Bindungstypen!
Die wichtigsten Reaktionstypen sind: SR (radikalische Substitution), AE (elektrophile Addition), E (Eliminierung), SN (nucleophile Substitution), AN (nucleophile Addition), Kondensation und Hydrolyse.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Das Orbitalmodell zeigt dir, wo sich Elektronen mit 90%iger Wahrscheinlichkeit aufhalten. Stell dir Orbitale als "Elektronenwolken" vor - s-Orbitale sind kugelförmig, p-Orbitale hantelförmig.
SP³-Hybridisierung erklärt, warum Kohlenstoff vier Bindungen eingehen kann, obwohl er nur zwei ungepaarte Elektronen hat. Durch "Promotion" wird ein Elektron angeregt, dann verschmelzen s- und p-Orbitale zu vier gleichwertigen sp³-Orbitalen.
SP²-Hybridisierung findest du bei Alkenen. Hier entstehen drei sp²-Orbitale für σ-Bindungen und ein p-Orbital bleibt für die π-Bindung der Doppelbindung übrig.
Praxistipp: SP³ = Einfachbindungen (Alkane), SP² = Doppelbindungen (Alkene)
Die Überlappung von Orbitalen bestimmt die Bindungsart: σ-Bindungen entstehen durch frontale Überlappung, π-Bindungen durch seitliche Überlappung von p-Orbitalen.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Oxidationszahlen sind deine Hilfsmittel zum Aufstellen von Formeln und Verstehen von Redoxreaktionen. Sie funktionieren wie Wertigkeiten mit Vorzeichen.
Die wichtigsten Regeln: Elementarsubstanzen haben die Oxidationszahl 0, Alkalimetalle immer +I, Erdalkalimetalle +II, Fluor immer -I, Wasserstoff +I, Sauerstoff -II. Die Summe aller Oxidationszahlen in neutralen Verbindungen ist null.
Bei Oxidationen steigt die Oxidationszahl, bei Reduktionen sinkt sie. Das merkst du dir mit "OIL RIG": Oxidation Is Loss (of electrons), Reduction Is Gain.
Eselsbrücke: Metalle sind immer positiv, Nichtmetalle meist negativ!
Mit diesen Regeln kannst du Formeln ableiten und Redoxgleichungen aufstellen - essentiell für Elektrochemie und viele andere Bereiche.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Siedetemperatur hängt von zwei Faktoren ab: der Molekülmasse und den zwischenmolekularen Kräften. Wasserstoffbrücken > Dipol-Dipol > Van-der-Waals-Kräfte in der Stärke.
I-Effekte beschreiben Elektronenverschiebungen: Der +I-Effekt (elektronenschiebend) tritt bei Alkylgruppen auf, der -I-Effekt (elektronenziehend) bei Halogenen. Für die Löslichkeit gilt: "Gleiches löst sich in Gleichem" - polar löst polar, unpolar löst unpolar.
Mesomerie stabilisiert Moleküle durch Elektronenverschiebung. Der +M-Effekt ist elektronenschiebend (NH₂, OH), der -M-Effekt elektronenziehend (NO₂, COOH).
Merkhilfe: Hydrophil = wasserlöslich, lipophil = fettlöslich!
Bei Konkurrenzreaktionen (SN1 vs. SN2, S vs. E) entscheiden Struktur, Lösungsmittel, Nucleophil und Abgangsgruppe über den Reaktionsweg. Säuren sind Protonendonatoren, Basen Protonenakzeptoren.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Isomere haben dieselbe Summenformel, aber unterschiedliche Struktur oder räumliche Anordnung. Das macht sie zu völlig verschiedenen Verbindungen mit anderen Eigenschaften.
Strukturisomerie bedeutet unterschiedliche Verknüpfung der Atome - wie bei den verschiedenen Pentanen .
Stereoisomerie teilt sich in Konformations- und Konfigurationsisomerie. E/Z-Isomerie entsteht bei Doppelbindungen durch eingeschränkte Drehbarkeit - E bedeutet "entgegen", Z "zusammen".
Visualisierungstipp: Baue Moleküle mit einem Modellbausatz - dann verstehst du Isomerie sofort!
Enantiomere sind Spiegelbilder , Diastereomere sind nicht spiegelbildliche Stereoisomere. Das meso-Isomer ist ein Spezialfall mit interner Spiegelebene.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Gasnachweise sind klassische Experimente: Knallgasprobe für H₂, Glimmspanprobe für O₂ (entflammt) und N₂ (erlischt). CO₂ trübt Kalkwasser durch CaCO₃-Bildung.
Ionnachweise funktionieren über charakteristische Reaktionen: Silbernitrat für Halogenide (weiße bis gelbe Niederschläge), Bariumchlorid für Sulfat (weißer Niederschlag).
Für organische Stoffklassen gibt's spezielle Tests: Bromwasser-Entfärbung für C=C-Bindungen, Fehling-Probe für Aldehyde (ziegelroter Niederschlag), Silberspiegelprobe nur für Aldehyde.
Prüfungstipp: Lerne die Farben der Nachweise auswendig - das bringt sichere Punkte!
Beilsteinprobe (grüne Flamme) für Halogenverbindungen, Ninhydrin (blau) für Aminosäuren, Iod-Stärke-Reaktion (tiefblau) für Stärke sind weitere wichtige Nachweise.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Keto-Gruppen reagieren nicht auf Fehling, Silberspiegel oder Schiff - das unterscheidet sie von Aldehyden. Carbonsäuren erkennst du an sauren Lösungen mit rotem pH-Papier.
Peptide weist du mit der Biuret-Probe nach . Aromatische Peptide reagieren mit der Xanthoprotein-Reaktion (gelb mit Salpetersäure).
Die Iod-Stärke-Reaktion mit Lugol'scher Lösung erzeugt die charakteristische Blaufärbung und ist ein zuverlässiger Stärke-Nachweis.
Abiturtipp: Übe die Nachweise praktisch - viele Schulen haben entsprechende Experimente in der mündlichen Prüfung!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Diese Seite dient als Übergang zu den organischen Stoffklassen und deren charakteristischen Reaktionen.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Diese Reaktionsübersicht zeigt dir alle wichtigen Umwandlungen zwischen organischen Stoffklassen. Alkane reagieren über SR zu Halogenalkanen, Alkene über AE mit verschiedenen Reagenzien.
Alkohole lassen sich durch Oxidation zu Aldehyden (primäre Alkohole) oder Ketonen (sekundäre Alkohole) umwandeln. Tertiäre Alkohole oxidieren nicht.
Aldehyde oxidieren weiter zu Carbonsäuren, beide lassen sich zu Alkoholen reduzieren. Ester entstehen aus Carbonsäuren und Alkoholen durch Kondensation.
Lernstrategie: Präge dir diese Reaktionswege als "chemische Landkarte" ein!
Ether entstehen durch Williamson'sche Ethersynthese, Acetale durch Addition von Alkoholen an Carbonylverbindungen. Aminosäuren kommen nur natürlich vor und haben besondere Eigenschaften.
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
41
Smart Tools NEU
Verwandle diesen Lernzettel in: ✓ 50+ Übungsfragen ✓ Interaktive Karteikarten ✓ Komplette Probeklausur ✓ Aufsatzgliederungen
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer