Chemische Reaktionen laufen meist nicht vollständig ab – stattdessen stellt... Mehr anzeigen
Chemie LK Abitur Hessen 2025 Q3: Chemisches Gleichgewicht, Lysereaktion, Puffer










Das Chemische Gleichgewicht
Du denkst vielleicht, dass chemische Reaktionen immer vollständig ablaufen, aber das stimmt nicht! Die meisten Reaktionen stoppen vorher und bilden ein chemisches Gleichgewicht.
Was passiert dabei? Am Anfang läuft die Hinreaktion schnell ab, weil viele Ausgangsstoffe da sind. Mit der Zeit werden es weniger, also wird die Reaktion langsamer. Gleichzeitig entstehen immer mehr Produkte, die auch zurückreagieren können – die Rückreaktion wird schneller.
Im Gleichgewichtszustand laufen Hin- und Rückreaktion gleich schnell ab. Die Konzentrationen ändern sich nicht mehr, obwohl die Reaktion weiterläuft. Deshalb nennt man es ein dynamisches Gleichgewicht.
Merke: Das Gleichgewicht bedeutet nicht Stillstand – es passiert immer noch etwas, aber die Geschwindigkeiten gleichen sich aus!
Klassische Beispiele sind das Estergleichgewicht (wichtig für Kunststoffe), die Ammoniak-Synthese (für Düngemittel) oder das Iod-Wasserstoff-Gleichgewicht.

Das Massenwirkungsgesetz
Jetzt wird's mathematisch – aber keine Sorge, das ist machbar! Für jedes Gleichgewicht gibt es eine Gleichgewichtskonstante Kc, die dir zeigt, wo das Gleichgewicht liegt.
Die Formel: Du teilst das Produkt der Produktkonzentrationen durch das Produkt der Eduktkonzentrationen. Die stöchiometrischen Faktoren (die Zahlen vor den Molekülen) werden zu Hochzahlen.
Was sagt dir Kc? Ist Kc > 1, liegt das Gleichgewicht auf der Produktseite (viel umgesetzt). Ist Kc < 1, liegt es auf der Eduktseite (wenig umgesetzt).
Bei Gasen kannst du auch mit Partialdrücken rechnen. Dann brauchst du noch einen Korrekturfaktor mit der Gasgleichung.
Tipp: Die Einheit von Kc hängt davon ab, wie viele Teilchen oben und unten stehen. Gleicht sich aus = keine Einheit!
Ein Beispiel: Beim Estergleichgewicht mit gleichen Konzentrationen von 6,2 mol/L ergibt sich Kc = 1,13 – das Gleichgewicht liegt leicht auf der Produktseite.

Gleichgewichte beeinflussen - Das Prinzip von Le Chatelier
Du kannst Gleichgewichte gezielt verschieben! Das Prinzip von Le Chatelier sagt: Störst du ein Gleichgewicht, weicht es in die Richtung aus, die die Störung kompensiert.
Konzentration ändern: Mehr Edukte dazugeben → Gleichgewicht geht nach rechts. Produkte wegnehmen → Gleichgewicht geht auch nach rechts. Das System will die Änderung ausgleichen.
Temperatur ändern: Temperatur erhöhen → endotherme Reaktionen werden bevorzugt (die brauchen Energie). Temperatur senken → exotherme Reaktionen werden bevorzugt (die geben Energie ab).
Druck ändern (nur bei Gasen): Druck erhöhen → das Gleichgewicht geht zu der Seite mit weniger Gasteilchen. Das System will dem Druck ausweichen.
Beispiel: Bei 2H₂ + O₂ ⇌ 2H₂O sind links 3 Gasteilchen, rechts 2. Druckerhöhung verschiebt nach rechts!
Diese Tricks nutzt die Industrie, um mehr Produkt zu bekommen.

Katalysatoren und Temperatur-Druck-Diagramme
Katalysatoren sind wie Abkürzungen für Reaktionen – sie machen alles schneller, ohne selbst verbraucht zu werden. Sie senken die Aktivierungsenergie ab, sodass mehr Teilchen reagieren können.
Wichtig: Katalysatoren beschleunigen das Erreichen des Gleichgewichts, aber sie ändern nicht die Zusammensetzung des Gleichgewichts. Das Verhältnis der Stoffe bleibt gleich.
Temperatur und Reaktionsgeschwindigkeit hängen zusammen: Höhere Temperatur = schnellere Teilchen = mehr Zusammenstöße = schnellere Reaktion.
Das Temperatur-Druck-Diagramm für Ammoniak zeigt dir perfekt, wie die Bedingungen die Ausbeute beeinflussen. Hoher Druck und niedrige Temperatur geben die beste Ausbeute.
Praxistipp: In der Industrie muss man Kompromisse machen – zu niedrige Temperatur = langsam, zu hoher Druck = teuer!
Optimale Bedingungen für hohe Ausbeute: Druck erhöhen, Temperatur geschickt wählen, mehr Edukte zuführen, Produkte kontinuierlich entfernen.

Enthalpie - Der Energiegehalt von Reaktionen
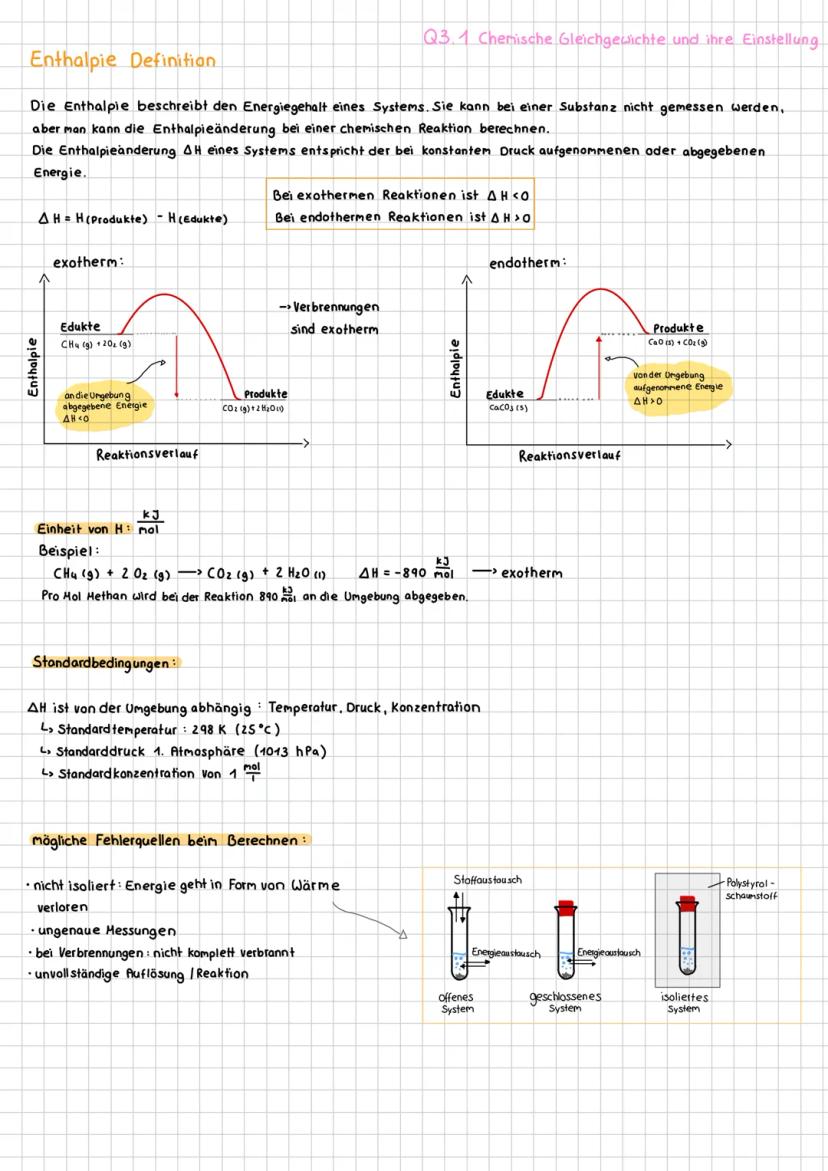
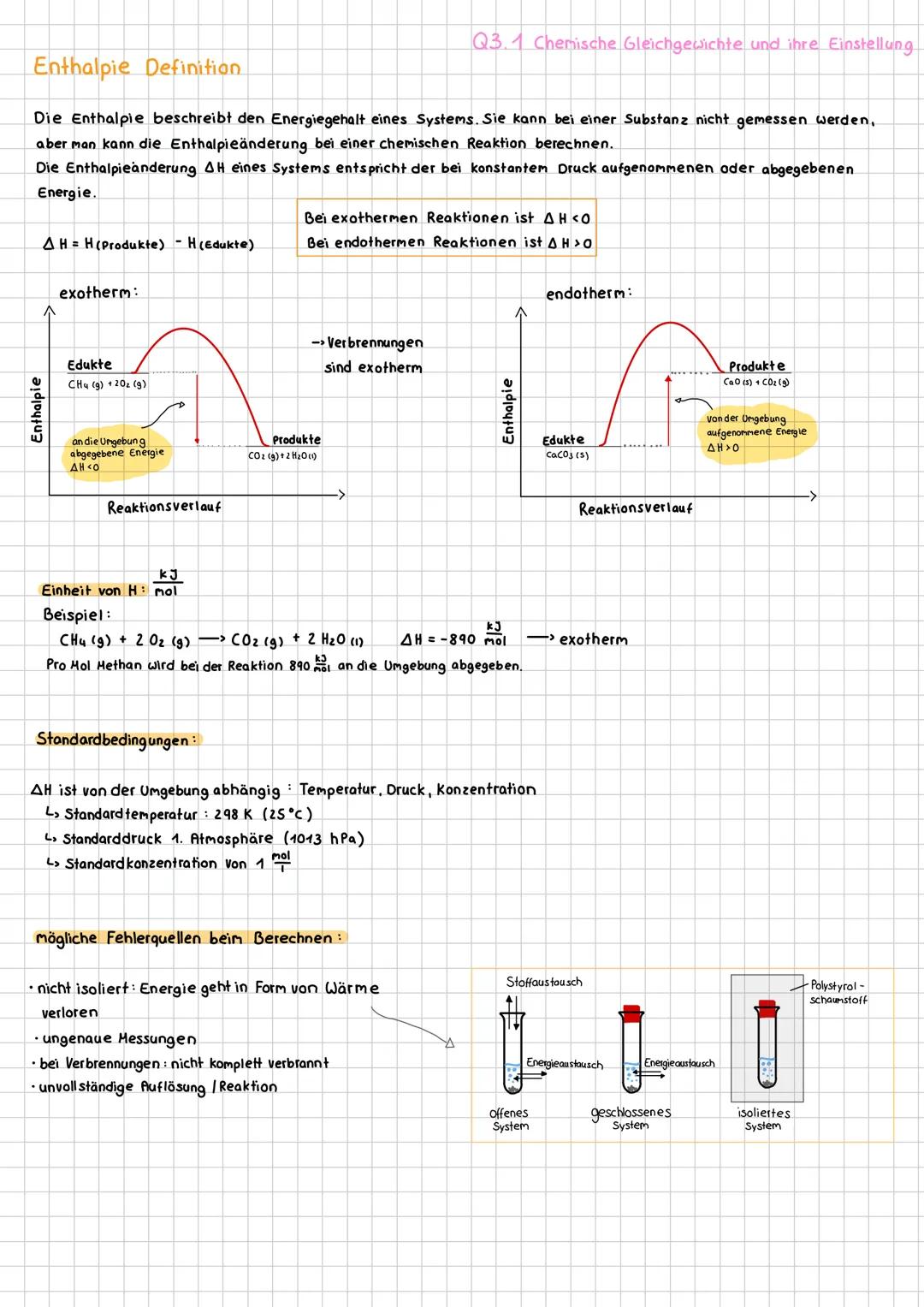
Enthalpie misst den Energiegehalt eines Systems. Du kannst nicht die absolute Enthalpie messen, aber die Enthalpieänderung ΔH bei Reaktionen schon.
Exotherme Reaktionen (ΔH < 0): Energie wird abgegeben → wird warm. Beispiel: Verbrennung von Methan gibt 890 kJ/mol ab. Das System verliert Energie an die Umgebung.
Endotherme Reaktionen (ΔH > 0): Energie wird aufgenommen → wird kalt. Das System braucht Energie aus der Umgebung.
Die Standardbedingungen sind wichtig für Vergleiche: 25°C, 1013 hPa und 1 mol/L Konzentration. So sind alle Werte vergleichbar.
Merkregel: Exotherm = Energie exit (geht raus), Endotherm = Energie enters (kommt rein)!
Bei Experimenten misst du die Temperaturänderung von Wasser mit Q = c·m·ΔT. Mögliche Fehlerquellen: Wärmeverlust, ungenaue Messungen, unvollständige Reaktionen.
Berechnung von Enthalpien
Es gibt verschiedene Wege, Enthalpieänderungen zu berechnen – je nachdem, welche Daten du hast.
Bildungsenthalpie: Die Energie, die frei wird oder gebraucht wird, wenn 1 Mol einer Verbindung aus den Elementen entsteht. Du findest die Werte in Tabellen und rechnest: ΔH = Bildungsenthalpien(Produkte) - Bildungsenthalpien(Edukte).
Bindungsenthalpie: Hier schaust du, welche Bindungen gebrochen und welche gebildet werden . Starke Bindungen haben hohe Bindungsenthalpien und sind kürzer.
Die Rechnung: ΔH = Energie für gebrochene Bindungen - Energie für gebildete Bindungen.
Faustregel: Bindungen brechen kostet immer Energie, Bindungen bilden gibt immer Energie frei!
Beispiel: Bei der Propan-Verbrennung musst du 5 O=O-Bindungen, 8 C-H-Bindungen und 2 C-C-Bindungen brechen, bildest aber 6 C=O-Bindungen und 8 O-H-Bindungen. Ergebnis: -2054 kJ/mol.

Enthalpiezyklen und der Satz von Hess
Manche Reaktionen laufen unter normalen Bedingungen nicht ab – trotzdem kannst du ihre Enthalpieänderung berechnen! Dafür nutzt du Enthalpiezyklen.
Der Satz von Hess ist dein Freund: Die Gesamtenthalpieänderung hängt nur vom Anfangs- und Endzustand ab, nicht vom Weg dazwischen. Du kannst also Umwege über andere Reaktionen nehmen.
Wie funktioniert's? Du suchst dir Reaktionen, die du kennst (oft Verbrennungsreaktionen), und kombinierst sie geschickt. Wenn eine Reaktion rückwärts läuft, drehst du das Vorzeichen um.
Praktisches Beispiel: Bildungsenthalpie von Methan über Verbrennungsenthalpien. Du verbrennst Kohlenstoff und Wasserstoff einzeln, dann Methan, und rechnest: ΔH = -394 kJ/mol + 2· - = -76 kJ/mol.
Tipp: Zeichne dir den Zyklus auf! Pfeile nach oben = positiv, nach unten = negativ.
Das ist wie bei Höhenunterschieden: Egal welchen Weg du nimmst, der Höhenunterschied zwischen Start und Ziel bleibt gleich.

Entropie - Das Maß für Unordnung
Entropie misst die Unordnung in einem System. Je unordentlicher, desto wahrscheinlicher ist der Zustand – und Natur liebt wahrscheinliche Zustände!
Entropie nimmt zu bei: Volumenvergrößerung, mehr Teilchen, höhere Temperatur, Durchmischung verschiedener Stoffe. Die Teilchen verteilen sich einfach lieber im ganzen verfügbaren Raum.
Reihenfolge der Entropiewerte: Gase > Flüssigkeiten > Feststoffe. Auch: Mischungen > Reinstoffe und große Moleküle > kleine Moleküle.
Die Berechnung funktioniert wie bei der Enthalpie: ΔS = S(Produkte) - S(Edukte). Die Werte stehen in Tabellen.
Alltagsbeispiel: Ein sauberes Zimmer wird von alleine unordentlich, aber nie umgekehrt – das ist Entropie!
Spontane Reaktionen haben zwei Triebkräfte: niedrige Energie (Enthalpie) UND hohe Unordnung (Entropie). Manchmal kämpfen beide gegeneinander – dann entscheidet die Temperatur.

Freie Enthalpie - Wann läuft eine Reaktion?
Die Gibbs-Helmholtz-Gleichung kombiniert Enthalpie und Entropie: ΔG = ΔH - T·ΔS. Sie sagt dir, ob eine Reaktion freiwillig abläuft.
Die Entscheidungsregel ist einfach: ΔG < 0 → Reaktion läuft freiwillig ab. ΔG > 0 → Reaktion läuft nicht freiwillig ab. ΔG = 0 → Gleichgewicht.
Verschiedene Kombinationen: Ist ΔH negativ (exotherm) UND ΔS positiv (mehr Unordnung), ist ΔG immer negativ – perfekt! Ist beides ungünstig, läuft nichts. Bei gemischten Vorzeichen entscheidet die Temperatur.
Beispiel mit HCl-Bildung: ΔH = -184 kJ/mol, ΔS = +20,3 J/mol. Bei Raumtemperatur: ΔG = -184 - 293·0,0203 = -190 kJ/mol. Stark negativ → läuft super ab.
Temperaturtrick: Bei ungünstiger Enthalpie, aber günstiger Entropie hilft Erhitzen – der T·ΔS-Term wird größer!
Die freie Enthalpie ist wie ein Reaktions-Kompass – sie zeigt dir die Richtung, in die eine Reaktion "will".

Säuren und Basen - Arrhenius vs. Brønsted
Es gibt verschiedene Definitionen für Säuren und Basen – heute nutzen wir meist die von Brønsted.
Arrhenius-Definition (veraltet): Säuren geben H⁺-Ionen in Wasser ab, Basen geben OH⁻-Ionen ab. Problem: Funktioniert nur in Wasser und Basen brauchen immer Sauerstoff.
Brønsted-Definition (modern): Säuren sind Protonendonatoren (geben H⁺ ab), Basen sind Protonenakzeptoren (nehmen H⁺ auf). Viel flexibler – funktioniert auch ohne Wasser!
Der große Unterschied: Nach Brønsted reagieren Säure und Base immer zusammen. Eine Säure kann nur Protonen abgeben, wenn eine Base da ist, die sie aufnimmt.
Ampholyte sind besonders interessant – sie können sowohl als Säure als auch als Base reagieren. Wasser ist das bekannteste Beispiel: Es kann Protonen abgeben (→ OH⁻) oder aufnehmen (→ H₃O⁺).
Eselsbrücke: Donator gibt ab, Akzeptor nimmt auf – wie bei Organspenden!
Weitere Ampholyte sind Ammoniak (NH₃) oder das Dihydrogenphosphat-Ion (H₂PO₄⁻). Diese Flexibilität macht sie wichtig für Puffersysteme.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Säure-Base-Gleichgewichte
9Säure-Base-Gleichgewichte und pH-Berechnung
Diese Zusammenfassung behandelt die Grundlagen der Säure-Base-Gleichgewichte, einschließlich Brønsted-Säuren und -Basen, Autoprotolyse des Wassers, pH-Wert-Berechnung, Pufferlösungen und Titrationen. Ideal für Schüler, die sich auf das Abitur vorbereiten und ein tiefes Verständnis der Säure-Base-Theorie entwickeln möchten.
pH-Wert und Säure-Base-Theorie
Entdecken Sie die Grundlagen der Säure-Base-Theorie, die Berechnung des pH-Werts, Pufferlösungen und Titration. Diese Zusammenfassung bietet eine klare Erklärung der Konzepte, einschließlich der Autoprotolyse, Indikatoren und der Bedeutung von konjugierten Säure-Base-Paaren. Ideal für Chemie-Studierende, die ihr Wissen vertiefen möchten.
Chemische Gleichgewichte & Puffersysteme
Vertiefte Analyse der chemischen Gleichgewichte, Puffersysteme und deren Anwendung in der Säure-Base-Titration. Erfahren Sie mehr über die Henderson-Hasselbalch-Gleichung, das Haber-Bosch-Verfahren und die Berechnung von pH-Werten. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten möchten.
Protolysereaktionen und pH-Berechnung
Erfahren Sie alles über Protolysereaktionen, die Autoprotolyse des Wassers und die Berechnung von pH- und pOH-Werten. Diese Zusammenfassung behandelt die Definitionen von Säuren und Basen, die Bedeutung von pKs- und pKb-Werten sowie die Grundlagen des Säure-Base-Gleichgewichts. Ideal für Chemie-Studierende, die ihr Wissen über Protolyse und pH-Wert vertiefen möchten.
Chemie Abi GK 2022: Wichtige Konzepte
Dieser Lernzettel für das Chemie-Abitur 2022 umfasst zentrale Themen wie Reaktionsenthalpie, Säure-Base-Gleichgewicht, Redoxreaktionen, elektrochemische Zellen und mehr. Ideal für die Prüfungsvorbereitung! Enthält auch wichtige Formeln und Reaktionsmechanismen.
Chemisches Gleichgewicht & pH-Wert
Diese Abiturzusammenfassung behandelt das chemische Gleichgewicht, einschließlich der Einflüsse von Temperatur, Druck und Konzentration. Sie erklärt das Massewirkungsgesetz, das Säure-Base-Gleichgewicht nach Brönsted, die Berechnung des pH-Wertes, Puffersysteme sowie Titrationen und deren Indikatoren. Ideal für Chemie LK Schüler.
Säure-Base-Gleichgewichte
Detaillierte Zusammenfassung zu Säure-Base-Gleichgewichten, einschließlich pH-Wert-Berechnung, Titrationskurven und der Rolle von Indikatoren. Ideal für die Klausurvorbereitung. Erfahren Sie mehr über Brønsted-Säure-Base-Begriffe, Protolyse und das Ionenprodukt des Wassers.
Kohlensäure: Chemie und Anwendung
Entdecken Sie die chemischen Eigenschaften und Anwendungen von Kohlensäure (HCO3). Diese Zusammenfassung behandelt die Dissoziation, den pH-Wert, die gesundheitlichen Aspekte und die Verwendung in der Industrie. Ideal für Studierende der Chemie, die ein tieferes Verständnis für diese zweiprotonige Säure und ihre Reaktionen in wässrigen Lösungen erlangen möchten.
Säure-Base-Gleichgewichte
Vertiefte Analyse der Säure-Base-Gleichgewichte, pH-Wert-Berechnungen und Pufferlösungen. Diese Klausur umfasst Aufgaben zu Phenylessigsäure, Chloressigsäure und Ammoniak, einschließlich der Berechnung von Dissoziationskonstanten und pH-Werten. Ideal für Chemie-Leistungskurse zur Vorbereitung auf Prüfungen.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Chemie LK Abitur Hessen 2025 Q3: Chemisches Gleichgewicht, Lysereaktion, Puffer
Chemische Reaktionen laufen meist nicht vollständig ab – stattdessen stellt sich ein dynamisches Gleichgewicht ein. Diese wichtigen Konzepte helfen dir zu verstehen, warum manche Reaktionen besser funktionieren als andere und wie du sie beeinflussen kannst.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Das Chemische Gleichgewicht
Du denkst vielleicht, dass chemische Reaktionen immer vollständig ablaufen, aber das stimmt nicht! Die meisten Reaktionen stoppen vorher und bilden ein chemisches Gleichgewicht.
Was passiert dabei? Am Anfang läuft die Hinreaktion schnell ab, weil viele Ausgangsstoffe da sind. Mit der Zeit werden es weniger, also wird die Reaktion langsamer. Gleichzeitig entstehen immer mehr Produkte, die auch zurückreagieren können – die Rückreaktion wird schneller.
Im Gleichgewichtszustand laufen Hin- und Rückreaktion gleich schnell ab. Die Konzentrationen ändern sich nicht mehr, obwohl die Reaktion weiterläuft. Deshalb nennt man es ein dynamisches Gleichgewicht.
Merke: Das Gleichgewicht bedeutet nicht Stillstand – es passiert immer noch etwas, aber die Geschwindigkeiten gleichen sich aus!
Klassische Beispiele sind das Estergleichgewicht (wichtig für Kunststoffe), die Ammoniak-Synthese (für Düngemittel) oder das Iod-Wasserstoff-Gleichgewicht.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Das Massenwirkungsgesetz
Jetzt wird's mathematisch – aber keine Sorge, das ist machbar! Für jedes Gleichgewicht gibt es eine Gleichgewichtskonstante Kc, die dir zeigt, wo das Gleichgewicht liegt.
Die Formel: Du teilst das Produkt der Produktkonzentrationen durch das Produkt der Eduktkonzentrationen. Die stöchiometrischen Faktoren (die Zahlen vor den Molekülen) werden zu Hochzahlen.
Was sagt dir Kc? Ist Kc > 1, liegt das Gleichgewicht auf der Produktseite (viel umgesetzt). Ist Kc < 1, liegt es auf der Eduktseite (wenig umgesetzt).
Bei Gasen kannst du auch mit Partialdrücken rechnen. Dann brauchst du noch einen Korrekturfaktor mit der Gasgleichung.
Tipp: Die Einheit von Kc hängt davon ab, wie viele Teilchen oben und unten stehen. Gleicht sich aus = keine Einheit!
Ein Beispiel: Beim Estergleichgewicht mit gleichen Konzentrationen von 6,2 mol/L ergibt sich Kc = 1,13 – das Gleichgewicht liegt leicht auf der Produktseite.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Gleichgewichte beeinflussen - Das Prinzip von Le Chatelier
Du kannst Gleichgewichte gezielt verschieben! Das Prinzip von Le Chatelier sagt: Störst du ein Gleichgewicht, weicht es in die Richtung aus, die die Störung kompensiert.
Konzentration ändern: Mehr Edukte dazugeben → Gleichgewicht geht nach rechts. Produkte wegnehmen → Gleichgewicht geht auch nach rechts. Das System will die Änderung ausgleichen.
Temperatur ändern: Temperatur erhöhen → endotherme Reaktionen werden bevorzugt (die brauchen Energie). Temperatur senken → exotherme Reaktionen werden bevorzugt (die geben Energie ab).
Druck ändern (nur bei Gasen): Druck erhöhen → das Gleichgewicht geht zu der Seite mit weniger Gasteilchen. Das System will dem Druck ausweichen.
Beispiel: Bei 2H₂ + O₂ ⇌ 2H₂O sind links 3 Gasteilchen, rechts 2. Druckerhöhung verschiebt nach rechts!
Diese Tricks nutzt die Industrie, um mehr Produkt zu bekommen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Katalysatoren und Temperatur-Druck-Diagramme
Katalysatoren sind wie Abkürzungen für Reaktionen – sie machen alles schneller, ohne selbst verbraucht zu werden. Sie senken die Aktivierungsenergie ab, sodass mehr Teilchen reagieren können.
Wichtig: Katalysatoren beschleunigen das Erreichen des Gleichgewichts, aber sie ändern nicht die Zusammensetzung des Gleichgewichts. Das Verhältnis der Stoffe bleibt gleich.
Temperatur und Reaktionsgeschwindigkeit hängen zusammen: Höhere Temperatur = schnellere Teilchen = mehr Zusammenstöße = schnellere Reaktion.
Das Temperatur-Druck-Diagramm für Ammoniak zeigt dir perfekt, wie die Bedingungen die Ausbeute beeinflussen. Hoher Druck und niedrige Temperatur geben die beste Ausbeute.
Praxistipp: In der Industrie muss man Kompromisse machen – zu niedrige Temperatur = langsam, zu hoher Druck = teuer!
Optimale Bedingungen für hohe Ausbeute: Druck erhöhen, Temperatur geschickt wählen, mehr Edukte zuführen, Produkte kontinuierlich entfernen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Enthalpie - Der Energiegehalt von Reaktionen
Enthalpie misst den Energiegehalt eines Systems. Du kannst nicht die absolute Enthalpie messen, aber die Enthalpieänderung ΔH bei Reaktionen schon.
Exotherme Reaktionen (ΔH < 0): Energie wird abgegeben → wird warm. Beispiel: Verbrennung von Methan gibt 890 kJ/mol ab. Das System verliert Energie an die Umgebung.
Endotherme Reaktionen (ΔH > 0): Energie wird aufgenommen → wird kalt. Das System braucht Energie aus der Umgebung.
Die Standardbedingungen sind wichtig für Vergleiche: 25°C, 1013 hPa und 1 mol/L Konzentration. So sind alle Werte vergleichbar.
Merkregel: Exotherm = Energie exit (geht raus), Endotherm = Energie enters (kommt rein)!
Bei Experimenten misst du die Temperaturänderung von Wasser mit Q = c·m·ΔT. Mögliche Fehlerquellen: Wärmeverlust, ungenaue Messungen, unvollständige Reaktionen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Berechnung von Enthalpien
Es gibt verschiedene Wege, Enthalpieänderungen zu berechnen – je nachdem, welche Daten du hast.
Bildungsenthalpie: Die Energie, die frei wird oder gebraucht wird, wenn 1 Mol einer Verbindung aus den Elementen entsteht. Du findest die Werte in Tabellen und rechnest: ΔH = Bildungsenthalpien(Produkte) - Bildungsenthalpien(Edukte).
Bindungsenthalpie: Hier schaust du, welche Bindungen gebrochen und welche gebildet werden . Starke Bindungen haben hohe Bindungsenthalpien und sind kürzer.
Die Rechnung: ΔH = Energie für gebrochene Bindungen - Energie für gebildete Bindungen.
Faustregel: Bindungen brechen kostet immer Energie, Bindungen bilden gibt immer Energie frei!
Beispiel: Bei der Propan-Verbrennung musst du 5 O=O-Bindungen, 8 C-H-Bindungen und 2 C-C-Bindungen brechen, bildest aber 6 C=O-Bindungen und 8 O-H-Bindungen. Ergebnis: -2054 kJ/mol.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Enthalpiezyklen und der Satz von Hess
Manche Reaktionen laufen unter normalen Bedingungen nicht ab – trotzdem kannst du ihre Enthalpieänderung berechnen! Dafür nutzt du Enthalpiezyklen.
Der Satz von Hess ist dein Freund: Die Gesamtenthalpieänderung hängt nur vom Anfangs- und Endzustand ab, nicht vom Weg dazwischen. Du kannst also Umwege über andere Reaktionen nehmen.
Wie funktioniert's? Du suchst dir Reaktionen, die du kennst (oft Verbrennungsreaktionen), und kombinierst sie geschickt. Wenn eine Reaktion rückwärts läuft, drehst du das Vorzeichen um.
Praktisches Beispiel: Bildungsenthalpie von Methan über Verbrennungsenthalpien. Du verbrennst Kohlenstoff und Wasserstoff einzeln, dann Methan, und rechnest: ΔH = -394 kJ/mol + 2· - = -76 kJ/mol.
Tipp: Zeichne dir den Zyklus auf! Pfeile nach oben = positiv, nach unten = negativ.
Das ist wie bei Höhenunterschieden: Egal welchen Weg du nimmst, der Höhenunterschied zwischen Start und Ziel bleibt gleich.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Entropie - Das Maß für Unordnung
Entropie misst die Unordnung in einem System. Je unordentlicher, desto wahrscheinlicher ist der Zustand – und Natur liebt wahrscheinliche Zustände!
Entropie nimmt zu bei: Volumenvergrößerung, mehr Teilchen, höhere Temperatur, Durchmischung verschiedener Stoffe. Die Teilchen verteilen sich einfach lieber im ganzen verfügbaren Raum.
Reihenfolge der Entropiewerte: Gase > Flüssigkeiten > Feststoffe. Auch: Mischungen > Reinstoffe und große Moleküle > kleine Moleküle.
Die Berechnung funktioniert wie bei der Enthalpie: ΔS = S(Produkte) - S(Edukte). Die Werte stehen in Tabellen.
Alltagsbeispiel: Ein sauberes Zimmer wird von alleine unordentlich, aber nie umgekehrt – das ist Entropie!
Spontane Reaktionen haben zwei Triebkräfte: niedrige Energie (Enthalpie) UND hohe Unordnung (Entropie). Manchmal kämpfen beide gegeneinander – dann entscheidet die Temperatur.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Freie Enthalpie - Wann läuft eine Reaktion?
Die Gibbs-Helmholtz-Gleichung kombiniert Enthalpie und Entropie: ΔG = ΔH - T·ΔS. Sie sagt dir, ob eine Reaktion freiwillig abläuft.
Die Entscheidungsregel ist einfach: ΔG < 0 → Reaktion läuft freiwillig ab. ΔG > 0 → Reaktion läuft nicht freiwillig ab. ΔG = 0 → Gleichgewicht.
Verschiedene Kombinationen: Ist ΔH negativ (exotherm) UND ΔS positiv (mehr Unordnung), ist ΔG immer negativ – perfekt! Ist beides ungünstig, läuft nichts. Bei gemischten Vorzeichen entscheidet die Temperatur.
Beispiel mit HCl-Bildung: ΔH = -184 kJ/mol, ΔS = +20,3 J/mol. Bei Raumtemperatur: ΔG = -184 - 293·0,0203 = -190 kJ/mol. Stark negativ → läuft super ab.
Temperaturtrick: Bei ungünstiger Enthalpie, aber günstiger Entropie hilft Erhitzen – der T·ΔS-Term wird größer!
Die freie Enthalpie ist wie ein Reaktions-Kompass – sie zeigt dir die Richtung, in die eine Reaktion "will".

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Säuren und Basen - Arrhenius vs. Brønsted
Es gibt verschiedene Definitionen für Säuren und Basen – heute nutzen wir meist die von Brønsted.
Arrhenius-Definition (veraltet): Säuren geben H⁺-Ionen in Wasser ab, Basen geben OH⁻-Ionen ab. Problem: Funktioniert nur in Wasser und Basen brauchen immer Sauerstoff.
Brønsted-Definition (modern): Säuren sind Protonendonatoren (geben H⁺ ab), Basen sind Protonenakzeptoren (nehmen H⁺ auf). Viel flexibler – funktioniert auch ohne Wasser!
Der große Unterschied: Nach Brønsted reagieren Säure und Base immer zusammen. Eine Säure kann nur Protonen abgeben, wenn eine Base da ist, die sie aufnimmt.
Ampholyte sind besonders interessant – sie können sowohl als Säure als auch als Base reagieren. Wasser ist das bekannteste Beispiel: Es kann Protonen abgeben (→ OH⁻) oder aufnehmen (→ H₃O⁺).
Eselsbrücke: Donator gibt ab, Akzeptor nimmt auf – wie bei Organspenden!
Weitere Ampholyte sind Ammoniak (NH₃) oder das Dihydrogenphosphat-Ion (H₂PO₄⁻). Diese Flexibilität macht sie wichtig für Puffersysteme.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Säure-Base-Gleichgewichte
9Säure-Base-Gleichgewichte und pH-Berechnung
Diese Zusammenfassung behandelt die Grundlagen der Säure-Base-Gleichgewichte, einschließlich Brønsted-Säuren und -Basen, Autoprotolyse des Wassers, pH-Wert-Berechnung, Pufferlösungen und Titrationen. Ideal für Schüler, die sich auf das Abitur vorbereiten und ein tiefes Verständnis der Säure-Base-Theorie entwickeln möchten.
pH-Wert und Säure-Base-Theorie
Entdecken Sie die Grundlagen der Säure-Base-Theorie, die Berechnung des pH-Werts, Pufferlösungen und Titration. Diese Zusammenfassung bietet eine klare Erklärung der Konzepte, einschließlich der Autoprotolyse, Indikatoren und der Bedeutung von konjugierten Säure-Base-Paaren. Ideal für Chemie-Studierende, die ihr Wissen vertiefen möchten.
Chemische Gleichgewichte & Puffersysteme
Vertiefte Analyse der chemischen Gleichgewichte, Puffersysteme und deren Anwendung in der Säure-Base-Titration. Erfahren Sie mehr über die Henderson-Hasselbalch-Gleichung, das Haber-Bosch-Verfahren und die Berechnung von pH-Werten. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten möchten.
Protolysereaktionen und pH-Berechnung
Erfahren Sie alles über Protolysereaktionen, die Autoprotolyse des Wassers und die Berechnung von pH- und pOH-Werten. Diese Zusammenfassung behandelt die Definitionen von Säuren und Basen, die Bedeutung von pKs- und pKb-Werten sowie die Grundlagen des Säure-Base-Gleichgewichts. Ideal für Chemie-Studierende, die ihr Wissen über Protolyse und pH-Wert vertiefen möchten.
Chemie Abi GK 2022: Wichtige Konzepte
Dieser Lernzettel für das Chemie-Abitur 2022 umfasst zentrale Themen wie Reaktionsenthalpie, Säure-Base-Gleichgewicht, Redoxreaktionen, elektrochemische Zellen und mehr. Ideal für die Prüfungsvorbereitung! Enthält auch wichtige Formeln und Reaktionsmechanismen.
Chemisches Gleichgewicht & pH-Wert
Diese Abiturzusammenfassung behandelt das chemische Gleichgewicht, einschließlich der Einflüsse von Temperatur, Druck und Konzentration. Sie erklärt das Massewirkungsgesetz, das Säure-Base-Gleichgewicht nach Brönsted, die Berechnung des pH-Wertes, Puffersysteme sowie Titrationen und deren Indikatoren. Ideal für Chemie LK Schüler.
Säure-Base-Gleichgewichte
Detaillierte Zusammenfassung zu Säure-Base-Gleichgewichten, einschließlich pH-Wert-Berechnung, Titrationskurven und der Rolle von Indikatoren. Ideal für die Klausurvorbereitung. Erfahren Sie mehr über Brønsted-Säure-Base-Begriffe, Protolyse und das Ionenprodukt des Wassers.
Kohlensäure: Chemie und Anwendung
Entdecken Sie die chemischen Eigenschaften und Anwendungen von Kohlensäure (HCO3). Diese Zusammenfassung behandelt die Dissoziation, den pH-Wert, die gesundheitlichen Aspekte und die Verwendung in der Industrie. Ideal für Studierende der Chemie, die ein tieferes Verständnis für diese zweiprotonige Säure und ihre Reaktionen in wässrigen Lösungen erlangen möchten.
Säure-Base-Gleichgewichte
Vertiefte Analyse der Säure-Base-Gleichgewichte, pH-Wert-Berechnungen und Pufferlösungen. Diese Klausur umfasst Aufgaben zu Phenylessigsäure, Chloressigsäure und Ammoniak, einschließlich der Berechnung von Dissoziationskonstanten und pH-Werten. Ideal für Chemie-Leistungskurse zur Vorbereitung auf Prüfungen.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.