Chemische Gleichgewichte sind überall um dich herum - von der... Mehr anzeigen
Chemisches Gleichgewicht und Protolyse – Themenübersicht Q3










Chemische Gleichgewichte und ihre Einstellung
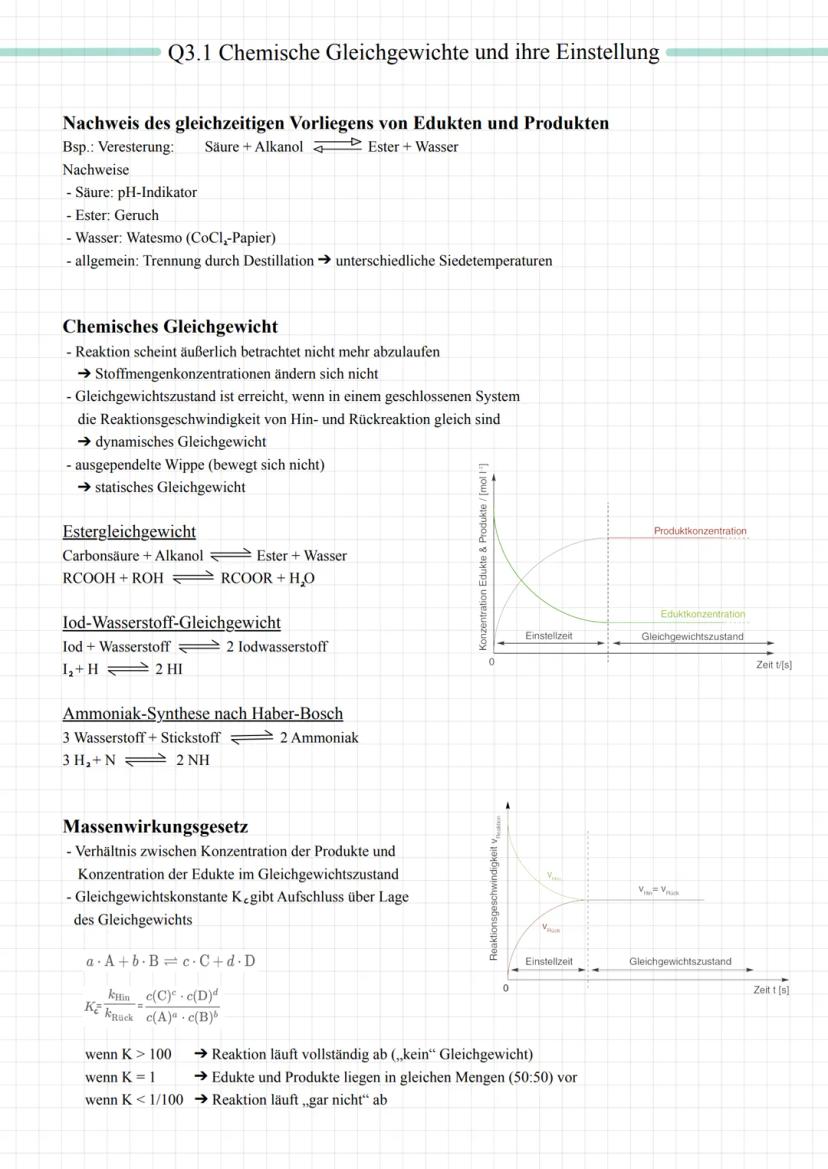
Du kennst das: Mischst du Essig mit Alkohol, riechst du nach kurzer Zeit einen fruchtigen Estergeruch - aber der Essiggeruch verschwindet nie komplett. Das liegt daran, dass sich ein chemisches Gleichgewicht einstellt.
Im Gleichgewichtszustand laufen Hin- und Rückreaktion gleich schnell ab. Das ist wie eine Wippe, die sich ständig bewegt, aber trotzdem im Gleichgewicht steht - deshalb heißt es dynamisches Gleichgewicht. Die Konzentrationen aller Stoffe bleiben dabei konstant.
Das Massenwirkungsgesetz hilft dir dabei, vorherzusagen, auf welcher Seite das Gleichgewicht liegt. Die Gleichgewichtskonstante K zeigt dir: Ist K > 100, läuft die Reaktion fast vollständig ab. Bei K = 1 hast du etwa gleich viele Edukte und Produkte. Ist K < 0,01, passiert praktisch nichts.
Merktipp: Ein großes K bedeutet viele Produkte, ein kleines K bedeutet viele Edukte übrig!

Berechnungen und das Prinzip des kleinsten Zwangs
Mit konkreten Zahlen wird's spannend! Bei der Reaktion von Iod mit Wasserstoff zu Iodwasserstoff kannst du genau berechnen, wie viel von jedem Stoff im Gleichgewicht vorliegt. Das funktioniert über das Aufstellen einer Gleichung mit der Unbekannten x.
Das Prinzip des kleinsten Zwangs (Le Chatelier) ist dein Werkzeug, um Gleichgewichte zu beeinflussen. Erhöhst du die Temperatur, begünstigt das die endotherme Reaktionsrichtung. Erhöhst du den Druck, verschiebt sich das Gleichgewicht zur Seite mit weniger Gasteilchen.
Bei Konzentrationsänderungen reagiert das System immer so, dass die Störung ausgeglichen wird. Fügst du mehr Edukte hinzu, entstehen mehr Produkte - das System "weicht aus".
Praxistipp: In der Klausur immer daran denken: Das System macht das Gegenteil von dem, was du störst!

Haber-Bosch-Verfahren und Energetik
Das Haber-Bosch-Verfahren zeigt perfekt, wie Theorie in die Praxis umgesetzt wird. Ammoniak entsteht aus Stickstoff und Wasserstoff, aber die Bedingungen müssen stimmen: Hoher Druck begünstigt die Reaktion (4 Gasteilchen werden zu 2), aber niedrige Temperaturen machen sie zu langsam.
Hier kommt die wirtschaftliche Optimierung ins Spiel. Niedrige Temperaturen = bessere Ausbeute, aber langsamere Reaktion = höhere Kosten. Ein Katalysator (meist Eisen) beschleunigt die Reaktion, ohne das Gleichgewicht zu verschieben.
Die Enthalpie (ΔH) sagt dir, ob Energie frei wird (exotherm, ΔH < 0) oder verbraucht wird (endotherm, ΔH > 0). Mit dem Satz von Hess kannst du Reaktionsenthalpien berechnen, auch wenn du die Reaktion nicht direkt messen kannst.
Die Entropie (ΔS) beschreibt die Unordnung im System. Gase haben höhere Entropie als Flüssigkeiten. Die freie Enthalpie (ΔG) kombiniert beide: ΔG = ΔH - T·ΔS. Ist ΔG < 0, läuft die Reaktion freiwillig ab.
Klausurtrick: Bei der Grenztemperatur ist ΔG = 0, dann gilt: T = ΔH/ΔS!

Grenztemperatur und freie Enthalpie
Die Grenztemperatur ist der Punkt, ab dem eine Reaktion thermodynamisch möglich wird. Du berechnest sie mit T = ΔH/ΔS, wenn ΔG = 0 ist. Das ist besonders wichtig für industrielle Prozesse - unterhalb dieser Temperatur läuft die Reaktion einfach nicht freiwillig ab.
Die freie Enthalpie ist dein Kompass für Reaktionen. Ist ΔG negativ, ist die Reaktion exergon (läuft freiwillig). Ist ΔG positiv, ist sie endergon (braucht Energiezufuhr). Bei ΔG = 0 bist du im Gleichgewicht.
Merkhilfe: Negative freie Enthalpie = Reaktion läuft von selbst!

Protolysegleichgewichte - Säuren und Basen
Nach Brønsted sind Säuren Protonendonatoren (geben H⁺ ab) und Basen Protonenakzeptoren (nehmen H⁺ auf). Diese Definition funktioniert perfekt für wässrige Lösungen und ist klausurrelevant.
Ampholyte wie Wasser können beides: als Säure oder Base reagieren. Bei der Autoprotolyse reagiert Wasser mit sich selbst und bildet H₃O⁺ und OH⁻ Ionen.
Die Säure- und Basenstärke wird durch pKₛ- und pKᵦ-Werte ausgedrückt. Je kleiner der pKₛ-Wert, desto stärker die Säure. Starke Säuren haben schwache konjugierte Basen - das ist ein fundamentales Prinzip.
Die wichtige Beziehung pKₛ + pKᵦ = 14 gilt für korrespondierende Säure-Base-Paare bei 25°C.
Eselsbrücke: pKₛ klein = Säure fein (stark)!

Autoprotolyse und pH-Wert
Die Autoprotolyse des Wassers ist die Grundlage für pH-Berechnungen. Selbst reines Wasser enthält H₃O⁺ und OH⁻ Ionen im Verhältnis 1:1, deshalb pH = 7.
Das Ionenprodukt des Wassers Kw = 10⁻¹⁴ ist eine wichtige Konstante. Daraus folgt: pH + pOH = 14. Diese Beziehung gilt für alle wässrigen Lösungen bei 25°C.
Für pH-Berechnungen gibt's einfache Faustregeln: Bei starken Säuren (pKₛ < 1) ist pH = -lg(c(Säure)). Bei schwachen Säuren (pKₛ > 4) verwendest du die Formel pH = ½.
Mehrprotonige Säuren wie H₂SO₄ können mehrere Protonen abgeben. Die erste Protolysestufe ist meist viel stärker als die zweite.
Rechentrick: Bei verdünnten starken Säuren kannst du die Konzentration direkt in die pH-Formel einsetzen!

Indikatoren und Titration
Säure-Base-Indikatoren sind schwache Säuren oder Basen, die bei verschiedenen pH-Werten ihre Farbe ändern. Sie müssen wasserlöslich sein und ein großes delokalisiertes Elektronensystem haben.
Der Umschlagbereich des Indikators sollte möglichst nah am Äquivalenzpunkt der Titration liegen. Das ist der Punkt, wo die Stoffmengen von Säure und Base gleich sind.
Bei der Titration bestimmst du unbekannte Konzentrationen durch Neutralisation mit einer Maßlösung bekannter Konzentration. Die Titrationskurve zeigt den pH-Verlauf während der Zugabe.
Wichtiger Unterschied: Der Äquivalenzpunkt ist nicht immer gleich dem Neutralpunkt . Das gilt nur bei der Titration starker Säuren mit starken Basen.
Prüfungstipp: Den richtigen Indikator wählen - sein Umschlagbereich muss zum Äquivalenzpunkt passen!

Titrationskurven verschiedener Säure-Base-Kombinationen
Bei der Titration starker Säuren mit starken Basen ist der Äquivalenzpunkt gleich dem Neutralpunkt . Die Kurve hat einen steilen Sprung am Äquivalenzpunkt.
Schwache Säuren mit starken Basen zeigen einen anderen Verlauf: Der Äquivalenzpunkt liegt im basischen Bereich, weil das entstehende Salz basisch reagiert. Der Halbäquivalenzpunkt ist besonders wichtig - hier gilt pH = pKₛ.
Die Henderson-Hasselbalch-Gleichung gilt im Pufferbereich: pH = pKₛ + lg. Diese Formel ist super wichtig für Pufferberechnungen.
Bei mehrprotonigen Säuren siehst du mehrere Äquivalenzpunkte - einen für jede Protolysestufe. Jeder Äquivalenzpunkt hat seine eigene Charakteristik.
Klausur-Kniff: Am Halbäquivalenzpunkt ist die Konzentration der schwachen Säure gleich der ihrer Base!

Mehrprotonige Säuren und Formeln
Mehrprotonige Säuren wie H₂SO₄ haben so viele Protolysestufen wie Protonen. Schwefelsäure zeigt zwei deutliche Äquivalenzpunkte: Der erste entspricht einer starken Säure, der zweite einer schwachen.
Bei der Berechnung von Titrationen brauchst du die Grundformeln: n = c·V für Stoffmengen, m = M·n für Massen und das Molarvolumen für Gase .
Die Interpretation der Kurven ist entscheidend: Zwischen den Äquivalenzpunkten liegt jeweils ein Pufferbereich vor, wo sich der pH-Wert nur wenig ändert.
Wichtig: Jede Protolysestufe hat ihren eigenen pKₛ-Wert!

Puffersysteme
Puffersysteme bestehen aus etwa gleichen Mengen einer schwachen Säure und ihrer korrespondierenden Base. Sie halten den pH-Wert auch bei Zugabe von Säuren oder Basen nahezu konstant.
Die optimale Pufferkapazität hast du bei pH = pKₛ. Dann sind die Konzentrationen von Säure und Base gleich groß, und das System kann sowohl zugegebene H⁺- als auch OH⁻-Ionen abfangen.
Das Kohlensäure-Hydrogencarbonat-Puffersystem in deinem Blut ist lebenswichtig. Es hält den pH-Wert konstant bei etwa 7,4. Bei Säurezugabe reagiert HCO₃⁻ zu H₂CO₃, bei Basenzugabe reagiert H₂CO₃ zu HCO₃⁻.
Die Funktionsweise beruht auf dem Prinzip des kleinsten Zwangs: Das Gleichgewicht weicht der Störung aus und stellt sich schnell wieder ein.
Bio-Bezug: Ohne Puffersysteme würde schon ein Glas Cola deinen Blut-pH tödlich verschieben!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Säure-Base-Gleichgewichte
9Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säure-Base-Gleichgewichte und pH-Berechnung
Diese Zusammenfassung behandelt die Grundlagen der Säure-Base-Gleichgewichte, einschließlich Brønsted-Säuren und -Basen, Autoprotolyse des Wassers, pH-Wert-Berechnung, Pufferlösungen und Titrationen. Ideal für Schüler, die sich auf das Abitur vorbereiten und ein tiefes Verständnis der Säure-Base-Theorie entwickeln möchten.
pH-Wert und Säure-Base-Theorie
Entdecken Sie die Grundlagen der Säure-Base-Theorie, die Berechnung des pH-Werts, Pufferlösungen und Titration. Diese Zusammenfassung bietet eine klare Erklärung der Konzepte, einschließlich der Autoprotolyse, Indikatoren und der Bedeutung von konjugierten Säure-Base-Paaren. Ideal für Chemie-Studierende, die ihr Wissen vertiefen möchten.
Protolysereaktionen und pH-Berechnung
Erfahren Sie alles über Protolysereaktionen, die Autoprotolyse des Wassers und die Berechnung von pH- und pOH-Werten. Diese Zusammenfassung behandelt die Definitionen von Säuren und Basen, die Bedeutung von pKs- und pKb-Werten sowie die Grundlagen des Säure-Base-Gleichgewichts. Ideal für Chemie-Studierende, die ihr Wissen über Protolyse und pH-Wert vertiefen möchten.
Chemie Abi GK 2022: Wichtige Konzepte
Dieser Lernzettel für das Chemie-Abitur 2022 umfasst zentrale Themen wie Reaktionsenthalpie, Säure-Base-Gleichgewicht, Redoxreaktionen, elektrochemische Zellen und mehr. Ideal für die Prüfungsvorbereitung! Enthält auch wichtige Formeln und Reaktionsmechanismen.
Chemisches Gleichgewicht & pH-Wert
Diese Abiturzusammenfassung behandelt das chemische Gleichgewicht, einschließlich der Einflüsse von Temperatur, Druck und Konzentration. Sie erklärt das Massewirkungsgesetz, das Säure-Base-Gleichgewicht nach Brönsted, die Berechnung des pH-Wertes, Puffersysteme sowie Titrationen und deren Indikatoren. Ideal für Chemie LK Schüler.
Säure-Base-Gleichgewichte
Detaillierte Zusammenfassung zu Säure-Base-Gleichgewichten, einschließlich pH-Wert-Berechnung, Titrationskurven und der Rolle von Indikatoren. Ideal für die Klausurvorbereitung. Erfahren Sie mehr über Brønsted-Säure-Base-Begriffe, Protolyse und das Ionenprodukt des Wassers.
Kohlensäure: Chemie und Anwendung
Entdecken Sie die chemischen Eigenschaften und Anwendungen von Kohlensäure (HCO3). Diese Zusammenfassung behandelt die Dissoziation, den pH-Wert, die gesundheitlichen Aspekte und die Verwendung in der Industrie. Ideal für Studierende der Chemie, die ein tieferes Verständnis für diese zweiprotonige Säure und ihre Reaktionen in wässrigen Lösungen erlangen möchten.
Säure-Base-Gleichgewichte
Vertiefte Analyse der Säure-Base-Gleichgewichte, pH-Wert-Berechnungen und Pufferlösungen. Diese Klausur umfasst Aufgaben zu Phenylessigsäure, Chloressigsäure und Ammoniak, einschließlich der Berechnung von Dissoziationskonstanten und pH-Werten. Ideal für Chemie-Leistungskurse zur Vorbereitung auf Prüfungen.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Chemisches Gleichgewicht und Protolyse – Themenübersicht Q3
Chemische Gleichgewichte sind überall um dich herum - von der Herstellung von Ammoniak bis hin zu den Pufferreaktionen in deinem Blut. In diesem Kapitel lernst du, wie Reaktionen ins Gleichgewicht kommen und warum sich manche Stoffe nicht komplett umwandeln.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Chemische Gleichgewichte und ihre Einstellung
Du kennst das: Mischst du Essig mit Alkohol, riechst du nach kurzer Zeit einen fruchtigen Estergeruch - aber der Essiggeruch verschwindet nie komplett. Das liegt daran, dass sich ein chemisches Gleichgewicht einstellt.
Im Gleichgewichtszustand laufen Hin- und Rückreaktion gleich schnell ab. Das ist wie eine Wippe, die sich ständig bewegt, aber trotzdem im Gleichgewicht steht - deshalb heißt es dynamisches Gleichgewicht. Die Konzentrationen aller Stoffe bleiben dabei konstant.
Das Massenwirkungsgesetz hilft dir dabei, vorherzusagen, auf welcher Seite das Gleichgewicht liegt. Die Gleichgewichtskonstante K zeigt dir: Ist K > 100, läuft die Reaktion fast vollständig ab. Bei K = 1 hast du etwa gleich viele Edukte und Produkte. Ist K < 0,01, passiert praktisch nichts.
Merktipp: Ein großes K bedeutet viele Produkte, ein kleines K bedeutet viele Edukte übrig!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Berechnungen und das Prinzip des kleinsten Zwangs
Mit konkreten Zahlen wird's spannend! Bei der Reaktion von Iod mit Wasserstoff zu Iodwasserstoff kannst du genau berechnen, wie viel von jedem Stoff im Gleichgewicht vorliegt. Das funktioniert über das Aufstellen einer Gleichung mit der Unbekannten x.
Das Prinzip des kleinsten Zwangs (Le Chatelier) ist dein Werkzeug, um Gleichgewichte zu beeinflussen. Erhöhst du die Temperatur, begünstigt das die endotherme Reaktionsrichtung. Erhöhst du den Druck, verschiebt sich das Gleichgewicht zur Seite mit weniger Gasteilchen.
Bei Konzentrationsänderungen reagiert das System immer so, dass die Störung ausgeglichen wird. Fügst du mehr Edukte hinzu, entstehen mehr Produkte - das System "weicht aus".
Praxistipp: In der Klausur immer daran denken: Das System macht das Gegenteil von dem, was du störst!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Haber-Bosch-Verfahren und Energetik
Das Haber-Bosch-Verfahren zeigt perfekt, wie Theorie in die Praxis umgesetzt wird. Ammoniak entsteht aus Stickstoff und Wasserstoff, aber die Bedingungen müssen stimmen: Hoher Druck begünstigt die Reaktion (4 Gasteilchen werden zu 2), aber niedrige Temperaturen machen sie zu langsam.
Hier kommt die wirtschaftliche Optimierung ins Spiel. Niedrige Temperaturen = bessere Ausbeute, aber langsamere Reaktion = höhere Kosten. Ein Katalysator (meist Eisen) beschleunigt die Reaktion, ohne das Gleichgewicht zu verschieben.
Die Enthalpie (ΔH) sagt dir, ob Energie frei wird (exotherm, ΔH < 0) oder verbraucht wird (endotherm, ΔH > 0). Mit dem Satz von Hess kannst du Reaktionsenthalpien berechnen, auch wenn du die Reaktion nicht direkt messen kannst.
Die Entropie (ΔS) beschreibt die Unordnung im System. Gase haben höhere Entropie als Flüssigkeiten. Die freie Enthalpie (ΔG) kombiniert beide: ΔG = ΔH - T·ΔS. Ist ΔG < 0, läuft die Reaktion freiwillig ab.
Klausurtrick: Bei der Grenztemperatur ist ΔG = 0, dann gilt: T = ΔH/ΔS!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Grenztemperatur und freie Enthalpie
Die Grenztemperatur ist der Punkt, ab dem eine Reaktion thermodynamisch möglich wird. Du berechnest sie mit T = ΔH/ΔS, wenn ΔG = 0 ist. Das ist besonders wichtig für industrielle Prozesse - unterhalb dieser Temperatur läuft die Reaktion einfach nicht freiwillig ab.
Die freie Enthalpie ist dein Kompass für Reaktionen. Ist ΔG negativ, ist die Reaktion exergon (läuft freiwillig). Ist ΔG positiv, ist sie endergon (braucht Energiezufuhr). Bei ΔG = 0 bist du im Gleichgewicht.
Merkhilfe: Negative freie Enthalpie = Reaktion läuft von selbst!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Protolysegleichgewichte - Säuren und Basen
Nach Brønsted sind Säuren Protonendonatoren (geben H⁺ ab) und Basen Protonenakzeptoren (nehmen H⁺ auf). Diese Definition funktioniert perfekt für wässrige Lösungen und ist klausurrelevant.
Ampholyte wie Wasser können beides: als Säure oder Base reagieren. Bei der Autoprotolyse reagiert Wasser mit sich selbst und bildet H₃O⁺ und OH⁻ Ionen.
Die Säure- und Basenstärke wird durch pKₛ- und pKᵦ-Werte ausgedrückt. Je kleiner der pKₛ-Wert, desto stärker die Säure. Starke Säuren haben schwache konjugierte Basen - das ist ein fundamentales Prinzip.
Die wichtige Beziehung pKₛ + pKᵦ = 14 gilt für korrespondierende Säure-Base-Paare bei 25°C.
Eselsbrücke: pKₛ klein = Säure fein (stark)!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Autoprotolyse und pH-Wert
Die Autoprotolyse des Wassers ist die Grundlage für pH-Berechnungen. Selbst reines Wasser enthält H₃O⁺ und OH⁻ Ionen im Verhältnis 1:1, deshalb pH = 7.
Das Ionenprodukt des Wassers Kw = 10⁻¹⁴ ist eine wichtige Konstante. Daraus folgt: pH + pOH = 14. Diese Beziehung gilt für alle wässrigen Lösungen bei 25°C.
Für pH-Berechnungen gibt's einfache Faustregeln: Bei starken Säuren (pKₛ < 1) ist pH = -lg(c(Säure)). Bei schwachen Säuren (pKₛ > 4) verwendest du die Formel pH = ½.
Mehrprotonige Säuren wie H₂SO₄ können mehrere Protonen abgeben. Die erste Protolysestufe ist meist viel stärker als die zweite.
Rechentrick: Bei verdünnten starken Säuren kannst du die Konzentration direkt in die pH-Formel einsetzen!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Indikatoren und Titration
Säure-Base-Indikatoren sind schwache Säuren oder Basen, die bei verschiedenen pH-Werten ihre Farbe ändern. Sie müssen wasserlöslich sein und ein großes delokalisiertes Elektronensystem haben.
Der Umschlagbereich des Indikators sollte möglichst nah am Äquivalenzpunkt der Titration liegen. Das ist der Punkt, wo die Stoffmengen von Säure und Base gleich sind.
Bei der Titration bestimmst du unbekannte Konzentrationen durch Neutralisation mit einer Maßlösung bekannter Konzentration. Die Titrationskurve zeigt den pH-Verlauf während der Zugabe.
Wichtiger Unterschied: Der Äquivalenzpunkt ist nicht immer gleich dem Neutralpunkt . Das gilt nur bei der Titration starker Säuren mit starken Basen.
Prüfungstipp: Den richtigen Indikator wählen - sein Umschlagbereich muss zum Äquivalenzpunkt passen!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Titrationskurven verschiedener Säure-Base-Kombinationen
Bei der Titration starker Säuren mit starken Basen ist der Äquivalenzpunkt gleich dem Neutralpunkt . Die Kurve hat einen steilen Sprung am Äquivalenzpunkt.
Schwache Säuren mit starken Basen zeigen einen anderen Verlauf: Der Äquivalenzpunkt liegt im basischen Bereich, weil das entstehende Salz basisch reagiert. Der Halbäquivalenzpunkt ist besonders wichtig - hier gilt pH = pKₛ.
Die Henderson-Hasselbalch-Gleichung gilt im Pufferbereich: pH = pKₛ + lg. Diese Formel ist super wichtig für Pufferberechnungen.
Bei mehrprotonigen Säuren siehst du mehrere Äquivalenzpunkte - einen für jede Protolysestufe. Jeder Äquivalenzpunkt hat seine eigene Charakteristik.
Klausur-Kniff: Am Halbäquivalenzpunkt ist die Konzentration der schwachen Säure gleich der ihrer Base!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Mehrprotonige Säuren und Formeln
Mehrprotonige Säuren wie H₂SO₄ haben so viele Protolysestufen wie Protonen. Schwefelsäure zeigt zwei deutliche Äquivalenzpunkte: Der erste entspricht einer starken Säure, der zweite einer schwachen.
Bei der Berechnung von Titrationen brauchst du die Grundformeln: n = c·V für Stoffmengen, m = M·n für Massen und das Molarvolumen für Gase .
Die Interpretation der Kurven ist entscheidend: Zwischen den Äquivalenzpunkten liegt jeweils ein Pufferbereich vor, wo sich der pH-Wert nur wenig ändert.
Wichtig: Jede Protolysestufe hat ihren eigenen pKₛ-Wert!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Puffersysteme
Puffersysteme bestehen aus etwa gleichen Mengen einer schwachen Säure und ihrer korrespondierenden Base. Sie halten den pH-Wert auch bei Zugabe von Säuren oder Basen nahezu konstant.
Die optimale Pufferkapazität hast du bei pH = pKₛ. Dann sind die Konzentrationen von Säure und Base gleich groß, und das System kann sowohl zugegebene H⁺- als auch OH⁻-Ionen abfangen.
Das Kohlensäure-Hydrogencarbonat-Puffersystem in deinem Blut ist lebenswichtig. Es hält den pH-Wert konstant bei etwa 7,4. Bei Säurezugabe reagiert HCO₃⁻ zu H₂CO₃, bei Basenzugabe reagiert H₂CO₃ zu HCO₃⁻.
Die Funktionsweise beruht auf dem Prinzip des kleinsten Zwangs: Das Gleichgewicht weicht der Störung aus und stellt sich schnell wieder ein.
Bio-Bezug: Ohne Puffersysteme würde schon ein Glas Cola deinen Blut-pH tödlich verschieben!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Beliebtester Inhalt: Säure-Base-Gleichgewichte
9Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säure-Base-Gleichgewichte und pH-Berechnung
Diese Zusammenfassung behandelt die Grundlagen der Säure-Base-Gleichgewichte, einschließlich Brønsted-Säuren und -Basen, Autoprotolyse des Wassers, pH-Wert-Berechnung, Pufferlösungen und Titrationen. Ideal für Schüler, die sich auf das Abitur vorbereiten und ein tiefes Verständnis der Säure-Base-Theorie entwickeln möchten.
pH-Wert und Säure-Base-Theorie
Entdecken Sie die Grundlagen der Säure-Base-Theorie, die Berechnung des pH-Werts, Pufferlösungen und Titration. Diese Zusammenfassung bietet eine klare Erklärung der Konzepte, einschließlich der Autoprotolyse, Indikatoren und der Bedeutung von konjugierten Säure-Base-Paaren. Ideal für Chemie-Studierende, die ihr Wissen vertiefen möchten.
Protolysereaktionen und pH-Berechnung
Erfahren Sie alles über Protolysereaktionen, die Autoprotolyse des Wassers und die Berechnung von pH- und pOH-Werten. Diese Zusammenfassung behandelt die Definitionen von Säuren und Basen, die Bedeutung von pKs- und pKb-Werten sowie die Grundlagen des Säure-Base-Gleichgewichts. Ideal für Chemie-Studierende, die ihr Wissen über Protolyse und pH-Wert vertiefen möchten.
Chemie Abi GK 2022: Wichtige Konzepte
Dieser Lernzettel für das Chemie-Abitur 2022 umfasst zentrale Themen wie Reaktionsenthalpie, Säure-Base-Gleichgewicht, Redoxreaktionen, elektrochemische Zellen und mehr. Ideal für die Prüfungsvorbereitung! Enthält auch wichtige Formeln und Reaktionsmechanismen.
Chemisches Gleichgewicht & pH-Wert
Diese Abiturzusammenfassung behandelt das chemische Gleichgewicht, einschließlich der Einflüsse von Temperatur, Druck und Konzentration. Sie erklärt das Massewirkungsgesetz, das Säure-Base-Gleichgewicht nach Brönsted, die Berechnung des pH-Wertes, Puffersysteme sowie Titrationen und deren Indikatoren. Ideal für Chemie LK Schüler.
Säure-Base-Gleichgewichte
Detaillierte Zusammenfassung zu Säure-Base-Gleichgewichten, einschließlich pH-Wert-Berechnung, Titrationskurven und der Rolle von Indikatoren. Ideal für die Klausurvorbereitung. Erfahren Sie mehr über Brønsted-Säure-Base-Begriffe, Protolyse und das Ionenprodukt des Wassers.
Kohlensäure: Chemie und Anwendung
Entdecken Sie die chemischen Eigenschaften und Anwendungen von Kohlensäure (HCO3). Diese Zusammenfassung behandelt die Dissoziation, den pH-Wert, die gesundheitlichen Aspekte und die Verwendung in der Industrie. Ideal für Studierende der Chemie, die ein tieferes Verständnis für diese zweiprotonige Säure und ihre Reaktionen in wässrigen Lösungen erlangen möchten.
Säure-Base-Gleichgewichte
Vertiefte Analyse der Säure-Base-Gleichgewichte, pH-Wert-Berechnungen und Pufferlösungen. Diese Klausur umfasst Aufgaben zu Phenylessigsäure, Chloressigsäure und Ammoniak, einschließlich der Berechnung von Dissoziationskonstanten und pH-Werten. Ideal für Chemie-Leistungskurse zur Vorbereitung auf Prüfungen.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.