Gleichgewichtsreaktionen zeigen dir, wie chemische Reaktionen funktionieren, wenn sie nicht... Mehr anzeigen
Abitur Chemie LK Lernzettel 2024 – Bestens vorbereitet!










Grundlagen Gleichgewichtsreaktionen
Dynamisches Gleichgewicht heißt: Die Reaktion läuft trotzdem weiter, aber Hin- und Rückreaktion sind gleich schnell. Du siehst keine Veränderung mehr, obwohl ständig Moleküle reagieren. Das ist der Unterschied zum statischen Gleichgewicht wie bei einer Waage.
Beim chemischen Gleichgewicht findest du sowohl Edukte als auch Produkte vor. Die Reaktion ist reversibel und läuft nie vollständig ab. Die Zeit bis zum Gleichgewicht nennt man Einstellzeit.
Das Massenwirkungsgesetz beschreibt mathematisch, wo das Gleichgewicht liegt. Die Gleichgewichtskonstante Kc zeigt dir: Ist Kc > 1, hast du mehr Produkte. Ist Kc < 1, überwiegen die Edukte.
Merke dir: Kc = (Konzentration Produkte)/(Konzentration Edukte) - dabei werden die Stöchiometriezahlen zu Exponenten!
Du rechnest drei Hauptaufgaben: Bestimmung von Kc aus Gleichgewichtskonzentrationen, Berechnung der Produktmenge bei bekanntem Kc und Ausbeute-Berechnungen.

Le Chatelier-Prinzip und Katalysatoren
Das Prinzip von Le Chatelier ist dein Werkzeug zur Vorhersage: Störst du ein Gleichgewicht, weicht das System so aus, dass die Störung minimiert wird.
Bei Temperaturerhöhung verschiebt sich das Gleichgewicht zur endothermen Seite. Bei Konzentrationserhöhung einer Komponente weicht das System durch deren Verbrauch aus.
Druckerhöhung (nur bei Gasen!) verschiebt das Gleichgewicht zur Seite mit weniger Teilchen - das System "macht sich kleiner". Das Haber-Bosch-Verfahren nutzt das: Hoher Druck und Katalysator für mehr Ammoniak.
Praxistipp: Die RGT-Regel besagt: +10°C verdoppelt die Reaktionsgeschwindigkeit!
Katalysatoren beschleunigen beide Reaktionsrichtungen gleich stark. Sie senken die Aktivierungsenergie durch alternative Reaktionswege, ändern aber nie die Lage des Gleichgewichts. Bei der heterogenen Katalyse (verschiedene Phasen) adsorbieren Moleküle an Metalloberflächen.

Energetik chemischer Reaktionen
Die innere Energie U setzt sich aus Kernenergie, chemischer Energie und thermischer Energie zusammen. Der 1. Hauptsatz besagt: Energie kann nicht verschwinden, nur umgewandelt werden.
Bei isobaren Prozessen (konstanter Druck) gilt: ΔU = Q - P·ΔV. Die Enthalpie H ist praktischer als U, weil sie die Volumenarbeit schon einrechnet: ΔH = ΔU + P·ΔV.
Exotherme Reaktionen (ΔH < 0) geben Wärme ab, endotherme (ΔH > 0) nehmen Wärme auf. Die molare Reaktionsenthalpie bezieht sich auf einen Formelumsatz.
Wichtig: Bei Gasen rechnest du: ΔrHm ≈ ΔrUm - P·R·T, bei Flüssigkeiten und Feststoffen: ΔrHm ≈ ΔrUm
Kalorimetrie misst Wärmemengen über Temperaturänderungen: Q = c·m·ΔT. Der Satz von Hess erlaubt dir, Reaktionsenthalpien aus Bildungsenthalpien zu berechnen.

Bildungs- und Verbrennungsenthalpien
Bildungsenthalpien geben an, wie viel Energie frei wird, wenn ein Stoff aus seinen Elementen entsteht. Die Standardbildungsenthalpie (ΔfH°m) gilt bei 25°C und 101,3 kPa - wichtige Referenzbedingungen für deine Berechnungen.
Elemente in ihrer stabilsten Form haben ΔfH°m = 0. Das ist dein Nullpunkt für alle Berechnungen. Bindungsenthalpien beschreiben die Energie zum Spalten von Bindungen (immer positiv!).
Mit dem Satz von Hess berechnest du: ΔrH° = Σn·ΔfH°(Produkte) - Σn·ΔfH°(Edukte). So findest du heraus, ob eine Reaktion Energie liefert oder kostet.
Rechentrick: Kreisprozesse helfen dir bei komplexen Reaktionen - der Gesamtweg ist egal, nur Start- und Endpunkt zählen!
Brennwert (H₆) und Heizwert (Hᵢ) unterscheiden sich durch den Aggregatzustand des entstehenden Wassers. Brennwerte sind höher, weil die Kondensationswärme mitgenutzt wird.

Entropie und spontane Reaktionen
Entropie S ist das Maß für Unordnung - und die Natur liebt Unordnung! Der 2. Hauptsatz besagt: In abgeschlossenen Systemen nimmt die Entropie niemals ab.
Die Entropie steigt bei: größerem Raum für Teilchen, höherer Temperatur, mehr Gasteilchen oder Durchmischung. Phasenumwandlungen sind bei konstanter Temperatur reversibel: ΔS = Q/T.
Spontane Vorgänge erhöhen die Gesamtentropie des Systems plus Umgebung. Die Umgebung verliert bei exothermen Reaktionen Entropie , gewinnt sie bei endothermen.
Eselsbrücke: Feste Stoffe = niedrige Entropie (ordentlich), Gase = hohe Entropie (chaotisch)
Bei Standardbedingungen berechnest du: ΔrS°m = Σν(RP)·S°m(RP) - Σν(ED)·S°m(ED). Der dritte Hauptsatz definiert: Bei 0 K ist S = 0 für perfekte Kristalle.

Freie Enthalpie und Reaktionsvorhersage
Die freie Enthalpie G entscheidet, ob Reaktionen freiwillig ablaufen. Die Gibbs-Helmholtz-Gleichung kombiniert Enthalpie und Entropie: ΔG = ΔH - T·ΔS.
Exergonische Reaktionen (ΔG < 0) laufen freiwillig ab und haben Kc > 1. Endergonische Reaktionen (ΔG > 0) brauchen Energiezufuhr und haben Kc < 1. Bei ΔG = 0 herrscht Gleichgewicht.
Die vier Fälle der Temperaturabhängigkeit sind entscheidend: Nur wenn ΔH < 0 und ΔS > 0, läuft die Reaktion bei jeder Temperatur freiwillig ab. Bei anderen Kombinationen entscheidet die Temperatur.
Faustregel: ΔG < -30 kJ → 100% Umsatz, ΔG > +30 kJ → 0% Umsatz, dazwischen → Gleichgewicht
Metastabile Systeme sind thermodynamisch instabil, aber kinetisch gehemmt. Sie brauchen erst Aktivierungsenergie, bevor sie spontan reagieren können.

Säure-Base-Theorie nach Brønsted
Nach Brønsted sind Säuren Protonendonatoren (geben H⁺ ab), Basen sind Protonenakzeptoren (nehmen H⁺ auf). Ampholyte wie Wasser können beides, je nach Reaktionspartner.
Korrespondierende Säure-Base-Paare gehören zusammen - sie unterscheiden sich nur um ein Proton. Für jede Protolyse brauchst du zwei solche Paare.
Die Autoprotolyse des Wassers liefert das Ionenprodukt: Kw = c(H₃O⁺)·c(OH⁻) = 10⁻¹⁴ mol²/L². Daraus folgt: pH + pOH = 14.
pH-Skala verstehen: pH < 7 = sauer, pH = 7 = neutral, pH > 7 = basisch
Säure- und Basestärke hängen von Ks bzw. KB ab. Starke Säuren (pKs < 1,74) dissoziieren fast vollständig, schwache (pKs > 4,75) nur teilweise. Bei korrespondierenden Paaren gilt: pKs + pKB = 14.

pH-Berechnungen und Titrationen
Für starke Säuren gilt: c(H₃O⁺) = c₀(Säure), also pH = -lg{c₀}. Bei schwachen Säuren musst du die Gleichgewichtslage berücksichtigen: pH über Ks berechnen.
Titrationen bestimmen unbekannte Konzentrationen. Am Äquivalenzpunkt sind alle H₃O⁺-Ionen neutralisiert: n₁ = n₂, also c₁V₁ = c₂V₂.
Bei starker Säure + starker Base liegt der Äquivalenzpunkt bei pH = 7. Bei schwacher Säure + starker Base liegt er im basischen Bereich, weil die korrespondierende Base reagiert.
Titrationskurven lesen: Starker pH-Sprung = Äquivalenzpunkt, flacher Bereich davor = Pufferbereich
Indikatoren sind schwache Säuren/Basen mit verschiedenfarbigen Formen. Der Umschlagpunkt liegt bei pH = pKs(Indikator) ± 1. Du wählst den Indikator so, dass er beim Äquivalenzpunkt umschlägt.
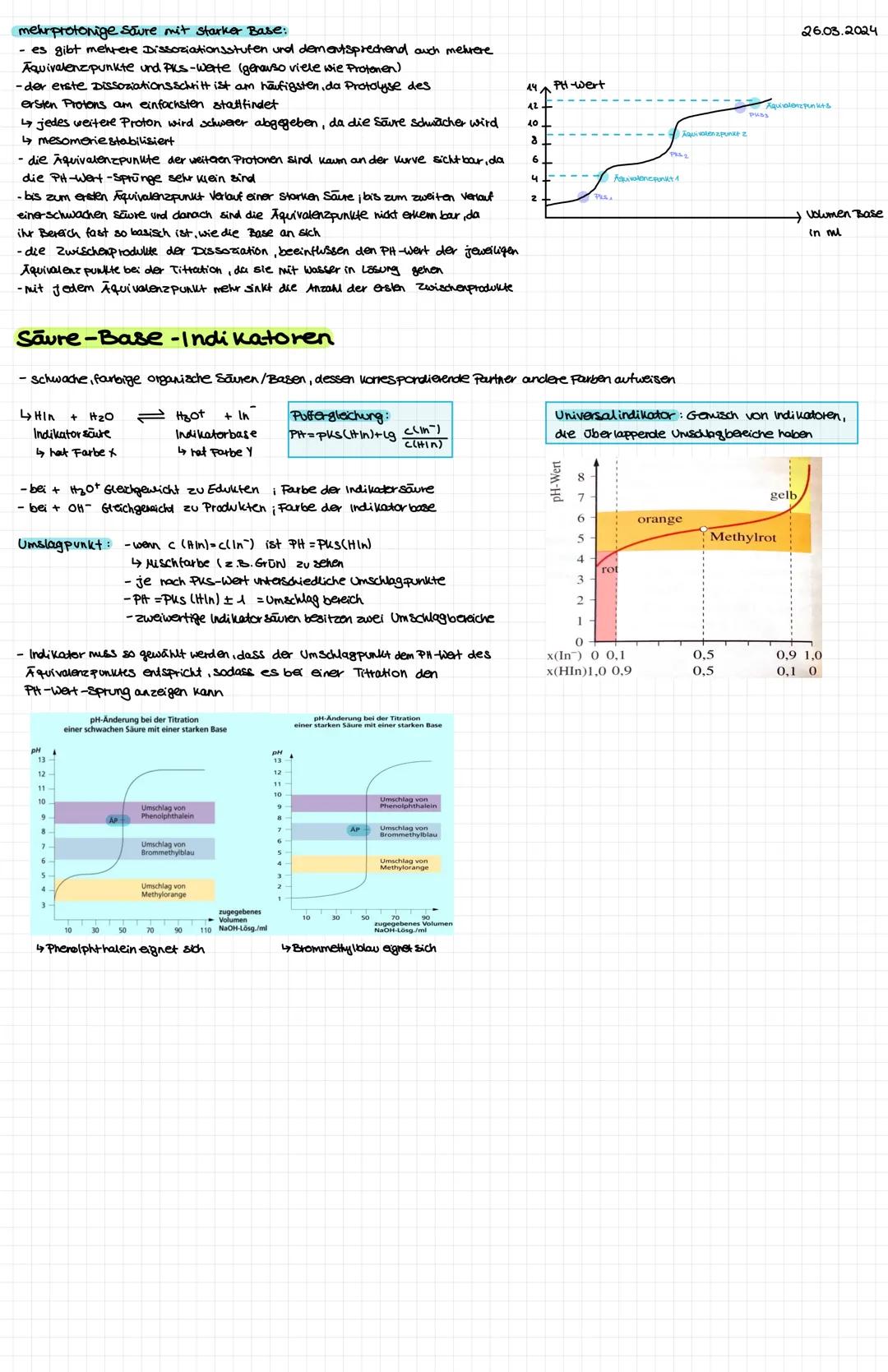
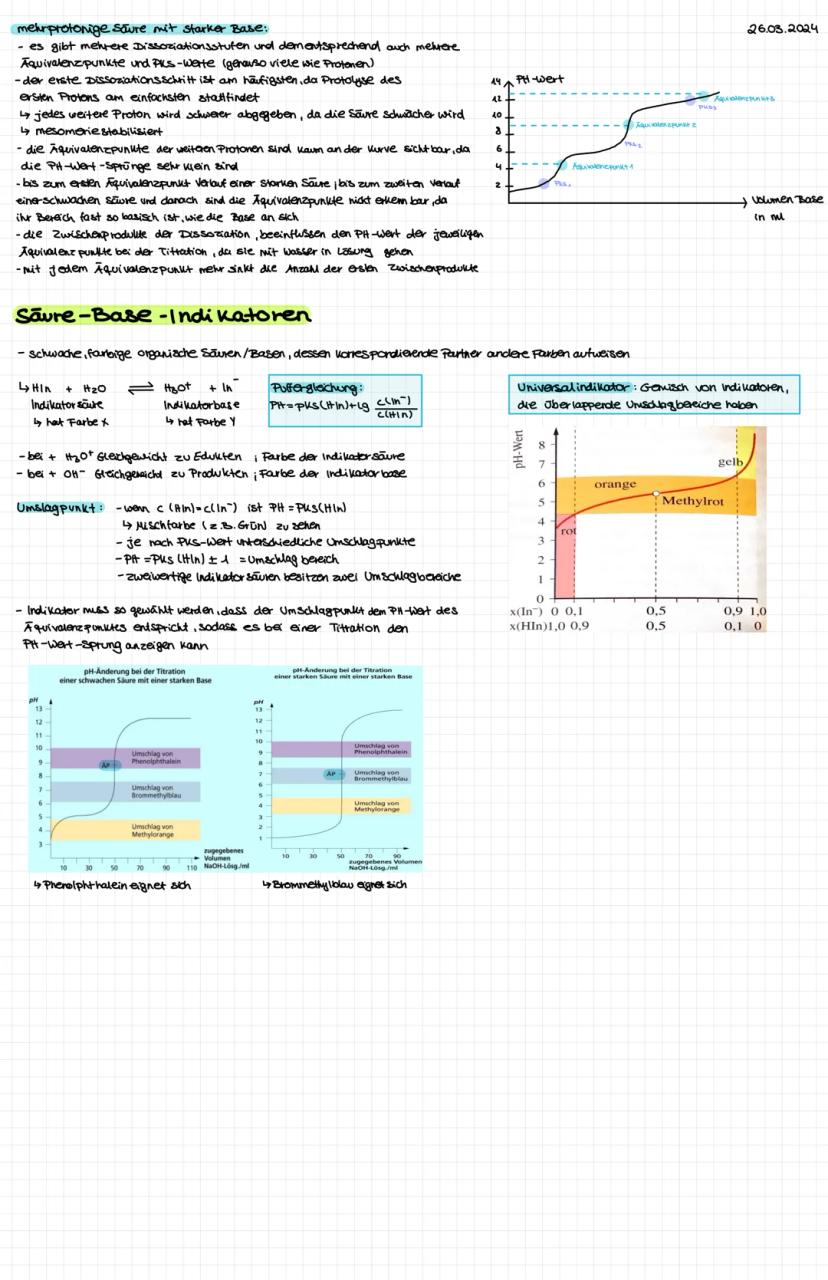
Mehrprotonige Säuren und Indikatorauswahl
Mehrprotonige Säuren haben mehrere Dissoziationsstufen und entsprechend viele pKs-Werte. Jedes weitere Proton wird schwerer abgegeben, weil die Säure schwächer wird.
Die Titrationskurve zeigt mehrere Äquivalenzpunkte, aber nur die ersten sind deutlich sichtbar. Spätere pH-Sprünge werden immer kleiner und sind kaum erkennbar.
Universalindikatoren sind Gemische verschiedener Indikatoren mit überlappenden Umschlagbereichen. Sie zeigen kontinuierliche Farbwechsel über große pH-Bereiche.
Indikatorwahl: Der Umschlagpunkt muss zum pH-Wert des Äquivalenzpunkts passen!
Zwischenprodukte der Dissoziation beeinflussen die pH-Werte der Äquivalenzpunkte, weil sie selbst als Säuren oder Basen wirken können. Das macht die Vorhersage komplexer.

Puffersysteme
Puffer bestehen aus einer schwachen Säure plus ihrem korrespondierenden Salz. Sie halten den pH-Wert konstant, indem sie zugegebene H₃O⁺ oder OH⁻ "abfangen".
Bei H₃O⁺-Zugabe reagiert die Pufferbase (A⁻): H₃O⁺ + A⁻ → HA + H₂O. Bei OH⁻-Zugabe reagiert die Puffersäure (HA): OH⁻ + HA → A⁻ + H₂O.
Die Henderson-Hasselbalch-Gleichung beschreibt Puffer: pH = pKs + lg. Bei pH = pKs ist die Pufferwirkung optimal .
Körperchemie: Der Blut-pH (7,4) wird durch den CO₂/HCO₃⁻-Puffer konstant gehalten - lebenswichtig!
Pufferkapazität zeigt, wie viel Säure/Base der Puffer verkraftet. Sie ist bei pH = pKs ± 1 noch gut, darüber hinaus bricht sie zusammen. Höhere Konzentrationen = größere Kapazität.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Equilibrium
9Chemisches Gleichgewicht verstehen
Erfahren Sie alles über das chemische Gleichgewicht, das Prinzip von Le Chatelier, das Massenwirkungsgesetz und die Bedeutung von Säure-Base-Titrationen. Diese Zusammenfassung behandelt die Temperatur- und Konzentrationsabhängigkeit von Reaktionen, die Berechnung von Gleichgewichtskonstanten und die Analyse von Titrationskurven. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemische Gleichgewichte & Säure-Base-Reaktionen
Vertiefte Analyse chemischer Gleichgewichte und Säure-Base-Reaktionen. Diese Klausur behandelt wichtige Konzepte wie das Massenwirkungsgesetz, pH-Wert-Berechnungen, das Deacon-Verfahren und die Veresterung von Carbonsäuren. Ideal für Schüler im Leistungskurs Chemie, die sich auf Prüfungen vorbereiten. Enthält Aufgaben zu ionischen Gleichungen, dem Haber-Bosch-Verfahren und der elektrolytischen Dissoziation.
Chemisches Gleichgewicht verstehen
Erforschen Sie die Konzepte des chemischen Gleichgewichts, einschließlich der Gleichgewichtskonstanten (K und k), dynamischen Gleichgewichts und des Prinzips von Le Chatelier. Diese Zusammenfassung bietet eine klare Erklärung der Reaktionsgeschwindigkeiten, der Massenwirkungsgesetze und der Unterschiede zwischen homogenen und heterogenen Gleichgewichten. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemisches Gleichgewicht und Katalysatoren
Erfahren Sie alles über das chemische Gleichgewicht, einschließlich der Merkmale, des Einflusses von Katalysatoren, des Massenwirkungsgesetzes, der Gleichgewichtskonstanten und des Prinzips von Le Chatelier. Diese Zusammenfassung bietet eine klare Übersicht über die Dynamik chemischer Reaktionen und deren Gleichgewichte, einschließlich Löslichkeitsprodukte und gekoppelte Gleichgewichte. Ideal für Studierende der Chemie.
Reaktionsgeschwindigkeit & Gleichgewicht
Erforschen Sie die Konzepte der Reaktionsgeschwindigkeit und des chemischen Gleichgewichts. Diese Zusammenfassung behandelt die Definitionen, Berechnungen und Einflussfaktoren auf die Reaktionsgeschwindigkeit sowie die Prinzipien des chemischen Gleichgewichts und deren Störungen. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Kinetik und Gleichgewicht
Entdecke die Grundlagen der Reaktionskinetik und des chemischen Gleichgewichts in dieser umfassenden Zusammenfassung. Enthält wichtige Konzepte wie endotherme und exotherme Reaktionen, dynamisches Gleichgewicht, sowie chemische Berechnungen. Ideal für die Vorbereitung auf Klausuren mit praktischen Übungsaufgaben zur Vertiefung des Wissens.
Gleichgewicht von Reaktionen
Erforschen Sie das Gleichgewicht chemischer Reaktionen mit diesem detaillierten Versuchsprotokoll. Der Versuch demonstriert die Prinzipien des Stoffumsatzes und der Reaktionsgeschwindigkeit durch den Einsatz von Messzylindern und Pipetten. Ideal für Studierende der Chemie, die ein tieferes Verständnis für chemische Gleichgewichte und deren Beobachtungen entwickeln möchten.
Chemisches Gleichgewicht Experiment
Entdecken Sie ein praktisches Modellexperiment, das die Prinzipien des chemischen Gleichgewichts veranschaulicht. Erfahren Sie, wie die Konzentrationen von Edukten und Produkten sich während einer umkehrbaren Reaktion verändern und wie Geschwindigkeitskonstanten die Reaktionsdynamik beeinflussen. Ideal für Chemie-Studierende, die die Konzepte von Reaktionsgeschwindigkeit und Gleichgewicht verstehen möchten.
Esterbildung und Gleichgewicht
Diese Zusammenfassung behandelt die Reaktion zwischen Ethanol und Essigsäure zur Bildung von Estern und Wasser. Sie erklärt das Konzept des chemischen Gleichgewichts, die Rolle der Diffusion und die Gleichverteilung der Moleküle. Ideal für Studierende der Chemie, die die Grundlagen der Esterbildung verstehen möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Abitur Chemie LK Lernzettel 2024 – Bestens vorbereitet!
Gleichgewichtsreaktionen zeigen dir, wie chemische Reaktionen funktionieren, wenn sie nicht vollständig ablaufen. Du lernst hier alles über dynamische Gleichgewichte, das Massenwirkungsgesetz und wie du vorhersagst, ob eine Reaktion freiwillig abläuft - wichtiges Wissen für dein Abi!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Grundlagen Gleichgewichtsreaktionen
Dynamisches Gleichgewicht heißt: Die Reaktion läuft trotzdem weiter, aber Hin- und Rückreaktion sind gleich schnell. Du siehst keine Veränderung mehr, obwohl ständig Moleküle reagieren. Das ist der Unterschied zum statischen Gleichgewicht wie bei einer Waage.
Beim chemischen Gleichgewicht findest du sowohl Edukte als auch Produkte vor. Die Reaktion ist reversibel und läuft nie vollständig ab. Die Zeit bis zum Gleichgewicht nennt man Einstellzeit.
Das Massenwirkungsgesetz beschreibt mathematisch, wo das Gleichgewicht liegt. Die Gleichgewichtskonstante Kc zeigt dir: Ist Kc > 1, hast du mehr Produkte. Ist Kc < 1, überwiegen die Edukte.
Merke dir: Kc = (Konzentration Produkte)/(Konzentration Edukte) - dabei werden die Stöchiometriezahlen zu Exponenten!
Du rechnest drei Hauptaufgaben: Bestimmung von Kc aus Gleichgewichtskonzentrationen, Berechnung der Produktmenge bei bekanntem Kc und Ausbeute-Berechnungen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Le Chatelier-Prinzip und Katalysatoren
Das Prinzip von Le Chatelier ist dein Werkzeug zur Vorhersage: Störst du ein Gleichgewicht, weicht das System so aus, dass die Störung minimiert wird.
Bei Temperaturerhöhung verschiebt sich das Gleichgewicht zur endothermen Seite. Bei Konzentrationserhöhung einer Komponente weicht das System durch deren Verbrauch aus.
Druckerhöhung (nur bei Gasen!) verschiebt das Gleichgewicht zur Seite mit weniger Teilchen - das System "macht sich kleiner". Das Haber-Bosch-Verfahren nutzt das: Hoher Druck und Katalysator für mehr Ammoniak.
Praxistipp: Die RGT-Regel besagt: +10°C verdoppelt die Reaktionsgeschwindigkeit!
Katalysatoren beschleunigen beide Reaktionsrichtungen gleich stark. Sie senken die Aktivierungsenergie durch alternative Reaktionswege, ändern aber nie die Lage des Gleichgewichts. Bei der heterogenen Katalyse (verschiedene Phasen) adsorbieren Moleküle an Metalloberflächen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Energetik chemischer Reaktionen
Die innere Energie U setzt sich aus Kernenergie, chemischer Energie und thermischer Energie zusammen. Der 1. Hauptsatz besagt: Energie kann nicht verschwinden, nur umgewandelt werden.
Bei isobaren Prozessen (konstanter Druck) gilt: ΔU = Q - P·ΔV. Die Enthalpie H ist praktischer als U, weil sie die Volumenarbeit schon einrechnet: ΔH = ΔU + P·ΔV.
Exotherme Reaktionen (ΔH < 0) geben Wärme ab, endotherme (ΔH > 0) nehmen Wärme auf. Die molare Reaktionsenthalpie bezieht sich auf einen Formelumsatz.
Wichtig: Bei Gasen rechnest du: ΔrHm ≈ ΔrUm - P·R·T, bei Flüssigkeiten und Feststoffen: ΔrHm ≈ ΔrUm
Kalorimetrie misst Wärmemengen über Temperaturänderungen: Q = c·m·ΔT. Der Satz von Hess erlaubt dir, Reaktionsenthalpien aus Bildungsenthalpien zu berechnen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Bildungs- und Verbrennungsenthalpien
Bildungsenthalpien geben an, wie viel Energie frei wird, wenn ein Stoff aus seinen Elementen entsteht. Die Standardbildungsenthalpie (ΔfH°m) gilt bei 25°C und 101,3 kPa - wichtige Referenzbedingungen für deine Berechnungen.
Elemente in ihrer stabilsten Form haben ΔfH°m = 0. Das ist dein Nullpunkt für alle Berechnungen. Bindungsenthalpien beschreiben die Energie zum Spalten von Bindungen (immer positiv!).
Mit dem Satz von Hess berechnest du: ΔrH° = Σn·ΔfH°(Produkte) - Σn·ΔfH°(Edukte). So findest du heraus, ob eine Reaktion Energie liefert oder kostet.
Rechentrick: Kreisprozesse helfen dir bei komplexen Reaktionen - der Gesamtweg ist egal, nur Start- und Endpunkt zählen!
Brennwert (H₆) und Heizwert (Hᵢ) unterscheiden sich durch den Aggregatzustand des entstehenden Wassers. Brennwerte sind höher, weil die Kondensationswärme mitgenutzt wird.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Entropie und spontane Reaktionen
Entropie S ist das Maß für Unordnung - und die Natur liebt Unordnung! Der 2. Hauptsatz besagt: In abgeschlossenen Systemen nimmt die Entropie niemals ab.
Die Entropie steigt bei: größerem Raum für Teilchen, höherer Temperatur, mehr Gasteilchen oder Durchmischung. Phasenumwandlungen sind bei konstanter Temperatur reversibel: ΔS = Q/T.
Spontane Vorgänge erhöhen die Gesamtentropie des Systems plus Umgebung. Die Umgebung verliert bei exothermen Reaktionen Entropie , gewinnt sie bei endothermen.
Eselsbrücke: Feste Stoffe = niedrige Entropie (ordentlich), Gase = hohe Entropie (chaotisch)
Bei Standardbedingungen berechnest du: ΔrS°m = Σν(RP)·S°m(RP) - Σν(ED)·S°m(ED). Der dritte Hauptsatz definiert: Bei 0 K ist S = 0 für perfekte Kristalle.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Freie Enthalpie und Reaktionsvorhersage
Die freie Enthalpie G entscheidet, ob Reaktionen freiwillig ablaufen. Die Gibbs-Helmholtz-Gleichung kombiniert Enthalpie und Entropie: ΔG = ΔH - T·ΔS.
Exergonische Reaktionen (ΔG < 0) laufen freiwillig ab und haben Kc > 1. Endergonische Reaktionen (ΔG > 0) brauchen Energiezufuhr und haben Kc < 1. Bei ΔG = 0 herrscht Gleichgewicht.
Die vier Fälle der Temperaturabhängigkeit sind entscheidend: Nur wenn ΔH < 0 und ΔS > 0, läuft die Reaktion bei jeder Temperatur freiwillig ab. Bei anderen Kombinationen entscheidet die Temperatur.
Faustregel: ΔG < -30 kJ → 100% Umsatz, ΔG > +30 kJ → 0% Umsatz, dazwischen → Gleichgewicht
Metastabile Systeme sind thermodynamisch instabil, aber kinetisch gehemmt. Sie brauchen erst Aktivierungsenergie, bevor sie spontan reagieren können.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Säure-Base-Theorie nach Brønsted
Nach Brønsted sind Säuren Protonendonatoren (geben H⁺ ab), Basen sind Protonenakzeptoren (nehmen H⁺ auf). Ampholyte wie Wasser können beides, je nach Reaktionspartner.
Korrespondierende Säure-Base-Paare gehören zusammen - sie unterscheiden sich nur um ein Proton. Für jede Protolyse brauchst du zwei solche Paare.
Die Autoprotolyse des Wassers liefert das Ionenprodukt: Kw = c(H₃O⁺)·c(OH⁻) = 10⁻¹⁴ mol²/L². Daraus folgt: pH + pOH = 14.
pH-Skala verstehen: pH < 7 = sauer, pH = 7 = neutral, pH > 7 = basisch
Säure- und Basestärke hängen von Ks bzw. KB ab. Starke Säuren (pKs < 1,74) dissoziieren fast vollständig, schwache (pKs > 4,75) nur teilweise. Bei korrespondierenden Paaren gilt: pKs + pKB = 14.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
pH-Berechnungen und Titrationen
Für starke Säuren gilt: c(H₃O⁺) = c₀(Säure), also pH = -lg{c₀}. Bei schwachen Säuren musst du die Gleichgewichtslage berücksichtigen: pH über Ks berechnen.
Titrationen bestimmen unbekannte Konzentrationen. Am Äquivalenzpunkt sind alle H₃O⁺-Ionen neutralisiert: n₁ = n₂, also c₁V₁ = c₂V₂.
Bei starker Säure + starker Base liegt der Äquivalenzpunkt bei pH = 7. Bei schwacher Säure + starker Base liegt er im basischen Bereich, weil die korrespondierende Base reagiert.
Titrationskurven lesen: Starker pH-Sprung = Äquivalenzpunkt, flacher Bereich davor = Pufferbereich
Indikatoren sind schwache Säuren/Basen mit verschiedenfarbigen Formen. Der Umschlagpunkt liegt bei pH = pKs(Indikator) ± 1. Du wählst den Indikator so, dass er beim Äquivalenzpunkt umschlägt.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Mehrprotonige Säuren und Indikatorauswahl
Mehrprotonige Säuren haben mehrere Dissoziationsstufen und entsprechend viele pKs-Werte. Jedes weitere Proton wird schwerer abgegeben, weil die Säure schwächer wird.
Die Titrationskurve zeigt mehrere Äquivalenzpunkte, aber nur die ersten sind deutlich sichtbar. Spätere pH-Sprünge werden immer kleiner und sind kaum erkennbar.
Universalindikatoren sind Gemische verschiedener Indikatoren mit überlappenden Umschlagbereichen. Sie zeigen kontinuierliche Farbwechsel über große pH-Bereiche.
Indikatorwahl: Der Umschlagpunkt muss zum pH-Wert des Äquivalenzpunkts passen!
Zwischenprodukte der Dissoziation beeinflussen die pH-Werte der Äquivalenzpunkte, weil sie selbst als Säuren oder Basen wirken können. Das macht die Vorhersage komplexer.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Puffersysteme
Puffer bestehen aus einer schwachen Säure plus ihrem korrespondierenden Salz. Sie halten den pH-Wert konstant, indem sie zugegebene H₃O⁺ oder OH⁻ "abfangen".
Bei H₃O⁺-Zugabe reagiert die Pufferbase (A⁻): H₃O⁺ + A⁻ → HA + H₂O. Bei OH⁻-Zugabe reagiert die Puffersäure (HA): OH⁻ + HA → A⁻ + H₂O.
Die Henderson-Hasselbalch-Gleichung beschreibt Puffer: pH = pKs + lg. Bei pH = pKs ist die Pufferwirkung optimal .
Körperchemie: Der Blut-pH (7,4) wird durch den CO₂/HCO₃⁻-Puffer konstant gehalten - lebenswichtig!
Pufferkapazität zeigt, wie viel Säure/Base der Puffer verkraftet. Sie ist bei pH = pKs ± 1 noch gut, darüber hinaus bricht sie zusammen. Höhere Konzentrationen = größere Kapazität.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Equilibrium
9Chemisches Gleichgewicht verstehen
Erfahren Sie alles über das chemische Gleichgewicht, das Prinzip von Le Chatelier, das Massenwirkungsgesetz und die Bedeutung von Säure-Base-Titrationen. Diese Zusammenfassung behandelt die Temperatur- und Konzentrationsabhängigkeit von Reaktionen, die Berechnung von Gleichgewichtskonstanten und die Analyse von Titrationskurven. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemische Gleichgewichte & Säure-Base-Reaktionen
Vertiefte Analyse chemischer Gleichgewichte und Säure-Base-Reaktionen. Diese Klausur behandelt wichtige Konzepte wie das Massenwirkungsgesetz, pH-Wert-Berechnungen, das Deacon-Verfahren und die Veresterung von Carbonsäuren. Ideal für Schüler im Leistungskurs Chemie, die sich auf Prüfungen vorbereiten. Enthält Aufgaben zu ionischen Gleichungen, dem Haber-Bosch-Verfahren und der elektrolytischen Dissoziation.
Chemisches Gleichgewicht verstehen
Erforschen Sie die Konzepte des chemischen Gleichgewichts, einschließlich der Gleichgewichtskonstanten (K und k), dynamischen Gleichgewichts und des Prinzips von Le Chatelier. Diese Zusammenfassung bietet eine klare Erklärung der Reaktionsgeschwindigkeiten, der Massenwirkungsgesetze und der Unterschiede zwischen homogenen und heterogenen Gleichgewichten. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemisches Gleichgewicht und Katalysatoren
Erfahren Sie alles über das chemische Gleichgewicht, einschließlich der Merkmale, des Einflusses von Katalysatoren, des Massenwirkungsgesetzes, der Gleichgewichtskonstanten und des Prinzips von Le Chatelier. Diese Zusammenfassung bietet eine klare Übersicht über die Dynamik chemischer Reaktionen und deren Gleichgewichte, einschließlich Löslichkeitsprodukte und gekoppelte Gleichgewichte. Ideal für Studierende der Chemie.
Reaktionsgeschwindigkeit & Gleichgewicht
Erforschen Sie die Konzepte der Reaktionsgeschwindigkeit und des chemischen Gleichgewichts. Diese Zusammenfassung behandelt die Definitionen, Berechnungen und Einflussfaktoren auf die Reaktionsgeschwindigkeit sowie die Prinzipien des chemischen Gleichgewichts und deren Störungen. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Kinetik und Gleichgewicht
Entdecke die Grundlagen der Reaktionskinetik und des chemischen Gleichgewichts in dieser umfassenden Zusammenfassung. Enthält wichtige Konzepte wie endotherme und exotherme Reaktionen, dynamisches Gleichgewicht, sowie chemische Berechnungen. Ideal für die Vorbereitung auf Klausuren mit praktischen Übungsaufgaben zur Vertiefung des Wissens.
Gleichgewicht von Reaktionen
Erforschen Sie das Gleichgewicht chemischer Reaktionen mit diesem detaillierten Versuchsprotokoll. Der Versuch demonstriert die Prinzipien des Stoffumsatzes und der Reaktionsgeschwindigkeit durch den Einsatz von Messzylindern und Pipetten. Ideal für Studierende der Chemie, die ein tieferes Verständnis für chemische Gleichgewichte und deren Beobachtungen entwickeln möchten.
Chemisches Gleichgewicht Experiment
Entdecken Sie ein praktisches Modellexperiment, das die Prinzipien des chemischen Gleichgewichts veranschaulicht. Erfahren Sie, wie die Konzentrationen von Edukten und Produkten sich während einer umkehrbaren Reaktion verändern und wie Geschwindigkeitskonstanten die Reaktionsdynamik beeinflussen. Ideal für Chemie-Studierende, die die Konzepte von Reaktionsgeschwindigkeit und Gleichgewicht verstehen möchten.
Esterbildung und Gleichgewicht
Diese Zusammenfassung behandelt die Reaktion zwischen Ethanol und Essigsäure zur Bildung von Estern und Wasser. Sie erklärt das Konzept des chemischen Gleichgewichts, die Rolle der Diffusion und die Gleichverteilung der Moleküle. Ideal für Studierende der Chemie, die die Grundlagen der Esterbildung verstehen möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.