Die Bindungslehre erklärt dir, wie Atome sich miteinander verbinden und... Mehr anzeigen
Melde dich an, um den Inhalt zu sehenKostenlos!
Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Knowunity KI
Fächer
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Alle Themen anzeigen
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Alle Themen anzeigen
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Alle Themen anzeigen
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Alle Themen anzeigen
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Alle Themen anzeigen
959
•
Aktualisiert Apr 27, 2026
•
Alex H
@lex_ouakt4o9nmkhbsv4
Die Bindungslehre erklärt dir, wie Atome sich miteinander verbinden und... Mehr anzeigen
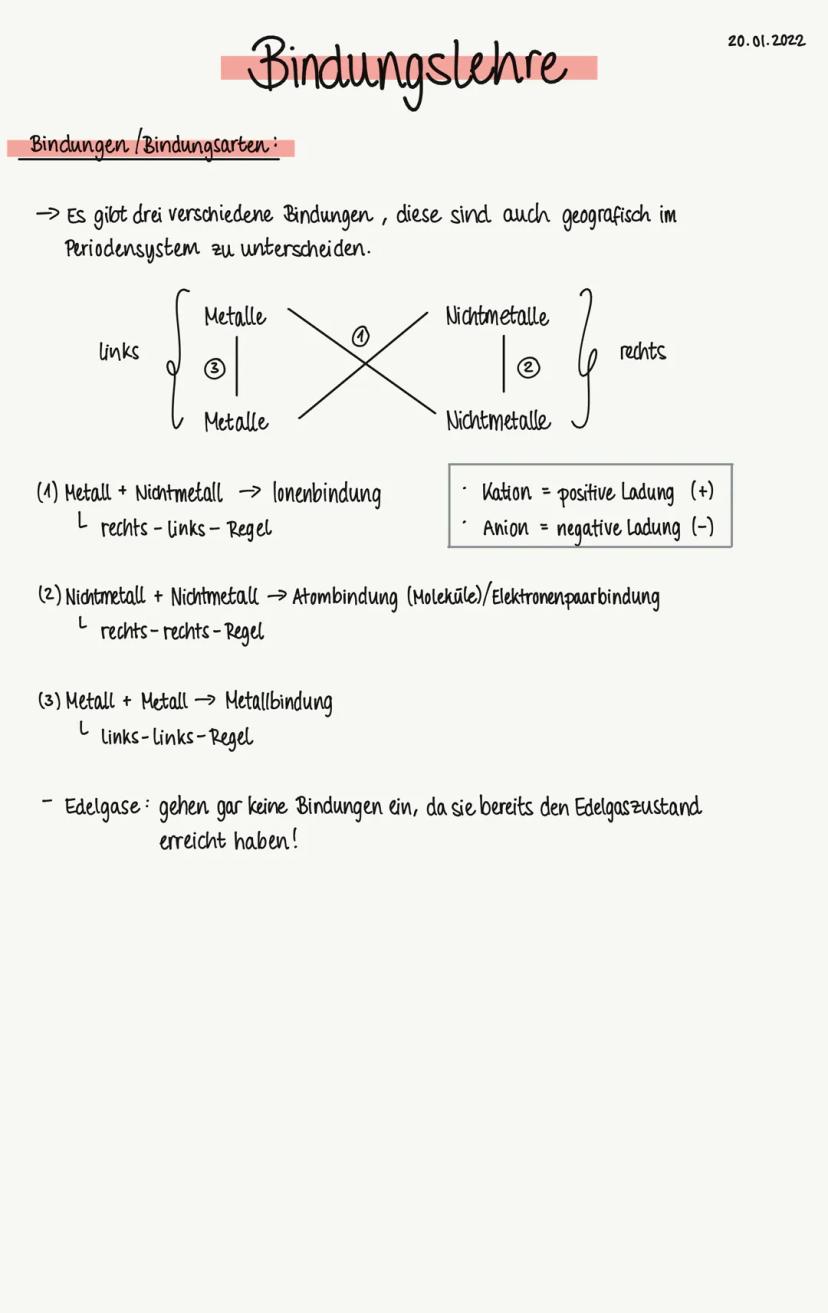





Stell dir das Periodensystem wie eine Landkarte vor: Links stehen die Metalle, rechts die Nichtmetalle. Je nachdem, welche "Nachbarn" sich treffen, entstehen verschiedene Bindungen.
Es gibt drei einfache Regeln: Metall + Nichtmetall ergibt eine Ionenbindung . Nichtmetall + Nichtmetall führt zur Atombindung . Metall + Metall bildet eine Metallbindung .
Die Edelgase sind die Einzelgänger - sie gehen gar keine Bindungen ein, weil sie bereits perfekt "zufrieden" sind! Wichtig für Tests: Kationen sind positiv geladen (+), Anionen negativ (-).
💡 Merktipp: Die Position im Periodensystem verrät dir sofort, welche Bindung entsteht!

Bei der Ionenbindung passiert ein echter Elektronentausch zwischen Metall und Nichtmetall. Das Metall gibt Elektronen ab und wird zum Kation (positiv geladen). Das Nichtmetall nimmt diese Elektronen auf und wird zum Anion (negativ geladen).
Der Grund liegt in der Elektronegativität: Nichtmetalle ziehen Elektronen stärker an als Metalle. Deshalb wandern die Elektronen vom Metall zum Nichtmetall - ein klarer Besitzerwechsel!
Diese gegensätzlich geladenen Teilchen ziehen sich stark an und bilden ein regelmäßiges Ionengitter. Je stabiler dieses Gitter, desto höher der Schmelzpunkt. Alle festen Stoffe mit Ionenbindung nennt man Salze.
Das bekannteste Beispiel kennst du aus der Küche: Natriumchlorid (NaCl) - unser Kochsalz!
🔥 Prüfungswissen: Oxidation = Elektronenabgabe, Reduktion = Elektronenaufnahme

Die Atombindung entsteht, wenn sich zwei Nichtmetalle treffen und beide den Edelgaszustand erreichen wollen. Da keiner deutlich "stärker" ist, teilen sie sich einfach die Elektronen!
Diese geteilten Elektronenpaare halten die Atome zusammen. Ein Elektronenpaar = Einfachbindung, zwei Paare = Doppelbindung, drei Paare = Dreifachbindung. Die Dreifachbindung ist am stärksten, aber auch am seltensten.
Verbindungen mit Atombindungen heißen Moleküle. Manche Elemente wie Wasserstoff (H₂), Stickstoff (N₂) oder Sauerstoff (O₂) kommen bei Zimmertemperatur nur als zweiatomige Moleküle vor.
Das Elektronenpaarabstoßungsmodell erklärt die Form der Moleküle: Elektronenpaare stoßen sich ab und ordnen sich so weit wie möglich voneinander entfernt an. Freie Elektronenpaare brauchen dabei mehr Platz als bindende.
⚡ Gut zu wissen: Die räumliche Anordnung bestimmt viele Eigenschaften des Moleküls!

Bei gleichen Atomen teilen sich die Elektronen fair - das bindende Elektronenpaar sitzt genau in der Mitte. Bei ungleichen Atomen zieht der elektronegativere Partner stärker und die Elektronen verschieben sich zu ihm hin.
Diese ungleiche Verteilung erzeugt Partialladungen: δ- (delta minus) für die negative, δ+ (delta plus) für die positive Seite. So entstehen Dipole - Moleküle mit einem Plus- und einem Minuspol.
Die Elektronegativitätsdifferenz entscheidet über die Bindungsart: 0-0,2 = unpolar, ab 0,3 = polar, über 1,7 = Ionenbindung. Aber Achtung: Eine polare Bindung macht noch kein polares Molekül!
Bei symmetrischem Molekülbau heben sich die Ladungen gegenseitig auf - das Molekül bleibt unpolar. Nur bei unsymmetrischem Bau entsteht ein echtes Dipolmolekül.
🎯 Eselsbrücke: Symmetrie = Ladungen fallen zusammen = unpolar!

Zwischenmolekulare Kräfte erklären, warum Wasser bei 100°C siedet, aber Methan schon bei -162°C. Diese Anziehungskräfte zwischen Molekülen bestimmen Schmelz- und Siedepunkte sowie die Löslichkeit.
Van-der-Waals-Kräfte sind die schwächsten Kräfte. Sie entstehen durch zufällige Elektronenbewegungen, die temporäre Dipole erzeugen. Diese beeinflussen benachbarte Moleküle und erzeugen weitere temporäre Dipole. Je mehr Elektronen ein Molekül hat, desto stärker werden diese Kräfte.
Dipol-Dipol-Wechselwirkungen sind stärker und wirken nur zwischen polaren Molekülen. Der negative Pol eines Moleküls zieht den positiven Pol eines anderen an.
Wasserstoffbrücken sind die stärksten zwischenmolekularen Kräfte. Du brauchst ein H-Atom an N, O oder F (aktive Stelle) und ein freies Elektronenpaar an N, O oder F (passive Stelle).
🔬 Laborwissen: Wasserstoffbrücken erklären, warum Wasser so besondere Eigenschaften hat!

Die räumliche Anordnung von Atomen bestimmt, ob ein Molekül polar oder unpolar ist. Zuerst berechnest du die Elektronegativitätsdifferenz: unter 0,3 = immer unpolar, über 0,3 = möglicherweise polar.
Bei polaren Bindungen entscheidet die Symmetrie: Symmetrischer Bau = Ladungsschwerpunkte fallen zusammen = unpolares Molekül. Unsymmetrischer Bau = Dipol.
Für die Molekülgeometrie zählst du alle Elektronenpaare am Zentralatom: Ein Elektronenpaar = nebeneinander. Zwei Paare = linear (180°) oder gewinkelt (105°) mit freiem Paar. Drei Paare = planar (120°) oder pyramidal (107°) mit freiem Paar.
Vier bindende Elektronenpaare ergeben immer eine tetraedrische Form (109,5°). Freie Elektronenpaare brauchen mehr Platz als bindende und "drücken" die anderen nach unten.
📐 Geometrie-Regel: Freies Elektronenpaar > Mehrfachbindung > Einfachbindung beim Raumbedarf!
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Alex H
@lex_ouakt4o9nmkhbsv4
Die Bindungslehre erklärt dir, wie Atome sich miteinander verbinden und warum verschiedene Stoffe so unterschiedliche Eigenschaften haben. Du lernst hier die drei wichtigsten Bindungsarten kennen und verstehst, warum manche Stoffe Strom leiten können und andere nicht.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
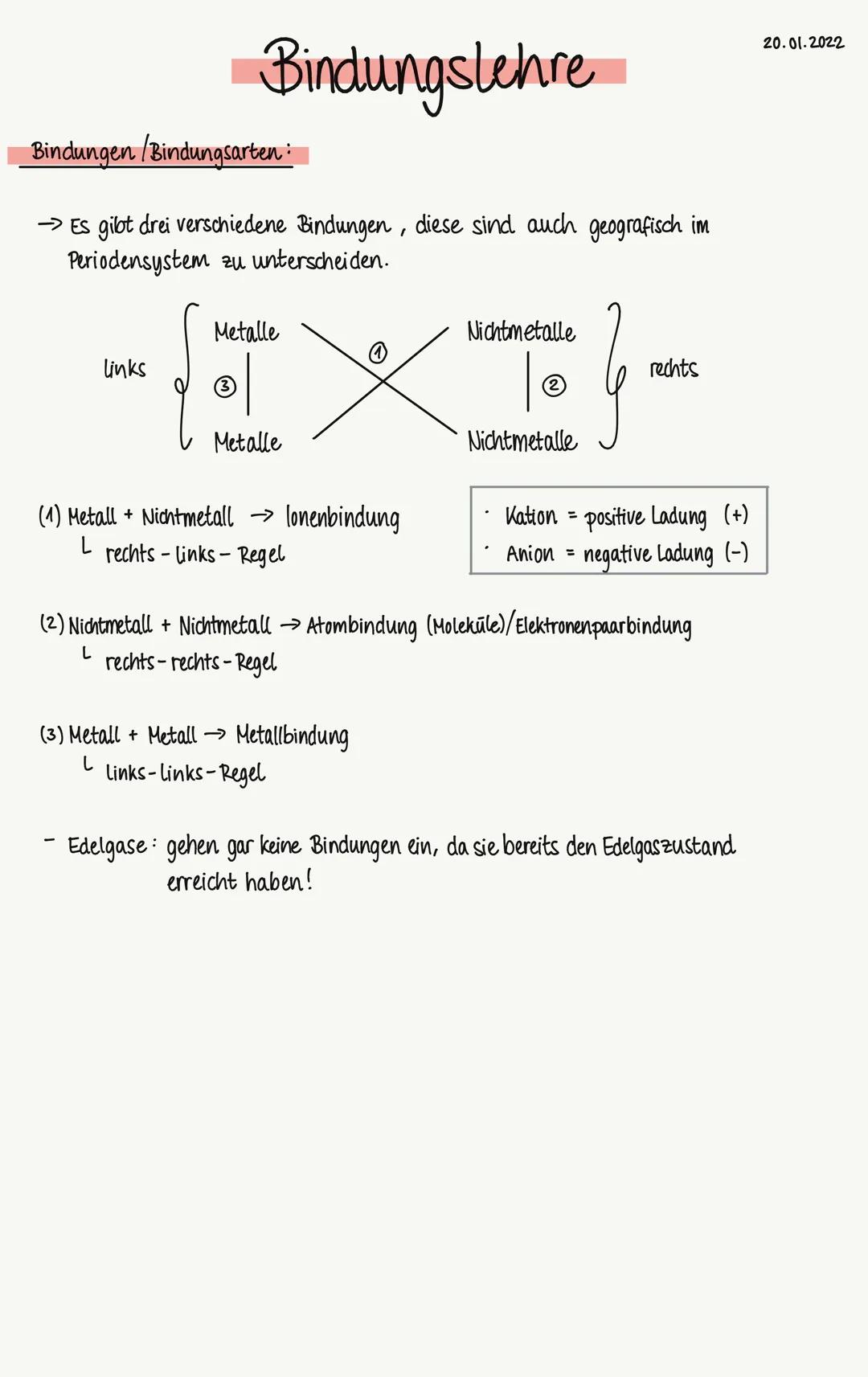
Stell dir das Periodensystem wie eine Landkarte vor: Links stehen die Metalle, rechts die Nichtmetalle. Je nachdem, welche "Nachbarn" sich treffen, entstehen verschiedene Bindungen.
Es gibt drei einfache Regeln: Metall + Nichtmetall ergibt eine Ionenbindung . Nichtmetall + Nichtmetall führt zur Atombindung . Metall + Metall bildet eine Metallbindung .
Die Edelgase sind die Einzelgänger - sie gehen gar keine Bindungen ein, weil sie bereits perfekt "zufrieden" sind! Wichtig für Tests: Kationen sind positiv geladen (+), Anionen negativ (-).
💡 Merktipp: Die Position im Periodensystem verrät dir sofort, welche Bindung entsteht!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Bei der Ionenbindung passiert ein echter Elektronentausch zwischen Metall und Nichtmetall. Das Metall gibt Elektronen ab und wird zum Kation (positiv geladen). Das Nichtmetall nimmt diese Elektronen auf und wird zum Anion (negativ geladen).
Der Grund liegt in der Elektronegativität: Nichtmetalle ziehen Elektronen stärker an als Metalle. Deshalb wandern die Elektronen vom Metall zum Nichtmetall - ein klarer Besitzerwechsel!
Diese gegensätzlich geladenen Teilchen ziehen sich stark an und bilden ein regelmäßiges Ionengitter. Je stabiler dieses Gitter, desto höher der Schmelzpunkt. Alle festen Stoffe mit Ionenbindung nennt man Salze.
Das bekannteste Beispiel kennst du aus der Küche: Natriumchlorid (NaCl) - unser Kochsalz!
🔥 Prüfungswissen: Oxidation = Elektronenabgabe, Reduktion = Elektronenaufnahme

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Atombindung entsteht, wenn sich zwei Nichtmetalle treffen und beide den Edelgaszustand erreichen wollen. Da keiner deutlich "stärker" ist, teilen sie sich einfach die Elektronen!
Diese geteilten Elektronenpaare halten die Atome zusammen. Ein Elektronenpaar = Einfachbindung, zwei Paare = Doppelbindung, drei Paare = Dreifachbindung. Die Dreifachbindung ist am stärksten, aber auch am seltensten.
Verbindungen mit Atombindungen heißen Moleküle. Manche Elemente wie Wasserstoff (H₂), Stickstoff (N₂) oder Sauerstoff (O₂) kommen bei Zimmertemperatur nur als zweiatomige Moleküle vor.
Das Elektronenpaarabstoßungsmodell erklärt die Form der Moleküle: Elektronenpaare stoßen sich ab und ordnen sich so weit wie möglich voneinander entfernt an. Freie Elektronenpaare brauchen dabei mehr Platz als bindende.
⚡ Gut zu wissen: Die räumliche Anordnung bestimmt viele Eigenschaften des Moleküls!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Bei gleichen Atomen teilen sich die Elektronen fair - das bindende Elektronenpaar sitzt genau in der Mitte. Bei ungleichen Atomen zieht der elektronegativere Partner stärker und die Elektronen verschieben sich zu ihm hin.
Diese ungleiche Verteilung erzeugt Partialladungen: δ- (delta minus) für die negative, δ+ (delta plus) für die positive Seite. So entstehen Dipole - Moleküle mit einem Plus- und einem Minuspol.
Die Elektronegativitätsdifferenz entscheidet über die Bindungsart: 0-0,2 = unpolar, ab 0,3 = polar, über 1,7 = Ionenbindung. Aber Achtung: Eine polare Bindung macht noch kein polares Molekül!
Bei symmetrischem Molekülbau heben sich die Ladungen gegenseitig auf - das Molekül bleibt unpolar. Nur bei unsymmetrischem Bau entsteht ein echtes Dipolmolekül.
🎯 Eselsbrücke: Symmetrie = Ladungen fallen zusammen = unpolar!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Zwischenmolekulare Kräfte erklären, warum Wasser bei 100°C siedet, aber Methan schon bei -162°C. Diese Anziehungskräfte zwischen Molekülen bestimmen Schmelz- und Siedepunkte sowie die Löslichkeit.
Van-der-Waals-Kräfte sind die schwächsten Kräfte. Sie entstehen durch zufällige Elektronenbewegungen, die temporäre Dipole erzeugen. Diese beeinflussen benachbarte Moleküle und erzeugen weitere temporäre Dipole. Je mehr Elektronen ein Molekül hat, desto stärker werden diese Kräfte.
Dipol-Dipol-Wechselwirkungen sind stärker und wirken nur zwischen polaren Molekülen. Der negative Pol eines Moleküls zieht den positiven Pol eines anderen an.
Wasserstoffbrücken sind die stärksten zwischenmolekularen Kräfte. Du brauchst ein H-Atom an N, O oder F (aktive Stelle) und ein freies Elektronenpaar an N, O oder F (passive Stelle).
🔬 Laborwissen: Wasserstoffbrücken erklären, warum Wasser so besondere Eigenschaften hat!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die räumliche Anordnung von Atomen bestimmt, ob ein Molekül polar oder unpolar ist. Zuerst berechnest du die Elektronegativitätsdifferenz: unter 0,3 = immer unpolar, über 0,3 = möglicherweise polar.
Bei polaren Bindungen entscheidet die Symmetrie: Symmetrischer Bau = Ladungsschwerpunkte fallen zusammen = unpolares Molekül. Unsymmetrischer Bau = Dipol.
Für die Molekülgeometrie zählst du alle Elektronenpaare am Zentralatom: Ein Elektronenpaar = nebeneinander. Zwei Paare = linear (180°) oder gewinkelt (105°) mit freiem Paar. Drei Paare = planar (120°) oder pyramidal (107°) mit freiem Paar.
Vier bindende Elektronenpaare ergeben immer eine tetraedrische Form (109,5°). Freie Elektronenpaare brauchen mehr Platz als bindende und "drücken" die anderen nach unten.
📐 Geometrie-Regel: Freies Elektronenpaar > Mehrfachbindung > Einfachbindung beim Raumbedarf!
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
8
Smart Tools NEU
Verwandle diesen Lernzettel in: ✓ 50+ Übungsfragen ✓ Interaktive Karteikarten ✓ Komplette Probeklausur ✓ Aufsatzgliederungen
Entdecke die Unterschiede zwischen Reinstoffen und Stoffgemischen in dieser Übersicht. Die Tabelle behandelt homogene und heterogene Gemische mit Beispielen wie Meerwasser, Zucker und Müsli. Ideal für das Verständnis der Klassifikation von Materie.
Entdecken Sie die wesentlichen Eigenschaften von Metallen, einschließlich Wärmeleitfähigkeit, elektrische Leitfähigkeit, Verformbarkeit und metallischem Glanz. Diese Zusammenfassung erklärt das Elektronengasmodell und die metallischen Bindungen, die für das Verhalten von Metallen verantwortlich sind. Ideal für Studierende der Chemie und Materialwissenschaften.
Entdecken Sie die Zusammensetzung der Luft, einschließlich der Siedetemperaturen von Stickstoff, Sauerstoff und Argon. Erfahren Sie, wie man den Sauerstoff- und Kohlenstoffdioxidgehalt mit einfachen Nachweisverfahren wie der Glimmspanprobe und der Kalkwasserprobe bestimmt. Ideal für Chemie-Studierende und Prüfungsrelevante Inhalte.
Entdecken Sie die grundlegenden Eigenschaften von Stoffen, einschließlich der Aggregatzustände, pH-Wert, Löslichkeit und chemischen Reaktionen. Diese Zusammenfassung bietet einen klaren Überblick über die atomare Struktur, die Unterschiede zwischen Säuren und Basen sowie wichtige chemische Berechnungen. Ideal für Schüler, die sich auf Prüfungen vorbereiten oder ihr Wissen über Chemie vertiefen möchten.
Erfahren Sie alles über den sicheren Umgang mit dem Bunsenbrenner, die wichtigsten Laborgeräte und die Fachraumordnung in der Chemie. Diese Zusammenfassung behandelt auch die Aggregatzustände und das Teilchenmodell, um ein umfassendes Verständnis der chemischen Grundlagen zu fördern.
Dieser Lernzettel behandelt die Konzepte endothermer und exothermer Reaktionen, einschließlich der Bedeutung von Aktivierungsenergie und der physikalischen Eigenschaften der Reaktionspartner. Erfahren Sie, wie chemische Reaktionen Energie abgeben oder aufnehmen und welche Rolle Aggregatzustände dabei spielen.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer