Die Chemie mag erst mal kompliziert wirken, aber sie folgt... Mehr anzeigen
Melde dich an, um den Inhalt zu sehenKostenlos!
Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Knowunity KI
Fächer
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Alle Themen anzeigen
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Alle Themen anzeigen
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Alle Themen anzeigen
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Alle Themen anzeigen
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Alle Themen anzeigen
989
•
Aktualisiert May 11, 2026
•
Finja
@finja_cqqf
Die Chemie mag erst mal kompliziert wirken, aber sie folgt... Mehr anzeigen








Alles um dich herum besteht aus Stoffen - entweder als Gemische oder Reinstoffe (die wiederum aus Verbindungen oder Elementen bestehen). Das Wichtigste dabei: Jede Stoffportion hat eine bestimmte Masse und ein bestimmtes Volumen.
Bei chemischen Bindungen wollen alle Atome dasselbe erreichen - die Edelgaskonfiguration. Bei der Ionenbindung geben Metalle Elektronen an Nichtmetalle ab, wodurch sich Kationen und Anionen bilden, die sich durch elektrostatische Kräfte anziehen. Das Ergebnis ist ein Ionengitter mit hohen Schmelztemperaturen.
Die Atombindung funktioniert anders: Hier teilen sich Nichtmetalle Elektronenpaare und bilden Moleküle. Mit Lewis-Formeln und dem Elektronenpaarabstoßungs-Modell kannst du die Struktur vorhersagen. Bei Metallbindungen bewegen sich die Valenzelektronen frei als "Elektronengas" zwischen den Atomrümpfen.
Merktipp: Die Elektronegativitätsdifferenz (ΔEN) entscheidet über den Bindungstyp: <0,4 = unpolar, 0,4-1,7 = polar, >1,7 = ionisch.

Atome bestehen aus einem Kern mit Protonen und Neutronen, umgeben von Elektronenschalen. Die K-Schale fasst maximal 2 Elektronen, jede weitere Schale maximal 8. Die Valenzelektronen in der äußersten Schale bestimmen das chemische Verhalten.
Isotope haben gleiche Protonenzahl, aber unterschiedliche Neutronenzahl. Die Gruppennummer im Periodensystem zeigt die Anzahl der Valenzelektronen, die Periodenzahl die Schalenanzahl. Beim Energiestufenmodell benötigst du Ionisierungsenergie, um Elektronen zu entfernen - je näher am Kern, desto mehr Energie.
Ionen sind geladene Teilchen: Metalle bilden positive Kationen, Nichtmetalle negative Anionen. Salze haben deshalb typische Eigenschaften: kristalline Struktur, hohe Schmelztemperaturen, Härte und Sprödigkeit. Sie leiten nur gelöst oder geschmolzen Strom, weil dann die Ionen beweglich sind.
Praxistipp: Die Elektrolyse ist die Umkehrung der Salzbildung - durch elektrische Spannung wandern Kationen zur Kathode und Anionen zur Anode.

Moleküle entstehen, wenn sich mindestens zwei Atome durch Elektronenpaarbindungen verbinden - so erreichen auch Nichtmetalle die Edelgaskonfiguration. Die Van-der-Waals-Kräfte zwischen Molekülen bestimmen viele Eigenschaften.
Die Dipol-Dipol-Wechselwirkungen wirken zwischen polaren Molekülen mit getrennten Ladungsschwerpunkten. Ion-Dipol-Wechselwirkungen erklären, warum sich Salze in Wasser lösen. Wasserstoffbrücken sind eine Sonderform - sie entstehen zwischen H und F, O oder N.
Das Struktur-Eigenschafts-Konzept ist der Schlüssel: Art, Anordnung und Wechselwirkungen bestimmen alle Eigenschaften. Beim Schmelzen und Sieden müssen diese Anziehungskräfte überwunden werden. Für die Löslichkeit gilt: Gleiches löst sich in Gleichem - polare Stoffe in polaren Lösungsmitteln, unpolare in unpolaren.
Eselsbrücke: Ion-Ion-Wechselwirkungen sind mit über 200 kJ/mol am stärksten - deshalb haben Salze so hohe Schmelzpunkte!

Diese Nachweisreaktionen brauchst du garantiert in Klausuren! Für Wasser nimmst du wasserfreies Kupfersulfat - wird es blau, ist Wasser da. Der Sauerstoff-Nachweis funktioniert mit der Glimmspanprobe: Ein glimmender Holzspan flammt in Sauerstoff auf.
Wasserstoff erkennst du an der Knallgasprobe - reiner Wasserstoff brennt ruhig ab, mit Luftbeimischung gibt's ein pfeifendes Geräusch oder sogar einen Knall. Kohlenstoffdioxid weist du mit Kalkwasser nach: Es entsteht ein weißer Niederschlag aus Calciumcarbonat.
Alkalimetalle zeigen charakteristische Flammenfärbungen - jedes Element hat seine typische Farbe. Die Halogenid-Ionen (Cl⁻, Br⁻, I⁻) erkennst du mit Silbernitratlösung: Chlorid gibt einen weißen, Bromid einen blassgelben und Iodid einen gelblichen Niederschlag.
Klausurtipp: Lerne die Reaktionsgleichungen auswendig - besonders die für CO₂-Nachweis und Halogenid-Nachweise kommen oft dran!
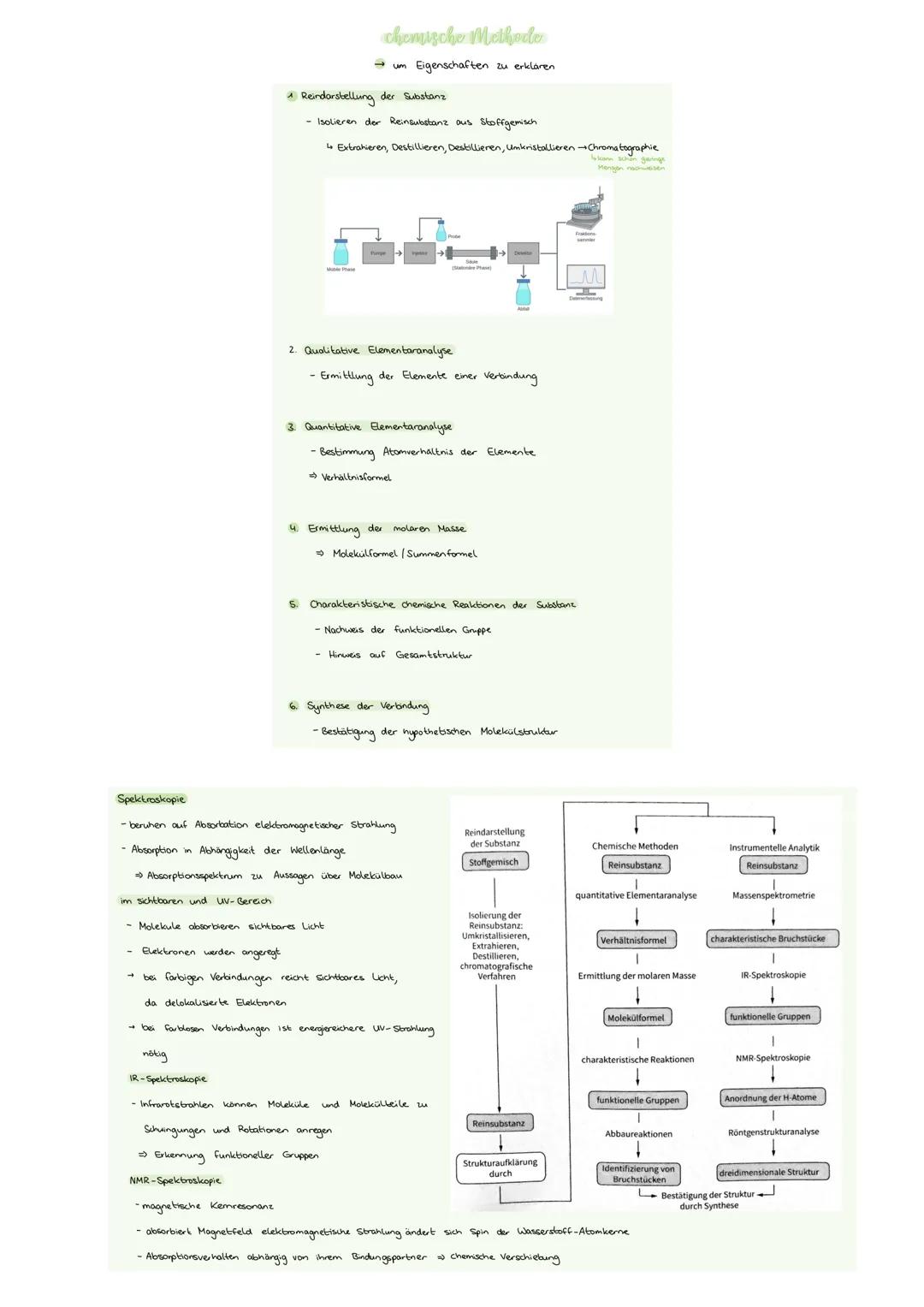
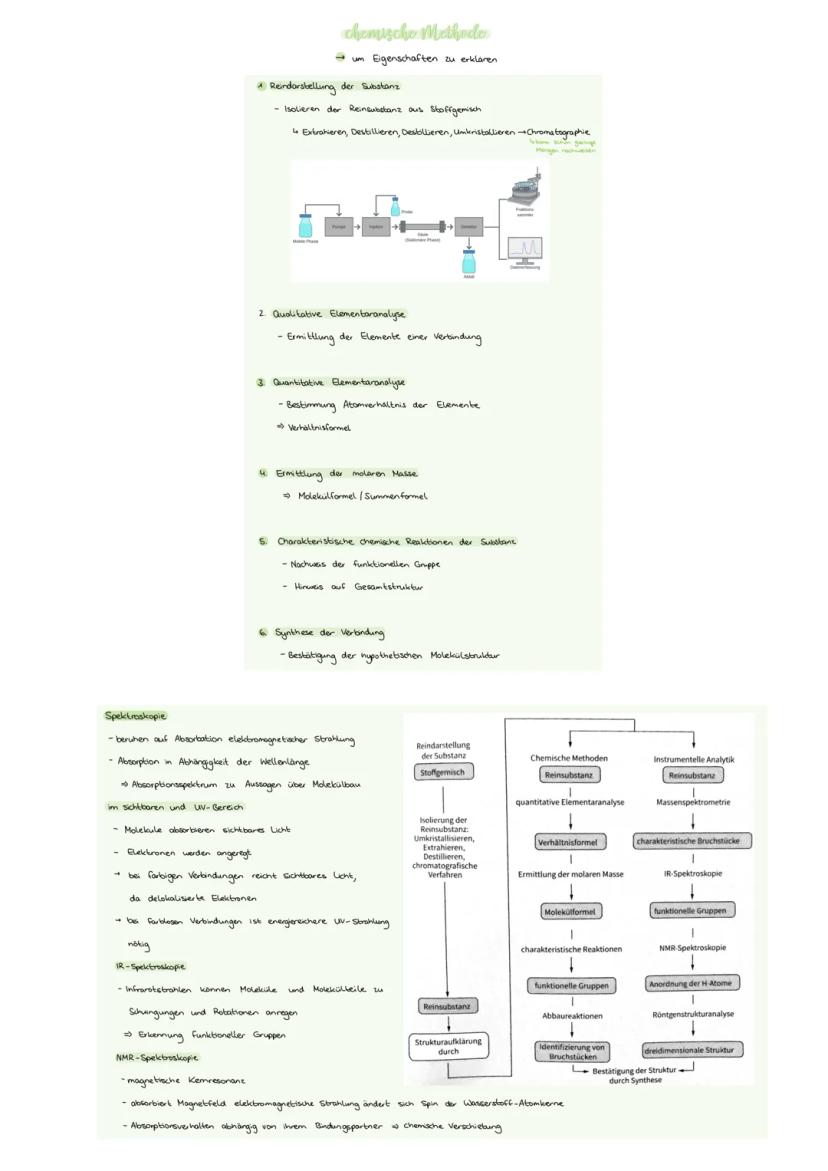
Die Strukturaufklärung folgt einem klaren System: Erst die Reindarstellung durch Extrahieren, Destillieren oder Chromatographie. Dann die qualitative Elementaranalyse (welche Elemente?) und die quantitative Analyse (in welchem Verhältnis?).
Aus der molaren Masse kriegst du die Molekülformel, charakteristische Reaktionen zeigen funktionelle Gruppen. Die Synthese bestätigt schließlich deine Struktur-Hypothese. Spektroskopie macht vieles einfacher: UV/Vis-Spektren zeigen delokalisierte Elektronen, IR-Spektroskopie erkennt funktionelle Gruppen durch Molekülschwingungen.
Die NMR-Spektroskopie nutzt magnetische Kernresonanz - Wasserstoff-Atomkerne absorbieren je nach Bindungspartner unterschiedlich (chemische Verschiebung). Moderne Methoden wie Massenspektrometrie und Röntgenstrukturanalyse geben zusätzliche Informationen über Bruchstücke und dreidimensionale Struktur.
Zukunftswissen: Die instrumentelle Analytik wird immer wichtiger - sie ist schneller und präziser als klassische chemische Methoden.

Stöchiometrisches Rechnen ist dein Werkzeug für Mengenberechnungen. Die Avogadro-Konstante (6·10²³ mol⁻¹) verbindet die Teilchenanzahl mit der Stoffmenge. Die molare Masse M sagt dir, wie schwer ein Mol eines Stoffes ist.
Bei Gasreaktionen ist das molare Volumen entscheidend: Bei Standardbedingungen (25°C, 1000 hPa) nimmt ein Mol Gas 24 L ein. Gasförmige Stoffe reagieren in ganzzahligen Volumenverhältnissen - das macht Berechnungen einfacher.
Die wichtigsten Formeln: Dichte ρ = m/V, und die drei Grundgleichungen je nach Aggregatzustand. Für Feststoffe: n = m/M, für Lösungen: n = c·V, für Gase: n = V/Vm. Diese Formeln sind deine Basis für alle Berechnungen in der Chemie.
Rechentrick: Merke dir die Standardbedingungen und dass 0°C = 273 K ist - das brauchst du ständig!

Die Chemie wirkt komplex, folgt aber eigentlich nur fünf Basiskonzepten, die alles strukturieren. Das Stoff-Teilchen-Konzept erklärt, wie aus Atomen durch verschiedene Bindungsarten größere Verbände entstehen - vom Schalenmodell bis zu Orbitalmodellen.
Das Struktur-Eigenschafts-Konzept zeigt den Zusammenhang zwischen Aufbau und Eigenschaften. Warum ist Diamant hart, Graphit weich? Alles hängt von der Anordnung der Kohlenstoffatome ab! Verschiedene Modifikationen desselben Elements haben völlig unterschiedliche Eigenschaften.
Diese Konzepte helfen dir, die "oft unüberschaubar erscheinende Vielfalt" der Chemie zu verstehen. Sie ermöglichen es, chemische Sachverhalte aus spezifischen Perspektiven zu betrachten und Zusammenhänge zu erkennen. Mit ihnen wird Chemie vom Auswendiglernen zum logischen Verstehen.
Lernstrategie: Nutze die Basiskonzepte als "roten Faden" - jedes neue Thema lässt sich einem oder mehreren Konzepten zuordnen.

Das Donator-Akzeptor-Konzept erklärt viele Reaktionen durch Teilchenaustausch: Elektronenübertragung bei Redoxreaktionen und Protonenübertragung bei Säure-Base-Reaktionen. Wer gibt ab (Donator), wer nimmt auf (Akzeptor)?
Das Energie-Konzept zeigt: Alle chemischen Reaktionen sind mit Energieumsatz verbunden. Exotherme Reaktionen geben Energie ab, endotherme nehmen sie auf. Die Aktivierungsenergie bestimmt, ob eine Reaktion spontan abläuft - Katalysatoren können sie senken.
Das Gleichgewichts- und Kinetik-Konzept erklärt, warum Reaktionen oft unvollständig ablaufen und unterschiedlich schnell sind. Das chemische Gleichgewicht zwischen NO₂ (braun) und N₂O₄ (farblos) zeigt schön, wie Temperatur das Gleichgewicht verschiebt. Temperatur, Konzentration und Katalysatoren beeinflussen die Reaktionsgeschwindigkeit.
Verstehenshilfe: Die Energiediagramme sind dein visueller Schlüssel - sie zeigen auf einen Blick, ob eine Reaktion exotherm oder endotherm ist und wie hoch die Aktivierungsbarriere liegt.
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Finja
@finja_cqqf
Die Chemie mag erst mal kompliziert wirken, aber sie folgt eigentlich fünf grundlegenden Konzepten, die dir helfen, alles zu verstehen. Von der Struktur der Atome bis hin zu chemischen Reaktionen - mit diesen Grundlagen checkst du jedes chemische Phänomen.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Alles um dich herum besteht aus Stoffen - entweder als Gemische oder Reinstoffe (die wiederum aus Verbindungen oder Elementen bestehen). Das Wichtigste dabei: Jede Stoffportion hat eine bestimmte Masse und ein bestimmtes Volumen.
Bei chemischen Bindungen wollen alle Atome dasselbe erreichen - die Edelgaskonfiguration. Bei der Ionenbindung geben Metalle Elektronen an Nichtmetalle ab, wodurch sich Kationen und Anionen bilden, die sich durch elektrostatische Kräfte anziehen. Das Ergebnis ist ein Ionengitter mit hohen Schmelztemperaturen.
Die Atombindung funktioniert anders: Hier teilen sich Nichtmetalle Elektronenpaare und bilden Moleküle. Mit Lewis-Formeln und dem Elektronenpaarabstoßungs-Modell kannst du die Struktur vorhersagen. Bei Metallbindungen bewegen sich die Valenzelektronen frei als "Elektronengas" zwischen den Atomrümpfen.
Merktipp: Die Elektronegativitätsdifferenz (ΔEN) entscheidet über den Bindungstyp: <0,4 = unpolar, 0,4-1,7 = polar, >1,7 = ionisch.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Atome bestehen aus einem Kern mit Protonen und Neutronen, umgeben von Elektronenschalen. Die K-Schale fasst maximal 2 Elektronen, jede weitere Schale maximal 8. Die Valenzelektronen in der äußersten Schale bestimmen das chemische Verhalten.
Isotope haben gleiche Protonenzahl, aber unterschiedliche Neutronenzahl. Die Gruppennummer im Periodensystem zeigt die Anzahl der Valenzelektronen, die Periodenzahl die Schalenanzahl. Beim Energiestufenmodell benötigst du Ionisierungsenergie, um Elektronen zu entfernen - je näher am Kern, desto mehr Energie.
Ionen sind geladene Teilchen: Metalle bilden positive Kationen, Nichtmetalle negative Anionen. Salze haben deshalb typische Eigenschaften: kristalline Struktur, hohe Schmelztemperaturen, Härte und Sprödigkeit. Sie leiten nur gelöst oder geschmolzen Strom, weil dann die Ionen beweglich sind.
Praxistipp: Die Elektrolyse ist die Umkehrung der Salzbildung - durch elektrische Spannung wandern Kationen zur Kathode und Anionen zur Anode.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Moleküle entstehen, wenn sich mindestens zwei Atome durch Elektronenpaarbindungen verbinden - so erreichen auch Nichtmetalle die Edelgaskonfiguration. Die Van-der-Waals-Kräfte zwischen Molekülen bestimmen viele Eigenschaften.
Die Dipol-Dipol-Wechselwirkungen wirken zwischen polaren Molekülen mit getrennten Ladungsschwerpunkten. Ion-Dipol-Wechselwirkungen erklären, warum sich Salze in Wasser lösen. Wasserstoffbrücken sind eine Sonderform - sie entstehen zwischen H und F, O oder N.
Das Struktur-Eigenschafts-Konzept ist der Schlüssel: Art, Anordnung und Wechselwirkungen bestimmen alle Eigenschaften. Beim Schmelzen und Sieden müssen diese Anziehungskräfte überwunden werden. Für die Löslichkeit gilt: Gleiches löst sich in Gleichem - polare Stoffe in polaren Lösungsmitteln, unpolare in unpolaren.
Eselsbrücke: Ion-Ion-Wechselwirkungen sind mit über 200 kJ/mol am stärksten - deshalb haben Salze so hohe Schmelzpunkte!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Diese Nachweisreaktionen brauchst du garantiert in Klausuren! Für Wasser nimmst du wasserfreies Kupfersulfat - wird es blau, ist Wasser da. Der Sauerstoff-Nachweis funktioniert mit der Glimmspanprobe: Ein glimmender Holzspan flammt in Sauerstoff auf.
Wasserstoff erkennst du an der Knallgasprobe - reiner Wasserstoff brennt ruhig ab, mit Luftbeimischung gibt's ein pfeifendes Geräusch oder sogar einen Knall. Kohlenstoffdioxid weist du mit Kalkwasser nach: Es entsteht ein weißer Niederschlag aus Calciumcarbonat.
Alkalimetalle zeigen charakteristische Flammenfärbungen - jedes Element hat seine typische Farbe. Die Halogenid-Ionen (Cl⁻, Br⁻, I⁻) erkennst du mit Silbernitratlösung: Chlorid gibt einen weißen, Bromid einen blassgelben und Iodid einen gelblichen Niederschlag.
Klausurtipp: Lerne die Reaktionsgleichungen auswendig - besonders die für CO₂-Nachweis und Halogenid-Nachweise kommen oft dran!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Strukturaufklärung folgt einem klaren System: Erst die Reindarstellung durch Extrahieren, Destillieren oder Chromatographie. Dann die qualitative Elementaranalyse (welche Elemente?) und die quantitative Analyse (in welchem Verhältnis?).
Aus der molaren Masse kriegst du die Molekülformel, charakteristische Reaktionen zeigen funktionelle Gruppen. Die Synthese bestätigt schließlich deine Struktur-Hypothese. Spektroskopie macht vieles einfacher: UV/Vis-Spektren zeigen delokalisierte Elektronen, IR-Spektroskopie erkennt funktionelle Gruppen durch Molekülschwingungen.
Die NMR-Spektroskopie nutzt magnetische Kernresonanz - Wasserstoff-Atomkerne absorbieren je nach Bindungspartner unterschiedlich (chemische Verschiebung). Moderne Methoden wie Massenspektrometrie und Röntgenstrukturanalyse geben zusätzliche Informationen über Bruchstücke und dreidimensionale Struktur.
Zukunftswissen: Die instrumentelle Analytik wird immer wichtiger - sie ist schneller und präziser als klassische chemische Methoden.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Stöchiometrisches Rechnen ist dein Werkzeug für Mengenberechnungen. Die Avogadro-Konstante (6·10²³ mol⁻¹) verbindet die Teilchenanzahl mit der Stoffmenge. Die molare Masse M sagt dir, wie schwer ein Mol eines Stoffes ist.
Bei Gasreaktionen ist das molare Volumen entscheidend: Bei Standardbedingungen (25°C, 1000 hPa) nimmt ein Mol Gas 24 L ein. Gasförmige Stoffe reagieren in ganzzahligen Volumenverhältnissen - das macht Berechnungen einfacher.
Die wichtigsten Formeln: Dichte ρ = m/V, und die drei Grundgleichungen je nach Aggregatzustand. Für Feststoffe: n = m/M, für Lösungen: n = c·V, für Gase: n = V/Vm. Diese Formeln sind deine Basis für alle Berechnungen in der Chemie.
Rechentrick: Merke dir die Standardbedingungen und dass 0°C = 273 K ist - das brauchst du ständig!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Chemie wirkt komplex, folgt aber eigentlich nur fünf Basiskonzepten, die alles strukturieren. Das Stoff-Teilchen-Konzept erklärt, wie aus Atomen durch verschiedene Bindungsarten größere Verbände entstehen - vom Schalenmodell bis zu Orbitalmodellen.
Das Struktur-Eigenschafts-Konzept zeigt den Zusammenhang zwischen Aufbau und Eigenschaften. Warum ist Diamant hart, Graphit weich? Alles hängt von der Anordnung der Kohlenstoffatome ab! Verschiedene Modifikationen desselben Elements haben völlig unterschiedliche Eigenschaften.
Diese Konzepte helfen dir, die "oft unüberschaubar erscheinende Vielfalt" der Chemie zu verstehen. Sie ermöglichen es, chemische Sachverhalte aus spezifischen Perspektiven zu betrachten und Zusammenhänge zu erkennen. Mit ihnen wird Chemie vom Auswendiglernen zum logischen Verstehen.
Lernstrategie: Nutze die Basiskonzepte als "roten Faden" - jedes neue Thema lässt sich einem oder mehreren Konzepten zuordnen.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Das Donator-Akzeptor-Konzept erklärt viele Reaktionen durch Teilchenaustausch: Elektronenübertragung bei Redoxreaktionen und Protonenübertragung bei Säure-Base-Reaktionen. Wer gibt ab (Donator), wer nimmt auf (Akzeptor)?
Das Energie-Konzept zeigt: Alle chemischen Reaktionen sind mit Energieumsatz verbunden. Exotherme Reaktionen geben Energie ab, endotherme nehmen sie auf. Die Aktivierungsenergie bestimmt, ob eine Reaktion spontan abläuft - Katalysatoren können sie senken.
Das Gleichgewichts- und Kinetik-Konzept erklärt, warum Reaktionen oft unvollständig ablaufen und unterschiedlich schnell sind. Das chemische Gleichgewicht zwischen NO₂ (braun) und N₂O₄ (farblos) zeigt schön, wie Temperatur das Gleichgewicht verschiebt. Temperatur, Konzentration und Katalysatoren beeinflussen die Reaktionsgeschwindigkeit.
Verstehenshilfe: Die Energiediagramme sind dein visueller Schlüssel - sie zeigen auf einen Blick, ob eine Reaktion exotherm oder endotherm ist und wie hoch die Aktivierungsbarriere liegt.
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
22
Smart Tools NEU
Verwandle diesen Lernzettel in: ✓ 50+ Übungsfragen ✓ Interaktive Karteikarten ✓ Komplette Probeklausur ✓ Aufsatzgliederungen
Entdecken Sie die Grundlagen des Orbitalmodells und der Hybridisierung. Diese Zusammenfassung behandelt die Besetzung von Elektronen in Orbitalen, die verschiedenen Orbitaltypen (s, p, d, f) und die Regeln für die Elektronenkonfiguration. Zudem wird erklärt, wie Hybridisierung die chemischen Bindungsverhältnisse in Molekülen wie Propen beeinflusst. Ideal für Studierende der Chemie, die ein tieferes Verständnis für chemische Bindungen und Orbitaltheorie entwickeln möchten.
Entdecken Sie die wichtigsten Merkregeln zur Erstellung von Lewis-Formeln. Dieser Leitfaden behandelt die Zählung von Valenzelektronen, die Anwendung der Oktettregel und die symmetrische Anordnung von Atomen. Ideal für Chemie-Studierende, die ein besseres Verständnis für Molekülstrukturen entwickeln möchten. Typ: Zusammenfassung.
Entdecken Sie die verschiedenen Derivate des Benzols, einschließlich Phenol, Anilin und Toluol. Erfahren Sie mehr über ihre chemischen Eigenschaften, Reaktionen und Anwendungen in der Industrie, wie z.B. in der Herstellung von Kunststoffen, Farben und Lebensmitteln. Diese Zusammenfassung bietet eine klare Übersicht über die Struktur und Verwendung von Benzolderivaten.
Entdecken Sie die Reaktionsmechanismen und Effekte von aromatischen Verbindungen wie Benzol, Phenol und Anilin. Diese Zusammenfassung behandelt den induktiven und mesomerischen Effekt sowie die elektrophile Substitution. Ideal für Chemie-Studierende, die ein vertieftes Verständnis der Aromaten und ihrer Reaktivität suchen.
Entdecken Sie die Grundlagen der Esterbildung, einschließlich der Kondensationsreaktion zwischen Carbonsäuren und Alkoholen. Diese Zusammenfassung behandelt den Mechanismus der Veresterung, die Benennung von Estern und bietet praktische Übungen zur Anwendung des Gelernten. Ideal für Studierende der organischen Chemie, die ihr Verständnis vertiefen möchten.
Entdecken Sie die Schlüsselkonzepte zu Dipolen, Wasserstoffbrücken und den Eigenschaften von Wasser. Diese Zusammenfassung behandelt die Elektronegativität, die Siedetemperatur, die Polarität von Molekülen und die Wechselwirkungen zwischen Dipolmolekülen und Salzen. Ideal für Studierende der Chemie, die ein tieferes Verständnis der molekularen Wechselwirkungen und der einzigartigen Eigenschaften von Wasser erlangen möchten.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer