Additionsreaktionen, elektrophile Substitution und Eliminierungsreaktionen sind die wichtigsten Reaktionstypen in... Mehr anzeigen
Grundlagen der Organischen Chemie: Wichtige Reaktionsmechanismen






Additionsreaktionen - Grundlagen
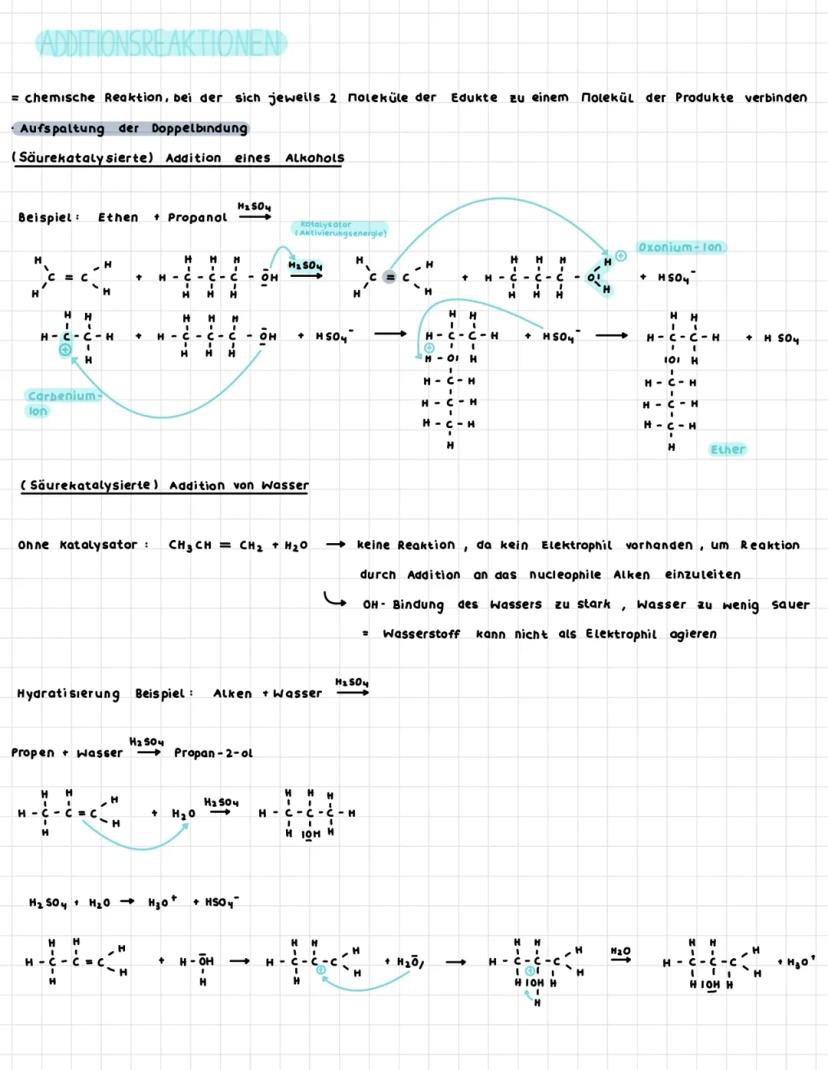
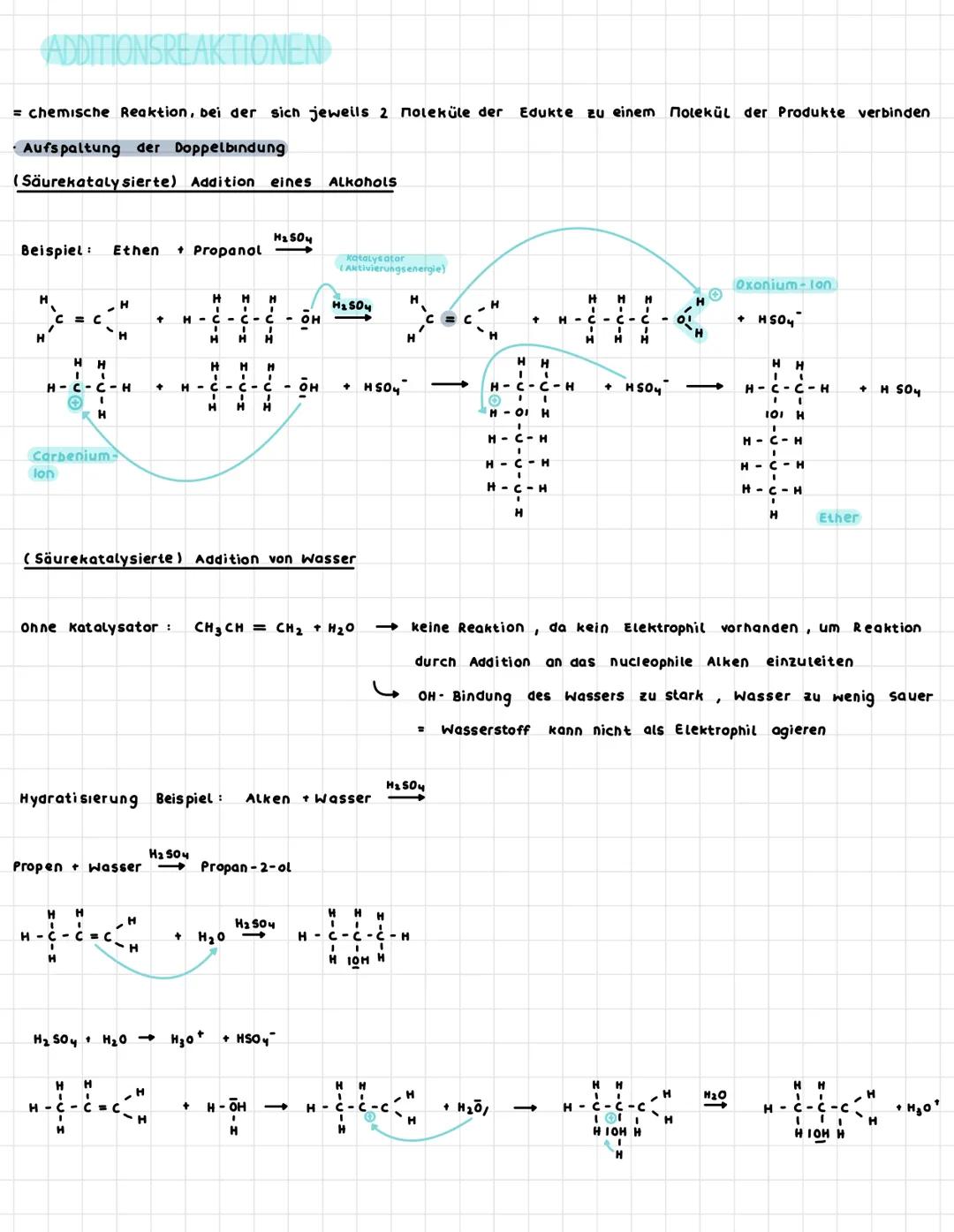
Additionsreaktionen sind super praktisch: Zwei Edukt-Moleküle verbinden sich zu einem einzigen Produkt-Molekül. Dabei wird die Doppelbindung aufgespalten - denk dir vor, wie ein Reißverschluss aufgeht.
Bei der säurekatalysierten Addition von Alkoholen oder Wasser brauchst du immer H₂SO₄ als Katalysator. Ohne Katalysator passiert nämlich nichts, weil Wasser zu wenig sauer ist und kein Elektrophil vorhanden ist.
Der Mechanismus läuft in zwei Schritten ab: Erst greift das Proton (H⁺) die Doppelbindung an und es entsteht ein positiv geladenes Carbenium-Ion. Dann greift das Nucleophil (wie OH⁻) das Carbenium-Ion an und das finale Produkt entsteht.
💡 Merktipp: Bei der Hydratisierung von Propen entsteht Propan-2-ol, nicht Propan-1-ol - das zeigt dir schon, dass die Addition nicht zufällig abläuft!
Elektrophile Addition mit Halogenen
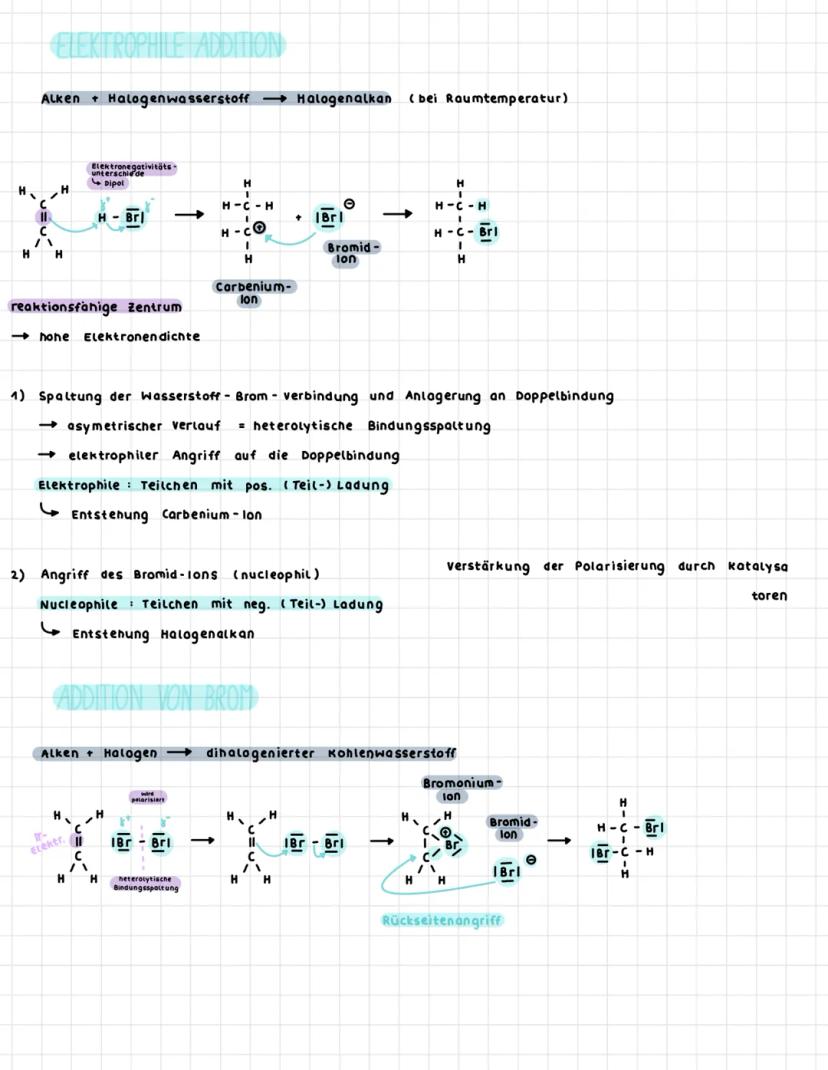
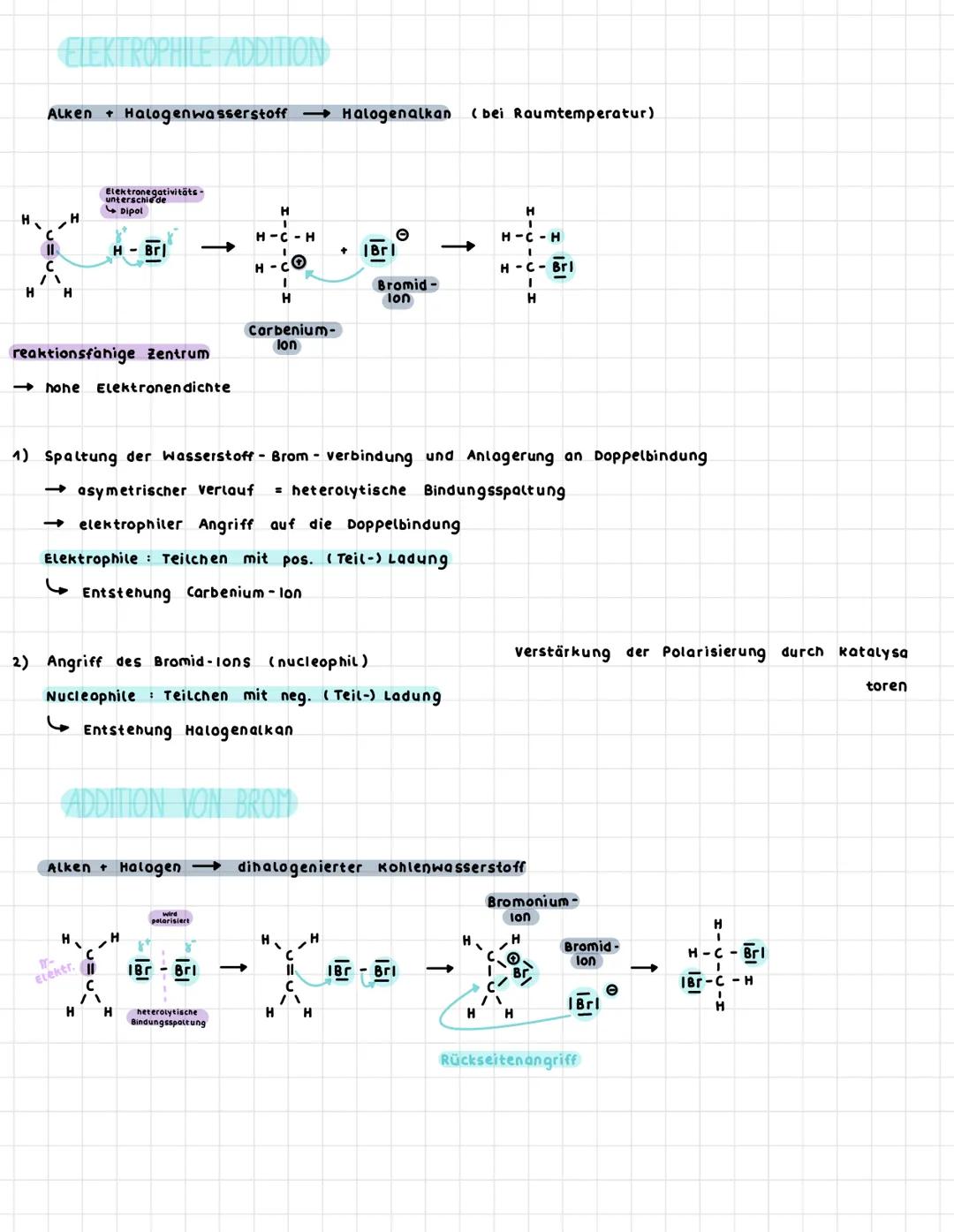
Die elektrophile Addition funktioniert durch Elektronegativitätsunterschiede - HBr ist polar und das macht die Reaktion erst möglich. Das elektronegative Brom zieht die Elektronen zu sich, wodurch Wasserstoff positiv wird.
Der Reaktionsmechanismus hat zwei klare Schritte: Zuerst erfolgt die heterolytische Bindungsspaltung von HBr, dann greift H⁺ elektrophil die elektronenreiche Doppelbindung an. Dadurch entsteht ein Carbenium-Ion.
Im zweiten Schritt greift das Bromid-Ion (nucleophil) das positiv geladene Carbenium-Ion an. So entsteht das finale Halogenalkan - bei Ethen und HBr wird daraus Ethan-1-brom.
Bei der Addition von Brom (Br₂) entsteht zuerst ein Bromonium-Ion durch Rückseitenangriff. Das ist stabiler als ein normales Carbenium-Ion und erklärt, warum diese Reaktion so glatt läuft.
💡 Praxistipp: Elektrophile haben positive Ladungen und lieben elektronenreiche Bereiche - wie die Doppelbindung in Alkenen!
Elektrophile Substitution am Benzolring
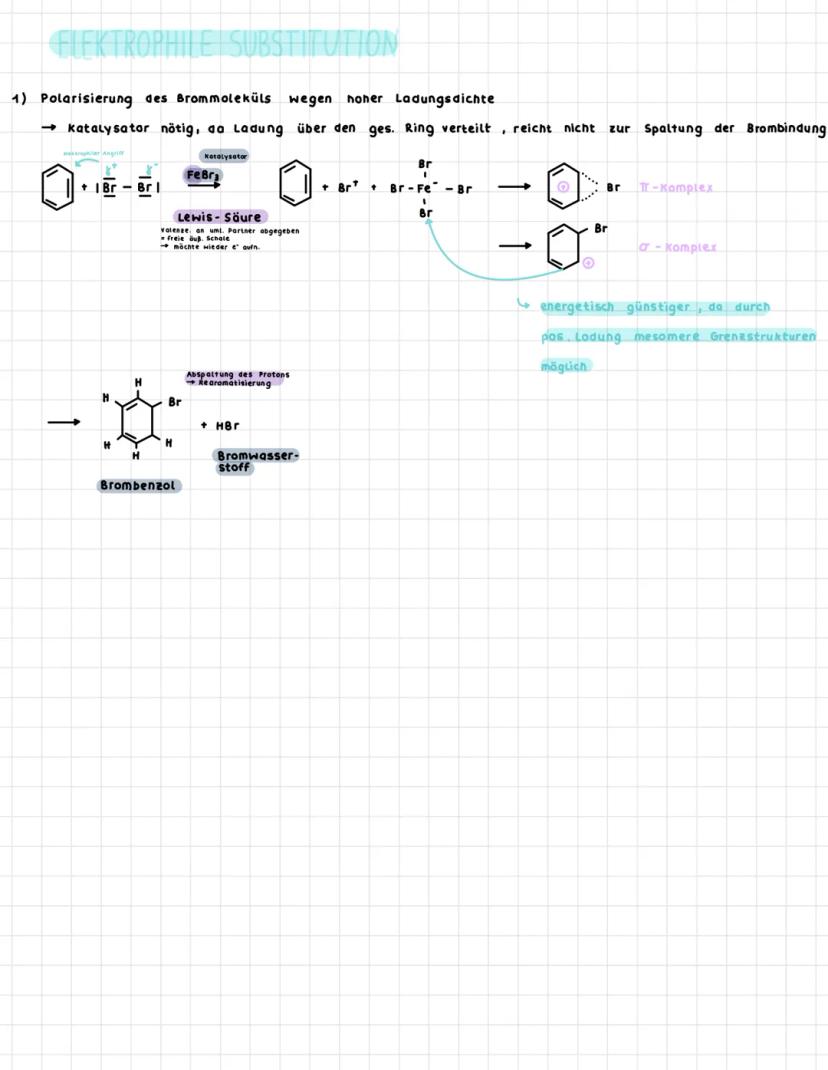
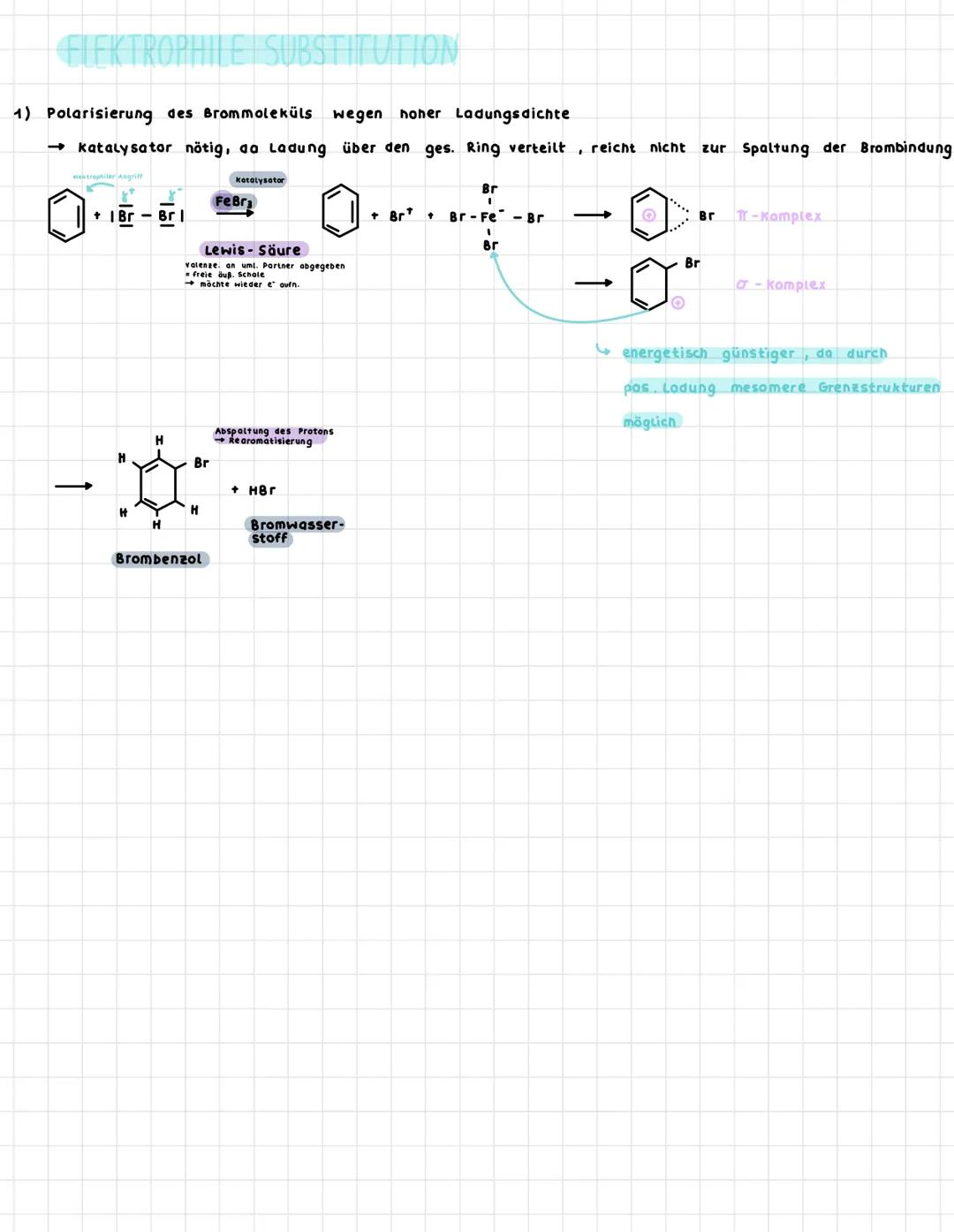
Elektrophile Substitution am Benzol braucht einen Katalysator wie FeBr₃, weil der Benzolring zu stabil ist. Die Ladungsdichte ist über den ganzen Ring verteilt - das reicht nicht zur Spaltung der Br-Br-Bindung.
Der Katalysator FeBr₃ ist eine Lewis-Säure mit freier äußerer Schale, die Elektronen aufnehmen möchte. Er polarisiert Br₂ zu Br⁺ und [FeBr₄]⁻, wodurch ein starkes Elektrophil entsteht.
Die Reaktion läuft über zwei Zwischenstuffe: Zuerst bildet sich der π-Komplex (schwache Wechselwirkung), dann der σ-Komplex (echte Bindung). Der σ-Komplex ist energetisch günstiger, weil mesomere Grenzstrukturen die positive Ladung stabilisieren.
Am Ende wird ein Proton abgespalten und die Aromatizität des Rings wiederhergestellt - das ist energetisch sehr günstig. Als Nebenprodukt entsteht Bromwasserstoff (HBr).
💡 Wichtig: Die Rearomatisierung ist der Grund, warum Substitution statt Addition stattfindet - der aromatische Ring ist einfach zu stabil!

Regioselektivität und Markownikow-Regel
Regioselektivität bedeutet, dass die Reaktion bevorzugt an einer bestimmten Stelle abläuft. Bei Alkenen kann das Elektrophil an zwei verschiedene Kohlenstoffatome addieren - aber eines ist deutlich bevorzugt.
Das Hauptprodukt entsteht immer über das stabilste Carbokation: tertiär > sekundär > primär. Ein tertiäres Carbokation bildet sich schneller und ist stabiler als ein sekundäres, weil mehr Alkylgruppen die positive Ladung stabilisieren.
Die Markownikow-Regel sagt dir genau vorher, welches Produkt entsteht: Das Elektrophil (meist H⁺) addiert an das Kohlenstoffatom mit den meisten Wasserstoffatomen. Dadurch bildet sich automatisch das stabilste Carbokation.
Je größer der Stabilitätsunterschied zwischen möglichen Carbokationen, desto regioselektiver ist die Reaktion. Tertiär vs. primär ist hochgradig regioselektiv, während sekundär vs. sekundär gar nicht regioselektiv ist.
💡 Eselsbrücke: "Der Reiche wird reicher" - das Kohlenstoffatom mit mehr H-Atomen bekommt noch ein H-Atom dazu!

Eliminierungsreaktionen im Überblick
Eliminierungsreaktionen sind das Gegenteil von Additionen - hier werden kleine Moleküle wie H₂O oder HBr abgespalten. Das ist super praktisch, um Alkene aus Alkoholen oder Halogenalkanen zu gewinnen.
Bei der Dehydratisierung von Alkanolen spaltest du Wasser ab. Tertiäre und sekundäre Alkohole reagieren leicht mit mittelstarken Säuren, primäre brauchen starke Säuren und hohe Temperaturen. Der Mechanismus läuft über Carbenium-Ionen - genau wie bei der Addition, nur rückwärts.
Die Dehydrohalogenierung verwendet starke Basen, um HX abzuspalten. Das funktioniert am besten bei tertiären Halogenalkanen und ist oft die bessere Alternative zur Dehydratisierung, weil weniger Nebenprodukte entstehen.
Dehydrierung von Alkanen braucht krasse Bedingungen: über 500°C ohne Luftzutritt. Mit Katalysatoren geht's schonender und du bekommst weniger Cracken .
💡 Reaktionsstrategie: Eliminierungen funktionieren am besten, je stabiler das entstehende Carbokation ist - genau wie bei Additionen!

Dehydrierung von Alkanen
Dehydrierung spaltet H₂ aus Alkanen ab und erzeugt dabei Alkene. Das ist industriell mega wichtig für die Herstellung von Ethen und Propen - den Grundbausteinen der Petrochemie.
Die krassen Reaktionsbedingungen (über 500°C unter Luftausschluss) führen leider auch zum Cracken - dabei brechen C-C-Bindungen und du bekommst ein Gemisch aus unterschiedlich langen Alkenen.
Katalysatoren sind hier deine Rettung: Sie ermöglichen Dehydrierung bei niedrigeren Temperaturen ohne C-C-Spaltung. Dadurch steigt die Ausbeute der gewünschten Alkene deutlich, auch wenn verschiedene Isomere in unterschiedlichen Anteilen entstehen.
In der Industrie läuft das über spezielle Metallkatalysatoren bei kontrollierten Bedingungen ab. So kannst du gezielt die Alkene herstellen, die du für weitere Synthesen brauchst.
💡 Industrietipp: Ohne Katalysatoren wäre die moderne Kunststoffproduktion unmöglich - Ethen und Propen sind die Basis für PE und PP!
Mesomerer und Induktiver Effekt
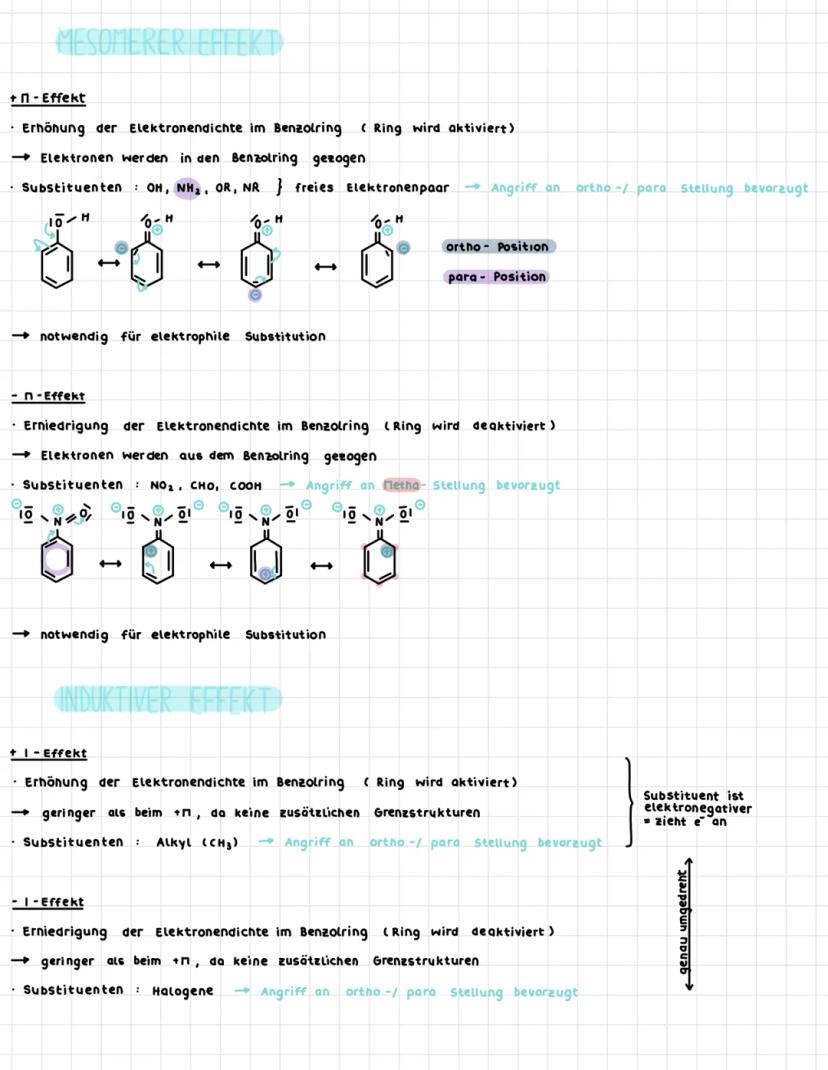
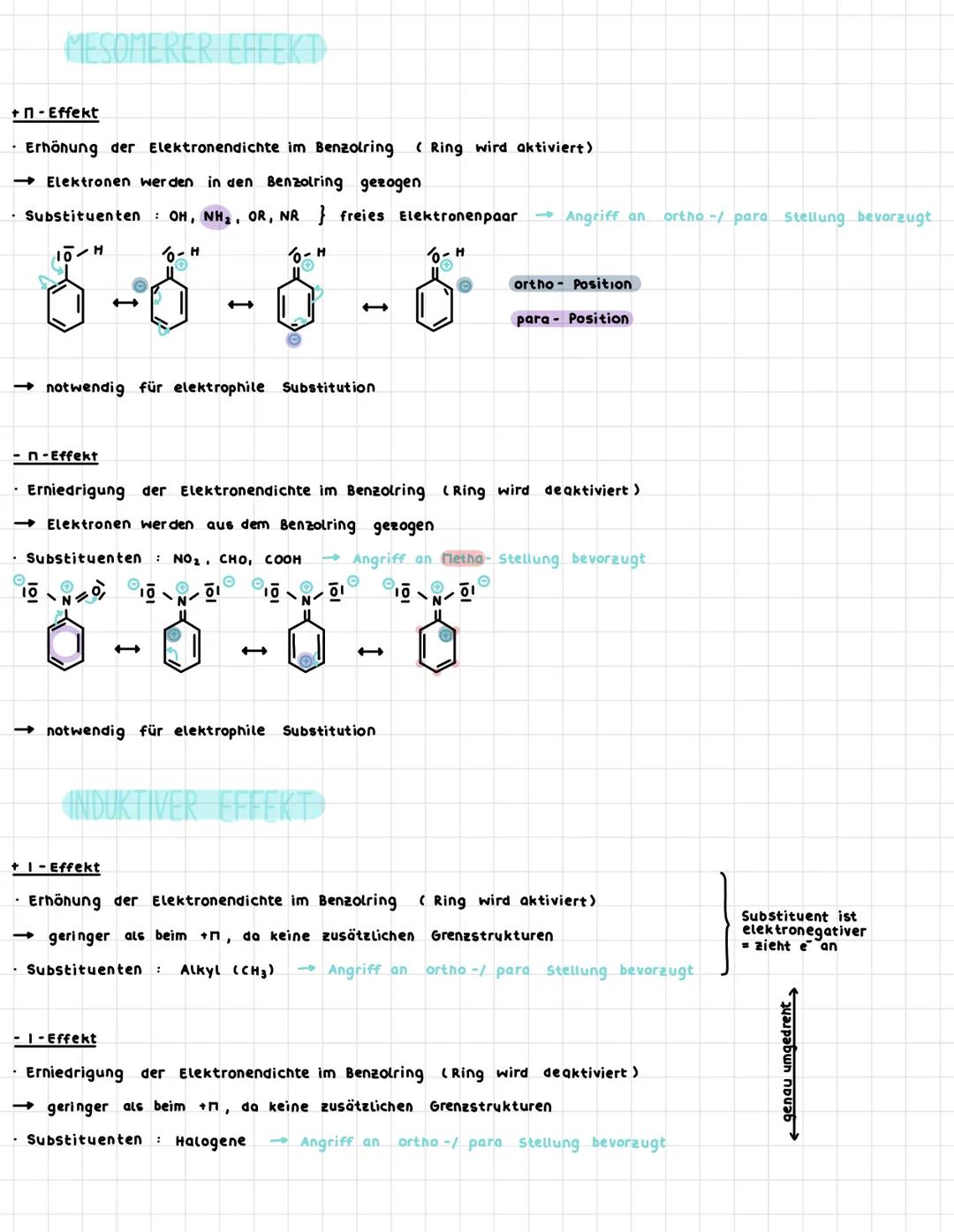
Mesomere Effekte entstehen durch freie Elektronenpaare oder π-Elektronen, die mit dem Benzolring wechselwirken. Der +π-Effekt erhöht die Elektronendichte im Ring und aktiviert ihn für elektrophile Substitution.
Substituenten wie OH, NH₂ oder OR haben freie Elektronenpaare, die in den Ring "geschoben" werden können. Dadurch wird besonders die ortho- und para-Position elektronenreich und für Elektrophile attraktiv.
Der -π-Effekt macht genau das Gegenteil: Substituenten wie NO₂, CHO oder COOH ziehen Elektronen aus dem Ring. Das deaktiviert ihn und macht die meta-Position am wenigsten ungünstig für Angriffe.
Induktive Effekte sind schwächer als mesomere, weil keine zusätzlichen Grenzstrukturen möglich sind. Alkylgruppen haben +I-Effekt (elektronenreich), Halogene haben -I-Effekt, dirigieren aber trotzdem nach ortho/para wegen ihrer freien Elektronenpaare.
💡 Faustregel: Mesomere Effekte schlagen induktive - deshalb dirigieren Halogene trotz -I-Effekt nach ortho/para!

Acidität von Phenol
Die Acidität von Phenol ist deutlich höher als die normaler Alkohole, weil das entstehende Phenolat-Ion mesomer stabilisiert wird. Die negative Ladung kann über den ganzen Benzolring delokalisiert werden.
Wenn Phenol ein Proton abgibt, entstehen mehrere mesomere Grenzstrukturen, die die negative Ladung auf verschiedene Positionen im Ring verteilen. Diese Delokalisierung macht das Phenolat-Ion viel stabiler als ein normales Alkoholat-Ion.
Deshalb reagiert Phenol schon mit schwachen Basen wie NaOH, während Alkohole starke Basen wie Natrium brauchen. Das ist ein wichtiger Unterschied in der Reaktivität zwischen aromatischen und aliphatischen Alkoholen.
💡 Chemie-Hack: Die Rotfärbung mit Eisen(III)-chlorid ist ein klassischer Phenol-Nachweis - nutze das im Labor!
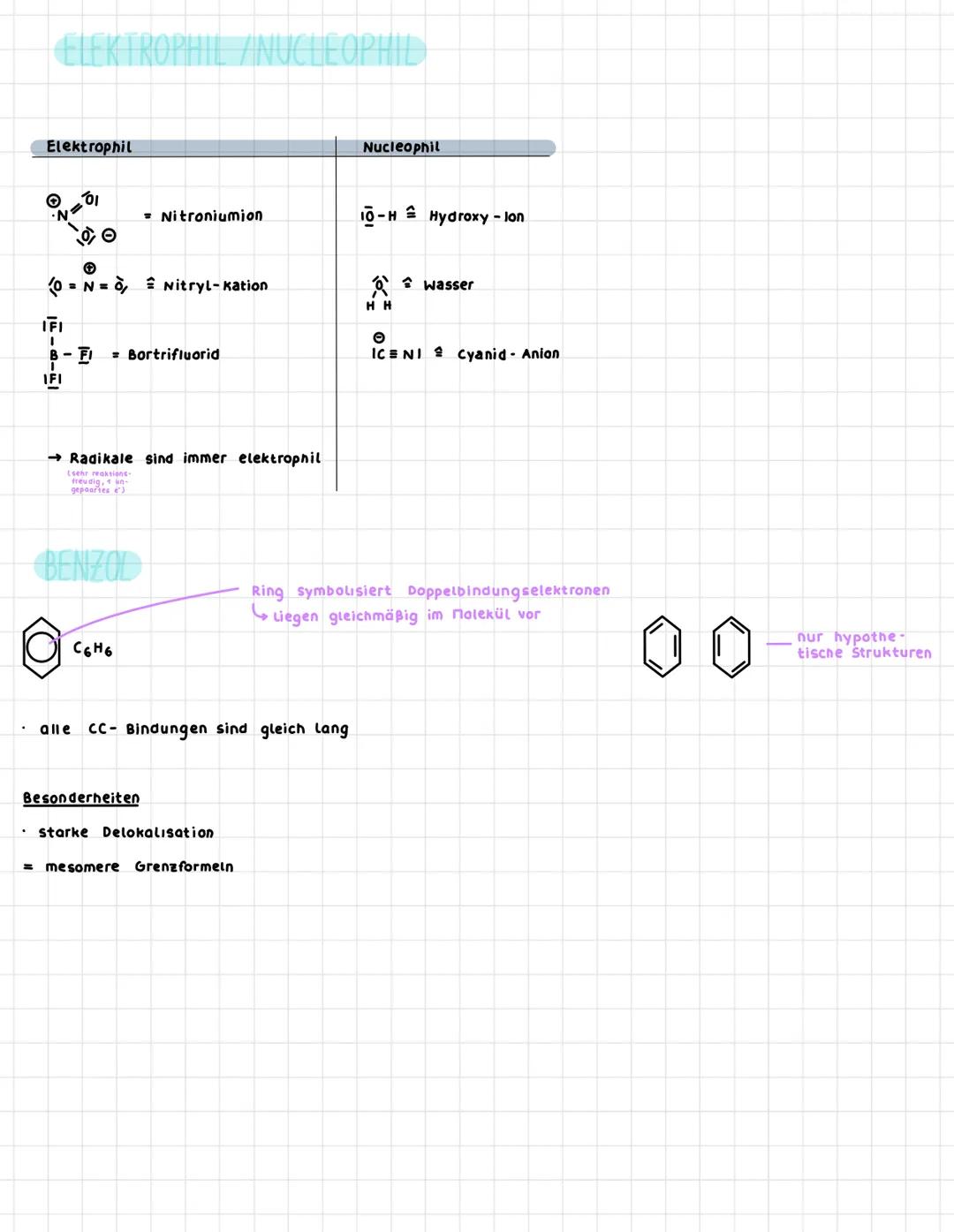
Elektrophile und Nucleophile Teilchen
Elektrophile sind Teilchen mit positiver Ladung oder Elektronenlücken, die elektronenreiche Bereiche angreifen. Wichtige Beispiele sind H⁺, NO₂⁺ oder BF₃ .
Nucleophile haben negative Ladungen oder freie Elektronenpaare und greifen elektronenarmere, positive Zentren an. Klassische Beispiele sind OH⁻, CN⁻ oder H₂O mit seinen freien Elektronenpaaren.
Radikale sind immer elektrophil, weil sie ein ungepaartes Elektron haben und sehr reaktionsfreudig sind. Sie können sowohl als Elektrophile als auch als Radikalstarter fungieren.
Der Benzolring mit seinem delokalisierten π-Elektronensystem ist elektronenreich und damit ein typisches Angriffsziel für Elektrophile. Alle C-C-Bindungen sind gleich lang wegen der mesomeren Grenzstrukturen.
💡 Denkhilfe: Elektrophile mögen Elektronen (sind elektronenhungrig), Nucleophile haben Elektronen zu verschenken!

Polyene und konjugierte Systeme
Polyene sind Moleküle mit mehreren C=C-Doppelbindungen, bei denen Doppelbindungsisomere möglich sind. Je nach Anordnung der Doppelbindungen entstehen völlig unterschiedliche Eigenschaften.
Bei isolierten Doppelbindungen liegen mehr als eine C-C-Einfachbindung zwischen den Doppelbindungen. Diese verhalten sich wie separate Alkene und zeigen keine besonderen Wechselwirkungen.
Konjugierte Doppelbindungen wechseln sich mit Einfachbindungen ab . Hier können die π-Elektronen über das ganze System delokalisiert werden, was zu besonderen optischen Eigenschaften führt - je länger das System, desto mehr verschiebt sich die Absorption in den sichtbaren Bereich.
Kumulierte Doppelbindungen sind selten und instabil. Die interessanten Systeme sind die konjugierten, die in vielen Naturstoffen wie Carotinoiden vorkommen und für deren Farbe verantwortlich sind.
💡 Alltags-Chemie: Die Farbe von Karotten, Tomaten und Herbstblättern kommt von konjugierten Polyenen!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Organische Chemie
9Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Organische Chemie: Grundlagen
Diese Zusammenfassung bietet einen umfassenden Überblick über die organische Chemie, einschließlich der homologen Reihen von Alkanen, Alkenen, Alkoholen, Aldehyden, Ketonen, Carbonsäuren, Estern und Ethern. Erfahren Sie mehr über Strukturformeln, chemische Bindungen, Reaktionen wie radikalische Substitution und Oxidation sowie deren Anwendungen und Gefahren. Ideal für Schüler und Studierende der Chemie.
Organische Chemie: Reaktionen & Strukturen
Entdecken Sie die Grundlagen der organischen Chemie, einschließlich Alkane, Halogenalkane, Alkene, Alkine, Alkohole, Ether, Aldehyde, Ketone, Carbonsäuren und Carbonsäureester. Erfahren Sie mehr über Reaktionsmechanismen wie Veresterung, nucleophile Substitution, elektrophile Substitution und die Bedeutung von cis-trans-Isomerie. Ideal für Studierende der Chemie, die ein umfassendes Verständnis der organischen Verbindungen und ihrer Eigenschaften erlangen möchten.
Alkane und ihre Eigenschaften
Entdecken Sie die Grundlagen der organischen Chemie mit einem Fokus auf Alkane, ihre homologe Reihe und Nomenklatur. Dieser Lernzettel bietet eine detaillierte Übersicht über molekulare Polarität, Erdölverarbeitung und die Strukturformeln von Alkanen. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Alkane, Alkene, Alkine und Alkanole
Grundlagen der organischen Chemie, zeichnen von Levis Formel, IUPAC Nomenklatur, Isomerie, Stoffklassen Alkane, Alkene, Alkine und Alkanole (auch Eigenschaften), alkoholische Gärung und Reaktionsgleichung zu den Stoffklassen aufstellen
Induktive Effekte in der Organik
Entdecken Sie die Schlüsselkonzepte der organischen Chemie, einschließlich induktiver Effekte, Substitution (nucleophil und radikalisch), Veresterung, Eliminierung und Addition. Diese Zusammenfassung bietet eine klare Übersicht über Enthalpie-Diagramme und die Regel von Markovnikov, um das Verständnis organischer Reaktionen zu vertiefen. Ideal für Studierende der Chemie.
Alkane Chemie und Reaktionen
Entdecken Sie die Welt der Alkane: von der homologen Reihe über Strukturformeln bis hin zu Eigenschaften und Reaktionen. Erfahren Sie mehr über Halogenalkane, radikale Substitution, die Zerstörung der Ozonschicht und die Bedeutung fossiler Brennstoffe. Diese Zusammenfassung bietet einen umfassenden Überblick über die organische Chemie der Alkane und deren Anwendungen in der Industrie.
Fette und Fettsäuren
Entdecken Sie die Grundlagen von Fetten und Fettsäuren in dieser umfassenden Übersicht. Erfahren Sie mehr über die Herstellung, Vorkommen, Struktur und Eigenschaften von Fetten. Lernen Sie den Unterschied zwischen gesättigten und ungesättigten Fetten, die Bedeutung der Fetthärtung und die Rolle von Fetten in der Verdauung. Ideal für Chemie-Studierende und alle, die sich für die Biochemie von Lipiden interessieren.
Alkane und ihre Eigenschaften
Entdecken Sie die Grundlagen der organischen Chemie mit einem Fokus auf Alkane. Dieser Lernzettel behandelt die Eigenschaften von Alkanen, ihre Nomenklatur, die homologe Reihe sowie Van-der-Waals-Kräfte und Isomere. Ideal für Chemie-Studierende, die sich auf Tests vorbereiten möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Grundlagen der Organischen Chemie: Wichtige Reaktionsmechanismen
Additionsreaktionen, elektrophile Substitution und Eliminierungsreaktionen sind die wichtigsten Reaktionstypen in der organischen Chemie. Diese Reaktionen bestimmen, wie sich Alkene, Benzol und andere organische Verbindungen verhalten und welche Produkte dabei entstehen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Additionsreaktionen - Grundlagen
Additionsreaktionen sind super praktisch: Zwei Edukt-Moleküle verbinden sich zu einem einzigen Produkt-Molekül. Dabei wird die Doppelbindung aufgespalten - denk dir vor, wie ein Reißverschluss aufgeht.
Bei der säurekatalysierten Addition von Alkoholen oder Wasser brauchst du immer H₂SO₄ als Katalysator. Ohne Katalysator passiert nämlich nichts, weil Wasser zu wenig sauer ist und kein Elektrophil vorhanden ist.
Der Mechanismus läuft in zwei Schritten ab: Erst greift das Proton (H⁺) die Doppelbindung an und es entsteht ein positiv geladenes Carbenium-Ion. Dann greift das Nucleophil (wie OH⁻) das Carbenium-Ion an und das finale Produkt entsteht.
💡 Merktipp: Bei der Hydratisierung von Propen entsteht Propan-2-ol, nicht Propan-1-ol - das zeigt dir schon, dass die Addition nicht zufällig abläuft!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Elektrophile Addition mit Halogenen
Die elektrophile Addition funktioniert durch Elektronegativitätsunterschiede - HBr ist polar und das macht die Reaktion erst möglich. Das elektronegative Brom zieht die Elektronen zu sich, wodurch Wasserstoff positiv wird.
Der Reaktionsmechanismus hat zwei klare Schritte: Zuerst erfolgt die heterolytische Bindungsspaltung von HBr, dann greift H⁺ elektrophil die elektronenreiche Doppelbindung an. Dadurch entsteht ein Carbenium-Ion.
Im zweiten Schritt greift das Bromid-Ion (nucleophil) das positiv geladene Carbenium-Ion an. So entsteht das finale Halogenalkan - bei Ethen und HBr wird daraus Ethan-1-brom.
Bei der Addition von Brom (Br₂) entsteht zuerst ein Bromonium-Ion durch Rückseitenangriff. Das ist stabiler als ein normales Carbenium-Ion und erklärt, warum diese Reaktion so glatt läuft.
💡 Praxistipp: Elektrophile haben positive Ladungen und lieben elektronenreiche Bereiche - wie die Doppelbindung in Alkenen!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Elektrophile Substitution am Benzolring
Elektrophile Substitution am Benzol braucht einen Katalysator wie FeBr₃, weil der Benzolring zu stabil ist. Die Ladungsdichte ist über den ganzen Ring verteilt - das reicht nicht zur Spaltung der Br-Br-Bindung.
Der Katalysator FeBr₃ ist eine Lewis-Säure mit freier äußerer Schale, die Elektronen aufnehmen möchte. Er polarisiert Br₂ zu Br⁺ und [FeBr₄]⁻, wodurch ein starkes Elektrophil entsteht.
Die Reaktion läuft über zwei Zwischenstuffe: Zuerst bildet sich der π-Komplex (schwache Wechselwirkung), dann der σ-Komplex (echte Bindung). Der σ-Komplex ist energetisch günstiger, weil mesomere Grenzstrukturen die positive Ladung stabilisieren.
Am Ende wird ein Proton abgespalten und die Aromatizität des Rings wiederhergestellt - das ist energetisch sehr günstig. Als Nebenprodukt entsteht Bromwasserstoff (HBr).
💡 Wichtig: Die Rearomatisierung ist der Grund, warum Substitution statt Addition stattfindet - der aromatische Ring ist einfach zu stabil!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Regioselektivität und Markownikow-Regel
Regioselektivität bedeutet, dass die Reaktion bevorzugt an einer bestimmten Stelle abläuft. Bei Alkenen kann das Elektrophil an zwei verschiedene Kohlenstoffatome addieren - aber eines ist deutlich bevorzugt.
Das Hauptprodukt entsteht immer über das stabilste Carbokation: tertiär > sekundär > primär. Ein tertiäres Carbokation bildet sich schneller und ist stabiler als ein sekundäres, weil mehr Alkylgruppen die positive Ladung stabilisieren.
Die Markownikow-Regel sagt dir genau vorher, welches Produkt entsteht: Das Elektrophil (meist H⁺) addiert an das Kohlenstoffatom mit den meisten Wasserstoffatomen. Dadurch bildet sich automatisch das stabilste Carbokation.
Je größer der Stabilitätsunterschied zwischen möglichen Carbokationen, desto regioselektiver ist die Reaktion. Tertiär vs. primär ist hochgradig regioselektiv, während sekundär vs. sekundär gar nicht regioselektiv ist.
💡 Eselsbrücke: "Der Reiche wird reicher" - das Kohlenstoffatom mit mehr H-Atomen bekommt noch ein H-Atom dazu!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Eliminierungsreaktionen im Überblick
Eliminierungsreaktionen sind das Gegenteil von Additionen - hier werden kleine Moleküle wie H₂O oder HBr abgespalten. Das ist super praktisch, um Alkene aus Alkoholen oder Halogenalkanen zu gewinnen.
Bei der Dehydratisierung von Alkanolen spaltest du Wasser ab. Tertiäre und sekundäre Alkohole reagieren leicht mit mittelstarken Säuren, primäre brauchen starke Säuren und hohe Temperaturen. Der Mechanismus läuft über Carbenium-Ionen - genau wie bei der Addition, nur rückwärts.
Die Dehydrohalogenierung verwendet starke Basen, um HX abzuspalten. Das funktioniert am besten bei tertiären Halogenalkanen und ist oft die bessere Alternative zur Dehydratisierung, weil weniger Nebenprodukte entstehen.
Dehydrierung von Alkanen braucht krasse Bedingungen: über 500°C ohne Luftzutritt. Mit Katalysatoren geht's schonender und du bekommst weniger Cracken .
💡 Reaktionsstrategie: Eliminierungen funktionieren am besten, je stabiler das entstehende Carbokation ist - genau wie bei Additionen!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Dehydrierung von Alkanen
Dehydrierung spaltet H₂ aus Alkanen ab und erzeugt dabei Alkene. Das ist industriell mega wichtig für die Herstellung von Ethen und Propen - den Grundbausteinen der Petrochemie.
Die krassen Reaktionsbedingungen (über 500°C unter Luftausschluss) führen leider auch zum Cracken - dabei brechen C-C-Bindungen und du bekommst ein Gemisch aus unterschiedlich langen Alkenen.
Katalysatoren sind hier deine Rettung: Sie ermöglichen Dehydrierung bei niedrigeren Temperaturen ohne C-C-Spaltung. Dadurch steigt die Ausbeute der gewünschten Alkene deutlich, auch wenn verschiedene Isomere in unterschiedlichen Anteilen entstehen.
In der Industrie läuft das über spezielle Metallkatalysatoren bei kontrollierten Bedingungen ab. So kannst du gezielt die Alkene herstellen, die du für weitere Synthesen brauchst.
💡 Industrietipp: Ohne Katalysatoren wäre die moderne Kunststoffproduktion unmöglich - Ethen und Propen sind die Basis für PE und PP!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Mesomerer und Induktiver Effekt
Mesomere Effekte entstehen durch freie Elektronenpaare oder π-Elektronen, die mit dem Benzolring wechselwirken. Der +π-Effekt erhöht die Elektronendichte im Ring und aktiviert ihn für elektrophile Substitution.
Substituenten wie OH, NH₂ oder OR haben freie Elektronenpaare, die in den Ring "geschoben" werden können. Dadurch wird besonders die ortho- und para-Position elektronenreich und für Elektrophile attraktiv.
Der -π-Effekt macht genau das Gegenteil: Substituenten wie NO₂, CHO oder COOH ziehen Elektronen aus dem Ring. Das deaktiviert ihn und macht die meta-Position am wenigsten ungünstig für Angriffe.
Induktive Effekte sind schwächer als mesomere, weil keine zusätzlichen Grenzstrukturen möglich sind. Alkylgruppen haben +I-Effekt (elektronenreich), Halogene haben -I-Effekt, dirigieren aber trotzdem nach ortho/para wegen ihrer freien Elektronenpaare.
💡 Faustregel: Mesomere Effekte schlagen induktive - deshalb dirigieren Halogene trotz -I-Effekt nach ortho/para!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Acidität von Phenol
Die Acidität von Phenol ist deutlich höher als die normaler Alkohole, weil das entstehende Phenolat-Ion mesomer stabilisiert wird. Die negative Ladung kann über den ganzen Benzolring delokalisiert werden.
Wenn Phenol ein Proton abgibt, entstehen mehrere mesomere Grenzstrukturen, die die negative Ladung auf verschiedene Positionen im Ring verteilen. Diese Delokalisierung macht das Phenolat-Ion viel stabiler als ein normales Alkoholat-Ion.
Deshalb reagiert Phenol schon mit schwachen Basen wie NaOH, während Alkohole starke Basen wie Natrium brauchen. Das ist ein wichtiger Unterschied in der Reaktivität zwischen aromatischen und aliphatischen Alkoholen.
💡 Chemie-Hack: Die Rotfärbung mit Eisen(III)-chlorid ist ein klassischer Phenol-Nachweis - nutze das im Labor!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Elektrophile und Nucleophile Teilchen
Elektrophile sind Teilchen mit positiver Ladung oder Elektronenlücken, die elektronenreiche Bereiche angreifen. Wichtige Beispiele sind H⁺, NO₂⁺ oder BF₃ .
Nucleophile haben negative Ladungen oder freie Elektronenpaare und greifen elektronenarmere, positive Zentren an. Klassische Beispiele sind OH⁻, CN⁻ oder H₂O mit seinen freien Elektronenpaaren.
Radikale sind immer elektrophil, weil sie ein ungepaartes Elektron haben und sehr reaktionsfreudig sind. Sie können sowohl als Elektrophile als auch als Radikalstarter fungieren.
Der Benzolring mit seinem delokalisierten π-Elektronensystem ist elektronenreich und damit ein typisches Angriffsziel für Elektrophile. Alle C-C-Bindungen sind gleich lang wegen der mesomeren Grenzstrukturen.
💡 Denkhilfe: Elektrophile mögen Elektronen (sind elektronenhungrig), Nucleophile haben Elektronen zu verschenken!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Polyene und konjugierte Systeme
Polyene sind Moleküle mit mehreren C=C-Doppelbindungen, bei denen Doppelbindungsisomere möglich sind. Je nach Anordnung der Doppelbindungen entstehen völlig unterschiedliche Eigenschaften.
Bei isolierten Doppelbindungen liegen mehr als eine C-C-Einfachbindung zwischen den Doppelbindungen. Diese verhalten sich wie separate Alkene und zeigen keine besonderen Wechselwirkungen.
Konjugierte Doppelbindungen wechseln sich mit Einfachbindungen ab . Hier können die π-Elektronen über das ganze System delokalisiert werden, was zu besonderen optischen Eigenschaften führt - je länger das System, desto mehr verschiebt sich die Absorption in den sichtbaren Bereich.
Kumulierte Doppelbindungen sind selten und instabil. Die interessanten Systeme sind die konjugierten, die in vielen Naturstoffen wie Carotinoiden vorkommen und für deren Farbe verantwortlich sind.
💡 Alltags-Chemie: Die Farbe von Karotten, Tomaten und Herbstblättern kommt von konjugierten Polyenen!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Organische Chemie
9Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Organische Chemie: Grundlagen
Diese Zusammenfassung bietet einen umfassenden Überblick über die organische Chemie, einschließlich der homologen Reihen von Alkanen, Alkenen, Alkoholen, Aldehyden, Ketonen, Carbonsäuren, Estern und Ethern. Erfahren Sie mehr über Strukturformeln, chemische Bindungen, Reaktionen wie radikalische Substitution und Oxidation sowie deren Anwendungen und Gefahren. Ideal für Schüler und Studierende der Chemie.
Organische Chemie: Reaktionen & Strukturen
Entdecken Sie die Grundlagen der organischen Chemie, einschließlich Alkane, Halogenalkane, Alkene, Alkine, Alkohole, Ether, Aldehyde, Ketone, Carbonsäuren und Carbonsäureester. Erfahren Sie mehr über Reaktionsmechanismen wie Veresterung, nucleophile Substitution, elektrophile Substitution und die Bedeutung von cis-trans-Isomerie. Ideal für Studierende der Chemie, die ein umfassendes Verständnis der organischen Verbindungen und ihrer Eigenschaften erlangen möchten.
Alkane und ihre Eigenschaften
Entdecken Sie die Grundlagen der organischen Chemie mit einem Fokus auf Alkane, ihre homologe Reihe und Nomenklatur. Dieser Lernzettel bietet eine detaillierte Übersicht über molekulare Polarität, Erdölverarbeitung und die Strukturformeln von Alkanen. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Alkane, Alkene, Alkine und Alkanole
Grundlagen der organischen Chemie, zeichnen von Levis Formel, IUPAC Nomenklatur, Isomerie, Stoffklassen Alkane, Alkene, Alkine und Alkanole (auch Eigenschaften), alkoholische Gärung und Reaktionsgleichung zu den Stoffklassen aufstellen
Induktive Effekte in der Organik
Entdecken Sie die Schlüsselkonzepte der organischen Chemie, einschließlich induktiver Effekte, Substitution (nucleophil und radikalisch), Veresterung, Eliminierung und Addition. Diese Zusammenfassung bietet eine klare Übersicht über Enthalpie-Diagramme und die Regel von Markovnikov, um das Verständnis organischer Reaktionen zu vertiefen. Ideal für Studierende der Chemie.
Alkane Chemie und Reaktionen
Entdecken Sie die Welt der Alkane: von der homologen Reihe über Strukturformeln bis hin zu Eigenschaften und Reaktionen. Erfahren Sie mehr über Halogenalkane, radikale Substitution, die Zerstörung der Ozonschicht und die Bedeutung fossiler Brennstoffe. Diese Zusammenfassung bietet einen umfassenden Überblick über die organische Chemie der Alkane und deren Anwendungen in der Industrie.
Fette und Fettsäuren
Entdecken Sie die Grundlagen von Fetten und Fettsäuren in dieser umfassenden Übersicht. Erfahren Sie mehr über die Herstellung, Vorkommen, Struktur und Eigenschaften von Fetten. Lernen Sie den Unterschied zwischen gesättigten und ungesättigten Fetten, die Bedeutung der Fetthärtung und die Rolle von Fetten in der Verdauung. Ideal für Chemie-Studierende und alle, die sich für die Biochemie von Lipiden interessieren.
Alkane und ihre Eigenschaften
Entdecken Sie die Grundlagen der organischen Chemie mit einem Fokus auf Alkane. Dieser Lernzettel behandelt die Eigenschaften von Alkanen, ihre Nomenklatur, die homologe Reihe sowie Van-der-Waals-Kräfte und Isomere. Ideal für Chemie-Studierende, die sich auf Tests vorbereiten möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.