Oxidation und Reduktion sind chemische Reaktionen, die dir ständig im... Mehr anzeigen
Oxidation und Reduktion einfach erklärt – Merksätze und Beispiele
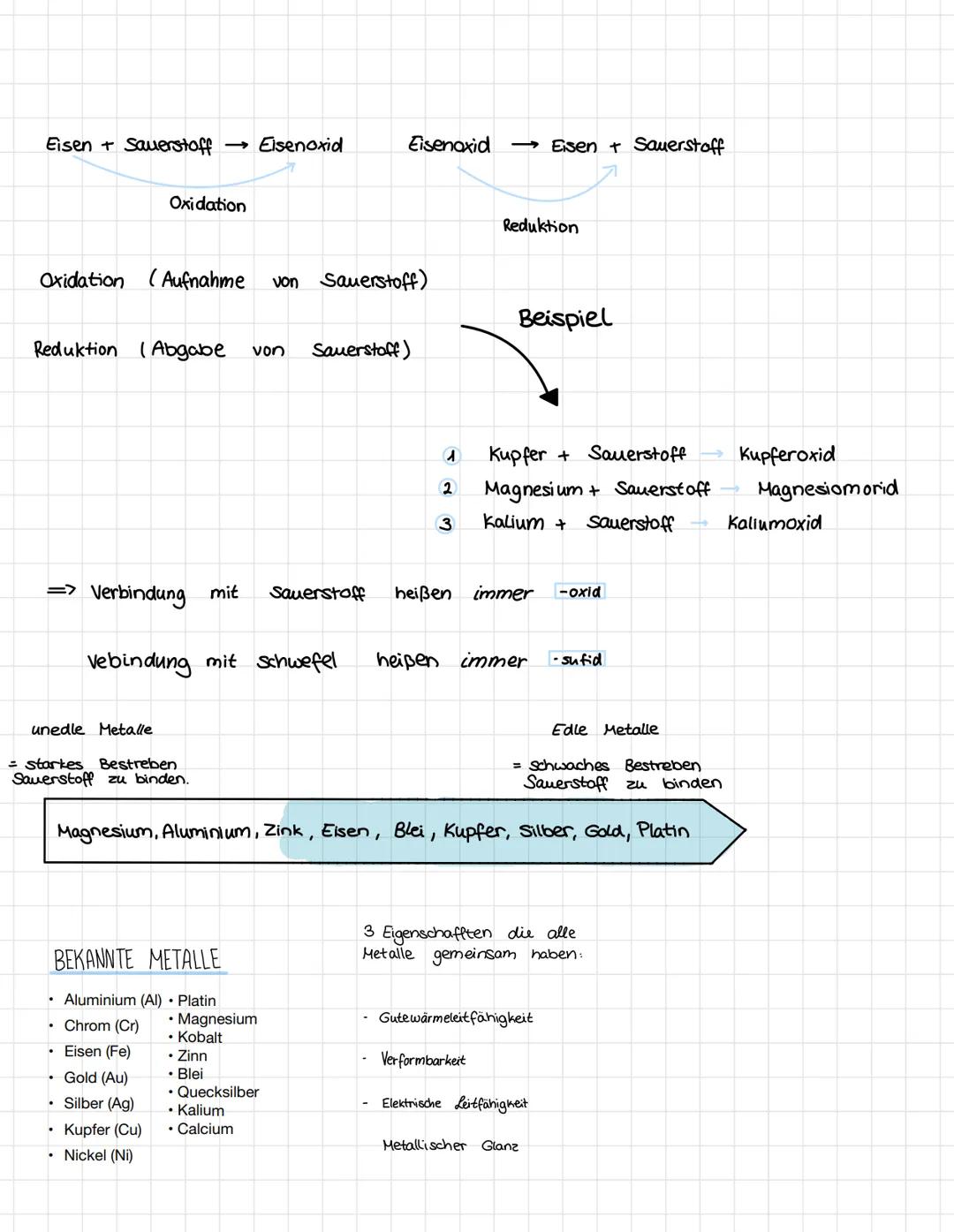
Oxidation und Reduktion - Metalle reagieren mit Sauerstoff
Oxidation bedeutet ganz einfach: Ein Stoff nimmt Sauerstoff auf. Wenn Eisen mit Sauerstoff reagiert, entsteht Eisenoxid (das kennst du als Rost!). Das passiert auch mit anderen Metallen wie Kupfer oder Magnesium.
Reduktion ist das Gegenteil - hier gibt ein Stoff Sauerstoff wieder ab. Aus Eisenoxid kann so wieder reines Eisen werden.
Eine praktische Regel: Alle Verbindungen mit Sauerstoff enden auf "-oxid", Verbindungen mit Schwefel auf "-sulfid". Das macht die Chemie viel übersichtlicher!
Bei Metallen unterscheiden wir zwischen edlen und unedlen Metallen. Unedle Metalle wie Magnesium oder Eisen wollen unbedingt Sauerstoff binden und rosten schnell. Edle Metalle wie Gold oder Silber sind viel entspannter und reagieren kaum mit Sauerstoff.
Merktipp: Gold rostet nie - deshalb ist es so wertvoll für Schmuck! Eisen dagegen rostet super schnell.
Alle Metalle haben drei wichtige Eigenschaften gemeinsam: Sie leiten Wärme und Strom gut, lassen sich verformen und glänzen metallisch. Deshalb nutzen wir Kupfer für Stromleitungen und Aluminium für Töpfe.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Reduktion
9Redoxreaktion Chemie
Erklärung kurz Oxidation und Reduktion, Einzelnen Schritte, Oxidationszahlen, Teilreaktionen
Elektrochemie
Zusammenfassung
Oxidation und Reduktion erklärt
Entdecken Sie die Grundlagen der Oxidation, Reduktion und Redoxreaktionen. Diese Zusammenfassung bietet einen klaren Vergleich zwischen Oxidation und Reduktion, erläutert wichtige chemische Reaktionen und deren Produkte, und enthält anschauliche Beispiele. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Redoxreaktionen verstehen
Erlernen Sie die Grundlagen der Redoxreaktionen, einschließlich der Aufstellung von Redoxgleichungen und der Bestimmung von Oxidationszahlen. Diese Zusammenfassung behandelt die Konzepte von Oxidation und Reduktion, die Rolle von Oxidations- und Reduktionsmitteln sowie die Elektronentransfermechanismen in chemischen Reaktionen. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Redoxreaktionen & Oxidationszahlen
Entdecke die Grundlagen von Oxidation und Reduktion! Diese Zusammenfassung behandelt die Definitionen von Oxidations- und Reduktionsmitteln, die fünf Regeln der Oxidationszahlen und bietet ein praktisches Beispiel zur Veranschaulichung. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Oxidation und Redoxreaktionen
Entdecken Sie die Grundlagen der Oxidation, Reduktion und Redoxreaktionen. Diese Zusammenfassung behandelt die exothermen Reaktionen, die Bildung von Metall- und Nichtmetalloxiden sowie die Rolle von Oxidations- und Reduktionsmitteln. Ideal für Chemie-Studierende, die die Gewinnung von Metallen aus Erzen verstehen möchten.
Redoxreaktionen verstehen
Detaillierte Anleitung zur Aufstellung komplexer Redoxgleichungen mit Wasserstoffperoxid und Permanganat-Ionen. Erfahren Sie, wie man Redoxpaare identifiziert, Oxidationszahlen ermittelt und den Ladungsausgleich durchführt. Ideal für Chemie-Studierende, die ihre Kenntnisse in Redoxreaktionen vertiefen möchten.
Redox-Reaktionen verstehen
Erfahren Sie alles über Redox-Reaktionen, einschließlich der Definition von Oxidation und Reduktion, der Aufstellung von Teilgleichungen und der Vereinfachung von Reaktionsgleichungen. Diese Zusammenfassung bietet eine klare Anleitung zur Durchführung von Redox-Reaktionen und ist ideal für Chemie-Studierende.
Ethanol-Kupferoxid Reaktion
Diese Zusammenfassung behandelt die Reaktion zwischen Ethanol und Kupferoxid, einschließlich der beobachteten Farbänderungen des Kupferstrumpfes und der chemischen Erklärungen. Es wird erläutert, wie Ethanol oxidiert wird und das stechend riechende Gas Acetaldehyd entsteht. Ideal für Studierende der Chemie, die sich mit Redoxreaktionen und den Eigenschaften von Ethanol beschäftigen.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Charaktere aus Heimsuchung von Jenny Erpenbeck
Mindmap, Allgemeines, Verlauf
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Oxidation und Reduktion einfach erklärt – Merksätze und Beispiele
Oxidation und Reduktion sind chemische Reaktionen, die dir ständig im Alltag begegnen - vom Rosten deines Fahrrads bis zum Verbrennen von Holz. Du lernst hier, wie Metalle mit Sauerstoff reagieren und warum manche Metalle wertvoller sind als andere.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Oxidation und Reduktion - Metalle reagieren mit Sauerstoff
Oxidation bedeutet ganz einfach: Ein Stoff nimmt Sauerstoff auf. Wenn Eisen mit Sauerstoff reagiert, entsteht Eisenoxid (das kennst du als Rost!). Das passiert auch mit anderen Metallen wie Kupfer oder Magnesium.
Reduktion ist das Gegenteil - hier gibt ein Stoff Sauerstoff wieder ab. Aus Eisenoxid kann so wieder reines Eisen werden.
Eine praktische Regel: Alle Verbindungen mit Sauerstoff enden auf "-oxid", Verbindungen mit Schwefel auf "-sulfid". Das macht die Chemie viel übersichtlicher!
Bei Metallen unterscheiden wir zwischen edlen und unedlen Metallen. Unedle Metalle wie Magnesium oder Eisen wollen unbedingt Sauerstoff binden und rosten schnell. Edle Metalle wie Gold oder Silber sind viel entspannter und reagieren kaum mit Sauerstoff.
Merktipp: Gold rostet nie - deshalb ist es so wertvoll für Schmuck! Eisen dagegen rostet super schnell.
Alle Metalle haben drei wichtige Eigenschaften gemeinsam: Sie leiten Wärme und Strom gut, lassen sich verformen und glänzen metallisch. Deshalb nutzen wir Kupfer für Stromleitungen und Aluminium für Töpfe.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Reduktion
9Redoxreaktion Chemie
Erklärung kurz Oxidation und Reduktion, Einzelnen Schritte, Oxidationszahlen, Teilreaktionen
Elektrochemie
Zusammenfassung
Oxidation und Reduktion erklärt
Entdecken Sie die Grundlagen der Oxidation, Reduktion und Redoxreaktionen. Diese Zusammenfassung bietet einen klaren Vergleich zwischen Oxidation und Reduktion, erläutert wichtige chemische Reaktionen und deren Produkte, und enthält anschauliche Beispiele. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Redoxreaktionen verstehen
Erlernen Sie die Grundlagen der Redoxreaktionen, einschließlich der Aufstellung von Redoxgleichungen und der Bestimmung von Oxidationszahlen. Diese Zusammenfassung behandelt die Konzepte von Oxidation und Reduktion, die Rolle von Oxidations- und Reduktionsmitteln sowie die Elektronentransfermechanismen in chemischen Reaktionen. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Redoxreaktionen & Oxidationszahlen
Entdecke die Grundlagen von Oxidation und Reduktion! Diese Zusammenfassung behandelt die Definitionen von Oxidations- und Reduktionsmitteln, die fünf Regeln der Oxidationszahlen und bietet ein praktisches Beispiel zur Veranschaulichung. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Oxidation und Redoxreaktionen
Entdecken Sie die Grundlagen der Oxidation, Reduktion und Redoxreaktionen. Diese Zusammenfassung behandelt die exothermen Reaktionen, die Bildung von Metall- und Nichtmetalloxiden sowie die Rolle von Oxidations- und Reduktionsmitteln. Ideal für Chemie-Studierende, die die Gewinnung von Metallen aus Erzen verstehen möchten.
Redoxreaktionen verstehen
Detaillierte Anleitung zur Aufstellung komplexer Redoxgleichungen mit Wasserstoffperoxid und Permanganat-Ionen. Erfahren Sie, wie man Redoxpaare identifiziert, Oxidationszahlen ermittelt und den Ladungsausgleich durchführt. Ideal für Chemie-Studierende, die ihre Kenntnisse in Redoxreaktionen vertiefen möchten.
Redox-Reaktionen verstehen
Erfahren Sie alles über Redox-Reaktionen, einschließlich der Definition von Oxidation und Reduktion, der Aufstellung von Teilgleichungen und der Vereinfachung von Reaktionsgleichungen. Diese Zusammenfassung bietet eine klare Anleitung zur Durchführung von Redox-Reaktionen und ist ideal für Chemie-Studierende.
Ethanol-Kupferoxid Reaktion
Diese Zusammenfassung behandelt die Reaktion zwischen Ethanol und Kupferoxid, einschließlich der beobachteten Farbänderungen des Kupferstrumpfes und der chemischen Erklärungen. Es wird erläutert, wie Ethanol oxidiert wird und das stechend riechende Gas Acetaldehyd entsteht. Ideal für Studierende der Chemie, die sich mit Redoxreaktionen und den Eigenschaften von Ethanol beschäftigen.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Charaktere aus Heimsuchung von Jenny Erpenbeck
Mindmap, Allgemeines, Verlauf
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.