Chemische Bindungen sind überall um dich herum - vom Wasser,... Mehr anzeigen
Was sind polare und unpolare Elektronenpaarbindungen?






Polare und unpolare Elektronenpaarbindung
Du kennst bestimmt das Gefühl, wenn sich jemand unfair verhält - genau so ist es auch bei Elektronenpaarbindungen! Diese entstehen, wenn sich zwei Atome Elektronen teilen, um stabile Verbindungen zu bilden.
Ob eine Bindung fair oder unfair ist, hängt davon ab, wie stark die beteiligten Atome an den gemeinsamen Elektronen "ziehen". Das ist wie beim Tauziehen - manchmal sind beide Teams gleich stark, manchmal gewinnt eindeutig eine Seite.
💡 Merktipp: Stelle dir Elektronen wie einen Kuchen vor, den sich zwei Freunde teilen - manchmal fair, manchmal nimmt einer mehr!

Elektronegativität verstehen
Die Elektronegativität ist dein Schlüssel zum Verständnis chemischer Bindungen. Sie zeigt dir, wie gierig ein Atom nach Elektronen ist - quasi wie hungrig es nach seinem Anteil am "Elektronen-Kuchen" ist.
Im Periodensystem findest du diese Werte direkt bei jedem Element. Wasserstoff hat zum Beispiel eine Elektronegativität von 2,1. Je höher der Wert, desto stärker zieht das Atom die Elektronen zu sich.
Mit der Elektronegativitätsdifferenz (ΔEN) kannst du vorhersagen, welche Art von Bindung entsteht. Ist ΔEN < 0,4, hast du eine unpolare Bindung. Liegt sie zwischen 0,4 und 1,7, ist die Bindung polar. Darüber hinaus entstehen Ionenbindungen.
💡 Prüfungstipp: Lerne die drei Bereiche auswendig - sie kommen garantiert in der Klassenarbeit vor!

Partialladungen erkennen
Wenn Atome unfair an Elektronen ziehen, entstehen Partialladungen - das sind Teilladungen, die mit δ+ und δ- gekennzeichnet werden. Das gierigere Atom bekommt eine negative Partialladung (δ-), das andere eine positive (δ+).
Diese asymmetrische Ladungsverteilung macht das gesamte Molekül polar. Stell dir vor, ein Magnet hätte plötzlich einen stärkeren Nord- und einen schwächeren Südpol - genau so funktioniert's bei polaren Molekülen.
Die Polarität des gesamten Moleküls beeinflusst viele Eigenschaften wie Löslichkeit oder Siedepunkt. Deshalb ist es super wichtig, dass du Partialladungen erkennen kannst.
💡 Eselsbrücke: δ+ bedeutet "delta plus" - das Atom hat Elektronen verloren, δ- bedeutet "delta minus" - das Atom hat Elektronen gewonnen!
Ladungsverteilung visualisieren
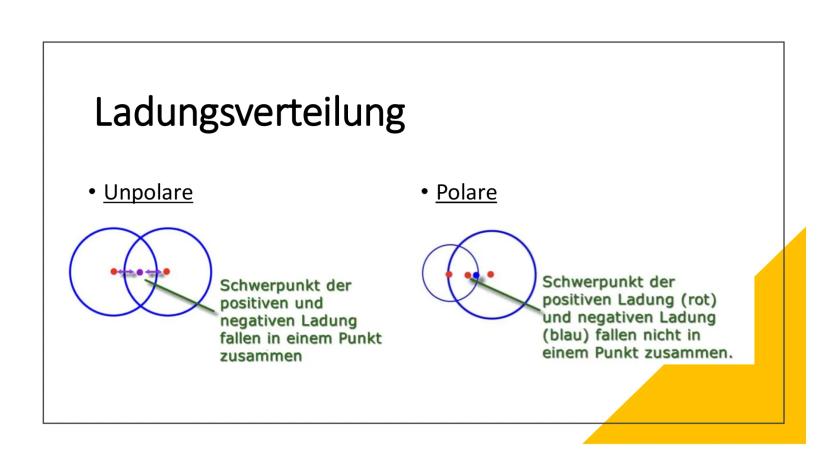
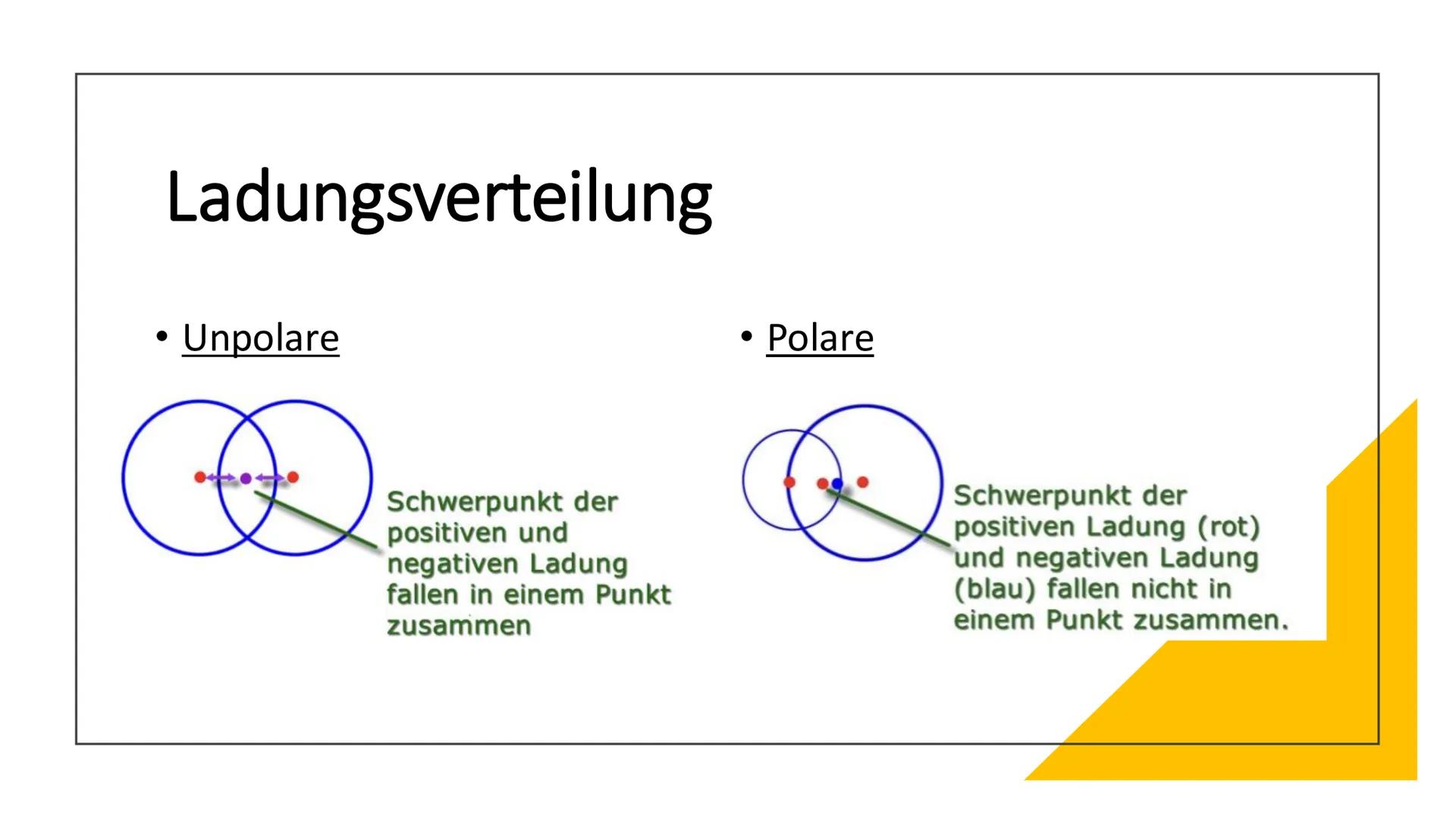
Bei der Ladungsverteilung geht es um die Schwerpunkte der positiven und negativen Ladungen im Molekül. Das klingt kompliziert, ist aber eigentlich ganz einfach zu verstehen.
Bei unpolaren Molekülen fallen die Schwerpunkte der positiven und negativen Ladung an derselben Stelle zusammen - wie zwei perfekt übereinanderliegende Kreise. Bei polaren Molekülen sind diese Schwerpunkte räumlich getrennt.
Du kannst dir das wie eine Waage vorstellen: Unpolare Moleküle sind perfekt ausbalanciert, polare Moleküle haben ein Ungleichgewicht. Diese räumliche Trennung ist der Grund, warum polare Moleküle so besondere Eigenschaften haben.
💡 Visualisierung: Zeichne dir die Schwerpunkte immer ein - das hilft beim Verstehen der Molekülform!
Praktische Beispiele berechnen
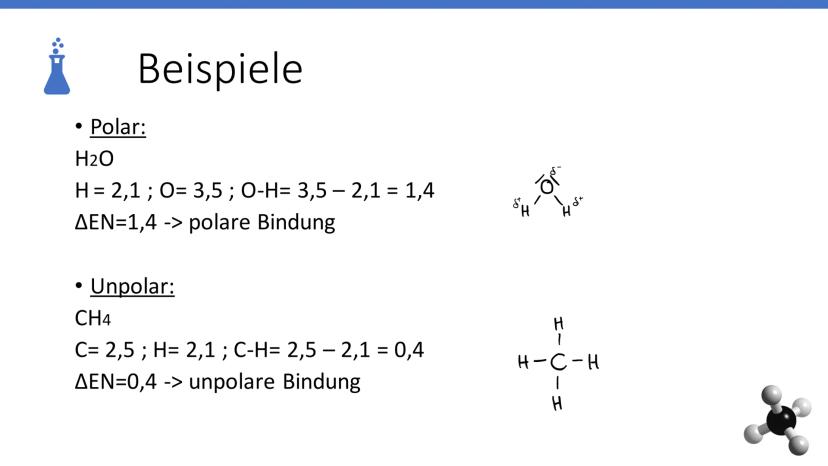
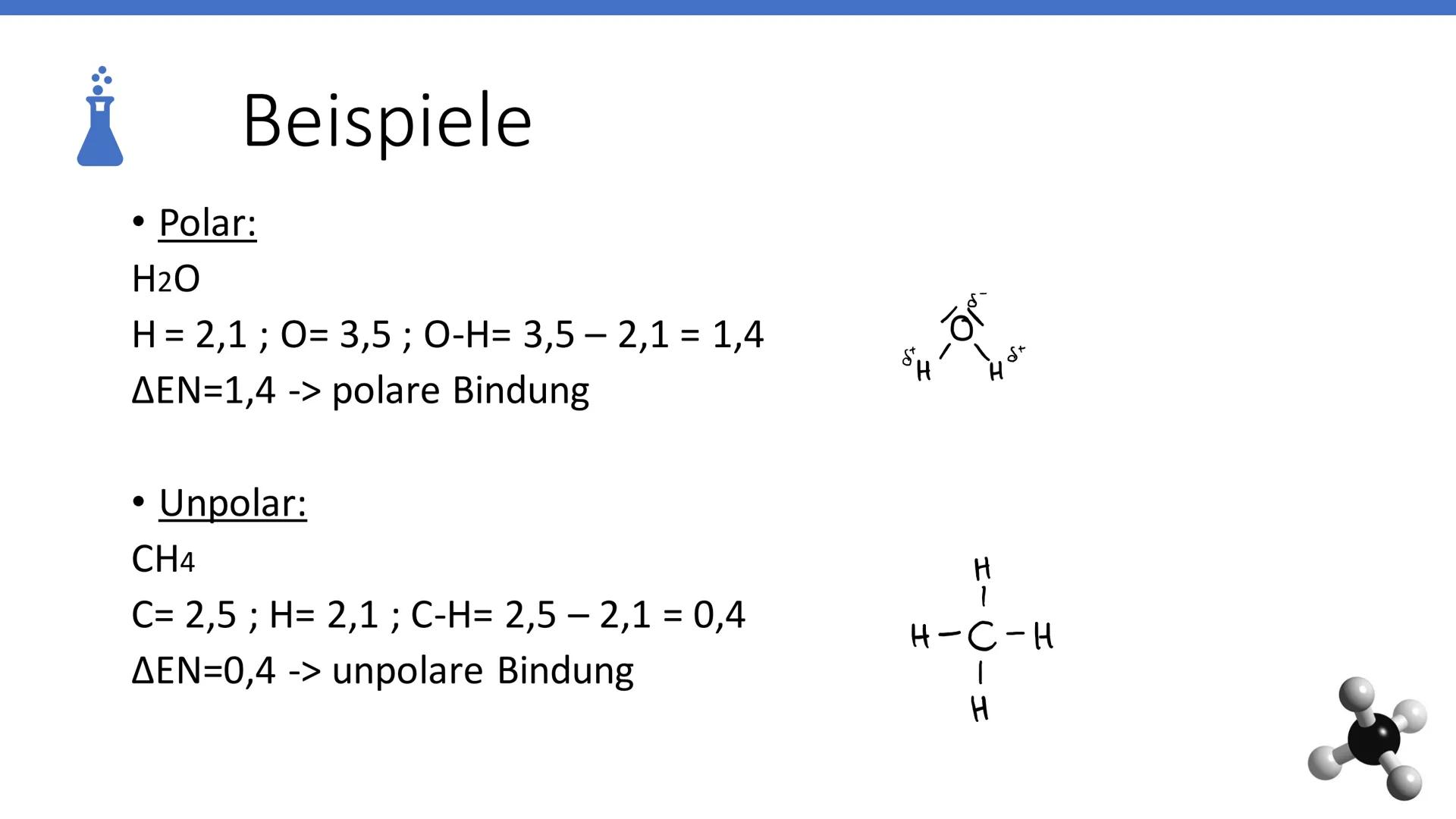
Wasser (H₂O) ist dein Paradebeispiel für polare Bindungen. Sauerstoff hat eine Elektronegativität von 3,5, Wasserstoff nur 2,1. Die Differenz beträgt 1,4 - das liegt im polaren Bereich zwischen 0,4 und 1,7.
Methan (CH₄) zeigt dir eine unpolare Bindung. Kohlenstoff (2,5) und Wasserstoff (2,1) haben eine Differenz von nur 0,4. Das ist genau die Grenze zur unpolaren Bindung.
Diese Berechnungen sind dein Handwerkszeug in der Chemie. Mit ein bisschen Übung rechnest du diese Werte schneller aus als dein Taschenrechner angeht!
💡 Übungstipp: Nimm dir fünf Moleküle aus deinem Chemiebuch und berechne deren Elektronegativitätsdifferenzen - Übung macht den Meister!


Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: polare kovalente Bindung
3Polare und Unpolare Moleküle
Entdecken Sie die Unterschiede zwischen polaren und unpolaren Molekülen. Diese Zusammenfassung behandelt die Definition von Molekülen, die Bedeutung der Elektronegativität, die Oktettregel sowie die Darstellung von Molekülformeln. Ideal für Chemie-Studierende, die ein besseres Verständnis für molekulare Bindungen und deren Eigenschaften entwickeln möchten.
Lewis-Strukturen und Bindungen
Erfahren Sie alles über Lewis-Strukturen, die Besatzungsregel und die Unterschiede zwischen polarer und unpolarer Bindung. Diese Zusammenfassung bietet eine klare Schritt-für-Schritt-Anleitung zur Erstellung von Lewis-Formeln und erklärt die Grundlagen der chemischen Bindungen. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Redoxreaktionen und Bindungen
Entdecken Sie die Grundlagen der Redoxreaktionen, Elektronegativität und die Unterschiede zwischen polaren und unpolaren Atombindungen. Diese Zusammenfassung bietet eine klare Erklärung der Konzepte, die für das Verständnis chemischer Reaktionen und Molekülstrukturen in der 10. Klasse entscheidend sind.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Charaktere aus Heimsuchung von Jenny Erpenbeck
Mindmap, Allgemeines, Verlauf
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Was sind polare und unpolare Elektronenpaarbindungen?
Chemische Bindungen sind überall um dich herum - vom Wasser, das du trinkst, bis zum Methan in deinem Gasherd. Aber nicht alle Bindungen sind gleich: Manche teilen Elektronen fair, andere sind ziemliche Egoisten.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Polare und unpolare Elektronenpaarbindung
Du kennst bestimmt das Gefühl, wenn sich jemand unfair verhält - genau so ist es auch bei Elektronenpaarbindungen! Diese entstehen, wenn sich zwei Atome Elektronen teilen, um stabile Verbindungen zu bilden.
Ob eine Bindung fair oder unfair ist, hängt davon ab, wie stark die beteiligten Atome an den gemeinsamen Elektronen "ziehen". Das ist wie beim Tauziehen - manchmal sind beide Teams gleich stark, manchmal gewinnt eindeutig eine Seite.
💡 Merktipp: Stelle dir Elektronen wie einen Kuchen vor, den sich zwei Freunde teilen - manchmal fair, manchmal nimmt einer mehr!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Elektronegativität verstehen
Die Elektronegativität ist dein Schlüssel zum Verständnis chemischer Bindungen. Sie zeigt dir, wie gierig ein Atom nach Elektronen ist - quasi wie hungrig es nach seinem Anteil am "Elektronen-Kuchen" ist.
Im Periodensystem findest du diese Werte direkt bei jedem Element. Wasserstoff hat zum Beispiel eine Elektronegativität von 2,1. Je höher der Wert, desto stärker zieht das Atom die Elektronen zu sich.
Mit der Elektronegativitätsdifferenz (ΔEN) kannst du vorhersagen, welche Art von Bindung entsteht. Ist ΔEN < 0,4, hast du eine unpolare Bindung. Liegt sie zwischen 0,4 und 1,7, ist die Bindung polar. Darüber hinaus entstehen Ionenbindungen.
💡 Prüfungstipp: Lerne die drei Bereiche auswendig - sie kommen garantiert in der Klassenarbeit vor!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Partialladungen erkennen
Wenn Atome unfair an Elektronen ziehen, entstehen Partialladungen - das sind Teilladungen, die mit δ+ und δ- gekennzeichnet werden. Das gierigere Atom bekommt eine negative Partialladung (δ-), das andere eine positive (δ+).
Diese asymmetrische Ladungsverteilung macht das gesamte Molekül polar. Stell dir vor, ein Magnet hätte plötzlich einen stärkeren Nord- und einen schwächeren Südpol - genau so funktioniert's bei polaren Molekülen.
Die Polarität des gesamten Moleküls beeinflusst viele Eigenschaften wie Löslichkeit oder Siedepunkt. Deshalb ist es super wichtig, dass du Partialladungen erkennen kannst.
💡 Eselsbrücke: δ+ bedeutet "delta plus" - das Atom hat Elektronen verloren, δ- bedeutet "delta minus" - das Atom hat Elektronen gewonnen!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Ladungsverteilung visualisieren
Bei der Ladungsverteilung geht es um die Schwerpunkte der positiven und negativen Ladungen im Molekül. Das klingt kompliziert, ist aber eigentlich ganz einfach zu verstehen.
Bei unpolaren Molekülen fallen die Schwerpunkte der positiven und negativen Ladung an derselben Stelle zusammen - wie zwei perfekt übereinanderliegende Kreise. Bei polaren Molekülen sind diese Schwerpunkte räumlich getrennt.
Du kannst dir das wie eine Waage vorstellen: Unpolare Moleküle sind perfekt ausbalanciert, polare Moleküle haben ein Ungleichgewicht. Diese räumliche Trennung ist der Grund, warum polare Moleküle so besondere Eigenschaften haben.
💡 Visualisierung: Zeichne dir die Schwerpunkte immer ein - das hilft beim Verstehen der Molekülform!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Praktische Beispiele berechnen
Wasser (H₂O) ist dein Paradebeispiel für polare Bindungen. Sauerstoff hat eine Elektronegativität von 3,5, Wasserstoff nur 2,1. Die Differenz beträgt 1,4 - das liegt im polaren Bereich zwischen 0,4 und 1,7.
Methan (CH₄) zeigt dir eine unpolare Bindung. Kohlenstoff (2,5) und Wasserstoff (2,1) haben eine Differenz von nur 0,4. Das ist genau die Grenze zur unpolaren Bindung.
Diese Berechnungen sind dein Handwerkszeug in der Chemie. Mit ein bisschen Übung rechnest du diese Werte schneller aus als dein Taschenrechner angeht!
💡 Übungstipp: Nimm dir fünf Moleküle aus deinem Chemiebuch und berechne deren Elektronegativitätsdifferenzen - Übung macht den Meister!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: polare kovalente Bindung
3Polare und Unpolare Moleküle
Entdecken Sie die Unterschiede zwischen polaren und unpolaren Molekülen. Diese Zusammenfassung behandelt die Definition von Molekülen, die Bedeutung der Elektronegativität, die Oktettregel sowie die Darstellung von Molekülformeln. Ideal für Chemie-Studierende, die ein besseres Verständnis für molekulare Bindungen und deren Eigenschaften entwickeln möchten.
Lewis-Strukturen und Bindungen
Erfahren Sie alles über Lewis-Strukturen, die Besatzungsregel und die Unterschiede zwischen polarer und unpolarer Bindung. Diese Zusammenfassung bietet eine klare Schritt-für-Schritt-Anleitung zur Erstellung von Lewis-Formeln und erklärt die Grundlagen der chemischen Bindungen. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Redoxreaktionen und Bindungen
Entdecken Sie die Grundlagen der Redoxreaktionen, Elektronegativität und die Unterschiede zwischen polaren und unpolaren Atombindungen. Diese Zusammenfassung bietet eine klare Erklärung der Konzepte, die für das Verständnis chemischer Reaktionen und Molekülstrukturen in der 10. Klasse entscheidend sind.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Kunststoffchemie und Recycling
Entdecken Sie die Grundlagen der Kunststoffchemie, einschließlich der Synthese von Polyethylen, Polykondensation und den verschiedenen Recyclingmethoden. Diese Zusammenfassung behandelt wichtige Konzepte wie Thermoplaste, Duroplaste und die Umweltauswirkungen von Kunststoffen. Ideal für Studierende der Chemie und Umweltwissenschaften.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Charaktere aus Heimsuchung von Jenny Erpenbeck
Mindmap, Allgemeines, Verlauf
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.