Redoxreaktionen sind überall um uns herum - von der Atmung... Mehr anzeigen
Melde dich an, um den Inhalt zu sehenKostenlos!
Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Knowunity KI
Fächer
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Alle Themen anzeigen
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Alle Themen anzeigen
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Alle Themen anzeigen
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Alle Themen anzeigen
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Alle Themen anzeigen
1,257
•
Aktualisiert Apr 17, 2026
•
Riccardo Celori
@riccardocelori_byea
Redoxreaktionen sind überall um uns herum - von der Atmung... Mehr anzeigen





Du kennst sicher Batterien oder das Rosten von Eisen - das sind alles Redoxreaktionen! Anders als bei Säure-Base-Reaktionen werden hier keine Protonen, sondern Elektronen übertragen.
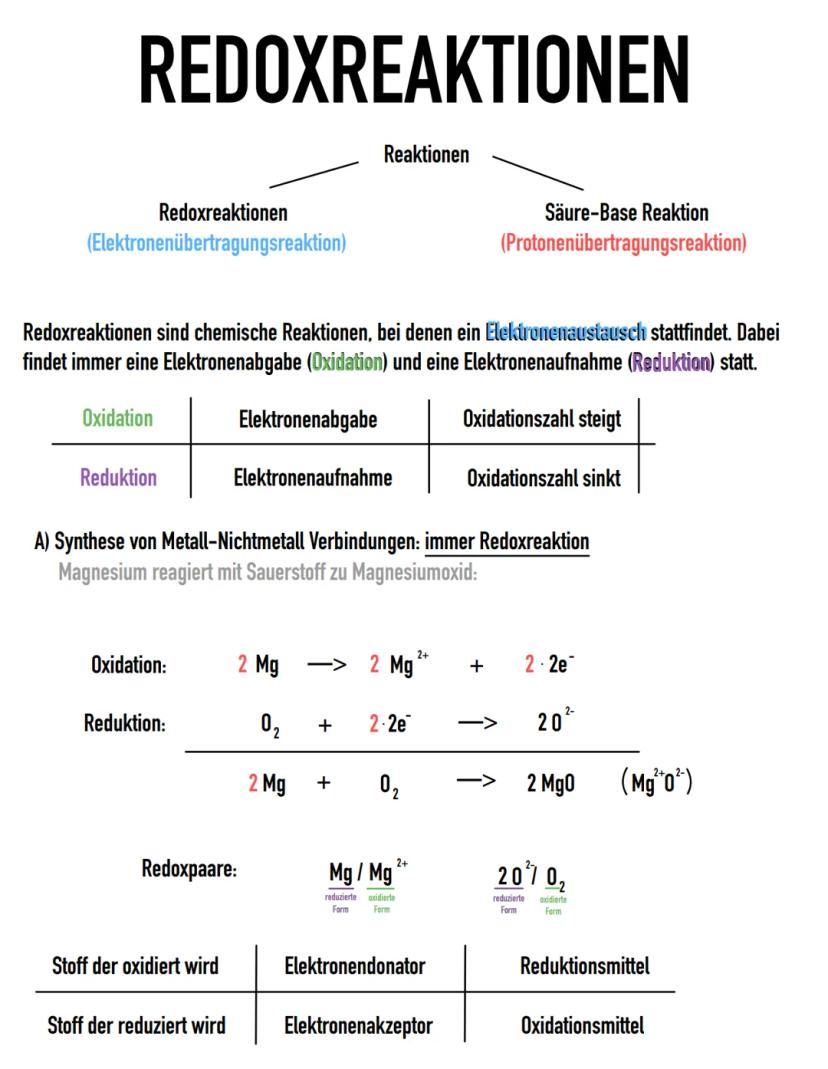
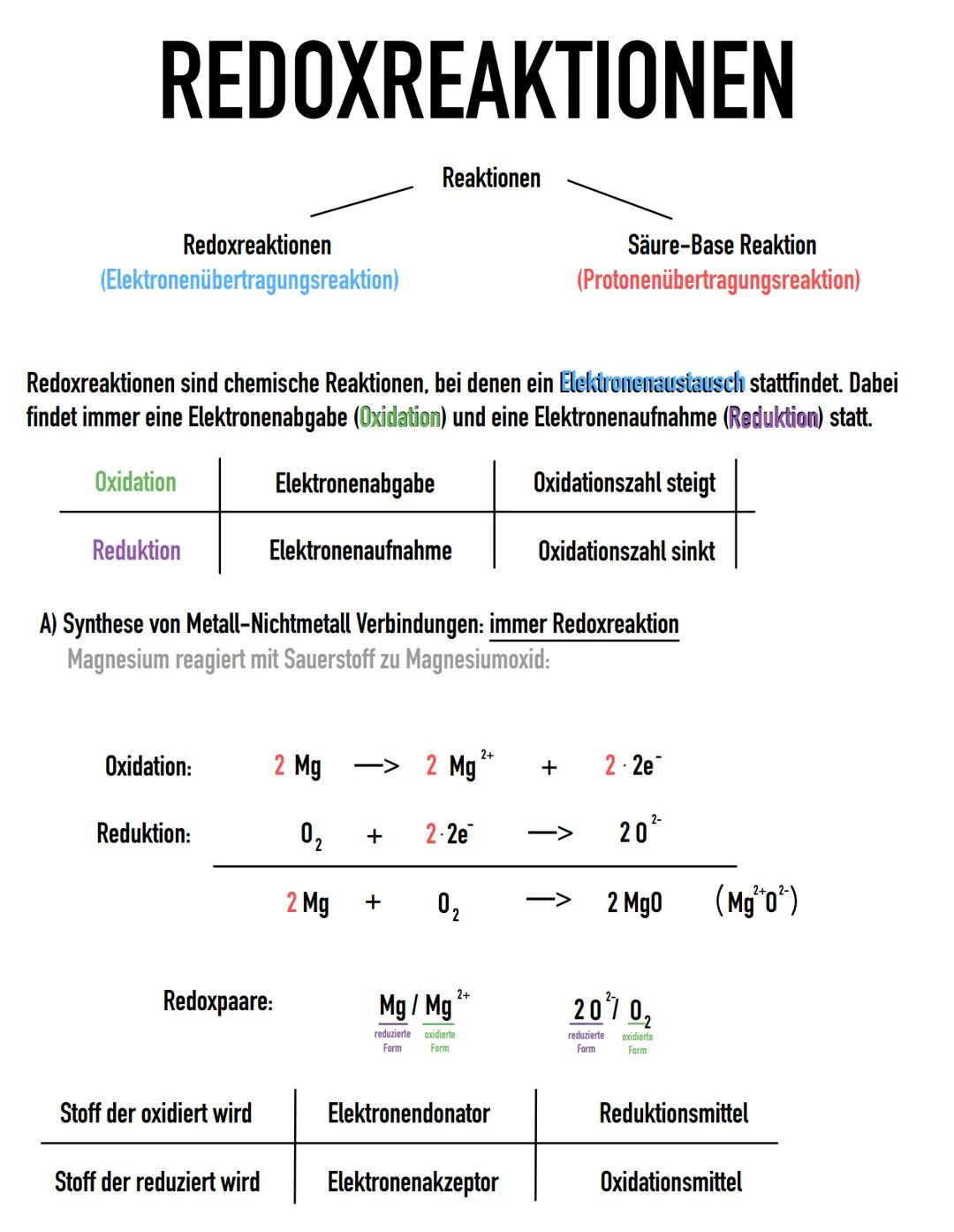
Bei jeder Redoxreaktion laufen zwei Prozesse gleichzeitig ab: die Oxidation (Elektronenabgabe) und die Reduktion (Elektronenaufnahme). Ein einfaches Beispiel ist die Reaktion von Magnesium mit Sauerstoff zu Magnesiumoxid.
Das Magnesium gibt dabei Elektronen ab (wird oxidiert) und fungiert als Reduktionsmittel. Der Sauerstoff nimmt diese Elektronen auf (wird reduziert) und ist das Oxidationsmittel. Die Oxidationszahlen helfen dir dabei, herauszufinden, welcher Stoff oxidiert und welcher reduziert wird.
Merktipp: Das Reduktionsmittel wird selbst oxidiert und das Oxidationsmittel wird selbst reduziert!

Die Synthese von Metall-Nichtmetall-Verbindungen sind immer Redoxreaktionen - das macht das Verstehen einfacher! Schauen wir uns konkrete Beispiele an.
Wenn Aluminium mit Sauerstoff reagiert, entstehen Al³⁺-Ionen und O²⁻-Ionen, die sich zu Al₂O₃ verbinden. Hier musst du die Elektronen ausgleichen: 4 Al-Atome geben je 3 Elektronen ab (12e⁻), während 3 O₂-Moleküle diese 12 Elektronen aufnehmen.
Bei der Reaktion von Kalium mit Sauerstoff zu K₂O läuft es ähnlich ab. Das Kalium wird zu K⁺ oxidiert, während Sauerstoff zu O²⁻ reduziert wird. Der Trick ist, die Anzahl der abgegebenen und aufgenommenen Elektronen gleich zu machen.
Praxistipp: Metalle geben immer Elektronen ab und werden oxidiert, Nichtmetalle nehmen sie auf und werden reduziert!

Das Aufstellen komplexer Redoxgleichungen sieht schwieriger aus, als es ist! Mit der richtigen Methode klappt es systematisch.
Am Beispiel der Permanganat-Reaktion siehst du das Vorgehen: Zuerst bestimmst du die Oxidationszahlen aller Elemente. Dann erkennst du, dass Fe²⁺ zu Fe³⁺ oxidiert wird (gibt 1e⁻ ab) und MnO₄⁻ zu Mn²⁺ reduziert wird (nimmt 5e⁻ auf).
Jetzt gleichst du die Elektronen aus: Du brauchst 5 Fe²⁺-Ionen für 1 MnO₄⁻-Ion. Danach gleichst du die Ladungen mit H₃O⁺-Ionen aus und zum Schluss die Atomanzahl mit H₂O-Molekülen. Kontrolle ist wichtig - zähle am Ende alle Atome und Ladungen nach!
Erfolgsgeheimnis: Arbeite Schritt für Schritt - erst Oxidationszahlen, dann Elektronen, dann Ladungen, zuletzt Atome!

Mit etwas Übung werden auch schwierigere Redoxgleichungen zum Kinderspiel! Die Wasserstoffperoxid-Permanganat-Reaktion zeigt dir, wie es geht.
H₂O₂ kann sowohl oxidiert als auch reduziert werden - hier wird es zu O₂ oxidiert (gibt 2e⁻ ab pro Molekül). Das Permanganat wird wie vorher zu Mn²⁺ reduziert (nimmt 5e⁻ auf). Also brauchst du 5 H₂O₂ für 2 MnO₄⁻.
Bei organischen Verbindungen wie Ethanol zu Ethanal läuft es genauso ab. Das Ethanol verliert Elektronen (wird oxidiert), während das Dichromat sie aufnimmt (wird zu Cr³⁺ reduziert). Der Elektronenausgleich funktioniert nach dem gleichen Schema.
Übungstipp: Je mehr Beispiele du rechnest, desto automatischer wird das Vorgehen - übung macht den Meister!
Stell dir vor, du kannst aus einer chemischen Reaktion direkt Strom erzeugen - genau das passiert in galvanischen Zellen! Wenn du einen Eisennagel in Kupfersulfat-Lösung tauchst, fließen Elektronen vom Eisen zu den Kupfer-Ionen.
In einer galvanischen Zelle trennst du die beiden Reaktionspartner räumlich voneinander. Die Zinkhalbzelle (wo die Oxidation stattfindet) ist die Anode und der Minuspol. Die Kupferhalbzelle (wo die Reduktion abläuft) ist die Kathode und der Pluspol.
Das Diaphragma zwischen den Halbzellen ist entscheidend - es lässt Ionen durch, verhindert aber das Vermischen der Lösungen. So entsteht ein geschlossener Stromkreis, während die Reaktion kontrolliert abläuft. Mit der Zeit wird der Zinkstab kleiner und der Kupferstab größer.
Anwendung: Deine Handy-Batterie funktioniert nach dem gleichen Prinzip - nur mit anderen Materialien!

Die Spannung in galvanischen Zellen entsteht durch unterschiedliche Elektrodenpotentiale der Metalle. Jedes Metall hat eine charakteristische Neigung, Ionen zu bilden - die sogenannte Lösungstension.
Unedle Metalle wie Zink geben leicht Elektronen ab und werden zur Anode (negativer Pol). Edle Metalle wie Silber nehmen lieber Elektronen auf und werden zur Kathode (positiver Pol). Die elektrochemische Doppelschicht an der Metalloberfläche erklärt, warum sich überhaupt ein Potential aufbaut.
Der Elektronenfluss geht immer vom Metall mit höherem Elektronendruck (negativeres Potential) zum Metall mit niedrigerem Elektronendruck (positiveres Potential). Deshalb fließt der Strom von der Zink- zur Kupferelektrode.
Merkregel: Unedel gibt ab, edel nimmt auf - wie beim Geben und Nehmen im echten Leben!

Mit der elektrochemischen Spannungsreihe kannst du vorhersagen, welche Spannung eine galvanische Zelle liefert! Die Einzelpotentiale lassen sich nicht messen, aber ihre Differenz schon.
Die Standard-Wasserstoffelektrode dient als Bezugspunkt mit 0,00 V. Alle anderen Standardelektrodenpotentiale werden gegen diese gemessen. Zink hat -0,76 V, Kupfer +0,34 V und Silber +0,80 V.
Die Formel U = U₀(Kathode) - U₀(Anode) gibt dir direkt die Spannung. Für eine Zink-Kupfer-Zelle rechnest du: 0,34 V - = 1,10 V. Je größer der Unterschied der Potentiale, desto höher die Spannung!
Prüfungstipp: Lerne die wichtigsten Standardpotentiale auswendig - sie kommen in fast jeder Klausur vor!
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Riccardo Celori
@riccardocelori_byea
Redoxreaktionen sind überall um uns herum - von der Atmung bis zur Handy-Batterie. Bei diesen chemischen Reaktionen werden Elektronen zwischen Atomen übertragen, wobei immer gleichzeitig eine Oxidation und eine Reduktion stattfindet.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Du kennst sicher Batterien oder das Rosten von Eisen - das sind alles Redoxreaktionen! Anders als bei Säure-Base-Reaktionen werden hier keine Protonen, sondern Elektronen übertragen.
Bei jeder Redoxreaktion laufen zwei Prozesse gleichzeitig ab: die Oxidation (Elektronenabgabe) und die Reduktion (Elektronenaufnahme). Ein einfaches Beispiel ist die Reaktion von Magnesium mit Sauerstoff zu Magnesiumoxid.
Das Magnesium gibt dabei Elektronen ab (wird oxidiert) und fungiert als Reduktionsmittel. Der Sauerstoff nimmt diese Elektronen auf (wird reduziert) und ist das Oxidationsmittel. Die Oxidationszahlen helfen dir dabei, herauszufinden, welcher Stoff oxidiert und welcher reduziert wird.
Merktipp: Das Reduktionsmittel wird selbst oxidiert und das Oxidationsmittel wird selbst reduziert!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Synthese von Metall-Nichtmetall-Verbindungen sind immer Redoxreaktionen - das macht das Verstehen einfacher! Schauen wir uns konkrete Beispiele an.
Wenn Aluminium mit Sauerstoff reagiert, entstehen Al³⁺-Ionen und O²⁻-Ionen, die sich zu Al₂O₃ verbinden. Hier musst du die Elektronen ausgleichen: 4 Al-Atome geben je 3 Elektronen ab (12e⁻), während 3 O₂-Moleküle diese 12 Elektronen aufnehmen.
Bei der Reaktion von Kalium mit Sauerstoff zu K₂O läuft es ähnlich ab. Das Kalium wird zu K⁺ oxidiert, während Sauerstoff zu O²⁻ reduziert wird. Der Trick ist, die Anzahl der abgegebenen und aufgenommenen Elektronen gleich zu machen.
Praxistipp: Metalle geben immer Elektronen ab und werden oxidiert, Nichtmetalle nehmen sie auf und werden reduziert!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Das Aufstellen komplexer Redoxgleichungen sieht schwieriger aus, als es ist! Mit der richtigen Methode klappt es systematisch.
Am Beispiel der Permanganat-Reaktion siehst du das Vorgehen: Zuerst bestimmst du die Oxidationszahlen aller Elemente. Dann erkennst du, dass Fe²⁺ zu Fe³⁺ oxidiert wird (gibt 1e⁻ ab) und MnO₄⁻ zu Mn²⁺ reduziert wird (nimmt 5e⁻ auf).
Jetzt gleichst du die Elektronen aus: Du brauchst 5 Fe²⁺-Ionen für 1 MnO₄⁻-Ion. Danach gleichst du die Ladungen mit H₃O⁺-Ionen aus und zum Schluss die Atomanzahl mit H₂O-Molekülen. Kontrolle ist wichtig - zähle am Ende alle Atome und Ladungen nach!
Erfolgsgeheimnis: Arbeite Schritt für Schritt - erst Oxidationszahlen, dann Elektronen, dann Ladungen, zuletzt Atome!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Mit etwas Übung werden auch schwierigere Redoxgleichungen zum Kinderspiel! Die Wasserstoffperoxid-Permanganat-Reaktion zeigt dir, wie es geht.
H₂O₂ kann sowohl oxidiert als auch reduziert werden - hier wird es zu O₂ oxidiert (gibt 2e⁻ ab pro Molekül). Das Permanganat wird wie vorher zu Mn²⁺ reduziert (nimmt 5e⁻ auf). Also brauchst du 5 H₂O₂ für 2 MnO₄⁻.
Bei organischen Verbindungen wie Ethanol zu Ethanal läuft es genauso ab. Das Ethanol verliert Elektronen (wird oxidiert), während das Dichromat sie aufnimmt (wird zu Cr³⁺ reduziert). Der Elektronenausgleich funktioniert nach dem gleichen Schema.
Übungstipp: Je mehr Beispiele du rechnest, desto automatischer wird das Vorgehen - übung macht den Meister!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
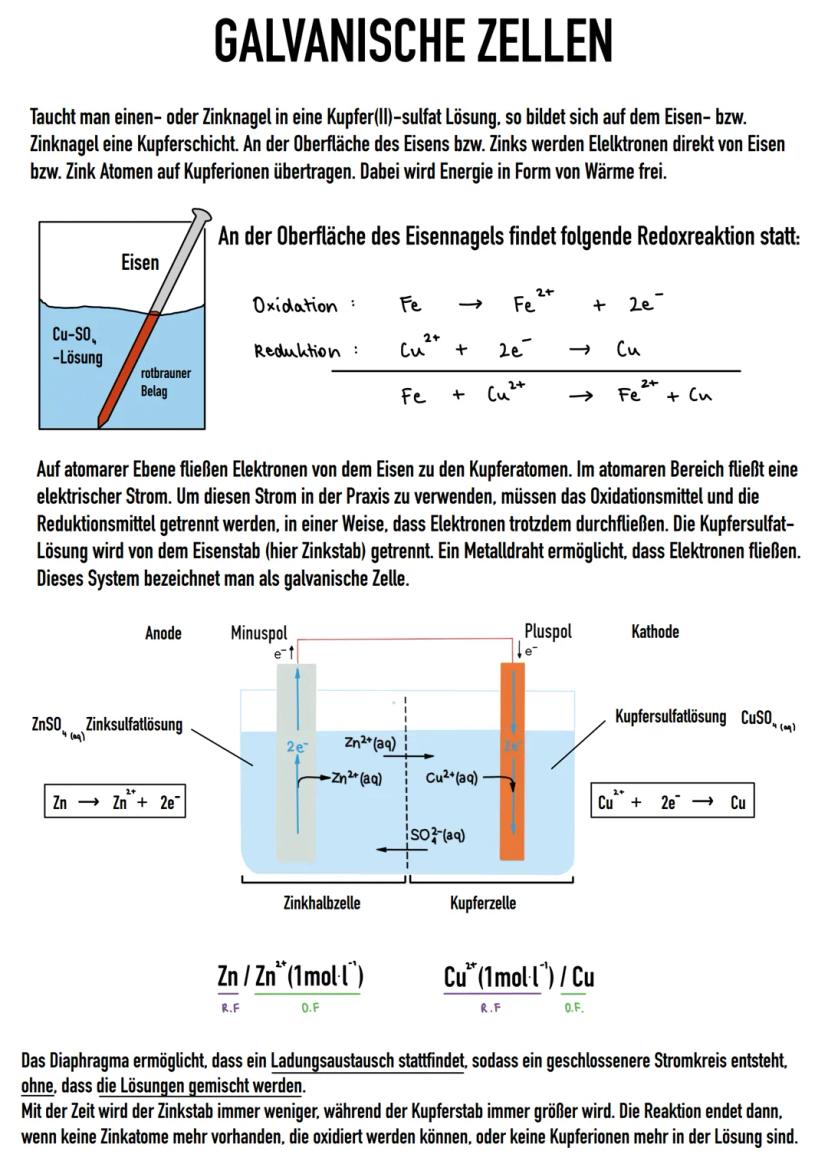
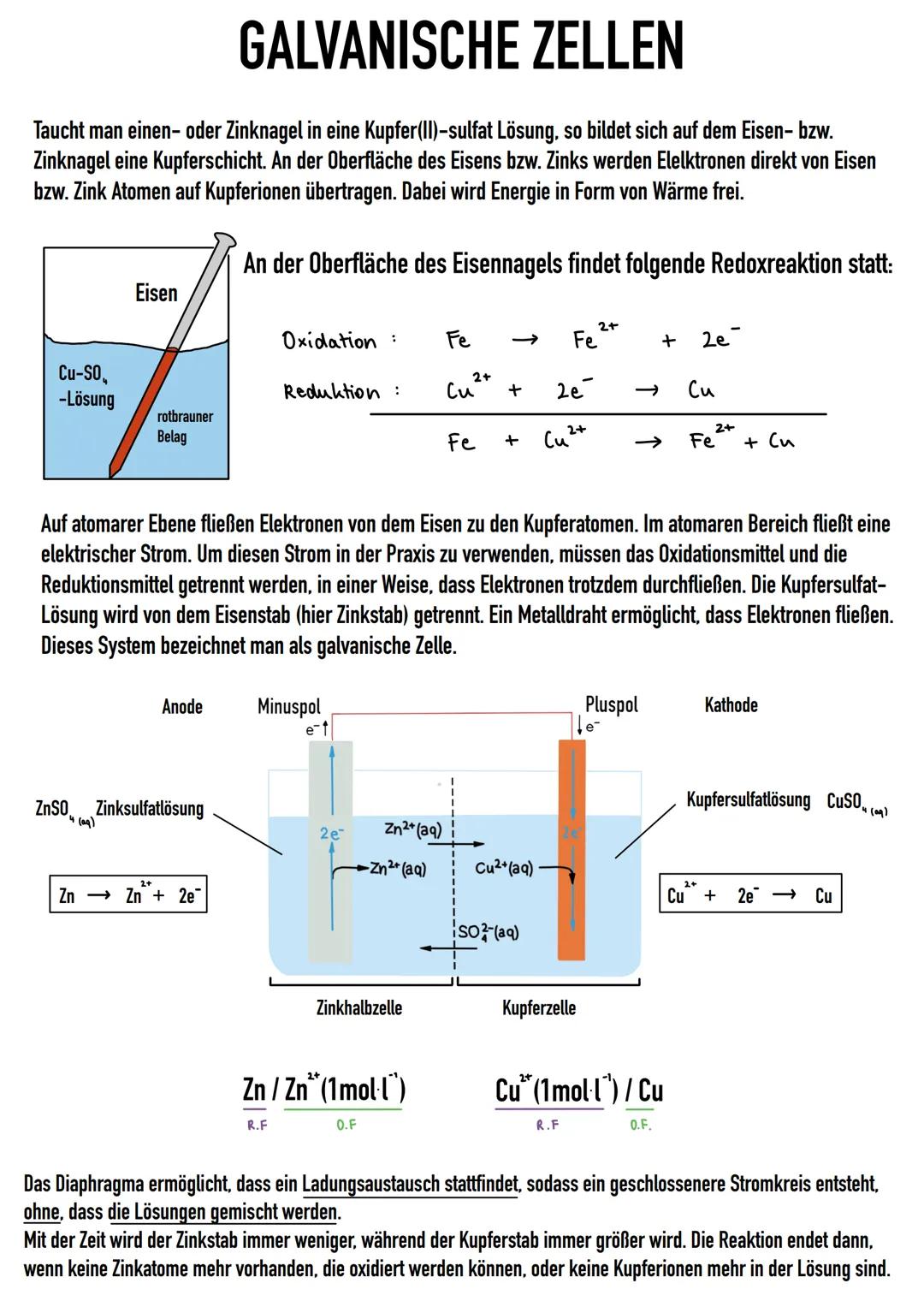
Stell dir vor, du kannst aus einer chemischen Reaktion direkt Strom erzeugen - genau das passiert in galvanischen Zellen! Wenn du einen Eisennagel in Kupfersulfat-Lösung tauchst, fließen Elektronen vom Eisen zu den Kupfer-Ionen.
In einer galvanischen Zelle trennst du die beiden Reaktionspartner räumlich voneinander. Die Zinkhalbzelle (wo die Oxidation stattfindet) ist die Anode und der Minuspol. Die Kupferhalbzelle (wo die Reduktion abläuft) ist die Kathode und der Pluspol.
Das Diaphragma zwischen den Halbzellen ist entscheidend - es lässt Ionen durch, verhindert aber das Vermischen der Lösungen. So entsteht ein geschlossener Stromkreis, während die Reaktion kontrolliert abläuft. Mit der Zeit wird der Zinkstab kleiner und der Kupferstab größer.
Anwendung: Deine Handy-Batterie funktioniert nach dem gleichen Prinzip - nur mit anderen Materialien!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Spannung in galvanischen Zellen entsteht durch unterschiedliche Elektrodenpotentiale der Metalle. Jedes Metall hat eine charakteristische Neigung, Ionen zu bilden - die sogenannte Lösungstension.
Unedle Metalle wie Zink geben leicht Elektronen ab und werden zur Anode (negativer Pol). Edle Metalle wie Silber nehmen lieber Elektronen auf und werden zur Kathode (positiver Pol). Die elektrochemische Doppelschicht an der Metalloberfläche erklärt, warum sich überhaupt ein Potential aufbaut.
Der Elektronenfluss geht immer vom Metall mit höherem Elektronendruck (negativeres Potential) zum Metall mit niedrigerem Elektronendruck (positiveres Potential). Deshalb fließt der Strom von der Zink- zur Kupferelektrode.
Merkregel: Unedel gibt ab, edel nimmt auf - wie beim Geben und Nehmen im echten Leben!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Mit der elektrochemischen Spannungsreihe kannst du vorhersagen, welche Spannung eine galvanische Zelle liefert! Die Einzelpotentiale lassen sich nicht messen, aber ihre Differenz schon.
Die Standard-Wasserstoffelektrode dient als Bezugspunkt mit 0,00 V. Alle anderen Standardelektrodenpotentiale werden gegen diese gemessen. Zink hat -0,76 V, Kupfer +0,34 V und Silber +0,80 V.
Die Formel U = U₀(Kathode) - U₀(Anode) gibt dir direkt die Spannung. Für eine Zink-Kupfer-Zelle rechnest du: 0,34 V - = 1,10 V. Je größer der Unterschied der Potentiale, desto höher die Spannung!
Prüfungstipp: Lerne die wichtigsten Standardpotentiale auswendig - sie kommen in fast jeder Klausur vor!
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
35
Smart Tools NEU
Verwandle diesen Lernzettel in: ✓ 50+ Übungsfragen ✓ Interaktive Karteikarten ✓ Komplette Probeklausur ✓ Aufsatzgliederungen
Erfahren Sie alles über Redoxreaktionen, einschließlich der Konzepte von Oxidation und Reduktion, der Entwicklung von Redoxgleichungen und der Durchführung von Redoxtitrationen. Dieser umfassende Überblick behandelt auch den Hochofenprozess zur Eisenherstellung. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Entdecken Sie die grundlegenden Konzepte von Redoxreaktionen, einschließlich der Definitionen von Oxidation, Reduktion und den beteiligten Reaktionspartnern. Diese Zusammenfassung bietet klare Erklärungen zu Elektronendonatoren und -akzeptoren sowie den Mechanismen von Redoxreaktionen. Ideal für Studierende der Chemie.
Detaillierte Anleitung zur Aufstellung komplexer Redoxgleichungen mit Wasserstoffperoxid und Permanganat-Ionen. Erfahren Sie, wie man Redoxpaare identifiziert, Oxidationszahlen ermittelt und den Ladungsausgleich durchführt. Ideal für Chemie-Studierende, die ihre Kenntnisse in Redoxreaktionen vertiefen möchten.
Erfahren Sie, wie man Oxidationszahlen bestimmt und Redoxreaktionen aufstellt. Diese Zusammenfassung behandelt die Schritte zur Zuordnung von Oxidationszahlen, die Berechnung von Teil- und Gesamtgleichungen sowie die Konzepte von Oxidation und Reduktion. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Entdecken Sie die verschiedenen Arten der Elektronenpaarbindung: Einfach-, Doppel- und Dreifachbindungen. Diese Zusammenfassung erklärt, wie Atome durch gemeinsame Elektronenpaare stabile Zustände erreichen und bietet Beispiele für Chlor-, Sauerstoff- und Stickstoffmoleküle. Ideal für Chemie-Studierende, die die Grundlagen der chemischen Bindungen verstehen möchten.
Erfahren Sie alles über Redoxreaktionen, einschließlich Oxidation, Reduktion und das Ponator-Akzeptor-Prinzip. Diese Zusammenfassung behandelt die Bestimmung von Oxidationszahlen, Teilgleichungen und die Rolle von Elektronendonatoren und -akzeptoren. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer