Redoxreaktionen sind chemische Prozesse, bei denen Elektronen zwischen Stoffen übertragen... Mehr anzeigen
Redoxreaktionen einfach erklärt - Chemie LK/GK Übersicht








Grundlagen der Redoxreaktionen
Redoxreaktionen sind Elektronenübertragungsreaktionen, bei denen ein Teilnehmer Elektronen abgibt (Oxidation) und ein anderer sie aufnimmt (Reduktion). Das Oxidationsmittel nimmt Elektronen auf und wird selbst reduziert, während das Reduktionsmittel Elektronen abgibt und selbst oxidiert wird.
Die Oxidationszahlen helfen uns, Redoxreaktionen zu verfolgen. Bei einer Oxidation erhöht sich die Oxidationszahl, bei einer Reduktion verringert sie sich. Typische Oxidationszahlen sind: Wasserstoff +I , Sauerstoff -II, Metalle positiv und Elemente im reinen Zustand 0.
💡 Beim Aufstellen von Redoxgleichungen hilft dir die "EELA"-Methode: Erst Elektronenausgleich, dann Ladungsausgleich und schließlich Atombilanz. So kannst du auch komplexe Reaktionen korrekt darstellen.
Zum Aufstellen einer vollständigen Redoxgleichung stellst du zuerst die Teilgleichungen für Oxidation und Reduktion auf, bestimmst die Anzahl der übertragenen Elektronen, gleicht die Ladungen aus (in saurer oder basischer Lösung) und verbindest schließlich beide Teilgleichungen zur Gesamtgleichung.
Die Redoxreihe der Metalle
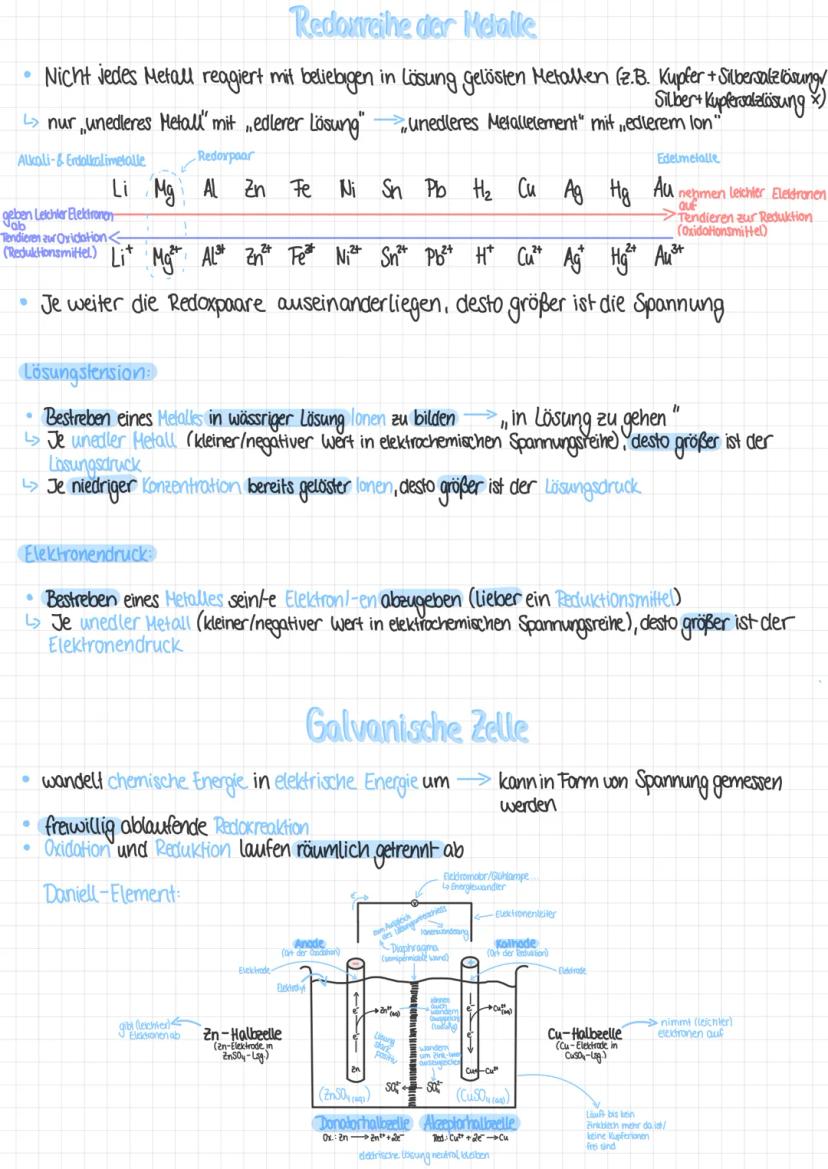
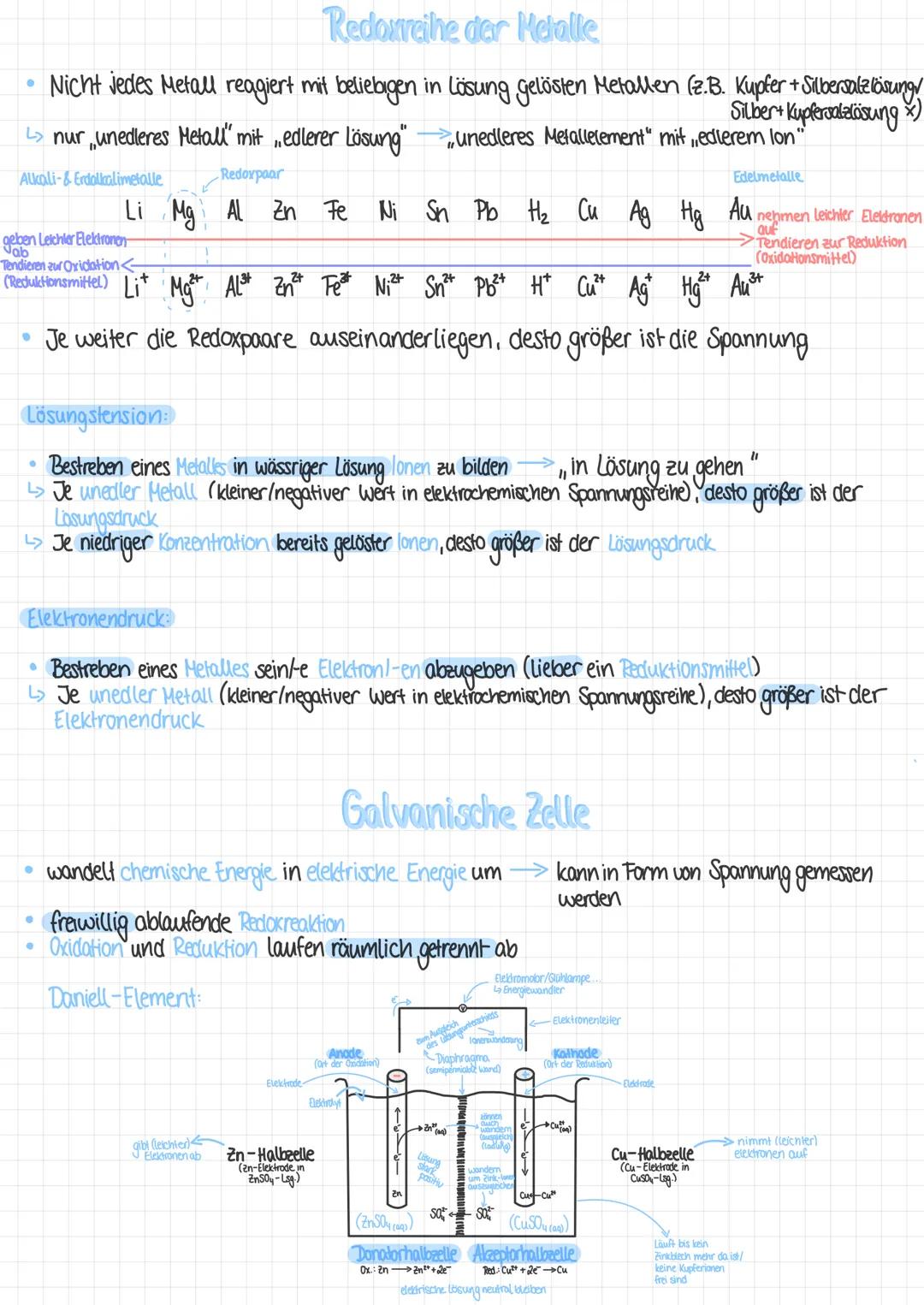
Nicht jedes Metall reagiert mit jedem Metallion. Es gilt die Regel: Ein unedleres Metall kann nur mit Ionen eines edleren Metalls reagieren. Diese Eigenschaft wird in der Redoxreihe abgebildet, die von unedlen Metallen wie Lithium bis zu edlen Metallen wie Gold reicht.
Die Position in der Redoxreihe bestimmt wichtige Eigenschaften: Je unedler ein Metall ist, desto größer ist sein Lösungsdruck (Bestreben, in wässrigen Lösungen Ionen zu bilden) und sein Elektronendruck (Bestreben, Elektronen abzugeben). Je weiter zwei Redoxpaare in der Reihe auseinanderliegen, desto größer ist die entstehende elektrische Spannung.
🔋 Das Daniell-Element ist ein perfektes Beispiel für eine galvanische Zelle: Hier wandelt die Reaktion zwischen unedlem Zink und edlerem Kupfer chemische Energie direkt in elektrische Energie um!
Eine galvanische Zelle wie das Daniell-Element nutzt diese Spannungsunterschiede: An der Anode (Zink) findet die Oxidation statt, während an der Kathode (Kupfer) die Reduktion erfolgt. Die Elektronen fließen über einen äußeren Stromkreis, während die Ionen durch das Diaphragma wandern, um die Ladungsbilanz auszugleichen.

Galvanische Zellen und Standardpotentiale
In einer galvanischen Zelle findet der Elektronenübergang an der Oberfläche des unedleren Metalls statt. Die Zelle besteht aus zwei Halbzellen, die durch ein Diaphragma getrennt sind. Im Zelldiagramm schreibt man: Elektrode 1 | Kation 1 || Kation 2 | Elektrode 2.
Um Potentiale verschiedener Halbzellen vergleichen zu können, wurde die Standardwasserstoffhalbzelle als Bezugssystem eingeführt. Sie besteht aus einer platinierten Platinelektrode, die von Wasserstoff unter 1013 mbar umspült wird, in einer Lösung mit pH = 0 bei 25°C. Ihr Potential wird als 0 Volt festgelegt.
⚡ Die Standardbedingungen sind wichtig, denn die Spannung einer galvanischen Zelle hängt von mehreren Faktoren ab: dem Elektrodenmaterial, den Elektrolytlösungen, deren Konzentrationen und der Temperatur!
Das Standardpotential einer Halbzelle ist die Spannung zwischen dieser Halbzelle unter Standardbedingungen und der Standard-Wasserstoff-Halbzelle. Dieses Potential wird in Volt angegeben und mit dem Symbol E° gekennzeichnet. Es bildet die Grundlage für die elektrochemische Spannungsreihe.

Die elektrochemische Spannungsreihe
Die elektrochemische Spannungsreihe ordnet Halbelemente nach ihren Standardpotentialen an. Das Vorzeichen verrät uns, ob ein Halbelement gegenüber der Standard-Wasserstoff-Halbzelle den Minus- oder Pluspol darstellt. Diese Spannungsreihe ist mit der Redoxreihe identisch.
Je negativer das Standardelektrodenpotential ist, desto stärker ist das Reduktionsmittel – es gibt also leichter Elektronen ab. Je positiver das Potential, desto stärker ist das Oxidationsmittel – es nimmt also leichter Elektronen auf.
🔑 Die Spannung einer galvanischen Zelle berechnet sich einfach durch Subtraktion: Uzelle = E°(Akzeptorzelle) - E°(Donatorhalbzelle). Diese Formel brauchst du für alle Berechnungen!
Die Berechnung der Zellspannung funktioniert durch Subtraktion der Standardpotentiale. Beim Daniell-Element beträgt die Spannung beispielsweise 1,1 V, berechnet aus dem Potential der Kupferzelle (0,337 V) minus dem Potential der Zinkzelle . Kationen sind übrigens positiv geladene Ionen, Anionen negativ geladene Ionen – diese Teilchen werden bei Redoxreaktionen übertragen.
Konzentrationszellen
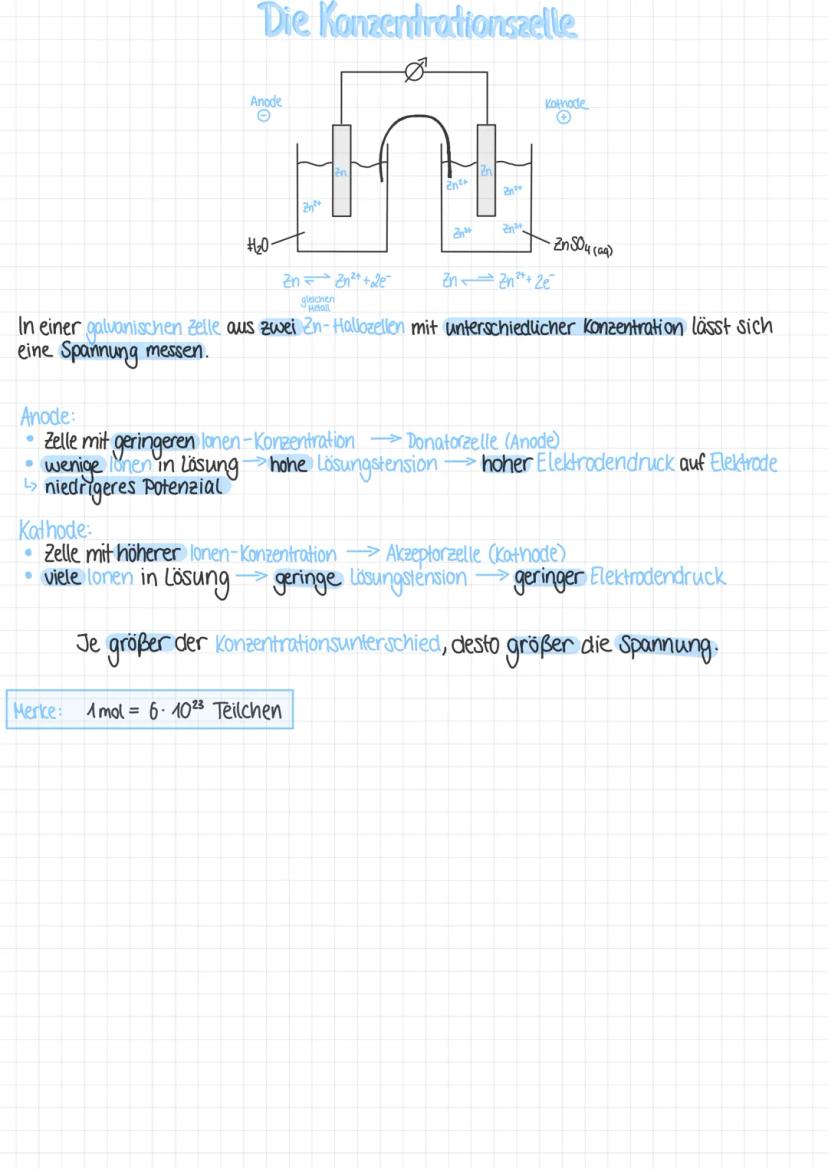
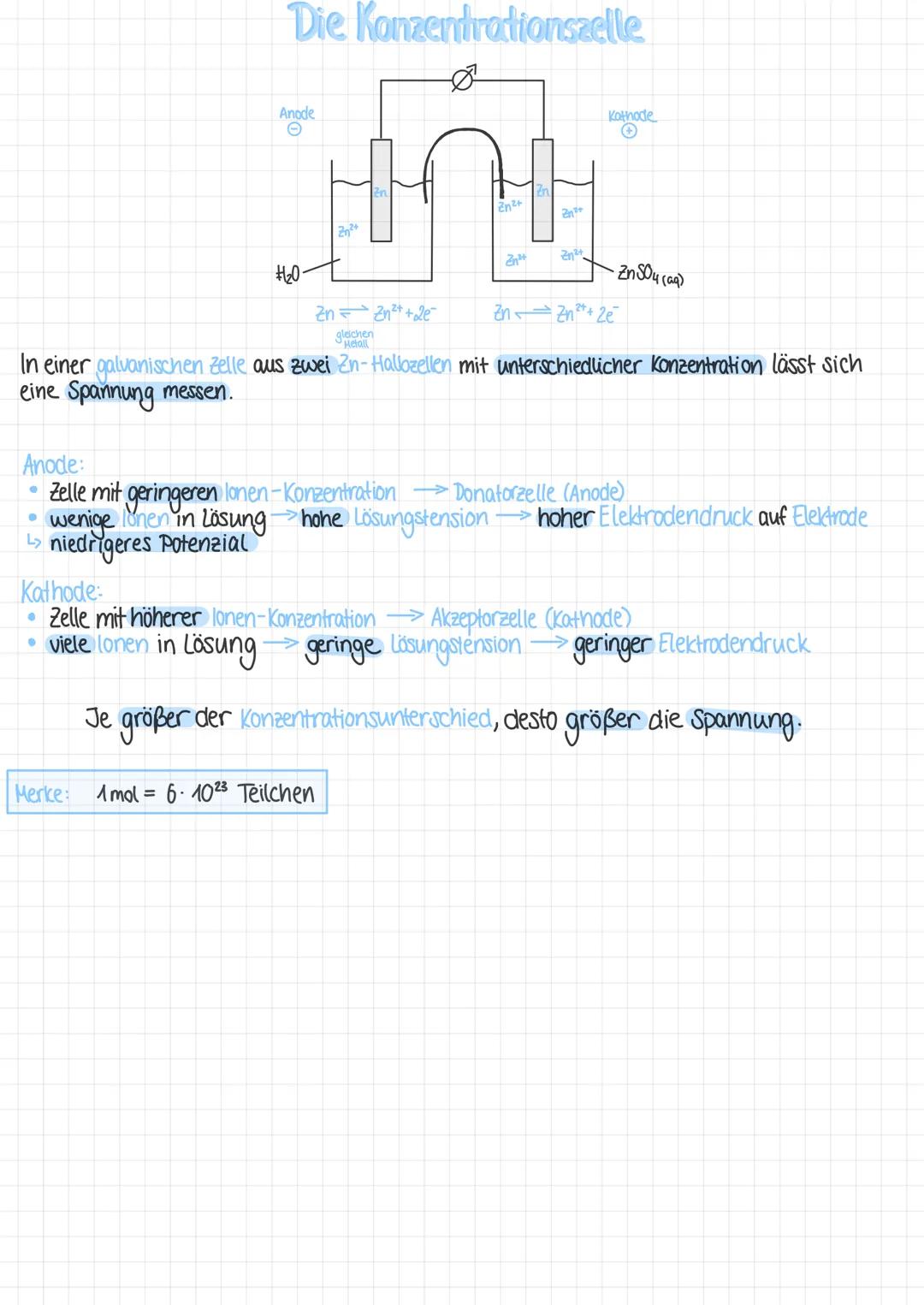
Eine Konzentrationszelle besteht aus zwei identischen Halbzellen mit unterschiedlichen Ionenkonzentrationen. Obwohl beide Elektroden aus demselben Metall bestehen (z.B. Zink), entsteht eine messbare Spannung aufgrund des Konzentrationsunterschieds.
Die Halbzelle mit der geringeren Ionenkonzentration wird zur Anode (Donatorzelle). Hier ist die Lösungstension hoch und der Elektrodendruck stark, was zu einem niedrigeren Potential führt. Die Halbzelle mit der höheren Ionenkonzentration wird zur Kathode (Akzeptorzelle) mit geringerem Lösungsdruck und Elektrodendruck.
📊 Eine wichtige Faustregel: Je größer der Konzentrationsunterschied zwischen den Halbzellen, desto größer die messbare Spannung!
Der Unterschied in der Ionenkonzentration führt zu einem Spannungsunterschied zwischen den Halbzellen. Die Elektronen fließen vom niedrigeren zum höheren Potential – also von der Halbzelle mit der niedrigeren zur Halbzelle mit der höheren Konzentration. Zur Erinnerung: Ein Mol eines Stoffes entspricht 6 · 10²³ Teilchen.

Die Nernstsche Gleichung
Die Nernstsche Gleichung beschreibt den Zusammenhang zwischen der Ionenkonzentration und dem Elektrodenpotential einer Halbzelle. Sie erklärt also, wie sich das Potential ändert, wenn wir von Standardbedingungen abweichen.
Die allgemeine Form lautet: E(Ox|Red) = E°(Ox|Red) + · lg. Hierbei ist E° das Standardpotential, z die Anzahl der übertragenen Elektronen und [Ox] bzw. [Red] stehen für die Konzentrationen der oxidierten und reduzierten Form.
🧪 Der pH-Wert kann die Zellspannung erheblich beeinflussen, da die H3O⁺-Konzentration direkt ins Elektrodenpotential eingeht. Diese Abhängigkeit ist besonders bei biochemischen Prozessen wichtig!
Feste Stoffe haben praktisch konstante Konzentrationen und gehen mit dem Wert 1 in die Gleichung ein. Der pH-Wert einer Lösung ist definiert als negativ dekadischer Logarithmus der H⁺-Ionenkonzentration: pH = -log₁₀(c(H⁺)). Bei pH = 0 ist c(H⁺) = 1, während bei neutralem pH = 7 die H⁺-Konzentration 10⁻⁷ mol/l beträgt.
Elektrolyse
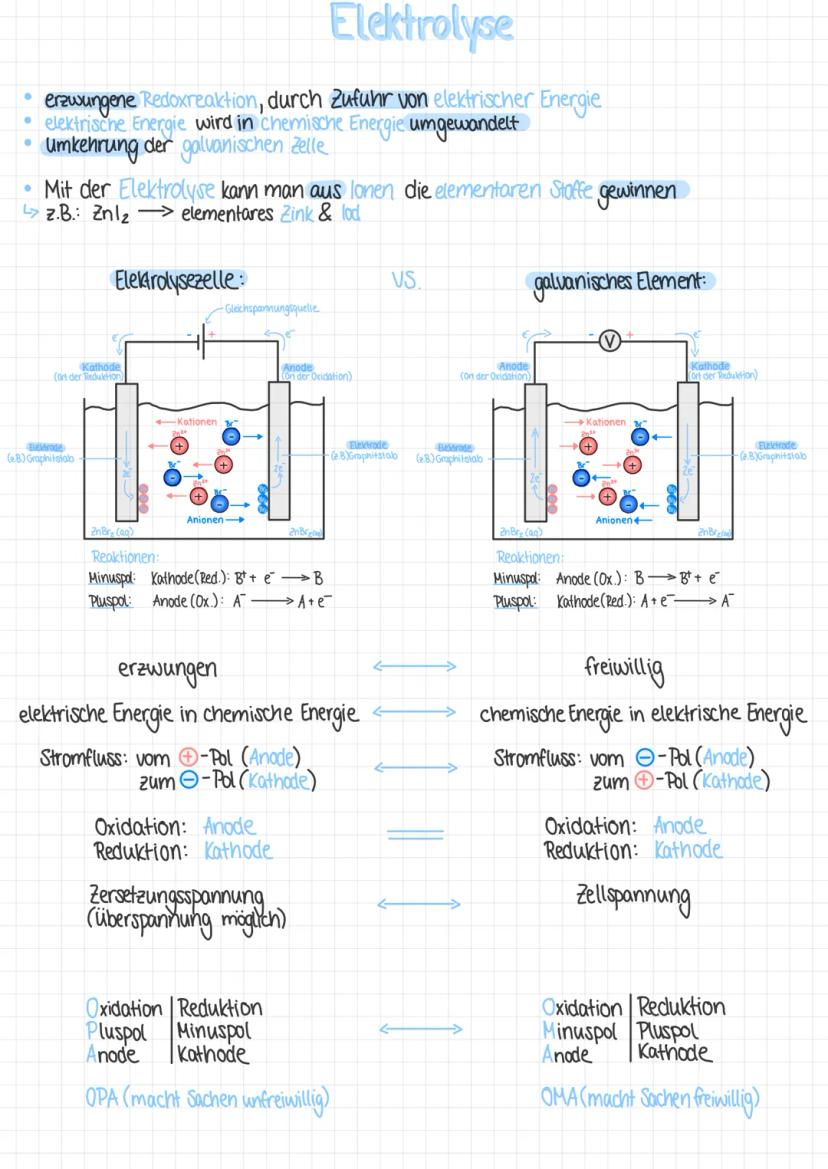
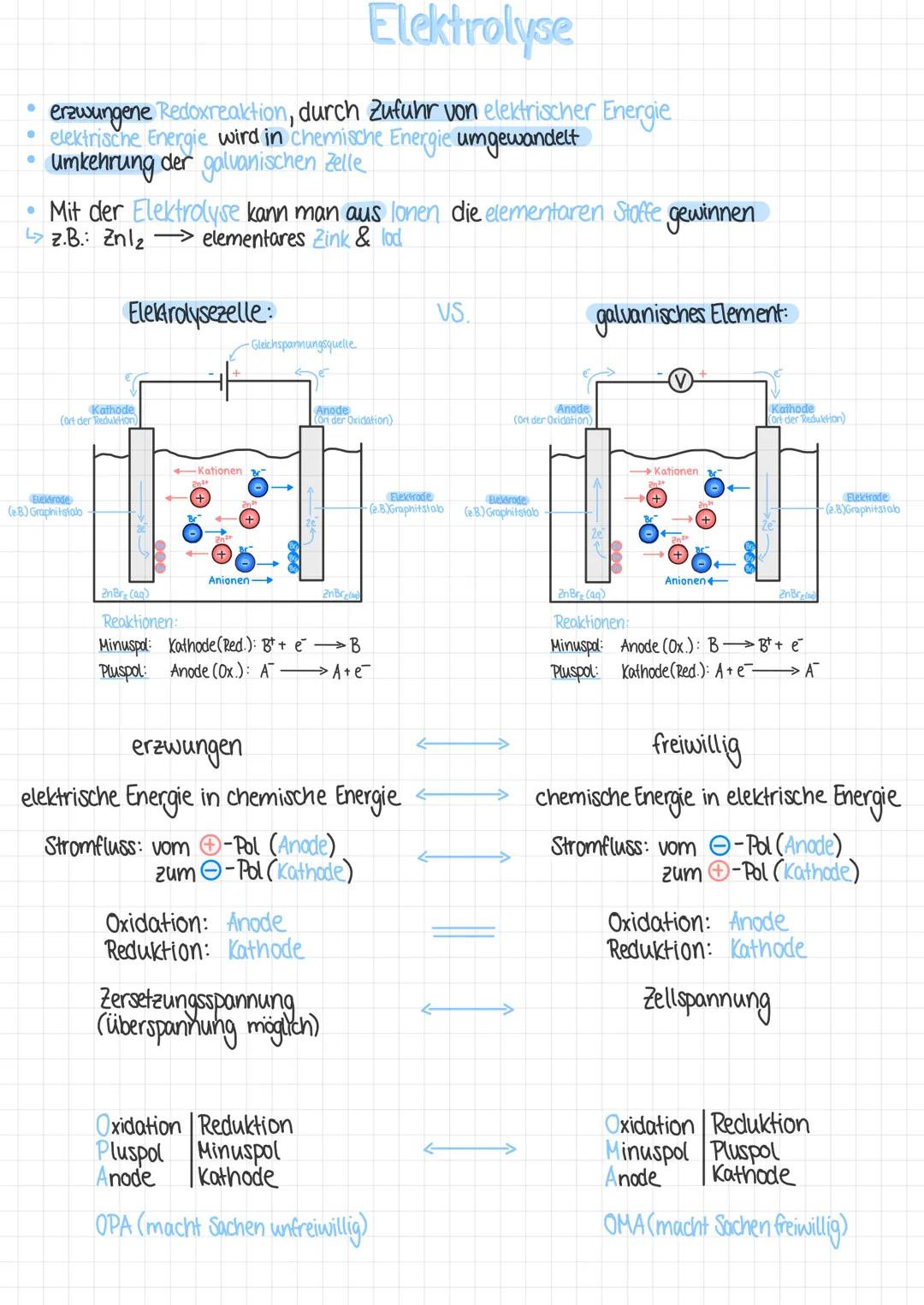
Die Elektrolyse ist eine erzwungene Redoxreaktion durch Zufuhr elektrischer Energie – quasi die Umkehrung der galvanischen Zelle. Dabei wird elektrische Energie in chemische Energie umgewandelt, um aus Ionen elementare Stoffe zu gewinnen, z.B. Zink und Iod aus Zinkiodid.
Bei der Elektrolyse ist die Anode der Pluspol und Ort der Oxidation, während die Kathode der Minuspol und Ort der Reduktion ist. Der Stromfluss geht vom Minuspol zum Pluspol, aber Elektronen fließen in die entgegengesetzte Richtung.
💡 Merke dir die Eselsbrücke: "OPA macht Sachen unfreiwillig" (Oxidation, Pluspol, Anode bei Elektrolyse) und "OMA macht Sachen freiwillig" (Oxidation, Minuspol, Anode bei galvanischen Zellen)!
Im Gegensatz zur galvanischen Zelle benötigt die Elektrolyse eine externe Stromquelle. Hier eine Gegenüberstellung:
- Galvanische Zelle: freiwillige Reaktion, chemische Energie → elektrische Energie
- Elektrolyse: erzwungene Reaktion, elektrische Energie → chemische Energie
Bei beiden fließt der Strom von der Anode zur Kathode, und die Oxidation findet an der Anode statt, während die Reduktion an der Kathode erfolgt.

Zersetzungsspannung und Überspannung
Die Zersetzungsspannung ist die Mindestspannung, die für eine Elektrolyse angelegt werden muss. Sie berechnet sich als Uz = E(Anode) - E(Kathode) und setzt sich aus den Abscheidungspotenzialen der Reaktionen am Plus- und Minuspol zusammen.
Bei konkurrierenden Reaktionen gilt: An der Anode wird der Stoff mit dem kleinsten Elektrodenpotential abgeschieden, an der Kathode der Stoff mit dem größten Potential. Dies hilft uns vorherzusagen, welche Reaktionen bei einer Elektrolyse tatsächlich ablaufen werden.
⚡ Die Überspannung ist wie ein zusätzlicher Energiebedarf, besonders bei der Abscheidung von Gasen. Sie hängt vom Elektrodenmaterial, dem abzuscheidenden Stoff und der Stromdichte ab!
Die Überspannung ist eine zusätzliche Spannung, die man benötigt, um eine Elektrolyse tatsächlich ablaufen zu lassen. Sie tritt besonders bei der Abscheidung von Gasen wie H₂, O₂ oder Cl₂ auf und hängt vom Elektrodenmaterial, dem abzuscheidenden Stoff und der Stromdichte ab. Die Gesamtspannung berechnet sich als: U = (EAnode + UAnode) - (EKathode + UKathode).

Faraday-Gesetze und Brennstoffzellen
Die Faraday-Gesetze erlauben uns, bei Elektrolysen die fließende Ladung und die abgeschiedenen Stoffmengen zu berechnen. Das erste Faraday-Gesetz besagt, dass die abgeschiedene Stoffmenge proportional zur geflossenen Ladungsmenge ist (n ~ Q).
In moderner Form lautet das Faraday-Gesetz: Q = I · t = n · z · F, wobei I die Stromstärke, t die Zeit, n die Stoffmenge, z die Anzahl der übertragenen Elektronen und F die Faraday-Konstante ist. Daraus lässt sich die Stoffmenge als n = Q/(z·F) berechnen.
🔋 Brennstoffzellen sind die Zukunftstechnologie für umweltfreundliche Energieerzeugung! Die Wasserstoff-Sauerstoff-Brennstoffzelle produziert nur Wasser als "Abfallprodukt".
Brennstoffzellen sind galvanische Elemente, bei denen Reduktionsmittel (Brennstoff) und Oxidationsmittel kontinuierlich zugeführt werden. Ein Beispiel ist die Wasserstoff-Sauerstoff-Brennstoffzelle, die mit katalytisch aktiven Elektroden (meist Platin) und einer protonendurchlässigen Elektrolytmembran arbeitet. An der Anode wird Wasserstoff oxidiert , während an der Kathode Sauerstoff reduziert wird .

Korrosion
Korrosion ist die Zersetzung von Metallen durch oxidative Prozesse – ein unerwünschter Redoxvorgang. Der bekannteste Fall ist das Rosten von Eisen. Korrosion entsteht oft als Lokalelement, wenn zwei verschiedene Metalle sich berühren und von einer Elektrolytlösung umgeben sind.
Es gibt verschiedene Korrosionstypen: Bei der Sauerstoffkorrosion wird das Metall durch Sauerstoff in leicht alkalischer Umgebung zersetzt . Bei der Säurekorrosion erfolgt die Zersetzung durch H₃O⁺-Ionen in saurer Umgebung .
🛡️ Beim Rosten von Eisen entsteht zunächst Eisen(II), das dann zu Eisen(III) oxidiert wird. Die Fällungsreaktion mit Hydroxidionen bildet schließlich den bekannten rotbraunen Rost (Fe(OH)₃).
Der passive Korrosionsschutz trennt Reaktionspartner räumlich durch eine nicht-reaktive Schutzschicht (z.B. durch Galvanisieren mit edlerem Metall oder Lackieren). Problematisch: Wenn der Überzug mit edlerem Metall Fehlstellen aufweist, beschleunigt sich die Korrosion sogar, da ein Lokalelement entsteht, bei dem das ungeschützte Grundmetall als Anode fungiert.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: galvanische Zelle
9Galvanische Zelle: Grundlagen
Erfahren Sie alles über die galvanische Zelle, einschließlich der Funktionsweise von Anode und Kathode, Zellendiagrammen und der Berechnung der Zellspannung unter Standardbedingungen. Diese Zusammenfassung behandelt wichtige Konzepte wie das Daniell-Element und die Redoxreaktionen. Ideal für Studierende der Chemie.
Galvanische Zellen und Batterien
Erfahren Sie alles über galvanische Zellen, deren Aufbau, Funktionsweise und die zugrunde liegenden Redoxreaktionen. Diese Zusammenfassung behandelt auch die Wasserstoff-Halbzelle und verschiedene Batterietypen, einschließlich der Daniell-Zelle. Ideal für Chemie GK Schüler in Baden-Württemberg, die sich auf das Abitur vorbereiten.
Elektrolyse vs. Galvanische Zellen
Erforschen Sie die Unterschiede zwischen Elektrolyse und galvanischen Zellen. Diese Zusammenfassung behandelt die Redoxreaktionen, den Aufbau einer galvanischen Zelle mit Zink- und Bromhalbzellen, die Reaktionsgleichungen an den Elektroden sowie den Vergleich der beiden Systeme. Ideal für Studierende der Chemie, die ein tiefes Verständnis für elektrochemische Prozesse entwickeln möchten.
Daniell-Zelle und Redoxreaktionen
Diese Zusammenfassung behandelt die Struktur und Funktionsweise der Daniell-Zelle, einschließlich der Teilreaktionen von Oxidation und Reduktion. Sie erklärt die Herstellung von Kupfersulfat aus Kupferoxid und Schwefelsäure, die Veränderungen der Elektroden während des Betriebs sowie die Bedeutung des Diaphragmas für den Ionenfluss. Ideal für Chemie LK Schüler zur Vorbereitung auf Klausuren.
Galvanische Zelle verstehen
Entdecken Sie die Funktionsweise der galvanischen Zelle und die zugrunde liegenden Redoxreaktionen. Diese Zusammenfassung behandelt die Struktur, die Rolle von Anode und Kathode, sowie die Bedeutung des Diaphragmas. Ideal für Studierende der Chemie, die sich mit elektrochemischen Zellen und dem Daniell-Element vertraut machen möchten.
Daniell-Element: Galvanische Zelle
Erforschen Sie den Aufbau und die Funktionsweise der galvanischen Zelle, insbesondere des Daniell-Elements. Diese Zusammenfassung behandelt die Redoxreaktionen, die Rolle von Zink und Kupfer, sowie die Bedeutung der Salzbrücke für den Elektronenfluss. Ideal für Studierende der Chemie, die sich mit elektrochemischen Zellen und Batterietechnologien beschäftigen.
Galvanische Zellen & Bleiakkumulator
Entdecken Sie die Grundlagen der galvanischen Zellen und des Bleiakkumulators in dieser umfassenden Zusammenfassung. Erfahren Sie mehr über das Standardelektrodenpotential, Redoxreaktionen und die Funktionsweise von Primär- und Sekundärzellen. Ideal für Chemie-Klausuren und das Verständnis elektrochemischer Prozesse.
Redoxchemie Grundlagen
Entdecken Sie die Grundlagen der Redoxchemie, einschließlich Oxidationszahlen, galvanischen Zellen, Elektrolyse, Redoxpotential und Faradays Gesetz. Diese Zusammenfassung bietet einen klaren Überblick über wichtige Konzepte wie Oxidation, Reduktion, Überspannung und Korrosion, ideal für Studierende der Chemie.
Elektrochemische Zellen
Entdecken Sie die Grundlagen der elektrochemischen Zellen, einschließlich galvanischer Zellen, Elektrolyse und Batterietechnologien. Erfahren Sie mehr über Redoxreaktionen, Zellpotentiale, das Daniell-Element und verschiedene Batterietypen wie Zink-Kohle-Batterien. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Redoxreaktionen einfach erklärt - Chemie LK/GK Übersicht
Redoxreaktionen sind chemische Prozesse, bei denen Elektronen zwischen Stoffen übertragen werden. Dieses Konzept ist grundlegend für viele Vorgänge in der Chemie - von Batterien über Metallgewinnung bis hin zur Korrosion. Die folgenden Zusammenfassungen erklären die wichtigsten Aspekte dieses spannenden Themas.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Grundlagen der Redoxreaktionen
Redoxreaktionen sind Elektronenübertragungsreaktionen, bei denen ein Teilnehmer Elektronen abgibt (Oxidation) und ein anderer sie aufnimmt (Reduktion). Das Oxidationsmittel nimmt Elektronen auf und wird selbst reduziert, während das Reduktionsmittel Elektronen abgibt und selbst oxidiert wird.
Die Oxidationszahlen helfen uns, Redoxreaktionen zu verfolgen. Bei einer Oxidation erhöht sich die Oxidationszahl, bei einer Reduktion verringert sie sich. Typische Oxidationszahlen sind: Wasserstoff +I , Sauerstoff -II, Metalle positiv und Elemente im reinen Zustand 0.
💡 Beim Aufstellen von Redoxgleichungen hilft dir die "EELA"-Methode: Erst Elektronenausgleich, dann Ladungsausgleich und schließlich Atombilanz. So kannst du auch komplexe Reaktionen korrekt darstellen.
Zum Aufstellen einer vollständigen Redoxgleichung stellst du zuerst die Teilgleichungen für Oxidation und Reduktion auf, bestimmst die Anzahl der übertragenen Elektronen, gleicht die Ladungen aus (in saurer oder basischer Lösung) und verbindest schließlich beide Teilgleichungen zur Gesamtgleichung.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Die Redoxreihe der Metalle
Nicht jedes Metall reagiert mit jedem Metallion. Es gilt die Regel: Ein unedleres Metall kann nur mit Ionen eines edleren Metalls reagieren. Diese Eigenschaft wird in der Redoxreihe abgebildet, die von unedlen Metallen wie Lithium bis zu edlen Metallen wie Gold reicht.
Die Position in der Redoxreihe bestimmt wichtige Eigenschaften: Je unedler ein Metall ist, desto größer ist sein Lösungsdruck (Bestreben, in wässrigen Lösungen Ionen zu bilden) und sein Elektronendruck (Bestreben, Elektronen abzugeben). Je weiter zwei Redoxpaare in der Reihe auseinanderliegen, desto größer ist die entstehende elektrische Spannung.
🔋 Das Daniell-Element ist ein perfektes Beispiel für eine galvanische Zelle: Hier wandelt die Reaktion zwischen unedlem Zink und edlerem Kupfer chemische Energie direkt in elektrische Energie um!
Eine galvanische Zelle wie das Daniell-Element nutzt diese Spannungsunterschiede: An der Anode (Zink) findet die Oxidation statt, während an der Kathode (Kupfer) die Reduktion erfolgt. Die Elektronen fließen über einen äußeren Stromkreis, während die Ionen durch das Diaphragma wandern, um die Ladungsbilanz auszugleichen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Galvanische Zellen und Standardpotentiale
In einer galvanischen Zelle findet der Elektronenübergang an der Oberfläche des unedleren Metalls statt. Die Zelle besteht aus zwei Halbzellen, die durch ein Diaphragma getrennt sind. Im Zelldiagramm schreibt man: Elektrode 1 | Kation 1 || Kation 2 | Elektrode 2.
Um Potentiale verschiedener Halbzellen vergleichen zu können, wurde die Standardwasserstoffhalbzelle als Bezugssystem eingeführt. Sie besteht aus einer platinierten Platinelektrode, die von Wasserstoff unter 1013 mbar umspült wird, in einer Lösung mit pH = 0 bei 25°C. Ihr Potential wird als 0 Volt festgelegt.
⚡ Die Standardbedingungen sind wichtig, denn die Spannung einer galvanischen Zelle hängt von mehreren Faktoren ab: dem Elektrodenmaterial, den Elektrolytlösungen, deren Konzentrationen und der Temperatur!
Das Standardpotential einer Halbzelle ist die Spannung zwischen dieser Halbzelle unter Standardbedingungen und der Standard-Wasserstoff-Halbzelle. Dieses Potential wird in Volt angegeben und mit dem Symbol E° gekennzeichnet. Es bildet die Grundlage für die elektrochemische Spannungsreihe.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Die elektrochemische Spannungsreihe
Die elektrochemische Spannungsreihe ordnet Halbelemente nach ihren Standardpotentialen an. Das Vorzeichen verrät uns, ob ein Halbelement gegenüber der Standard-Wasserstoff-Halbzelle den Minus- oder Pluspol darstellt. Diese Spannungsreihe ist mit der Redoxreihe identisch.
Je negativer das Standardelektrodenpotential ist, desto stärker ist das Reduktionsmittel – es gibt also leichter Elektronen ab. Je positiver das Potential, desto stärker ist das Oxidationsmittel – es nimmt also leichter Elektronen auf.
🔑 Die Spannung einer galvanischen Zelle berechnet sich einfach durch Subtraktion: Uzelle = E°(Akzeptorzelle) - E°(Donatorhalbzelle). Diese Formel brauchst du für alle Berechnungen!
Die Berechnung der Zellspannung funktioniert durch Subtraktion der Standardpotentiale. Beim Daniell-Element beträgt die Spannung beispielsweise 1,1 V, berechnet aus dem Potential der Kupferzelle (0,337 V) minus dem Potential der Zinkzelle . Kationen sind übrigens positiv geladene Ionen, Anionen negativ geladene Ionen – diese Teilchen werden bei Redoxreaktionen übertragen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Konzentrationszellen
Eine Konzentrationszelle besteht aus zwei identischen Halbzellen mit unterschiedlichen Ionenkonzentrationen. Obwohl beide Elektroden aus demselben Metall bestehen (z.B. Zink), entsteht eine messbare Spannung aufgrund des Konzentrationsunterschieds.
Die Halbzelle mit der geringeren Ionenkonzentration wird zur Anode (Donatorzelle). Hier ist die Lösungstension hoch und der Elektrodendruck stark, was zu einem niedrigeren Potential führt. Die Halbzelle mit der höheren Ionenkonzentration wird zur Kathode (Akzeptorzelle) mit geringerem Lösungsdruck und Elektrodendruck.
📊 Eine wichtige Faustregel: Je größer der Konzentrationsunterschied zwischen den Halbzellen, desto größer die messbare Spannung!
Der Unterschied in der Ionenkonzentration führt zu einem Spannungsunterschied zwischen den Halbzellen. Die Elektronen fließen vom niedrigeren zum höheren Potential – also von der Halbzelle mit der niedrigeren zur Halbzelle mit der höheren Konzentration. Zur Erinnerung: Ein Mol eines Stoffes entspricht 6 · 10²³ Teilchen.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Die Nernstsche Gleichung
Die Nernstsche Gleichung beschreibt den Zusammenhang zwischen der Ionenkonzentration und dem Elektrodenpotential einer Halbzelle. Sie erklärt also, wie sich das Potential ändert, wenn wir von Standardbedingungen abweichen.
Die allgemeine Form lautet: E(Ox|Red) = E°(Ox|Red) + · lg. Hierbei ist E° das Standardpotential, z die Anzahl der übertragenen Elektronen und [Ox] bzw. [Red] stehen für die Konzentrationen der oxidierten und reduzierten Form.
🧪 Der pH-Wert kann die Zellspannung erheblich beeinflussen, da die H3O⁺-Konzentration direkt ins Elektrodenpotential eingeht. Diese Abhängigkeit ist besonders bei biochemischen Prozessen wichtig!
Feste Stoffe haben praktisch konstante Konzentrationen und gehen mit dem Wert 1 in die Gleichung ein. Der pH-Wert einer Lösung ist definiert als negativ dekadischer Logarithmus der H⁺-Ionenkonzentration: pH = -log₁₀(c(H⁺)). Bei pH = 0 ist c(H⁺) = 1, während bei neutralem pH = 7 die H⁺-Konzentration 10⁻⁷ mol/l beträgt.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Elektrolyse
Die Elektrolyse ist eine erzwungene Redoxreaktion durch Zufuhr elektrischer Energie – quasi die Umkehrung der galvanischen Zelle. Dabei wird elektrische Energie in chemische Energie umgewandelt, um aus Ionen elementare Stoffe zu gewinnen, z.B. Zink und Iod aus Zinkiodid.
Bei der Elektrolyse ist die Anode der Pluspol und Ort der Oxidation, während die Kathode der Minuspol und Ort der Reduktion ist. Der Stromfluss geht vom Minuspol zum Pluspol, aber Elektronen fließen in die entgegengesetzte Richtung.
💡 Merke dir die Eselsbrücke: "OPA macht Sachen unfreiwillig" (Oxidation, Pluspol, Anode bei Elektrolyse) und "OMA macht Sachen freiwillig" (Oxidation, Minuspol, Anode bei galvanischen Zellen)!
Im Gegensatz zur galvanischen Zelle benötigt die Elektrolyse eine externe Stromquelle. Hier eine Gegenüberstellung:
- Galvanische Zelle: freiwillige Reaktion, chemische Energie → elektrische Energie
- Elektrolyse: erzwungene Reaktion, elektrische Energie → chemische Energie
Bei beiden fließt der Strom von der Anode zur Kathode, und die Oxidation findet an der Anode statt, während die Reduktion an der Kathode erfolgt.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Zersetzungsspannung und Überspannung
Die Zersetzungsspannung ist die Mindestspannung, die für eine Elektrolyse angelegt werden muss. Sie berechnet sich als Uz = E(Anode) - E(Kathode) und setzt sich aus den Abscheidungspotenzialen der Reaktionen am Plus- und Minuspol zusammen.
Bei konkurrierenden Reaktionen gilt: An der Anode wird der Stoff mit dem kleinsten Elektrodenpotential abgeschieden, an der Kathode der Stoff mit dem größten Potential. Dies hilft uns vorherzusagen, welche Reaktionen bei einer Elektrolyse tatsächlich ablaufen werden.
⚡ Die Überspannung ist wie ein zusätzlicher Energiebedarf, besonders bei der Abscheidung von Gasen. Sie hängt vom Elektrodenmaterial, dem abzuscheidenden Stoff und der Stromdichte ab!
Die Überspannung ist eine zusätzliche Spannung, die man benötigt, um eine Elektrolyse tatsächlich ablaufen zu lassen. Sie tritt besonders bei der Abscheidung von Gasen wie H₂, O₂ oder Cl₂ auf und hängt vom Elektrodenmaterial, dem abzuscheidenden Stoff und der Stromdichte ab. Die Gesamtspannung berechnet sich als: U = (EAnode + UAnode) - (EKathode + UKathode).

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Faraday-Gesetze und Brennstoffzellen
Die Faraday-Gesetze erlauben uns, bei Elektrolysen die fließende Ladung und die abgeschiedenen Stoffmengen zu berechnen. Das erste Faraday-Gesetz besagt, dass die abgeschiedene Stoffmenge proportional zur geflossenen Ladungsmenge ist (n ~ Q).
In moderner Form lautet das Faraday-Gesetz: Q = I · t = n · z · F, wobei I die Stromstärke, t die Zeit, n die Stoffmenge, z die Anzahl der übertragenen Elektronen und F die Faraday-Konstante ist. Daraus lässt sich die Stoffmenge als n = Q/(z·F) berechnen.
🔋 Brennstoffzellen sind die Zukunftstechnologie für umweltfreundliche Energieerzeugung! Die Wasserstoff-Sauerstoff-Brennstoffzelle produziert nur Wasser als "Abfallprodukt".
Brennstoffzellen sind galvanische Elemente, bei denen Reduktionsmittel (Brennstoff) und Oxidationsmittel kontinuierlich zugeführt werden. Ein Beispiel ist die Wasserstoff-Sauerstoff-Brennstoffzelle, die mit katalytisch aktiven Elektroden (meist Platin) und einer protonendurchlässigen Elektrolytmembran arbeitet. An der Anode wird Wasserstoff oxidiert , während an der Kathode Sauerstoff reduziert wird .

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Korrosion
Korrosion ist die Zersetzung von Metallen durch oxidative Prozesse – ein unerwünschter Redoxvorgang. Der bekannteste Fall ist das Rosten von Eisen. Korrosion entsteht oft als Lokalelement, wenn zwei verschiedene Metalle sich berühren und von einer Elektrolytlösung umgeben sind.
Es gibt verschiedene Korrosionstypen: Bei der Sauerstoffkorrosion wird das Metall durch Sauerstoff in leicht alkalischer Umgebung zersetzt . Bei der Säurekorrosion erfolgt die Zersetzung durch H₃O⁺-Ionen in saurer Umgebung .
🛡️ Beim Rosten von Eisen entsteht zunächst Eisen(II), das dann zu Eisen(III) oxidiert wird. Die Fällungsreaktion mit Hydroxidionen bildet schließlich den bekannten rotbraunen Rost (Fe(OH)₃).
Der passive Korrosionsschutz trennt Reaktionspartner räumlich durch eine nicht-reaktive Schutzschicht (z.B. durch Galvanisieren mit edlerem Metall oder Lackieren). Problematisch: Wenn der Überzug mit edlerem Metall Fehlstellen aufweist, beschleunigt sich die Korrosion sogar, da ein Lokalelement entsteht, bei dem das ungeschützte Grundmetall als Anode fungiert.
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: galvanische Zelle
9Galvanische Zelle: Grundlagen
Erfahren Sie alles über die galvanische Zelle, einschließlich der Funktionsweise von Anode und Kathode, Zellendiagrammen und der Berechnung der Zellspannung unter Standardbedingungen. Diese Zusammenfassung behandelt wichtige Konzepte wie das Daniell-Element und die Redoxreaktionen. Ideal für Studierende der Chemie.
Galvanische Zellen und Batterien
Erfahren Sie alles über galvanische Zellen, deren Aufbau, Funktionsweise und die zugrunde liegenden Redoxreaktionen. Diese Zusammenfassung behandelt auch die Wasserstoff-Halbzelle und verschiedene Batterietypen, einschließlich der Daniell-Zelle. Ideal für Chemie GK Schüler in Baden-Württemberg, die sich auf das Abitur vorbereiten.
Elektrolyse vs. Galvanische Zellen
Erforschen Sie die Unterschiede zwischen Elektrolyse und galvanischen Zellen. Diese Zusammenfassung behandelt die Redoxreaktionen, den Aufbau einer galvanischen Zelle mit Zink- und Bromhalbzellen, die Reaktionsgleichungen an den Elektroden sowie den Vergleich der beiden Systeme. Ideal für Studierende der Chemie, die ein tiefes Verständnis für elektrochemische Prozesse entwickeln möchten.
Daniell-Zelle und Redoxreaktionen
Diese Zusammenfassung behandelt die Struktur und Funktionsweise der Daniell-Zelle, einschließlich der Teilreaktionen von Oxidation und Reduktion. Sie erklärt die Herstellung von Kupfersulfat aus Kupferoxid und Schwefelsäure, die Veränderungen der Elektroden während des Betriebs sowie die Bedeutung des Diaphragmas für den Ionenfluss. Ideal für Chemie LK Schüler zur Vorbereitung auf Klausuren.
Galvanische Zelle verstehen
Entdecken Sie die Funktionsweise der galvanischen Zelle und die zugrunde liegenden Redoxreaktionen. Diese Zusammenfassung behandelt die Struktur, die Rolle von Anode und Kathode, sowie die Bedeutung des Diaphragmas. Ideal für Studierende der Chemie, die sich mit elektrochemischen Zellen und dem Daniell-Element vertraut machen möchten.
Daniell-Element: Galvanische Zelle
Erforschen Sie den Aufbau und die Funktionsweise der galvanischen Zelle, insbesondere des Daniell-Elements. Diese Zusammenfassung behandelt die Redoxreaktionen, die Rolle von Zink und Kupfer, sowie die Bedeutung der Salzbrücke für den Elektronenfluss. Ideal für Studierende der Chemie, die sich mit elektrochemischen Zellen und Batterietechnologien beschäftigen.
Galvanische Zellen & Bleiakkumulator
Entdecken Sie die Grundlagen der galvanischen Zellen und des Bleiakkumulators in dieser umfassenden Zusammenfassung. Erfahren Sie mehr über das Standardelektrodenpotential, Redoxreaktionen und die Funktionsweise von Primär- und Sekundärzellen. Ideal für Chemie-Klausuren und das Verständnis elektrochemischer Prozesse.
Redoxchemie Grundlagen
Entdecken Sie die Grundlagen der Redoxchemie, einschließlich Oxidationszahlen, galvanischen Zellen, Elektrolyse, Redoxpotential und Faradays Gesetz. Diese Zusammenfassung bietet einen klaren Überblick über wichtige Konzepte wie Oxidation, Reduktion, Überspannung und Korrosion, ideal für Studierende der Chemie.
Elektrochemische Zellen
Entdecken Sie die Grundlagen der elektrochemischen Zellen, einschließlich galvanischer Zellen, Elektrolyse und Batterietechnologien. Erfahren Sie mehr über Redoxreaktionen, Zellpotentiale, das Daniell-Element und verschiedene Batterietypen wie Zink-Kohle-Batterien. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.