Säure-Base-Reaktionen sind grundlegende Vorgänge in der Chemie, bei denen es... Mehr anzeigen
Chemie LK: Säuren, Basen, Puffer und Titration verstehen





Säuren und Basen – Definitionen und Grundlagen
Eine Säure (HA) ist ein Protonendonator – sie gibt Protonen (H⁺) ab. Eine Base (B) funktioniert als Protonenakzeptor und nimmt Protonen auf. Diese Definition geht auf das Brønsted-Konzept zurück.
Bei Säure-Base-Reaktionen bilden sich sogenannte korrespondierende Säure-Base-Paare. Dabei handelt es sich um Teilchenpaare, die sich nur durch ein Proton unterscheiden. Beispiele sind NH₄⁺ & NH₃ oder CH₃COOH & CH₃COO⁻.
Ampholyte sind besonders interessante Teilchen, die je nach Reaktionspartner als Säure oder Base reagieren können. Beispiele dafür sind Wasser (H₂O), Ammoniak (NH₃) oder das Hydrogencarbonat-Ion (HCO₃⁻). Sie können sowohl Protonen aufnehmen als auch abgeben.
💡 Die Autoprotolyse des Wassers ist ein wichtiger Spezialfall, bei dem Wasser gleichzeitig als Säure und Base reagiert. Das Ionenprodukt K𝘸 = c(H₃O⁺)·c(OH⁻) = 10⁻¹⁴ mol²·l⁻² bei 25°C ist eine fundamentale Konstante in der Chemie.

pH- und pOH-Werte
Der pH-Wert gibt an, wie viele H⁺-Ionen bzw. Oxonium-Ionen (H₃O⁺) in einer Lösung vorhanden sind. Eine saure Lösung hat eine hohe Konzentration an H⁺-Ionen, die mit Wasser zu H₃O⁺ reagieren. Der pOH-Wert bezieht sich auf die Konzentration der OH⁻-Ionen in alkalischen Lösungen.
Beide Werte hängen zusammen: pH + pOH = 14. Bei starken Säuren (pKₛ < 4) berechnet man den pH-Wert mit pH = -log(c(HA)). Bei schwachen Säuren (pKₛ > 4) nutzt man die Formel pH = ½. Ähnliche Formeln gelten für den pOH-Wert.
Die Stärke einer Säure oder Base wird durch die Säurekonstante Kₛ bzw. die Basenkonstante K𝘣 ausgedrückt. Je größer der Kₛ-Wert, desto kleiner ist der pKₛ-Wert und desto stärker ist die Säure. Wichtig: Je stärker eine Säure, desto schwächer ist ihre korrespondierende Base.
🧪 Die pH-Skala reicht von 0 bis 14: Starke Säuren liegen zwischen 0-3, Essig etwa bei 3-4, reines Wasser bei 7 (neutral), Seife bei 9-10 und Abflussreiniger im stark basischen Bereich bei 13-14.

Puffersysteme
Pufferlösungen halten den pH-Wert konstant, auch wenn Säuren oder Basen in geringen Mengen zugegeben werden. Sie bestehen aus einer schwachen Säure/Base und ihrer korrespondierenden Base/Säure im Verhältnis von etwa 1:1.
Bei Zugabe von H₃O⁺ reagiert die Pufferbase (A⁻) mit den Oxonium-Ionen: H₃O⁺ + A⁻ → HA + H₂O. Bei Zugabe von OH⁻ reagiert die Puffersäure mit den Hydroxid-Ionen: OH⁻ + HA → A⁻ + H₂O. In beiden Fällen werden die zugeführten Ionen abgefangen und der pH-Wert bleibt nahezu konstant.
Für die Berechnung des pH-Werts einer Pufferlösung verwendet man die Henderson-Hasselbalch-Gleichung: pH = pKₛ(HA) + log. Diese Formel ermöglicht es auch, das Konzentrationsverhältnis der Pufferkomponenten für einen gewünschten pH-Wert zu berechnen.
🔬 Wichtige Puffersysteme sind der Acetatpuffer , der Hydrogencarbonatpuffer , der Phosphatpuffer und der Ammoniakpuffer . Der Phosphatpuffer spielt eine entscheidende Rolle in unserem Blut!
Indikatoren und ihre Anwendung
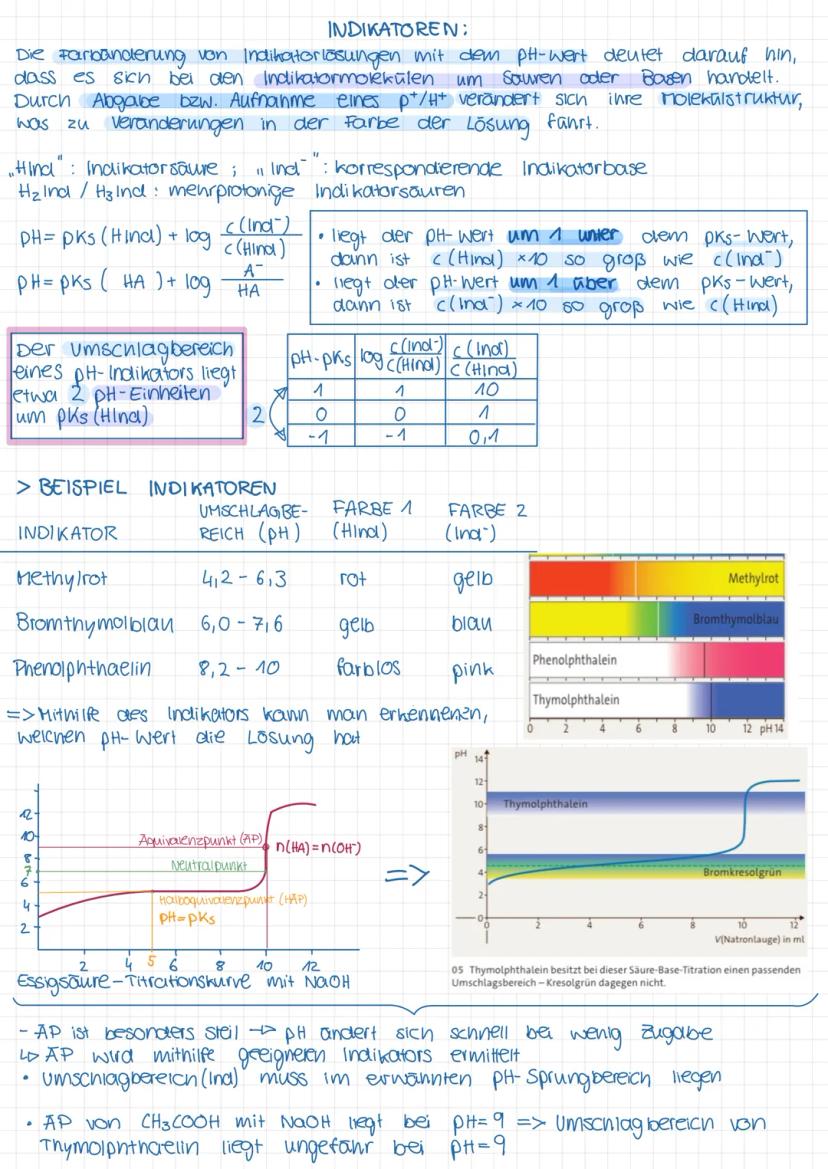
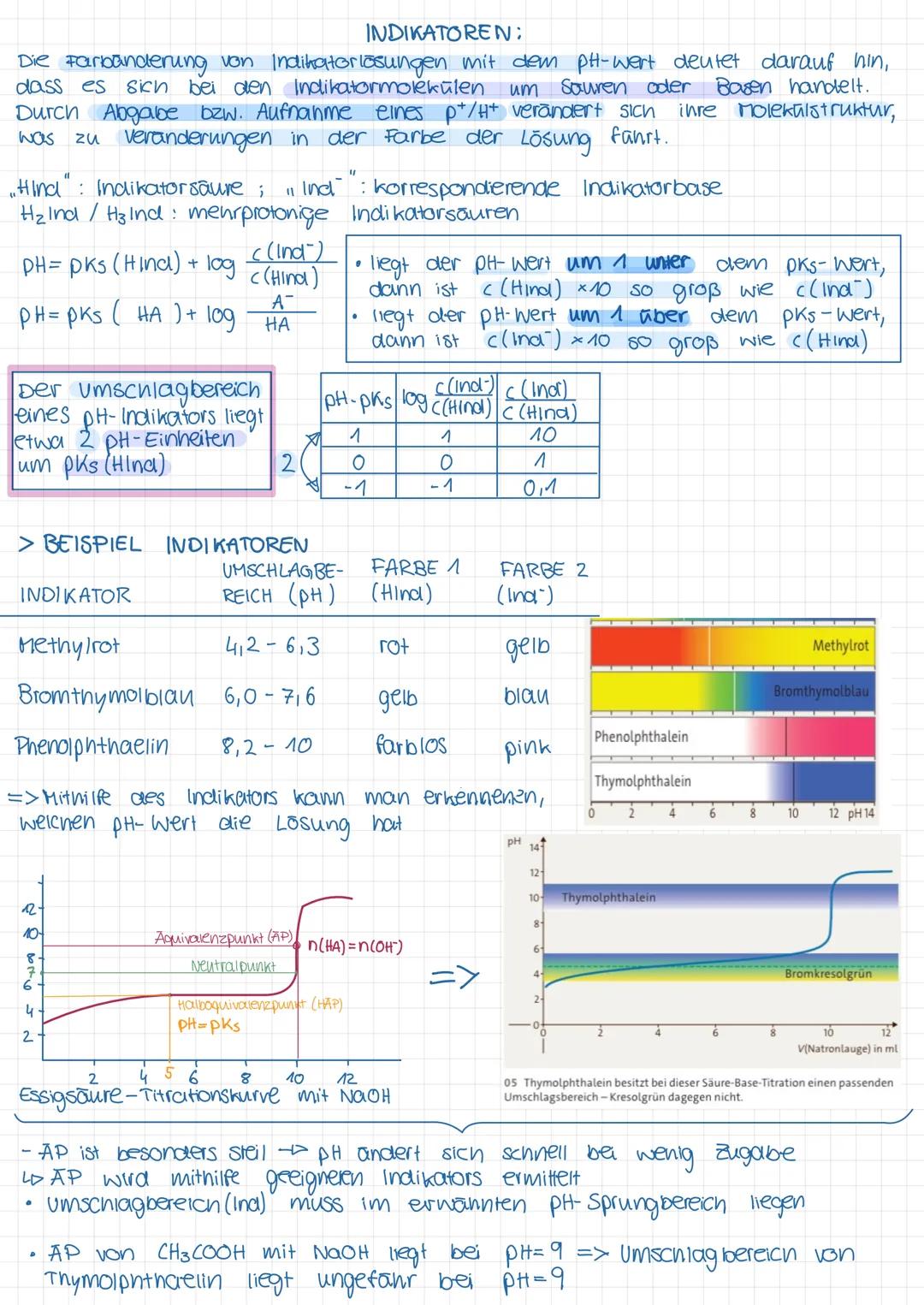
Indikatoren sind selbst schwache Säuren oder Basen, deren Molekülstruktur sich durch Abgabe oder Aufnahme eines Protons verändert, was zu einem Farbwechsel führt. Die Indikatorsäure (HInd) und ihre korrespondierende Base (Ind⁻) haben unterschiedliche Farben.
Der Farbumschlag eines Indikators erfolgt in einem bestimmten pH-Bereich, der etwa 2 pH-Einheiten um den pKₛ-Wert des Indikators liegt. Der pH-Wert kann mit der Formel pH = pKₛ(HInd) + log berechnet werden.
Für Säure-Base-Titrationen ist die Wahl des richtigen Indikators entscheidend. Der Umschlagsbereich muss im pH-Sprungbereich des Äquivalenzpunkts liegen. Beispielsweise eignet sich Phenolphthalein gut für die Titration von Essigsäure mit Natronlauge, da der Äquivalenzpunkt bei etwa pH 9 liegt.
📝 Beim Äquivalenzpunkt einer Titration sind die Stoffmengen der Säure und Base gleich . Die Titrationskurve zeigt hier einen steilen Anstieg, was bedeutet, dass sich der pH-Wert bei geringer Zugabe stark ändert – genau hier muss der Indikator umschlagen!
Titrationskurven und Äquivalenzpunkte
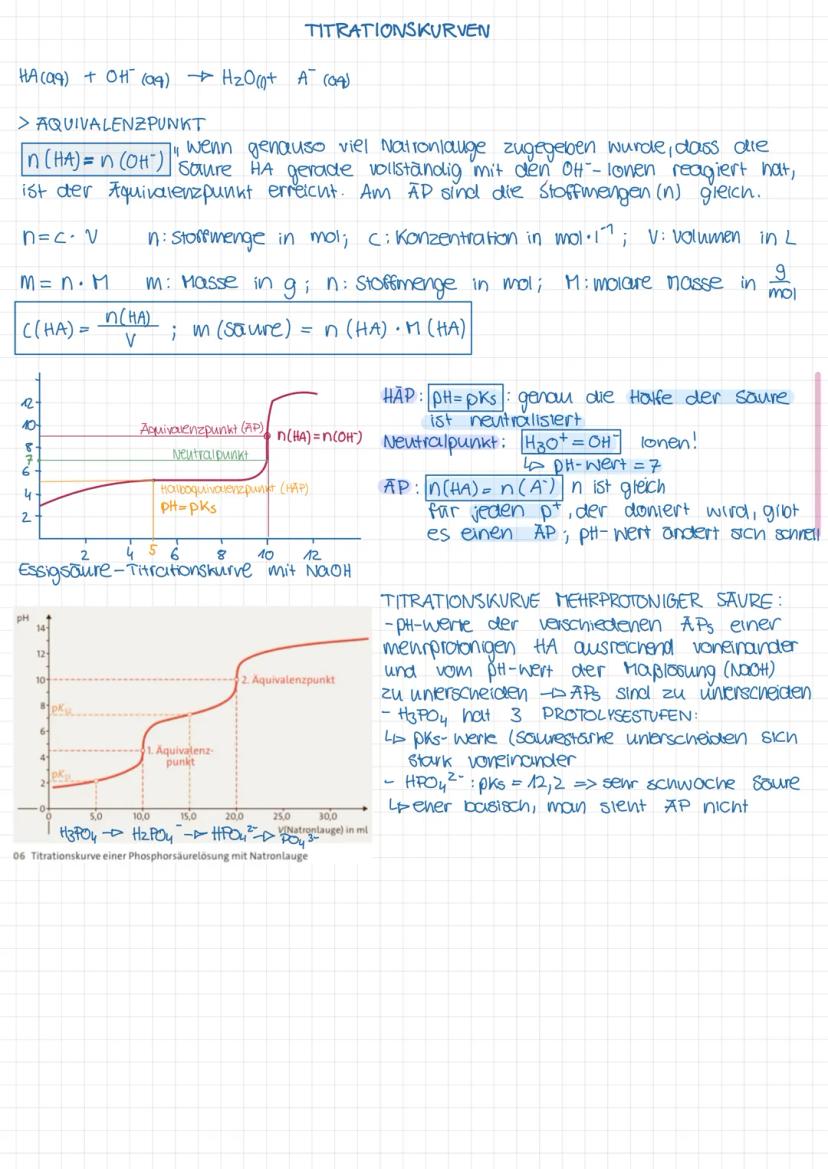
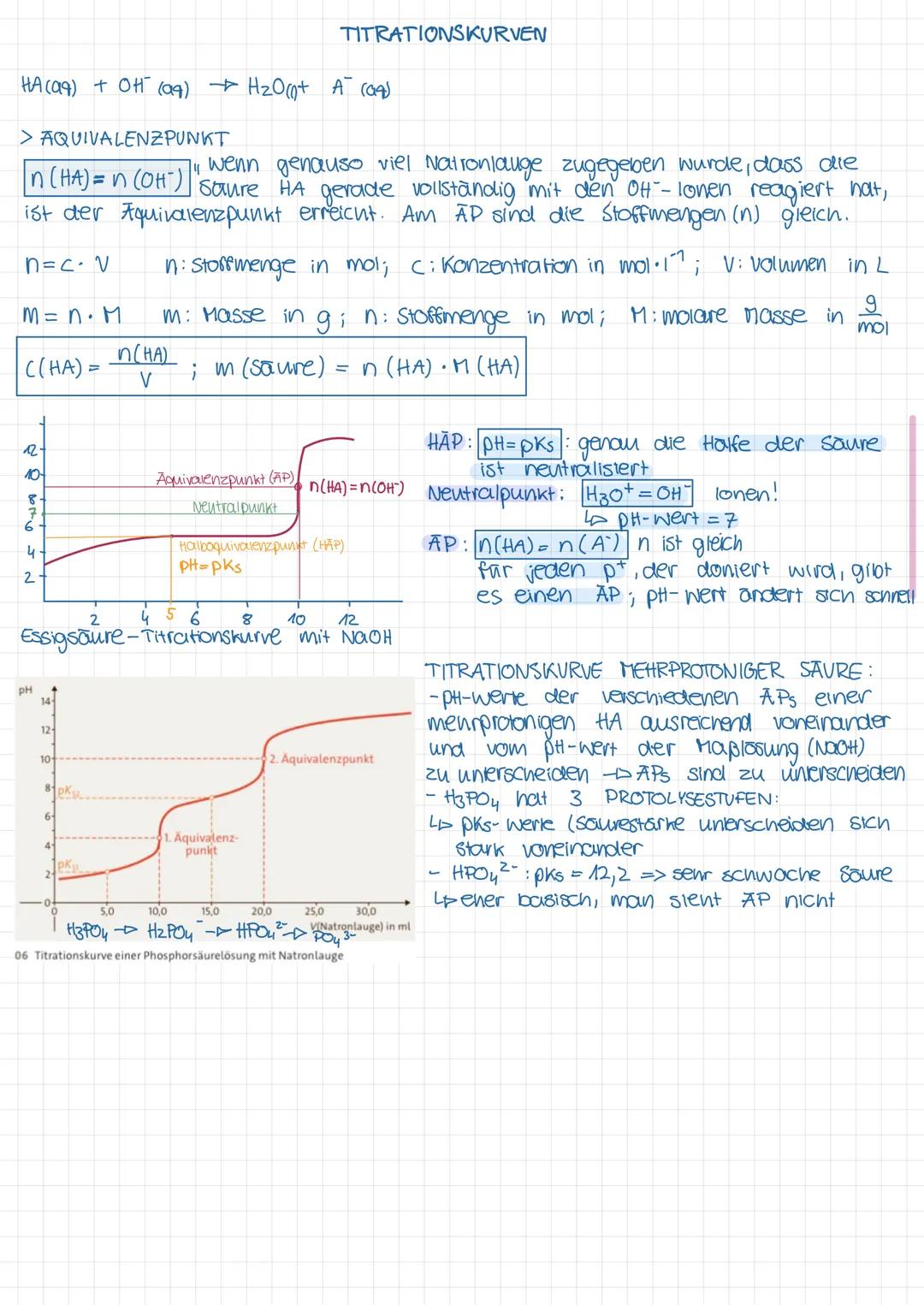
Bei der Titration reagiert die Säure HA mit Hydroxid-Ionen: HA(aq) + OH⁻(aq) → H₂O(l) + A⁻(aq). Der Äquivalenzpunkt (AP) ist erreicht, wenn genau so viel Base zugegeben wurde, dass die Säure vollständig neutralisiert ist. Am AP gilt: n(HA) = n(OH⁻).
Für die Berechnung der Stoffmenge nutzt man die Formel n = c · V, wobei n die Stoffmenge in mol, c die Konzentration in mol/l und V das Volumen in Liter ist. Die Masse kann über m = n · M berechnet werden, mit M als molare Masse in g/mol.
Bei mehrprotonigen Säuren wie Phosphorsäure (H₃PO₄) gibt es mehrere Protolysestufen und damit mehrere Äquivalenzpunkte in der Titrationskurve. Jede Stufe entspricht der Abgabe eines Protons (H₃PO₄ → H₂PO₄⁻ → HPO₄²⁻ → PO₄³⁻). Die pKₛ-Werte der verschiedenen Stufen unterscheiden sich deutlich voneinander.
⚠️ Nicht alle Äquivalenzpunkte einer mehrprotonigen Säure sind in der Titrationskurve gleich gut zu erkennen! Bei der Phosphorsäure ist der dritte AP bei pH ≈ 12,2 kaum sichtbar, da HPO₄²⁻ eine sehr schwache Säure ist und eher basisch reagiert.

Wichtige Formeln im Überblick
Der Zusammenhang zwischen pH und pOH ist durch pH = 14 - pOH gegeben. Für starke Säuren (pKₛ < 4) berechnet man den pH-Wert mit pH = -log · c(HA), für schwache Säuren (pKₛ > 4) mit pH = ½ · .
Die Stärke einer Säure oder Base wird durch den pKₛ- bzw. pKᵦ-Wert angegeben: pKₛ(HA) = -log Kₛ(HA) und pKᵦ(B) = -log Kᵦ(B). Es gilt stets: pKₛ(HA) + pKᵦ(A⁻) = 14.
Für Pufferlösungen verwendet man die Henderson-Hasselbalch-Gleichung: pH = pKₛ(HA) + log. Bei Indikatoren gilt analog: pH = pKₛ(HInd) + log.
🔢 In Titrationen brauchst du folgende Formeln: n = c · V, m = n · M und c(HA) = n(HA)/V. Diese helfen dir, Stoffmengen, Konzentrationen und benötigte Volumina zu berechnen. Stelle dir vor, du musst berechnen, wie viel Natronlauge du für die vollständige Neutralisation einer Säurelösung brauchst!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Säure-Base-Chemie
9Säure-Base-Gleichgewicht und Titration
Entdecken Sie die Grundlagen des chemischen Gleichgewichts und der Säure-Base-Reaktionen. Diese Zusammenfassung behandelt Le Chateliers Prinzip, Titrationskurven, pH-Wert-Berechnungen, Pufferlösungen und die Autoprotolyse von Wasser. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten. Enthält wichtige Formeln und Beispiele zur Veranschaulichung der Konzepte.
Chemie LK Abitur Zusammenfassung
Diese umfassende Zusammenfassung für den Chemie Leistungskurs (LK) in Baden-Württemberg deckt alle relevanten Themen ab, die für das Abitur 2022 wichtig sind. Sie enthält wichtige Konzepte wie Aromaten, chemische Gleichgewichte, Säuren und Basen, Elektrochemie, organische Chemie und mehr. Ideal zur Vorbereitung auf Prüfungen und zur Vertiefung des Verständnisses. Bei Interesse an der PDF-Version, kontaktieren Sie bitte [email protected].
Chemie Lernzettel Q1 - Aminosäuren/Enzyme/Proteine….
Lernzettel umfassend für die erste Klausur in der Oberstufe in Chemie- alles um Aminosäuren, Proteinen( mit Beispielen) als auch Enzymen (einfach erklärt und schlüssig )
Säure-Base-Gleichgewichte, Naturstoffe
1. Säure-Base-Gleichgewichte Säure-Base-Theorie nach Brønsted, Autoprotolyse und pH-Wert, Säure- & Basenstärke, pH-Werte berechnen, Säure-Base-Titration 2. Naturstoffe Chiralität, Optische Aktivität, Fischerprojektion, Kohlenhydrate, Ringform
Säure-Base-Reaktionen
Vertiefte Kenntnisse über Säure-Base-Chemie: Erfahren Sie alles über die Dissoziation von Säuren und Basen, pH-Wert-Berechnungen, Titrationskurven und Puffersysteme. Diese Zusammenfassung bietet eine klare Übersicht über die wichtigsten Konzepte, einschließlich der Henderson-Hasselbalch-Gleichung und der Neutralisationsreaktionen. Ideal für Chemie-Studierende und zur Vorbereitung auf Prüfungen.
Chemie Abitur 2024: Grundlagen
Umfassender Lernzettel für das Chemie-Abitur 2024 in Hessen. Behandelt zentrale Themen wie Enthalpie, Säure-Base-Gleichgewichte, chemische Reaktionen, Isomerie, und die Struktur von Proteinen und Kohlenhydraten. Ideal für die Prüfungsvorbereitung und das Verständnis chemischer Konzepte. Enthält wichtige Formeln, Reaktionsmechanismen und Nachweisreaktionen.
Säure-Base-Reaktionen verstehen
Entdecken Sie die Grundlagen der Säure-Base-Chemie, einschließlich pH-Wert-Berechnung, Pufferlösungen, und Titrationsmethoden. Diese Zusammenfassung bietet eine klare Übersicht über wichtige Konzepte wie das Ionenprodukt des Wassers, Brønsted-Theorie und die Rolle von Indikatoren in chemischen Reaktionen. Ideal für die Vorbereitung auf das Abitur 2024.
Chemie Leistungskurs Abitur Lernzettel
Chemie Leistungskurs Abitur Lernzettel
Säure-Base Grundlagen
Umfassende Zusammenfassung der Säure-Base-Theorie für das Abitur 2023. Behandelt pH-Wert-Berechnungen, Neutralisationsreaktionen, Indikatoren, Pufferlösungen, Titrationskurven und die Autoprotolyse von Wasser. Ideal für Chemie LK Schüler zur Prüfungsvorbereitung.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Chemie LK: Säuren, Basen, Puffer und Titration verstehen
Säure-Base-Reaktionen sind grundlegende Vorgänge in der Chemie, bei denen es um den Austausch von Protonen geht. Hier findest du eine übersichtliche Zusammenfassung der wichtigsten Konzepte, die dir hilft, diese manchmal komplizierten Zusammenhänge besser zu verstehen und für deine Prüfungen gut... Mehr anzeigen

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Säuren und Basen – Definitionen und Grundlagen
Eine Säure (HA) ist ein Protonendonator – sie gibt Protonen (H⁺) ab. Eine Base (B) funktioniert als Protonenakzeptor und nimmt Protonen auf. Diese Definition geht auf das Brønsted-Konzept zurück.
Bei Säure-Base-Reaktionen bilden sich sogenannte korrespondierende Säure-Base-Paare. Dabei handelt es sich um Teilchenpaare, die sich nur durch ein Proton unterscheiden. Beispiele sind NH₄⁺ & NH₃ oder CH₃COOH & CH₃COO⁻.
Ampholyte sind besonders interessante Teilchen, die je nach Reaktionspartner als Säure oder Base reagieren können. Beispiele dafür sind Wasser (H₂O), Ammoniak (NH₃) oder das Hydrogencarbonat-Ion (HCO₃⁻). Sie können sowohl Protonen aufnehmen als auch abgeben.
💡 Die Autoprotolyse des Wassers ist ein wichtiger Spezialfall, bei dem Wasser gleichzeitig als Säure und Base reagiert. Das Ionenprodukt K𝘸 = c(H₃O⁺)·c(OH⁻) = 10⁻¹⁴ mol²·l⁻² bei 25°C ist eine fundamentale Konstante in der Chemie.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
pH- und pOH-Werte
Der pH-Wert gibt an, wie viele H⁺-Ionen bzw. Oxonium-Ionen (H₃O⁺) in einer Lösung vorhanden sind. Eine saure Lösung hat eine hohe Konzentration an H⁺-Ionen, die mit Wasser zu H₃O⁺ reagieren. Der pOH-Wert bezieht sich auf die Konzentration der OH⁻-Ionen in alkalischen Lösungen.
Beide Werte hängen zusammen: pH + pOH = 14. Bei starken Säuren (pKₛ < 4) berechnet man den pH-Wert mit pH = -log(c(HA)). Bei schwachen Säuren (pKₛ > 4) nutzt man die Formel pH = ½. Ähnliche Formeln gelten für den pOH-Wert.
Die Stärke einer Säure oder Base wird durch die Säurekonstante Kₛ bzw. die Basenkonstante K𝘣 ausgedrückt. Je größer der Kₛ-Wert, desto kleiner ist der pKₛ-Wert und desto stärker ist die Säure. Wichtig: Je stärker eine Säure, desto schwächer ist ihre korrespondierende Base.
🧪 Die pH-Skala reicht von 0 bis 14: Starke Säuren liegen zwischen 0-3, Essig etwa bei 3-4, reines Wasser bei 7 (neutral), Seife bei 9-10 und Abflussreiniger im stark basischen Bereich bei 13-14.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Puffersysteme
Pufferlösungen halten den pH-Wert konstant, auch wenn Säuren oder Basen in geringen Mengen zugegeben werden. Sie bestehen aus einer schwachen Säure/Base und ihrer korrespondierenden Base/Säure im Verhältnis von etwa 1:1.
Bei Zugabe von H₃O⁺ reagiert die Pufferbase (A⁻) mit den Oxonium-Ionen: H₃O⁺ + A⁻ → HA + H₂O. Bei Zugabe von OH⁻ reagiert die Puffersäure mit den Hydroxid-Ionen: OH⁻ + HA → A⁻ + H₂O. In beiden Fällen werden die zugeführten Ionen abgefangen und der pH-Wert bleibt nahezu konstant.
Für die Berechnung des pH-Werts einer Pufferlösung verwendet man die Henderson-Hasselbalch-Gleichung: pH = pKₛ(HA) + log. Diese Formel ermöglicht es auch, das Konzentrationsverhältnis der Pufferkomponenten für einen gewünschten pH-Wert zu berechnen.
🔬 Wichtige Puffersysteme sind der Acetatpuffer , der Hydrogencarbonatpuffer , der Phosphatpuffer und der Ammoniakpuffer . Der Phosphatpuffer spielt eine entscheidende Rolle in unserem Blut!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Indikatoren und ihre Anwendung
Indikatoren sind selbst schwache Säuren oder Basen, deren Molekülstruktur sich durch Abgabe oder Aufnahme eines Protons verändert, was zu einem Farbwechsel führt. Die Indikatorsäure (HInd) und ihre korrespondierende Base (Ind⁻) haben unterschiedliche Farben.
Der Farbumschlag eines Indikators erfolgt in einem bestimmten pH-Bereich, der etwa 2 pH-Einheiten um den pKₛ-Wert des Indikators liegt. Der pH-Wert kann mit der Formel pH = pKₛ(HInd) + log berechnet werden.
Für Säure-Base-Titrationen ist die Wahl des richtigen Indikators entscheidend. Der Umschlagsbereich muss im pH-Sprungbereich des Äquivalenzpunkts liegen. Beispielsweise eignet sich Phenolphthalein gut für die Titration von Essigsäure mit Natronlauge, da der Äquivalenzpunkt bei etwa pH 9 liegt.
📝 Beim Äquivalenzpunkt einer Titration sind die Stoffmengen der Säure und Base gleich . Die Titrationskurve zeigt hier einen steilen Anstieg, was bedeutet, dass sich der pH-Wert bei geringer Zugabe stark ändert – genau hier muss der Indikator umschlagen!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Titrationskurven und Äquivalenzpunkte
Bei der Titration reagiert die Säure HA mit Hydroxid-Ionen: HA(aq) + OH⁻(aq) → H₂O(l) + A⁻(aq). Der Äquivalenzpunkt (AP) ist erreicht, wenn genau so viel Base zugegeben wurde, dass die Säure vollständig neutralisiert ist. Am AP gilt: n(HA) = n(OH⁻).
Für die Berechnung der Stoffmenge nutzt man die Formel n = c · V, wobei n die Stoffmenge in mol, c die Konzentration in mol/l und V das Volumen in Liter ist. Die Masse kann über m = n · M berechnet werden, mit M als molare Masse in g/mol.
Bei mehrprotonigen Säuren wie Phosphorsäure (H₃PO₄) gibt es mehrere Protolysestufen und damit mehrere Äquivalenzpunkte in der Titrationskurve. Jede Stufe entspricht der Abgabe eines Protons (H₃PO₄ → H₂PO₄⁻ → HPO₄²⁻ → PO₄³⁻). Die pKₛ-Werte der verschiedenen Stufen unterscheiden sich deutlich voneinander.
⚠️ Nicht alle Äquivalenzpunkte einer mehrprotonigen Säure sind in der Titrationskurve gleich gut zu erkennen! Bei der Phosphorsäure ist der dritte AP bei pH ≈ 12,2 kaum sichtbar, da HPO₄²⁻ eine sehr schwache Säure ist und eher basisch reagiert.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Wichtige Formeln im Überblick
Der Zusammenhang zwischen pH und pOH ist durch pH = 14 - pOH gegeben. Für starke Säuren (pKₛ < 4) berechnet man den pH-Wert mit pH = -log · c(HA), für schwache Säuren (pKₛ > 4) mit pH = ½ · .
Die Stärke einer Säure oder Base wird durch den pKₛ- bzw. pKᵦ-Wert angegeben: pKₛ(HA) = -log Kₛ(HA) und pKᵦ(B) = -log Kᵦ(B). Es gilt stets: pKₛ(HA) + pKᵦ(A⁻) = 14.
Für Pufferlösungen verwendet man die Henderson-Hasselbalch-Gleichung: pH = pKₛ(HA) + log. Bei Indikatoren gilt analog: pH = pKₛ(HInd) + log.
🔢 In Titrationen brauchst du folgende Formeln: n = c · V, m = n · M und c(HA) = n(HA)/V. Diese helfen dir, Stoffmengen, Konzentrationen und benötigte Volumina zu berechnen. Stelle dir vor, du musst berechnen, wie viel Natronlauge du für die vollständige Neutralisation einer Säurelösung brauchst!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Säure-Base-Chemie
9Säure-Base-Gleichgewicht und Titration
Entdecken Sie die Grundlagen des chemischen Gleichgewichts und der Säure-Base-Reaktionen. Diese Zusammenfassung behandelt Le Chateliers Prinzip, Titrationskurven, pH-Wert-Berechnungen, Pufferlösungen und die Autoprotolyse von Wasser. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten. Enthält wichtige Formeln und Beispiele zur Veranschaulichung der Konzepte.
Chemie LK Abitur Zusammenfassung
Diese umfassende Zusammenfassung für den Chemie Leistungskurs (LK) in Baden-Württemberg deckt alle relevanten Themen ab, die für das Abitur 2022 wichtig sind. Sie enthält wichtige Konzepte wie Aromaten, chemische Gleichgewichte, Säuren und Basen, Elektrochemie, organische Chemie und mehr. Ideal zur Vorbereitung auf Prüfungen und zur Vertiefung des Verständnisses. Bei Interesse an der PDF-Version, kontaktieren Sie bitte [email protected].
Chemie Lernzettel Q1 - Aminosäuren/Enzyme/Proteine….
Lernzettel umfassend für die erste Klausur in der Oberstufe in Chemie- alles um Aminosäuren, Proteinen( mit Beispielen) als auch Enzymen (einfach erklärt und schlüssig )
Säure-Base-Gleichgewichte, Naturstoffe
1. Säure-Base-Gleichgewichte Säure-Base-Theorie nach Brønsted, Autoprotolyse und pH-Wert, Säure- & Basenstärke, pH-Werte berechnen, Säure-Base-Titration 2. Naturstoffe Chiralität, Optische Aktivität, Fischerprojektion, Kohlenhydrate, Ringform
Säure-Base-Reaktionen
Vertiefte Kenntnisse über Säure-Base-Chemie: Erfahren Sie alles über die Dissoziation von Säuren und Basen, pH-Wert-Berechnungen, Titrationskurven und Puffersysteme. Diese Zusammenfassung bietet eine klare Übersicht über die wichtigsten Konzepte, einschließlich der Henderson-Hasselbalch-Gleichung und der Neutralisationsreaktionen. Ideal für Chemie-Studierende und zur Vorbereitung auf Prüfungen.
Chemie Abitur 2024: Grundlagen
Umfassender Lernzettel für das Chemie-Abitur 2024 in Hessen. Behandelt zentrale Themen wie Enthalpie, Säure-Base-Gleichgewichte, chemische Reaktionen, Isomerie, und die Struktur von Proteinen und Kohlenhydraten. Ideal für die Prüfungsvorbereitung und das Verständnis chemischer Konzepte. Enthält wichtige Formeln, Reaktionsmechanismen und Nachweisreaktionen.
Säure-Base-Reaktionen verstehen
Entdecken Sie die Grundlagen der Säure-Base-Chemie, einschließlich pH-Wert-Berechnung, Pufferlösungen, und Titrationsmethoden. Diese Zusammenfassung bietet eine klare Übersicht über wichtige Konzepte wie das Ionenprodukt des Wassers, Brønsted-Theorie und die Rolle von Indikatoren in chemischen Reaktionen. Ideal für die Vorbereitung auf das Abitur 2024.
Chemie Leistungskurs Abitur Lernzettel
Chemie Leistungskurs Abitur Lernzettel
Säure-Base Grundlagen
Umfassende Zusammenfassung der Säure-Base-Theorie für das Abitur 2023. Behandelt pH-Wert-Berechnungen, Neutralisationsreaktionen, Indikatoren, Pufferlösungen, Titrationskurven und die Autoprotolyse von Wasser. Ideal für Chemie LK Schüler zur Prüfungsvorbereitung.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.