In der Chemie-Klausur geht's um zwei große Themen: Wie schnell... Mehr anzeigen
Kinetik und Chemisches Gleichgewicht: Zusammenfassung und Übungen








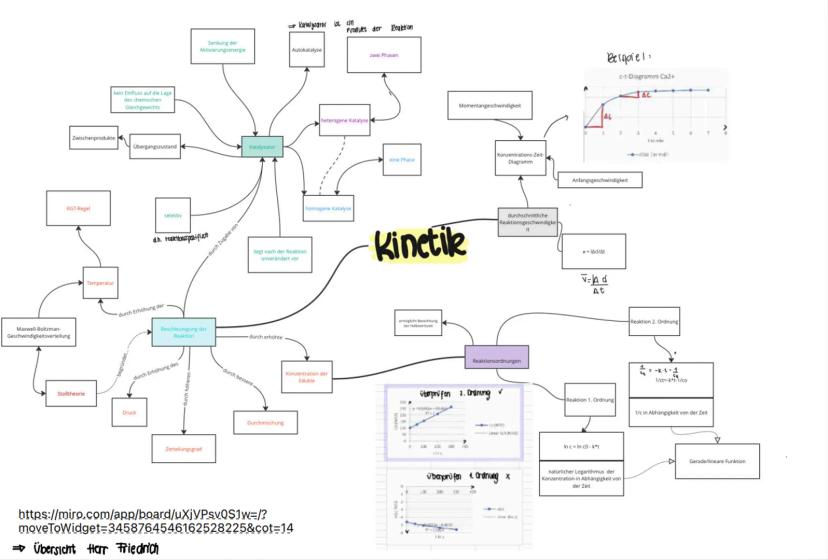


Klausur-Überblick
Die Kinetik beschäftigt sich mit der Geschwindigkeit chemischer Reaktionen. Du lernst, wie man sie berechnet und was sie beeinflusst.
Beim chemischen Gleichgewicht geht's darum, wann Hin- und Rückreaktion gleich schnell ablaufen. Das Massenwirkungsgesetz und das Prinzip von Le Chatelier sind hier deine wichtigsten Werkzeuge.
Tipp: Übungsaufgaben und c-t-Diagramme sind typische Klausuraufgaben - übe sie gut!

Kinetik - Grundlagen und Definitionen
Die Reaktionsgeschwindigkeit zeigt dir, wie viele wirksame Zusammenstöße pro Zeiteinheit stattfinden. Du berechnest sie mit der Formel: RG = Δc/Δt.
Die Stoßtheorie erklärt, wann Teilchen erfolgreich reagieren: Sie brauchen die richtige räumliche Anordnung und die Mindestenergie Emin. Nur dann entstehen neue Bindungen.
Sechs Faktoren beeinflussen die Reaktionsgeschwindigkeit: Temperatur, Druck, Konzentration, Durchmischung, Zerteilungsgrad und Katalysatoren. Je höher diese Werte, desto schneller läuft die Reaktion ab.
Die Reaktionsordnung (erste oder zweite Ordnung) zeigt dir, von welchen Ausgangsstoffen die Geschwindigkeit abhängt. Das musst du aus Messwerten ermitteln können.
Merkhilfe: Höhere Temperatur = höhere kinetische Energie = mehr wirksame Stöße!

Stoßtheorie und Einflussfaktoren
Stell dir alle Teilchen als winzige Kugeln vor, die sich ungeordnet bewegen. Ein wirksamer Stoß passiert nur bei korrekter räumlicher Anordnung und wenn die Mindestenergie Emin erreicht wird.
Temperatur erhöht die kinetische Energie der Teilchen. Druck und Konzentration sorgen für mehr Teilchen pro Volumen. Ein größerer Zerteilungsgrad schafft mehr Reaktionsfläche.
Durchmischung erhöht die Wahrscheinlichkeit für wirksame Zusammenstöße. Katalysatoren senken die Aktivierungsenergie, ohne selbst verbraucht zu werden.
Diese Faktoren kannst du gezielt nutzen, um Reaktionen zu beschleunigen - das ist auch in der Industrie wichtig!
Praxis-Tipp: Denk an das Kochen - kleinere Kartoffelstücke garen schneller als ganze!

c-t-Diagramme und chemisches Rechnen
c-t-Diagramme zeigen dir, wie sich Konzentrationen über die Zeit ändern. Edukte nehmen ab (fallende Kurve), Produkte nehmen zu (steigende Kurve).
Aus der Steigung berechnest du die durchschnittliche Reaktionsgeschwindigkeit: Je steiler die Kurve, desto schneller die Reaktion. Am Anfang ist sie meist am höchsten.
Beim chemischen Rechnen brauchst du die Grundformeln: n = m/M, c = n/V und ρ = m/V. Das molare Volumen Vm verwendest du nur bei Gasen!
Der Rechenweg ist immer gleich: 1. Reaktionsgleichung aufstellen, 2. Stoffmenge eines Stoffs berechnen, 3. fehlende Größen über die Stoffmenge ermitteln.
Achtung: Bei Produkten musst du an die Ausgangsgröße x₀ denken und entsprechend addieren!

Geschwindigkeitsgleichungen und Reaktionsordnungen
Höhere Konzentrationen der Edukte begünstigen wirksame Zusammenstöße. Die allgemeine Geschwindigkeitsgleichung lautet: V = k · c^a(A) · c^b(B).
Die Geschwindigkeitskonstante k ist reaktionsspezifisch und temperaturabhängig, aber konzentrationsunabhängig. Die Summe der Exponenten ergibt die Reaktionsordnung.
Reaktionen 1. Ordnung hängen nur von einem Ausgangsstoff ab: V = k · c(A). Beispiele sind radioaktiver Zerfall oder der Zerfall von N₂O₅.
Reaktionen 2. Ordnung haben zwei Varianten: Abhängigkeit von beiden Ausgangsstoffen oder vom Quadrat eines Stoffs .
Experimenteller Hinweis: Die Reaktionsordnung muss immer experimentell bestimmt werden!

Von Geschwindigkeitsgleichungen zu Zeitgesetzen
Durch Integration der Geschwindigkeitsgleichungen erhältst du die Zeitgesetze. Diese helfen dir, die Reaktionsordnung zu bestimmen.
Für 1. Ordnung gilt: ln c(A) = ln c₀(A) - kt. Wenn du ln c gegen die Zeit aufträgst und eine Gerade erhältst, handelt es sich um eine Reaktion 1. Ordnung.
Für 2. Ordnung gilt: 1/c(A) = -kt + 1/c₀(A). Hier trägst du 1/c gegen die Zeit auf. Eine Gerade zeigt dir eine Reaktion 2. Ordnung an.
Diese graphische Methode ist super praktisch, um die Reaktionsordnung aus Messwerten zu ermitteln. Du musst nur schauen, welche Auftragung eine Gerade ergibt!
Klausur-Trick: Beide Auftragungen probieren - nur eine ergibt eine schöne Gerade!
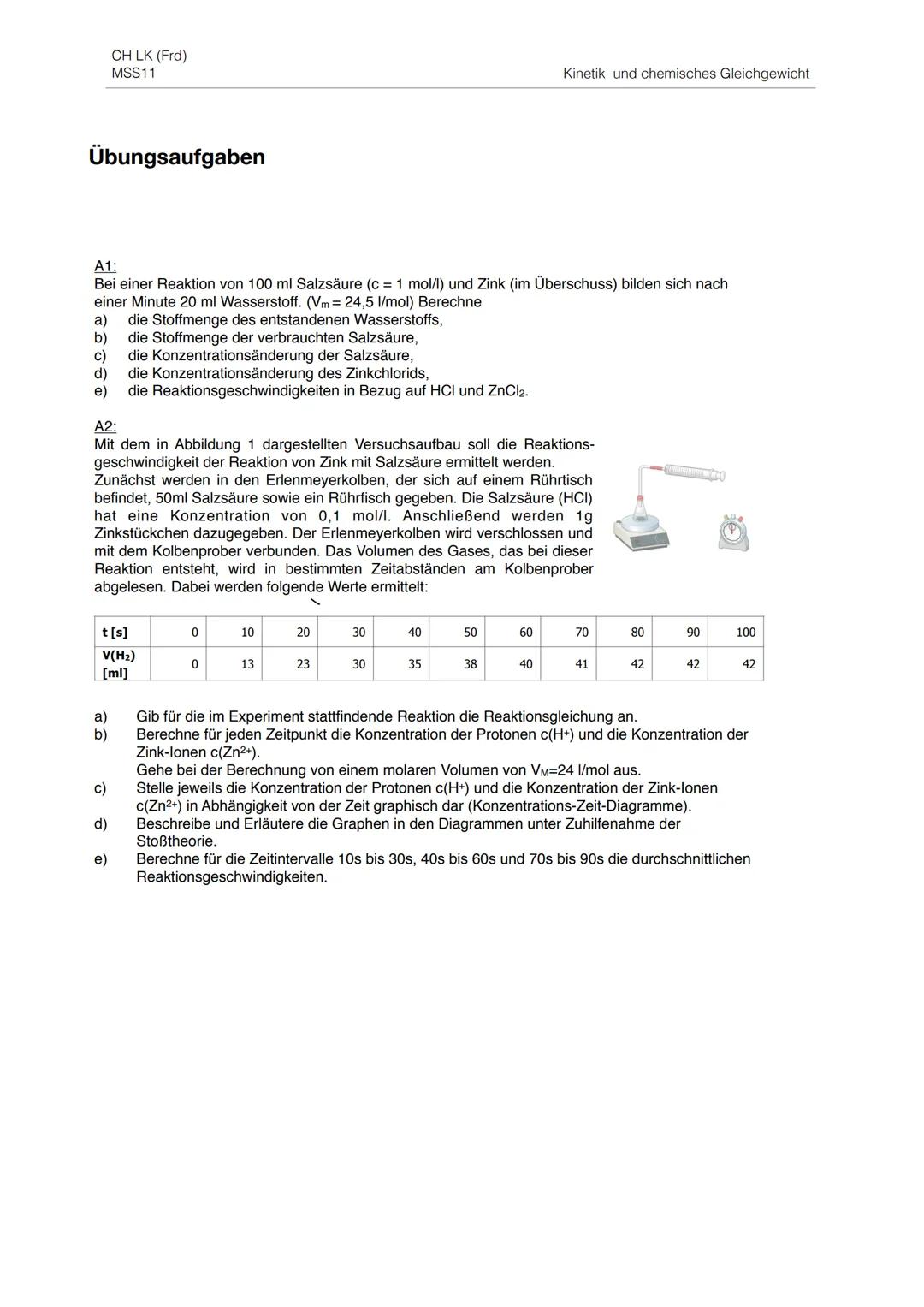
Übungsaufgaben zur Kinetik
Die Übungsaufgaben zeigen dir typische Klausuraufgaben. Bei Aufgabe 1 berechnest du aus dem entstandenen Wasserstoffvolumen die Stoffmengen und Konzentrationsänderungen.
Aufgabe 2 ist komplexer: Du führst Berechnungen mit Messwerten durch und erstellst c-t-Diagramme. Die Reaktionsgleichung lautet: Zn + 2HCl → ZnCl₂ + H₂.
Wichtige Schritte: Aus dem Gasvolumen die Stoffmenge berechnen , dann die Konzentrationen von H⁺ und Zn²⁺ bestimmen. Vergiss nicht das Volumen der Lösung!
Die durchschnittlichen Reaktionsgeschwindigkeiten berechnest du für verschiedene Zeitintervalle mit Δc/Δt. Die Werte werden mit der Zeit kleiner.
Praxis-Tipp: Bei Gasreaktionen immer das molare Volumen Vm = 24 l/mol verwenden!

Bestimmung der Reaktionsordnung
Die Integrationsmethode hilft dir, die Reaktionsordnung systematisch zu bestimmen. Zuerst führst du das Experiment durch und ermittelst Messwerte.
Falls nötig, berechnest du aus den Messwerten die Konzentrationen zu verschiedenen Zeitpunkten. Das ist oft der zeitaufwändigste Schritt.
Dann prüfst du mit den Zeitgesetzen: Für 1. Ordnung trägst du ln c gegen t auf, für 2. Ordnung 1/c gegen t. Die zutreffende Ordnung ergibt eine Gerade.
Aus der Steigung der Geraden bestimmst du die Geschwindigkeitskonstante k. Das Steigungsdreieck hilft dir dabei.
Methoden-Tipp: Beide Auftragungen probieren - nur die richtige Ordnung gibt eine schöne Gerade!
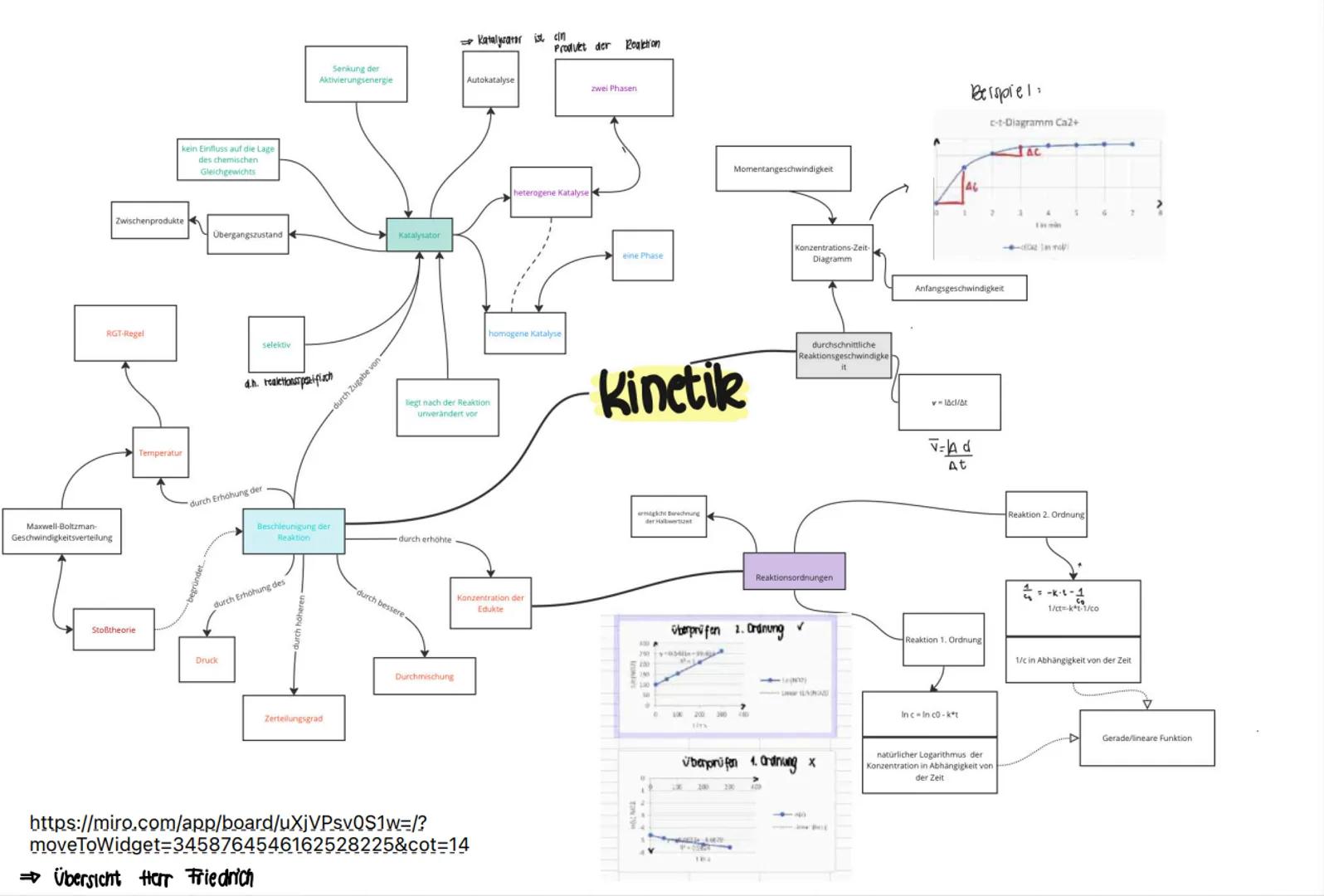
Kinetik - Übersicht und Zusammenhänge
Die Maxwell-Boltzmann-Verteilung zeigt, wie sich die Teilchengeschwindigkeiten bei verschiedenen Temperaturen verteilen. Höhere Temperatur bedeutet mehr schnelle Teilchen.
Katalysatoren sind genial: Sie senken die Aktivierungsenergie und beschleunigen Reaktionen, ohne selbst verbraucht zu werden. Bei der Autokatalyse ist ein Reaktionsprodukt selbst der Katalysator.
Man unterscheidet homogene (eine Phase) und heterogene Katalyse (zwei Phasen). Beide sind industriell wichtig.
Die RGT-Regel besagt: 10°C Temperaturerhöhung verdoppelt bis vervierfacht die Reaktionsgeschwindigkeit. Das ist eine Faustformel, die oft zutrifft.
Industrie-Bezug: Katalysatoren im Auto wandeln Schadstoffe um, ohne selbst verbraucht zu werden!

Chemisches Gleichgewicht
Das chemische Gleichgewicht ist erreicht, wenn Hin- und Rückreaktion gleich schnell ablaufen. Makroskopisch sieht alles stillstehen aus, mikroskopisch läuft noch viel ab.
Wichtige Merkmale: Das System muss reversibel und geschlossen sein. Es ist makroskopisch stationär aber mikroskopisch dynamisch.
Das Massenwirkungsgesetz beschreibt das Verhältnis der Konzentrationen: Kc = c(Produkte)/c(Edukte). Die Gleichgewichtskonstante ist temperatur- und reaktionsspezifisch.
Das Prinzip von Le Chatelier hilft dir zu verstehen, wie sich das Gleichgewicht bei Störungen verhält: Das System weicht dem Zwang aus.
Gleichgewichts-Regel: Störung von außen → System weicht aus und stellt neues Gleichgewicht ein!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Equilibrium
9Chemie: Thermodynamik & Gleichgewicht
Vertiefte Lerninhalte zu chemischen Reaktionen, Entropie, Enthalpie, freier Enthalpie, Säure-Base-Chemie, Titration und Puffersystemen. Ideal für das Abitur im Chemie Leistungskurs Q3 2024. Enthält wichtige Formeln, Konzepte und Berechnungen zur Unterstützung bei Prüfungen.
Chemisches Gleichgewicht verstehen
Erfahren Sie alles über das chemische Gleichgewicht, das Prinzip von Le Chatelier, das Massenwirkungsgesetz und die Bedeutung von Säure-Base-Titrationen. Diese Zusammenfassung behandelt die Temperatur- und Konzentrationsabhängigkeit von Reaktionen, die Berechnung von Gleichgewichtskonstanten und die Analyse von Titrationskurven. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemische Gleichgewichte & Säure-Base-Reaktionen
Vertiefte Analyse chemischer Gleichgewichte und Säure-Base-Reaktionen. Diese Klausur behandelt wichtige Konzepte wie das Massenwirkungsgesetz, pH-Wert-Berechnungen, das Deacon-Verfahren und die Veresterung von Carbonsäuren. Ideal für Schüler im Leistungskurs Chemie, die sich auf Prüfungen vorbereiten. Enthält Aufgaben zu ionischen Gleichungen, dem Haber-Bosch-Verfahren und der elektrolytischen Dissoziation.
Chemisches Gleichgewicht verstehen
Erforschen Sie die Konzepte des chemischen Gleichgewichts, einschließlich der Gleichgewichtskonstanten (K und k), dynamischen Gleichgewichts und des Prinzips von Le Chatelier. Diese Zusammenfassung bietet eine klare Erklärung der Reaktionsgeschwindigkeiten, der Massenwirkungsgesetze und der Unterschiede zwischen homogenen und heterogenen Gleichgewichten. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemisches Gleichgewicht und Katalysatoren
Erfahren Sie alles über das chemische Gleichgewicht, einschließlich der Merkmale, des Einflusses von Katalysatoren, des Massenwirkungsgesetzes, der Gleichgewichtskonstanten und des Prinzips von Le Chatelier. Diese Zusammenfassung bietet eine klare Übersicht über die Dynamik chemischer Reaktionen und deren Gleichgewichte, einschließlich Löslichkeitsprodukte und gekoppelte Gleichgewichte. Ideal für Studierende der Chemie.
Reaktionsgeschwindigkeit & Gleichgewicht
Erforschen Sie die Konzepte der Reaktionsgeschwindigkeit und des chemischen Gleichgewichts. Diese Zusammenfassung behandelt die Definitionen, Berechnungen und Einflussfaktoren auf die Reaktionsgeschwindigkeit sowie die Prinzipien des chemischen Gleichgewichts und deren Störungen. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Gleichgewicht von Reaktionen
Erforschen Sie das Gleichgewicht chemischer Reaktionen mit diesem detaillierten Versuchsprotokoll. Der Versuch demonstriert die Prinzipien des Stoffumsatzes und der Reaktionsgeschwindigkeit durch den Einsatz von Messzylindern und Pipetten. Ideal für Studierende der Chemie, die ein tieferes Verständnis für chemische Gleichgewichte und deren Beobachtungen entwickeln möchten.
Chemisches Gleichgewicht Experiment
Entdecken Sie ein praktisches Modellexperiment, das die Prinzipien des chemischen Gleichgewichts veranschaulicht. Erfahren Sie, wie die Konzentrationen von Edukten und Produkten sich während einer umkehrbaren Reaktion verändern und wie Geschwindigkeitskonstanten die Reaktionsdynamik beeinflussen. Ideal für Chemie-Studierende, die die Konzepte von Reaktionsgeschwindigkeit und Gleichgewicht verstehen möchten.
Esterbildung und Gleichgewicht
Diese Zusammenfassung behandelt die Reaktion zwischen Ethanol und Essigsäure zur Bildung von Estern und Wasser. Sie erklärt das Konzept des chemischen Gleichgewichts, die Rolle der Diffusion und die Gleichverteilung der Moleküle. Ideal für Studierende der Chemie, die die Grundlagen der Esterbildung verstehen möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Kinetik und Chemisches Gleichgewicht: Zusammenfassung und Übungen
In der Chemie-Klausur geht's um zwei große Themen: Wie schnell Reaktionen ablaufen (Kinetik) und wann sie ins Gleichgewicht kommen. Diese Konzepte helfen dir zu verstehen, warum manche Reaktionen blitzschnell passieren und andere ewig dauern.

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Klausur-Überblick
Die Kinetik beschäftigt sich mit der Geschwindigkeit chemischer Reaktionen. Du lernst, wie man sie berechnet und was sie beeinflusst.
Beim chemischen Gleichgewicht geht's darum, wann Hin- und Rückreaktion gleich schnell ablaufen. Das Massenwirkungsgesetz und das Prinzip von Le Chatelier sind hier deine wichtigsten Werkzeuge.
Tipp: Übungsaufgaben und c-t-Diagramme sind typische Klausuraufgaben - übe sie gut!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Kinetik - Grundlagen und Definitionen
Die Reaktionsgeschwindigkeit zeigt dir, wie viele wirksame Zusammenstöße pro Zeiteinheit stattfinden. Du berechnest sie mit der Formel: RG = Δc/Δt.
Die Stoßtheorie erklärt, wann Teilchen erfolgreich reagieren: Sie brauchen die richtige räumliche Anordnung und die Mindestenergie Emin. Nur dann entstehen neue Bindungen.
Sechs Faktoren beeinflussen die Reaktionsgeschwindigkeit: Temperatur, Druck, Konzentration, Durchmischung, Zerteilungsgrad und Katalysatoren. Je höher diese Werte, desto schneller läuft die Reaktion ab.
Die Reaktionsordnung (erste oder zweite Ordnung) zeigt dir, von welchen Ausgangsstoffen die Geschwindigkeit abhängt. Das musst du aus Messwerten ermitteln können.
Merkhilfe: Höhere Temperatur = höhere kinetische Energie = mehr wirksame Stöße!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Stoßtheorie und Einflussfaktoren
Stell dir alle Teilchen als winzige Kugeln vor, die sich ungeordnet bewegen. Ein wirksamer Stoß passiert nur bei korrekter räumlicher Anordnung und wenn die Mindestenergie Emin erreicht wird.
Temperatur erhöht die kinetische Energie der Teilchen. Druck und Konzentration sorgen für mehr Teilchen pro Volumen. Ein größerer Zerteilungsgrad schafft mehr Reaktionsfläche.
Durchmischung erhöht die Wahrscheinlichkeit für wirksame Zusammenstöße. Katalysatoren senken die Aktivierungsenergie, ohne selbst verbraucht zu werden.
Diese Faktoren kannst du gezielt nutzen, um Reaktionen zu beschleunigen - das ist auch in der Industrie wichtig!
Praxis-Tipp: Denk an das Kochen - kleinere Kartoffelstücke garen schneller als ganze!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
c-t-Diagramme und chemisches Rechnen
c-t-Diagramme zeigen dir, wie sich Konzentrationen über die Zeit ändern. Edukte nehmen ab (fallende Kurve), Produkte nehmen zu (steigende Kurve).
Aus der Steigung berechnest du die durchschnittliche Reaktionsgeschwindigkeit: Je steiler die Kurve, desto schneller die Reaktion. Am Anfang ist sie meist am höchsten.
Beim chemischen Rechnen brauchst du die Grundformeln: n = m/M, c = n/V und ρ = m/V. Das molare Volumen Vm verwendest du nur bei Gasen!
Der Rechenweg ist immer gleich: 1. Reaktionsgleichung aufstellen, 2. Stoffmenge eines Stoffs berechnen, 3. fehlende Größen über die Stoffmenge ermitteln.
Achtung: Bei Produkten musst du an die Ausgangsgröße x₀ denken und entsprechend addieren!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Geschwindigkeitsgleichungen und Reaktionsordnungen
Höhere Konzentrationen der Edukte begünstigen wirksame Zusammenstöße. Die allgemeine Geschwindigkeitsgleichung lautet: V = k · c^a(A) · c^b(B).
Die Geschwindigkeitskonstante k ist reaktionsspezifisch und temperaturabhängig, aber konzentrationsunabhängig. Die Summe der Exponenten ergibt die Reaktionsordnung.
Reaktionen 1. Ordnung hängen nur von einem Ausgangsstoff ab: V = k · c(A). Beispiele sind radioaktiver Zerfall oder der Zerfall von N₂O₅.
Reaktionen 2. Ordnung haben zwei Varianten: Abhängigkeit von beiden Ausgangsstoffen oder vom Quadrat eines Stoffs .
Experimenteller Hinweis: Die Reaktionsordnung muss immer experimentell bestimmt werden!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Von Geschwindigkeitsgleichungen zu Zeitgesetzen
Durch Integration der Geschwindigkeitsgleichungen erhältst du die Zeitgesetze. Diese helfen dir, die Reaktionsordnung zu bestimmen.
Für 1. Ordnung gilt: ln c(A) = ln c₀(A) - kt. Wenn du ln c gegen die Zeit aufträgst und eine Gerade erhältst, handelt es sich um eine Reaktion 1. Ordnung.
Für 2. Ordnung gilt: 1/c(A) = -kt + 1/c₀(A). Hier trägst du 1/c gegen die Zeit auf. Eine Gerade zeigt dir eine Reaktion 2. Ordnung an.
Diese graphische Methode ist super praktisch, um die Reaktionsordnung aus Messwerten zu ermitteln. Du musst nur schauen, welche Auftragung eine Gerade ergibt!
Klausur-Trick: Beide Auftragungen probieren - nur eine ergibt eine schöne Gerade!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Übungsaufgaben zur Kinetik
Die Übungsaufgaben zeigen dir typische Klausuraufgaben. Bei Aufgabe 1 berechnest du aus dem entstandenen Wasserstoffvolumen die Stoffmengen und Konzentrationsänderungen.
Aufgabe 2 ist komplexer: Du führst Berechnungen mit Messwerten durch und erstellst c-t-Diagramme. Die Reaktionsgleichung lautet: Zn + 2HCl → ZnCl₂ + H₂.
Wichtige Schritte: Aus dem Gasvolumen die Stoffmenge berechnen , dann die Konzentrationen von H⁺ und Zn²⁺ bestimmen. Vergiss nicht das Volumen der Lösung!
Die durchschnittlichen Reaktionsgeschwindigkeiten berechnest du für verschiedene Zeitintervalle mit Δc/Δt. Die Werte werden mit der Zeit kleiner.
Praxis-Tipp: Bei Gasreaktionen immer das molare Volumen Vm = 24 l/mol verwenden!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Bestimmung der Reaktionsordnung
Die Integrationsmethode hilft dir, die Reaktionsordnung systematisch zu bestimmen. Zuerst führst du das Experiment durch und ermittelst Messwerte.
Falls nötig, berechnest du aus den Messwerten die Konzentrationen zu verschiedenen Zeitpunkten. Das ist oft der zeitaufwändigste Schritt.
Dann prüfst du mit den Zeitgesetzen: Für 1. Ordnung trägst du ln c gegen t auf, für 2. Ordnung 1/c gegen t. Die zutreffende Ordnung ergibt eine Gerade.
Aus der Steigung der Geraden bestimmst du die Geschwindigkeitskonstante k. Das Steigungsdreieck hilft dir dabei.
Methoden-Tipp: Beide Auftragungen probieren - nur die richtige Ordnung gibt eine schöne Gerade!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Kinetik - Übersicht und Zusammenhänge
Die Maxwell-Boltzmann-Verteilung zeigt, wie sich die Teilchengeschwindigkeiten bei verschiedenen Temperaturen verteilen. Höhere Temperatur bedeutet mehr schnelle Teilchen.
Katalysatoren sind genial: Sie senken die Aktivierungsenergie und beschleunigen Reaktionen, ohne selbst verbraucht zu werden. Bei der Autokatalyse ist ein Reaktionsprodukt selbst der Katalysator.
Man unterscheidet homogene (eine Phase) und heterogene Katalyse (zwei Phasen). Beide sind industriell wichtig.
Die RGT-Regel besagt: 10°C Temperaturerhöhung verdoppelt bis vervierfacht die Reaktionsgeschwindigkeit. Das ist eine Faustformel, die oft zutrifft.
Industrie-Bezug: Katalysatoren im Auto wandeln Schadstoffe um, ohne selbst verbraucht zu werden!

Melde dich an, um den Inhalt zu sehen. Kostenlos!
- Zugriff auf alle Dokumente
- Verbessere deine Noten
- Schließ dich Millionen Schülern an
Chemisches Gleichgewicht
Das chemische Gleichgewicht ist erreicht, wenn Hin- und Rückreaktion gleich schnell ablaufen. Makroskopisch sieht alles stillstehen aus, mikroskopisch läuft noch viel ab.
Wichtige Merkmale: Das System muss reversibel und geschlossen sein. Es ist makroskopisch stationär aber mikroskopisch dynamisch.
Das Massenwirkungsgesetz beschreibt das Verhältnis der Konzentrationen: Kc = c(Produkte)/c(Edukte). Die Gleichgewichtskonstante ist temperatur- und reaktionsspezifisch.
Das Prinzip von Le Chatelier hilft dir zu verstehen, wie sich das Gleichgewicht bei Störungen verhält: Das System weicht dem Zwang aus.
Gleichgewichts-Regel: Störung von außen → System weicht aus und stellt neues Gleichgewicht ein!
Wir dachten schon, du fragst nie...
Was ist der Knowunity KI-Begleiter?
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Wo kann ich die Knowunity-App herunterladen?
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Ist Knowunity wirklich kostenlos?
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
Ähnlicher Inhalt
Beliebtester Inhalt: Equilibrium
9Chemie: Thermodynamik & Gleichgewicht
Vertiefte Lerninhalte zu chemischen Reaktionen, Entropie, Enthalpie, freier Enthalpie, Säure-Base-Chemie, Titration und Puffersystemen. Ideal für das Abitur im Chemie Leistungskurs Q3 2024. Enthält wichtige Formeln, Konzepte und Berechnungen zur Unterstützung bei Prüfungen.
Chemisches Gleichgewicht verstehen
Erfahren Sie alles über das chemische Gleichgewicht, das Prinzip von Le Chatelier, das Massenwirkungsgesetz und die Bedeutung von Säure-Base-Titrationen. Diese Zusammenfassung behandelt die Temperatur- und Konzentrationsabhängigkeit von Reaktionen, die Berechnung von Gleichgewichtskonstanten und die Analyse von Titrationskurven. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemische Gleichgewichte & Säure-Base-Reaktionen
Vertiefte Analyse chemischer Gleichgewichte und Säure-Base-Reaktionen. Diese Klausur behandelt wichtige Konzepte wie das Massenwirkungsgesetz, pH-Wert-Berechnungen, das Deacon-Verfahren und die Veresterung von Carbonsäuren. Ideal für Schüler im Leistungskurs Chemie, die sich auf Prüfungen vorbereiten. Enthält Aufgaben zu ionischen Gleichungen, dem Haber-Bosch-Verfahren und der elektrolytischen Dissoziation.
Chemisches Gleichgewicht verstehen
Erforschen Sie die Konzepte des chemischen Gleichgewichts, einschließlich der Gleichgewichtskonstanten (K und k), dynamischen Gleichgewichts und des Prinzips von Le Chatelier. Diese Zusammenfassung bietet eine klare Erklärung der Reaktionsgeschwindigkeiten, der Massenwirkungsgesetze und der Unterschiede zwischen homogenen und heterogenen Gleichgewichten. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Chemisches Gleichgewicht und Katalysatoren
Erfahren Sie alles über das chemische Gleichgewicht, einschließlich der Merkmale, des Einflusses von Katalysatoren, des Massenwirkungsgesetzes, der Gleichgewichtskonstanten und des Prinzips von Le Chatelier. Diese Zusammenfassung bietet eine klare Übersicht über die Dynamik chemischer Reaktionen und deren Gleichgewichte, einschließlich Löslichkeitsprodukte und gekoppelte Gleichgewichte. Ideal für Studierende der Chemie.
Reaktionsgeschwindigkeit & Gleichgewicht
Erforschen Sie die Konzepte der Reaktionsgeschwindigkeit und des chemischen Gleichgewichts. Diese Zusammenfassung behandelt die Definitionen, Berechnungen und Einflussfaktoren auf die Reaktionsgeschwindigkeit sowie die Prinzipien des chemischen Gleichgewichts und deren Störungen. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Gleichgewicht von Reaktionen
Erforschen Sie das Gleichgewicht chemischer Reaktionen mit diesem detaillierten Versuchsprotokoll. Der Versuch demonstriert die Prinzipien des Stoffumsatzes und der Reaktionsgeschwindigkeit durch den Einsatz von Messzylindern und Pipetten. Ideal für Studierende der Chemie, die ein tieferes Verständnis für chemische Gleichgewichte und deren Beobachtungen entwickeln möchten.
Chemisches Gleichgewicht Experiment
Entdecken Sie ein praktisches Modellexperiment, das die Prinzipien des chemischen Gleichgewichts veranschaulicht. Erfahren Sie, wie die Konzentrationen von Edukten und Produkten sich während einer umkehrbaren Reaktion verändern und wie Geschwindigkeitskonstanten die Reaktionsdynamik beeinflussen. Ideal für Chemie-Studierende, die die Konzepte von Reaktionsgeschwindigkeit und Gleichgewicht verstehen möchten.
Esterbildung und Gleichgewicht
Diese Zusammenfassung behandelt die Reaktion zwischen Ethanol und Essigsäure zur Bildung von Estern und Wasser. Sie erklärt das Konzept des chemischen Gleichgewichts, die Rolle der Diffusion und die Gleichverteilung der Moleküle. Ideal für Studierende der Chemie, die die Grundlagen der Esterbildung verstehen möchten.
Beliebtester Inhalt in Chemie
9Stoffwechselprozesse im Fokus
Entdecken Sie die zentralen Stoffwechselprozesse wie Fotosynthese, Zellatmung und Gärung. Dieser Lernzettel bietet eine umfassende Übersicht über den Calvin-Zyklus, die Lichtreaktionen, den Citratzyklus und die Regulation der Glykolyse. Ideal für die Vorbereitung auf das Abitur in Biologie. Enthält wichtige Konzepte wie C3- und C4-Pflanzen, chemiosmotische ATP-Produktion und die Rolle von Chloroplasten.
Chemie LK Abitur 2025 Hessen Q3 chemische Gleichgewicht, Portlysereaktion, Puffer
Lernzettel für Chemie Abitur Q3 2025 Hessen, alle Themen von chemischen Gleichgewicht (auch Enthalpie/Entropie), Pod Lysereaktionen und Puffer (alle Berechnungen)
Säuren & Basen - Chemie LK/GK
Säuren & Basen Lernzettel für Chemie LK/GK. Unterthemen: Arrhenius/Brönsted,Protolyse,Säure-Base-Paare,Autoprotolyse,pH-Wert,pOH-Wert,Säurestärke,Basenstärke,starke/schwache Säuren/Basen,Titration. Weitere Lernzettel in Chemie sind auf meinem Profil.
Isomerie und Reaktionen der Organischen Chemie
Diese Zusammenfassung behandelt die wichtigsten Konzepte der organischen Chemie, einschließlich Isomerie, Reaktionsmechanismen, Nachweisreaktionen für Aldehyde, Alkohole und Aromaten. Ideal für das Abitur 2023, bietet sie klare Erklärungen zu nucleophilen und elektrophilen Substitutionen sowie zur Nomenklatur von Alkoholen und Alkanen.
Alkene und Alkine: Eigenschaften & Nomenklatur
Entdecken Sie die Eigenschaften und Nomenklatur von Alkenen und Alkinen in der organischen Chemie. Diese Zusammenfassung behandelt die Struktur, Isomerie, allgemeine Formeln und Reaktionen ungesättigter Kohlenwasserstoffe. Ideal für Studierende der Chemie, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Elektrochemie: Grundlagen und Anwendungen
Entdecken Sie die wesentlichen Konzepte der Elektrochemie, einschließlich galvanischer Zellen, Elektrolyse, Redoxreaktionen und der Herstellung von Aluminium. Diese Zusammenfassung bietet einen klaren Überblick über Standardelektrodenpotentiale, elektrochemische Serien und die Funktionsweise von Batterien und Brennstoffzellen. Ideal für das Abi in Chemie.
Proteinstrukturen und Aminosäuren
Erforschen Sie die vier Strukturebenen von Proteinen: Primär-, Sekundär-, Tertiär- und Quatärstruktur. Lernen Sie die Rolle von Aminosäuren und Peptidbindungen in der Proteinbildung kennen. Ideal für Biologie-Studierende, die ein tiefes Verständnis der Proteinarchitektur entwickeln möchten.
Konzentrationsberechnung im Gleichgewicht
Erfahren Sie alles über die Berechnung von Konzentrationen im chemischen Gleichgewicht, das Prinzip von Le Chatelier und die Gleichgewichtskonstante. Diese Zusammenfassung bietet eine klare Anleitung zur Aufstellung von Reaktionsgleichungen und zur Anwendung des Massenwirkungsgesetzes. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Chemie Q2 LK Abi 2025 Hessen Natustoffe; Kohlenhydrate, Peptide, Kunststoffe, Fette
Alle Themen des Chemie Abiturs 2025 in Hessen LK, Q2, der Naturstoffe und Synthesen. Kohlenhydrate, Peptide/Aminosäuren, Kunstoffe und der Reaktion, Mechanismen und Fette im Alltag.
Beliebtester Inhalt
9Der zerbrochene Krug
Szenenzusammenfassunfen, Figurenkonstellationen, Aufbau des Stücks, Sprache und Stilbesonderheiten, Aussageabsicht, Thematik, Interpretation
Der zerbrochene Krug von Heinrich von Kleist
Hier steht so ziemlich alles drinnen von Zusammenfassungen der einzelnen Auftritte bis hin zu den einzelnen Perosn und noch einiges mehr
Der zerbrochne Krug
Ausführliche Lernzettel zu: Basisdaten, Handlung, ausführliche Zusammenfassungen der Auftritte, zentrale Themen, Symbolische Bedeutung, Merkmale der Komödie
Heimsuchung_JennyErpenbeck_Abitur
Zusammenfassungen für jedes Kapitel, Analysen und Zitate
Der zerbrochene Krug: Analyse
Diese umfassende Analyse von 'Der zerbrochene Krug' von Heinrich von Kleist bietet eine detaillierte Kapitelzusammenfassung, Charakterisierungen, historische Kontexte, sowie den Aufbau und die sprachlichen Merkmale des Dramas. Ideal für Studierende, die sich auf Prüfungen vorbereiten oder tiefere Einblicke in Kleists Werk gewinnen möchten.
Englisch LK Abitur 2025
Komplette Englisch LK Abi Zusammenfassung 2025
ZP10 Mathe Zusammenfassung NRW
Lernzettel für die ZP10 Mathe in NRW mit allen Themen außer Sinusfunktionen.
Abilernzettel Heimsuchung 2025
Figurenkonstellation, Kapitel Zusammenfassung, Charaktere, Motive, Deutungsansätze,
Heimsuchung - Jenny Erpenbeck
Inhalt, Entstehung und Quellen, Figuren, Geschichtliche Hintergründe, Motive, Erzählstruktur/- stil
Findest du nicht, was du suchst? Entdecke andere Fächer.
Schüler lieben uns — und du auch.
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.