Säuren und Basen begegnen dir täglich - vom Reinigungsmittel bis... Mehr anzeigen
Melde dich an, um den Inhalt zu sehenKostenlos!
Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Knowunity KI
Fächer
Triangle Congruence and Similarity Theorems
Triangle Properties and Classification
Linear Equations and Graphs
Geometric Angle Relationships
Trigonometric Functions and Identities
Equation Solving Techniques
Circle Geometry Fundamentals
Division Operations and Methods
Basic Differentiation Rules
Exponent and Logarithm Properties
Alle Themen anzeigen
Human Organ Systems
Reproductive Cell Cycles
Biological Sciences Subdisciplines
Cellular Energy Metabolism
Autotrophic Energy Processes
Inheritance Patterns and Principles
Biomolecular Structure and Organization
Cell Cycle and Division Mechanics
Cellular Organization and Development
Biological Structural Organization
Alle Themen anzeigen
Chemical Sciences and Applications
Atomic Structure and Composition
Molecular Electron Structure Representation
Atomic Electron Behavior
Matter Properties and Water
Mole Concept and Calculations
Gas Laws and Behavior
Periodic Table Organization
Chemical Thermodynamics Fundamentals
Chemical Bond Types and Properties
Alle Themen anzeigen
European Renaissance and Enlightenment
European Cultural Movements 800-1920
American Revolution Era 1763-1797
American Civil War 1861-1865
Global Imperial Systems
Mongol and Chinese Dynasties
U.S. Presidents and World Leaders
Historical Sources and Documentation
World Wars Era and Impact
World Religious Systems
Alle Themen anzeigen
Classic and Contemporary Novels
Literary Character Analysis
Rhetorical Theory and Practice
Classic Literary Narratives
Reading Analysis and Interpretation
Narrative Structure and Techniques
English Language Components
Influential English-Language Authors
Basic Sentence Structure
Narrative Voice and Perspective
Alle Themen anzeigen
3,741
•
Aktualisiert May 14, 2026
•
Sophia
@sophiad._xhjt
Säuren und Basen begegnen dir täglich - vom Reinigungsmittel bis... Mehr anzeigen








Basen sind die Superhelden der Reinigung - ihre negativ geladenen Teilchen heften sich an Schmutz und sorgen dafür, dass sich dieser leichter ablöst. Außerdem zersetzen sie hartnäckige Proteine und Fette.
Säuren hingegen sind perfekt gegen Kalk und Urinstein. Sie lösen diese Ablagerungen durch chemische Reaktionen auf und werden deshalb oft in WC-Reinigern verwendet. In Lebensmitteln hemmen Säuren das Wachstum von Mikroorganismen und sorgen für längere Haltbarkeit.
Nach Brönsted sind Säuren Protonendonatoren und Basen Protonenakzeptoren (nehmen Protonen auf). Diese Definition ist viel praktischer als die von Arrhenius, weil sie nicht nur auf wässrige Lösungen beschränkt ist.
Merke: Säure-Base-Reaktionen funktionieren nach dem Donator-Akzeptor-Prinzip - es braucht immer beide Partner für eine Reaktion!

Protolyse ist der Fachbegriff für jede Säure-Base-Reaktion, bei der Protonen von einer Säure auf eine Base übertragen werden. Ohne eine passende Base kann eine Säure kein Proton abgeben - sie braucht einen "Empfänger".
Korrespondierende Säure-Base-Paare unterscheiden sich nur um ein Proton. Wenn HCl ein Proton abgibt, entsteht Cl⁻ - diese beiden bilden ein korrespondierendes Paar. An jeder Protolyse sind immer zwei solcher Paare beteiligt.
Ampholyte sind echte Alleskönner - sie können je nach Reaktionspartner sowohl als Säure als auch als Base reagieren. Das bekannteste Beispiel ist Wasser: Mit starken Säuren verhält es sich wie eine Base, mit starken Basen wie eine Säure.
Tipp: Mehrprotonige Säuren wie H₂SO₄ können mehrere Protonen nacheinander abgeben - jedes Mal entsteht eine schwächere korrespondierende Base!

Wasser führt ständig Selbstgespräche auf molekularer Ebene! Bei der Autoprotolyse übertragen sich Wassermoleküle gegenseitig Protonen: H₂O + H₂O ⇌ H₃O⁺ + OH⁻.
Das Ionenprodukt des Wassers Kw = 10⁻¹⁴ mol²/L² ist bei 25°C konstant. Daraus folgt: pKw = pH + pOH = 14. Diese Formel ist dein bester Freund bei pH-Berechnungen!
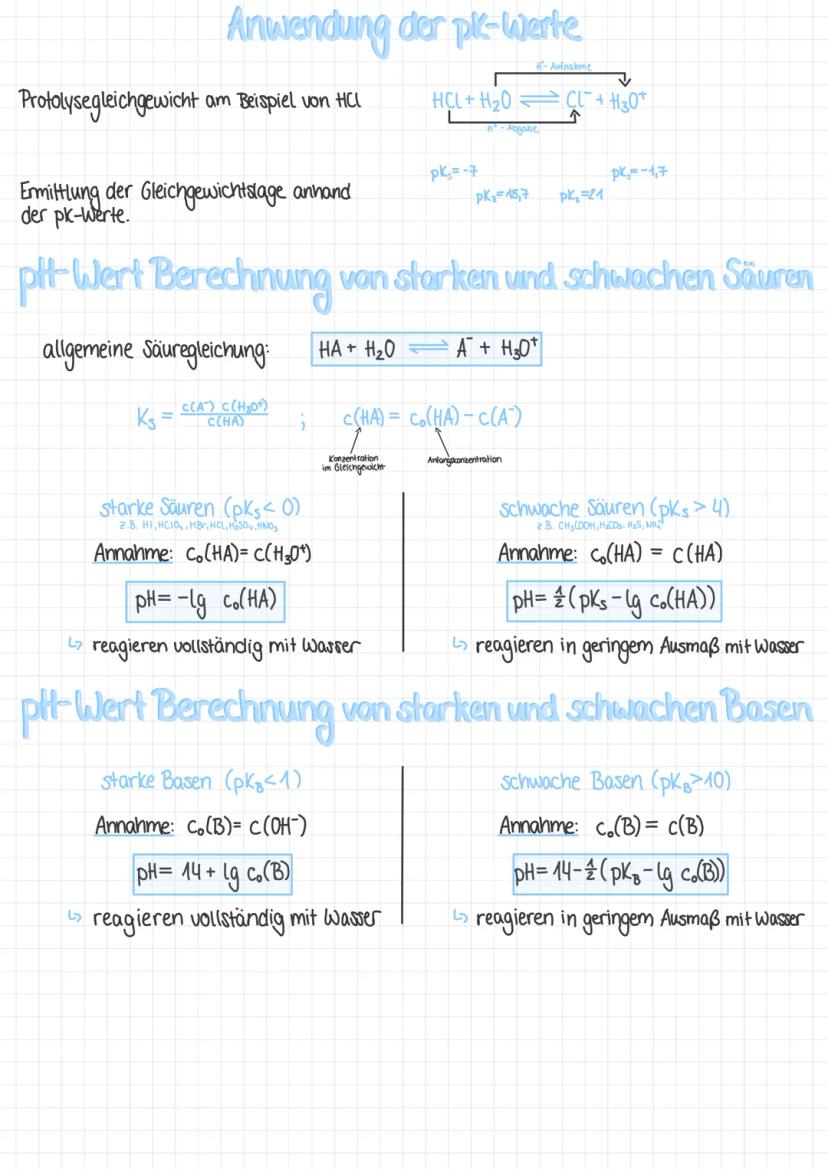
Der pH-Wert ist der negative Zehnerlogarithmus der H₃O⁺-Konzentration: pH = -lg c(H₃O⁺). Die Skala reicht meist von 0-14:
Praxistipp: Bei pH-Rechnungen immer daran denken, dass sich die Konzentrationen von H₃O⁺ und OH⁻ umgekehrt proportional verhalten!

Die Säurekonstante Ks zeigt dir, wie gerne eine Säure ihre Protonen abgibt. Je größer Ks, desto stärker die Säure. Analog dazu misst die Basenkonstante KB die Protonengier einer Base.
Um mit den vielen Zehnerpotenzen klarzukommen, verwendest du pKs = -lg Ks. Hier gilt: Je kleiner der pKs-Wert, desto stärker die Säure! HCl hat pKs = -7 (sehr stark), Essigsäure pKs = 4,8 (schwach).
Ein geniales Gesetz verbindet korrespondierende Paare: pKs + pKB = 14. Ist eine Säure stark (kleiner pKs), ist ihre korrespondierende Base automatisch schwach (großer pKB).
Eselsbrücke: Starke Säuren haben schwache korrespondierende Basen - wie bei einer Wippe: ist eine Seite oben, ist die andere unten!
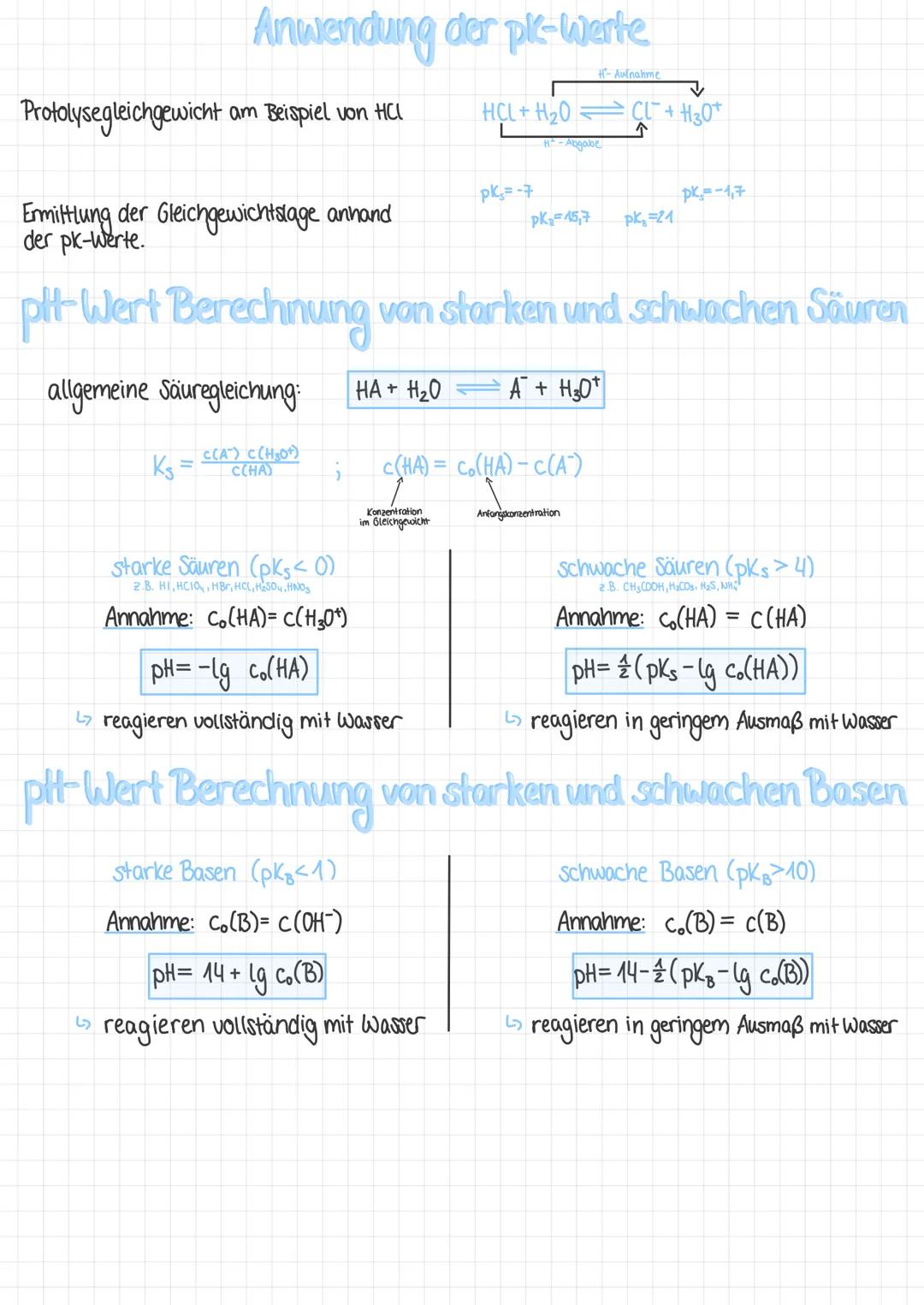
Bei starken Säuren (pKs < 1) wie HCl geht alles schnell und einfach: Sie reagieren vollständig mit Wasser. Deshalb gilt: pH = -lg c₀(HA). Eine 0,1 M HCl-Lösung hat also pH = 1.
Schwache Säuren (pKs > 4) sind komplizierter, weil sie nur teilweise reagieren. Hier brauchst du die Formel: pH = ½. Bei Essigsäure mit c = 0,1 M ergibt das pH = 2,9.
Für starke Basen berechnest du erst pOH = -lg c₀(B), dann pH = 14 - pOH. Bei schwachen Basen verwendest du: pH = 14 - ½.
Achtung: Die Vereinfachungsformeln gelten nur, wenn die Annahmen erfüllt sind - bei sehr verdünnten Lösungen musst du genauer rechnen!

Warum ist Methansäure stärker als Butansäure? Die Antwort liegt im induktiven Effekt! Alkylketten wie -CH₃ haben einen +I-Effekt - sie "schieben" Elektronen zum Sauerstoff der Säuregruppe.
Mehr Elektronendichte am Sauerstoff bedeutet: Die O-H-Bindung wird stärker, das Proton lässt sich schwerer abspalten. Je länger die Alkylkette, desto stärker der +I-Effekt und desto schwächer die Säure.
Umgekehrt haben elektronegative Gruppen wie Fluor einen -I-Effekt - sie ziehen Elektronen ab. Das schwächt die O-H-Bindung und macht die Säure stärker. Trichloressigsäure ist deshalb viel stärker als Essigsäure.
Merkregel: Alkylreste machen Säuren schwächer , elektronegative Gruppen machen sie stärker !
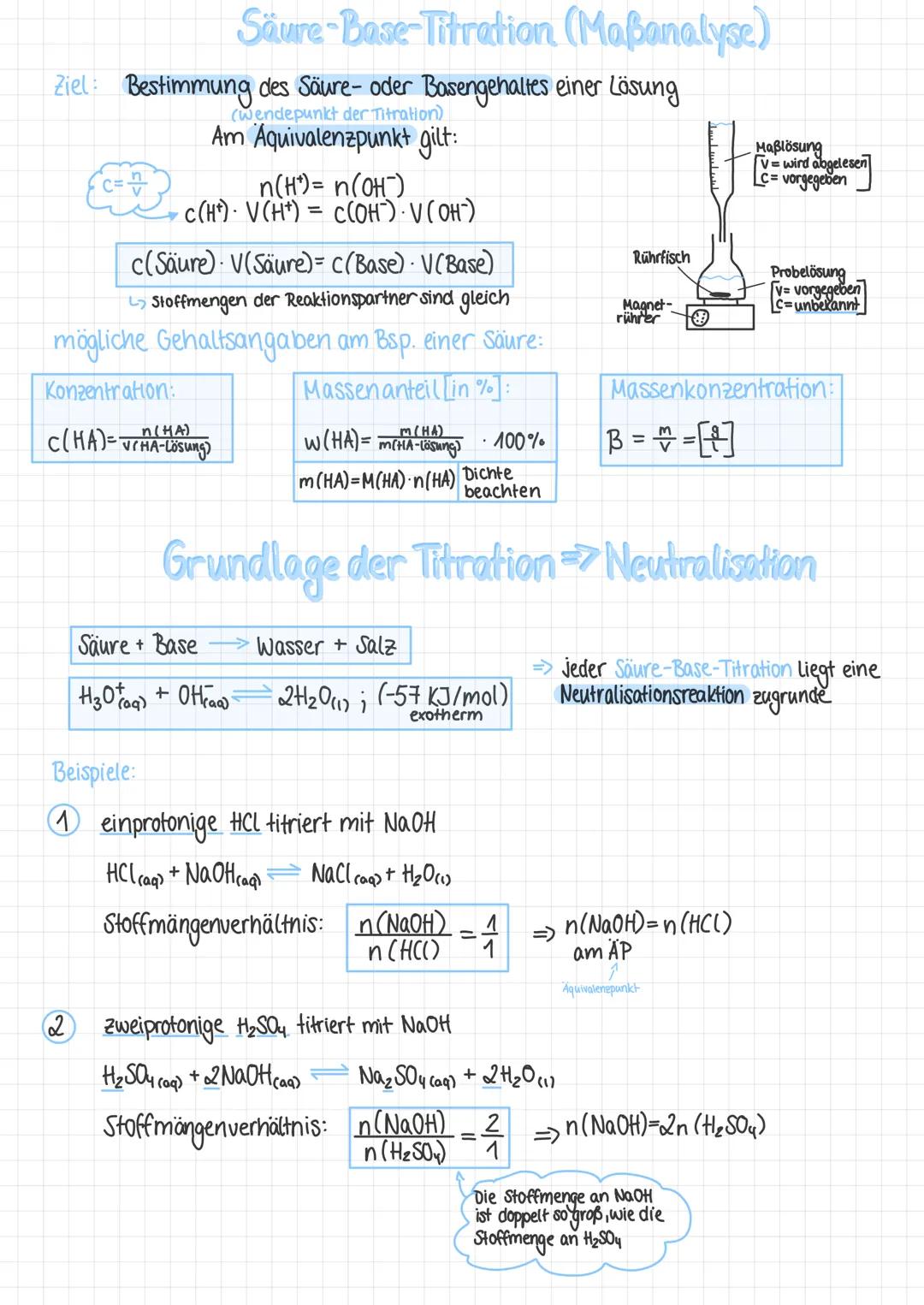
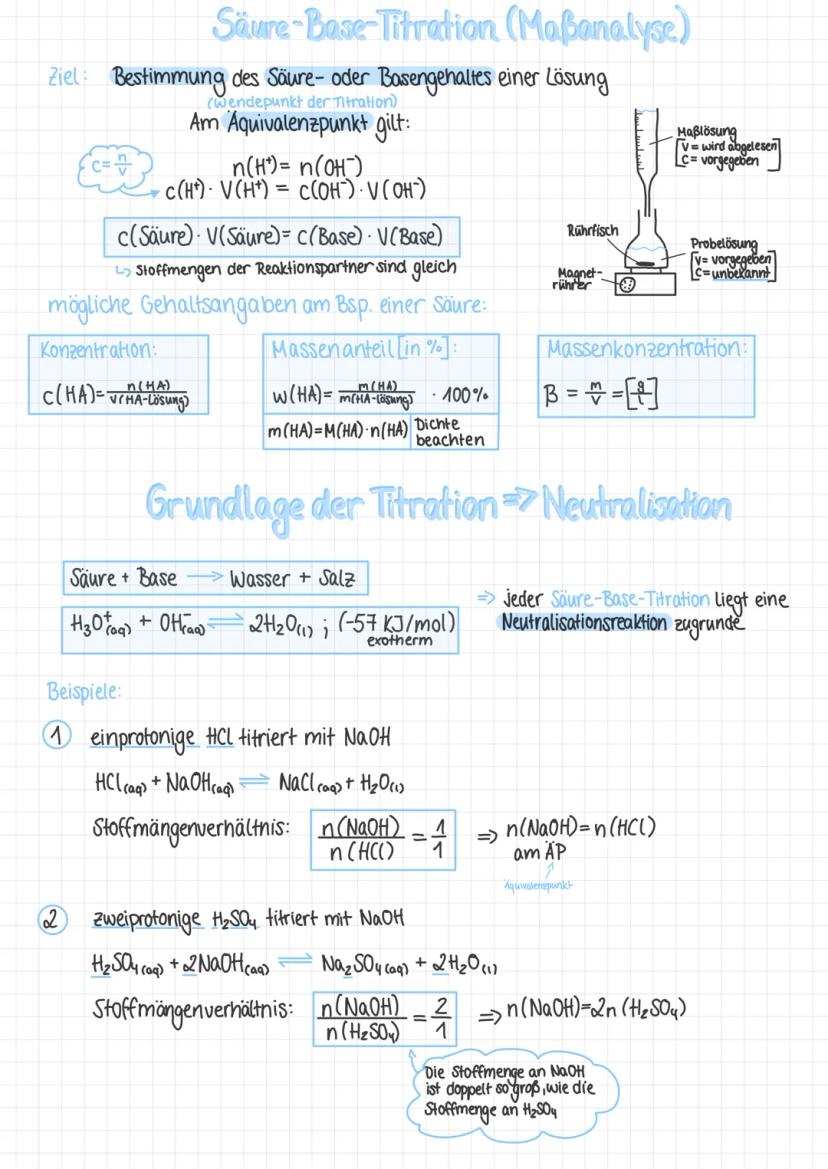
Bei der Titration bestimmst du unbekannte Säure- oder Basenkonzentrationen durch kontrollierte Neutralisation. Das Ziel ist der Äquivalenzpunkt (AP), wo gilt: n(H⁺) = n(OH⁻).
Die zentrale Formel lautet: c(Säure) × V(Säure) = c(Base) × V(Base). Bei zweiprotonigen Säuren wie H₂SO₄ musst du das Stoffmengenverhältnis beachten: n(NaOH) = 2 × n(H₂SO₄).
Jeder Titration liegt eine Neutralisation zugrunde: H₃O⁺ + OH⁻ → 2H₂O. Diese Reaktion ist exotherm und läuft bei allen Säure-Base-Titrationen gleich ab.
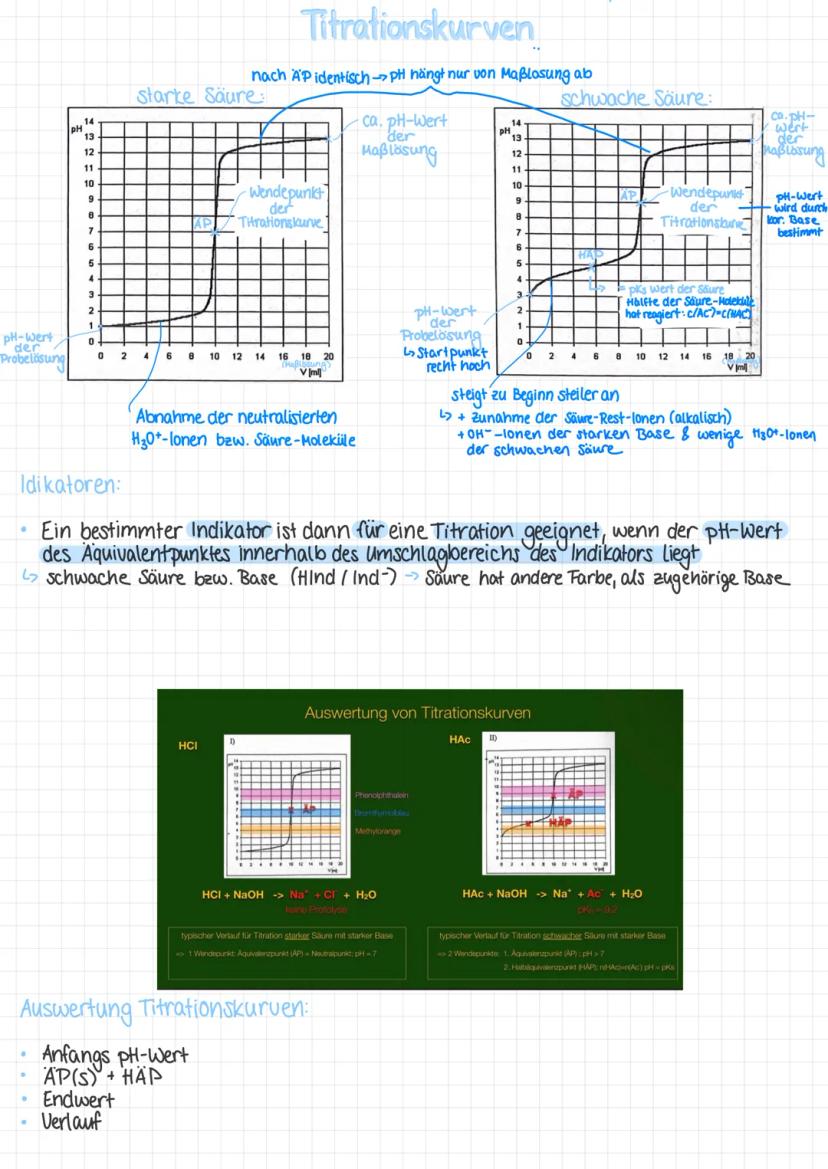
Praxistipp: Den Äquivalenzpunkt erkennst du am steilsten Anstieg der Titrationskurve - hier ändert sich der pH-Wert am stärksten!

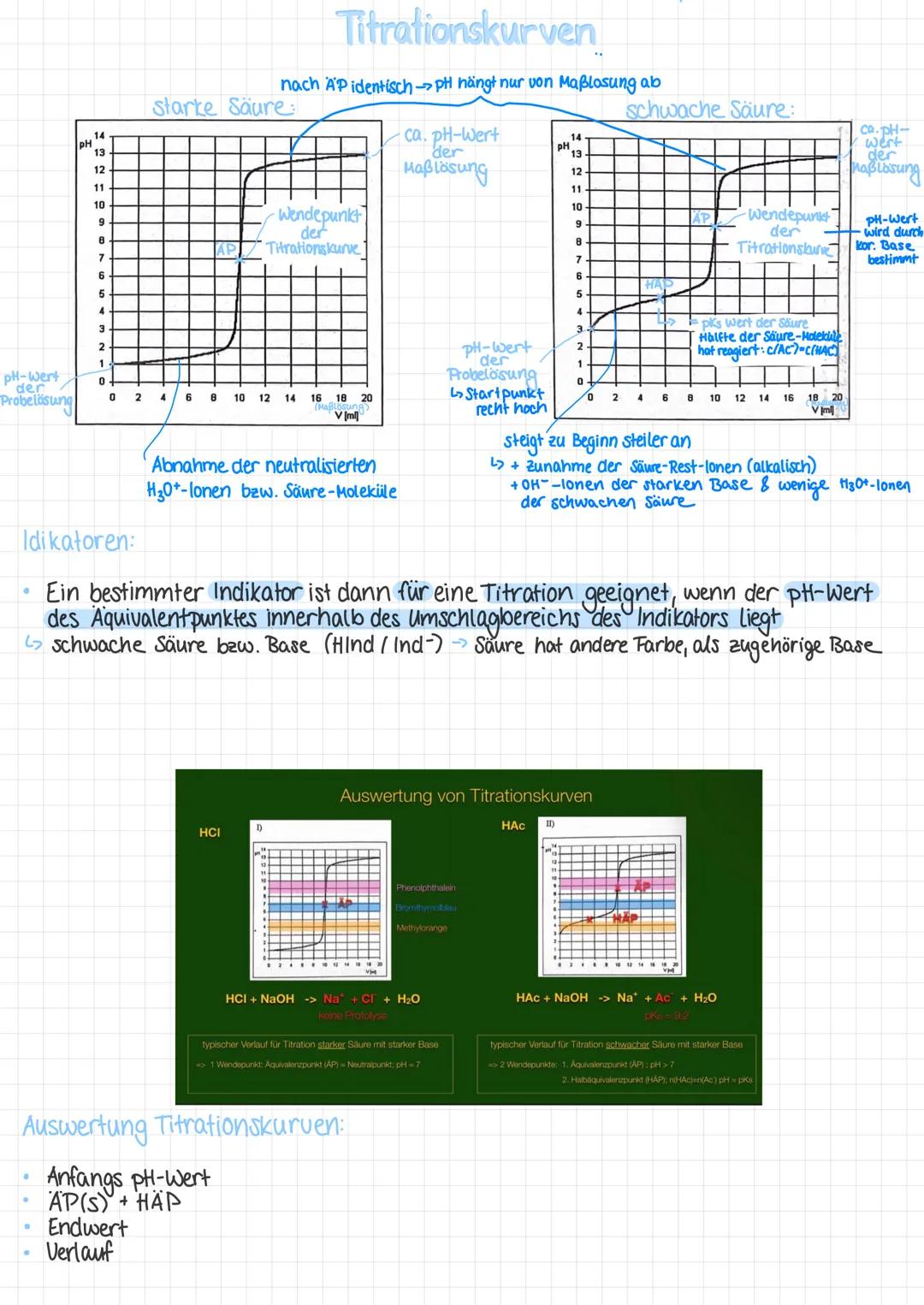
Bei der Titration von 0,1 M HCl mit 1 M NaOH kannst du jeden Punkt der Titrationskurve berechnen. Start: HCl ist eine starke Säure, also pH = -lg(0,1) = 1.
Äquivalenzpunkt: Hier sind alle H₃O⁺-Ionen neutralisiert. Der pH-Wert wird nur noch durch die Autoprotolyse des Wassers bestimmt → pH = 7. Das ist der charakteristische Neutralpunkt bei starken Säure-Base-Titrationen.
Nach dem AP: Überschüssige NaOH bestimmt den pH-Wert. Bei 10 mL Überschuss erhältst du c(OH⁻) = 0,083 mol/L und damit pH = 12,92.
Wichtig: Bei starken Säuren und Basen liegt der Äquivalenzpunkt immer bei pH = 7, weil keine Hydrolyse stattfindet!

Die Titration schwacher Säuren ist komplexer! Start: Essigsäure ergibt pH = 2,9 bei c = 0,1 M.
Halbäquivalenzpunkt (HAP): Hier ist die Hälfte der Säure neutralisiert. Es gilt c(HAc) = c(Ac⁻), deshalb: pH = pKs = 4,8. Diese Henderson-Hasselbalch-Beziehung ist goldwert!
Äquivalenzpunkt: Jetzt bestimmt das entstandene Acetat-Ion den pH-Wert. Ac⁻ ist eine schwache Base , daher pH > 7. Konkret: pH ≈ 8,8.
Achtung: Bei schwachen Säuren liegt der AP immer im basischen Bereich - vergiss das nicht bei der Indikator-Auswahl!
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Sophia
@sophiad._xhjt
Säuren und Basen begegnen dir täglich - vom Reinigungsmittel bis zum Aspirin in der Hausapotheke. Diese wichtigen chemischen Verbindungen bestimmen nicht nur den pH-Wert deines Shampoos, sondern auch, warum manche Stoffe ätzend wirken und andere neutralisierend.

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Basen sind die Superhelden der Reinigung - ihre negativ geladenen Teilchen heften sich an Schmutz und sorgen dafür, dass sich dieser leichter ablöst. Außerdem zersetzen sie hartnäckige Proteine und Fette.
Säuren hingegen sind perfekt gegen Kalk und Urinstein. Sie lösen diese Ablagerungen durch chemische Reaktionen auf und werden deshalb oft in WC-Reinigern verwendet. In Lebensmitteln hemmen Säuren das Wachstum von Mikroorganismen und sorgen für längere Haltbarkeit.
Nach Brönsted sind Säuren Protonendonatoren und Basen Protonenakzeptoren (nehmen Protonen auf). Diese Definition ist viel praktischer als die von Arrhenius, weil sie nicht nur auf wässrige Lösungen beschränkt ist.
Merke: Säure-Base-Reaktionen funktionieren nach dem Donator-Akzeptor-Prinzip - es braucht immer beide Partner für eine Reaktion!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Protolyse ist der Fachbegriff für jede Säure-Base-Reaktion, bei der Protonen von einer Säure auf eine Base übertragen werden. Ohne eine passende Base kann eine Säure kein Proton abgeben - sie braucht einen "Empfänger".
Korrespondierende Säure-Base-Paare unterscheiden sich nur um ein Proton. Wenn HCl ein Proton abgibt, entsteht Cl⁻ - diese beiden bilden ein korrespondierendes Paar. An jeder Protolyse sind immer zwei solcher Paare beteiligt.
Ampholyte sind echte Alleskönner - sie können je nach Reaktionspartner sowohl als Säure als auch als Base reagieren. Das bekannteste Beispiel ist Wasser: Mit starken Säuren verhält es sich wie eine Base, mit starken Basen wie eine Säure.
Tipp: Mehrprotonige Säuren wie H₂SO₄ können mehrere Protonen nacheinander abgeben - jedes Mal entsteht eine schwächere korrespondierende Base!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Wasser führt ständig Selbstgespräche auf molekularer Ebene! Bei der Autoprotolyse übertragen sich Wassermoleküle gegenseitig Protonen: H₂O + H₂O ⇌ H₃O⁺ + OH⁻.
Das Ionenprodukt des Wassers Kw = 10⁻¹⁴ mol²/L² ist bei 25°C konstant. Daraus folgt: pKw = pH + pOH = 14. Diese Formel ist dein bester Freund bei pH-Berechnungen!
Der pH-Wert ist der negative Zehnerlogarithmus der H₃O⁺-Konzentration: pH = -lg c(H₃O⁺). Die Skala reicht meist von 0-14:
Praxistipp: Bei pH-Rechnungen immer daran denken, dass sich die Konzentrationen von H₃O⁺ und OH⁻ umgekehrt proportional verhalten!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Säurekonstante Ks zeigt dir, wie gerne eine Säure ihre Protonen abgibt. Je größer Ks, desto stärker die Säure. Analog dazu misst die Basenkonstante KB die Protonengier einer Base.
Um mit den vielen Zehnerpotenzen klarzukommen, verwendest du pKs = -lg Ks. Hier gilt: Je kleiner der pKs-Wert, desto stärker die Säure! HCl hat pKs = -7 (sehr stark), Essigsäure pKs = 4,8 (schwach).
Ein geniales Gesetz verbindet korrespondierende Paare: pKs + pKB = 14. Ist eine Säure stark (kleiner pKs), ist ihre korrespondierende Base automatisch schwach (großer pKB).
Eselsbrücke: Starke Säuren haben schwache korrespondierende Basen - wie bei einer Wippe: ist eine Seite oben, ist die andere unten!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Bei starken Säuren (pKs < 1) wie HCl geht alles schnell und einfach: Sie reagieren vollständig mit Wasser. Deshalb gilt: pH = -lg c₀(HA). Eine 0,1 M HCl-Lösung hat also pH = 1.
Schwache Säuren (pKs > 4) sind komplizierter, weil sie nur teilweise reagieren. Hier brauchst du die Formel: pH = ½. Bei Essigsäure mit c = 0,1 M ergibt das pH = 2,9.
Für starke Basen berechnest du erst pOH = -lg c₀(B), dann pH = 14 - pOH. Bei schwachen Basen verwendest du: pH = 14 - ½.
Achtung: Die Vereinfachungsformeln gelten nur, wenn die Annahmen erfüllt sind - bei sehr verdünnten Lösungen musst du genauer rechnen!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Warum ist Methansäure stärker als Butansäure? Die Antwort liegt im induktiven Effekt! Alkylketten wie -CH₃ haben einen +I-Effekt - sie "schieben" Elektronen zum Sauerstoff der Säuregruppe.
Mehr Elektronendichte am Sauerstoff bedeutet: Die O-H-Bindung wird stärker, das Proton lässt sich schwerer abspalten. Je länger die Alkylkette, desto stärker der +I-Effekt und desto schwächer die Säure.
Umgekehrt haben elektronegative Gruppen wie Fluor einen -I-Effekt - sie ziehen Elektronen ab. Das schwächt die O-H-Bindung und macht die Säure stärker. Trichloressigsäure ist deshalb viel stärker als Essigsäure.
Merkregel: Alkylreste machen Säuren schwächer , elektronegative Gruppen machen sie stärker !

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Bei der Titration bestimmst du unbekannte Säure- oder Basenkonzentrationen durch kontrollierte Neutralisation. Das Ziel ist der Äquivalenzpunkt (AP), wo gilt: n(H⁺) = n(OH⁻).
Die zentrale Formel lautet: c(Säure) × V(Säure) = c(Base) × V(Base). Bei zweiprotonigen Säuren wie H₂SO₄ musst du das Stoffmengenverhältnis beachten: n(NaOH) = 2 × n(H₂SO₄).
Jeder Titration liegt eine Neutralisation zugrunde: H₃O⁺ + OH⁻ → 2H₂O. Diese Reaktion ist exotherm und läuft bei allen Säure-Base-Titrationen gleich ab.
Praxistipp: Den Äquivalenzpunkt erkennst du am steilsten Anstieg der Titrationskurve - hier ändert sich der pH-Wert am stärksten!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Bei der Titration von 0,1 M HCl mit 1 M NaOH kannst du jeden Punkt der Titrationskurve berechnen. Start: HCl ist eine starke Säure, also pH = -lg(0,1) = 1.
Äquivalenzpunkt: Hier sind alle H₃O⁺-Ionen neutralisiert. Der pH-Wert wird nur noch durch die Autoprotolyse des Wassers bestimmt → pH = 7. Das ist der charakteristische Neutralpunkt bei starken Säure-Base-Titrationen.
Nach dem AP: Überschüssige NaOH bestimmt den pH-Wert. Bei 10 mL Überschuss erhältst du c(OH⁻) = 0,083 mol/L und damit pH = 12,92.
Wichtig: Bei starken Säuren und Basen liegt der Äquivalenzpunkt immer bei pH = 7, weil keine Hydrolyse stattfindet!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Die Titration schwacher Säuren ist komplexer! Start: Essigsäure ergibt pH = 2,9 bei c = 0,1 M.
Halbäquivalenzpunkt (HAP): Hier ist die Hälfte der Säure neutralisiert. Es gilt c(HAc) = c(Ac⁻), deshalb: pH = pKs = 4,8. Diese Henderson-Hasselbalch-Beziehung ist goldwert!
Äquivalenzpunkt: Jetzt bestimmt das entstandene Acetat-Ion den pH-Wert. Ac⁻ ist eine schwache Base , daher pH > 7. Konkret: pH ≈ 8,8.
Achtung: Bei schwachen Säuren liegt der AP immer im basischen Bereich - vergiss das nicht bei der Indikator-Auswahl!

Zugriff auf alle Dokumente
Verbessere deine Noten
Schließ dich Millionen Schülern an
Unser KI-Begleiter ist ein speziell für Schüler entwickeltes KI-Tool, das mehr als nur Antworten bietet. Basierend auf Millionen von Knowunity-Inhalten liefert er relevante Informationen, personalisierte Lernpläne, Quizze und Inhalte direkt im Chat und passt sich deinem individuellen Lernweg an.
Du kannst die App im Google Play Store und im Apple App Store herunterladen.
Genau! Genieße kostenlosen Zugang zu Lerninhalten, vernetze dich mit anderen Schülern und hol dir sofortige Hilfe – alles direkt auf deinem Handy.
63
Smart Tools NEU
Verwandle diesen Lernzettel in: ✓ 50+ Übungsfragen ✓ Interaktive Karteikarten ✓ Komplette Probeklausur ✓ Aufsatzgliederungen
Entdecken Sie die Chemie der Kohlenhydrate, einschließlich Pyranose und Furanose, Chiralität, Reaktionsmechanismen und die Bedeutung von Aldosen und Ketosen. Diese Zusammenfassung behandelt auch Disaccharide und Polysaccharide sowie deren chemische Eigenschaften und Reaktionen, wie die Fehling-Probe. Ideal für Chemie LK-Studierende.
Erfahren Sie alles über Pufferlösungen: Definition, Beispiele und die Berechnung des pH-Wertes mithilfe der Henderson-Hasselbalch-Gleichung. Entdecken Sie die maximale Pufferwirkung, Pufferdiagramme und die Grenzen des Pufferbereichs. Ideal für Chemie-Studierende, die ein tiefes Verständnis für Säure-Base-Gleichgewichte entwickeln möchten.
Entdecken Sie die Grundlagen der pH-Wert-Berechnung und die Säure-Basen-Theorie in dieser Klausurvorbereitung. Die Inhalte umfassen die elektrolytische Dissoziation, das Säure-Base-Gleichgewicht sowie spezifische Berechnungen für verschiedene Säuren wie Salzsäure, Essigsäure und Milchsäure. Ideal für Studierende, die sich auf Prüfungen im Bereich Chemie vorbereiten.
Erfahren Sie alles über die Berechnung des pH-Werts, die Titration von Essigsäure mit Natronlauge und die Brönsted-Säure-Base-Theorie. Diese Zusammenfassung behandelt wichtige Konzepte wie die Titrationskurve, das Gleichgewicht in wässrigen Lösungen und die Pufferformel. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten.
Erfahren Sie alles über Säure-Base-Titrationen und die Rolle von pH-Indikatoren. Diese Zusammenfassung behandelt die Funktionsweise von Indikatoren, den Einfluss von pH-Werten auf die Farbdarstellung und die Anwendung der Henderson-Hasselbalch-Gleichung. Ideal für Chemie-Studierende, die sich auf Prüfungen vorbereiten oder ihr Wissen vertiefen möchten.
Entdecken Sie die Grundlagen der Säure-Base-Chemie: von der Brønsted-Theorie über Säurestärken (Ks und pKs) bis hin zu Protolysegraden, pH-Wert-Berechnungen, Titrationsmethoden und Puffersystemen. Diese Zusammenfassung bietet eine klare Übersicht über Neutralisationsreaktionen und das Verhalten von Säuren und Basen in wässrigen Lösungen.
App Store
Google Play
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer
Die App ist sehr einfach zu bedienen und gut gestaltet. Ich habe bisher alles gefunden, wonach ich gesucht habe, und konnte viel aus den Präsentationen lernen! Ich werde die App definitiv für ein Schulprojekt nutzen! Und natürlich hilft sie auch sehr als Inspiration.
Stefan S
iOS-Nutzer
Diese App ist wirklich super. Es gibt so viele Lernzettel und Hilfen [...]. Mein Problemfach ist zum Beispiel Französisch und die App hat so viele Möglichkeiten zur Hilfe. Dank dieser App habe ich mich in Französisch verbessert. Ich würde sie jedem empfehlen.
Samantha Klich
Android-Nutzerin
Wow, ich bin wirklich begeistert. Ich habe die App einfach mal ausprobiert, weil ich sie schon oft beworben gesehen habe und war absolut beeindruckt. Diese App ist DIE HILFE, die man für die Schule braucht und vor allem bietet sie so viele Dinge wie Übungen und Lernzettel, die mir persönlich SEHR geholfen haben.
Anna
iOS-Nutzerin
Beste App der Welt! Keine Worte, weil sie einfach zu gut ist
Thomas R
iOS-Nutzer
Einfach genial. Lässt mich 10x besser lernen, diese App ist eine glatte 10/10. Ich empfehle sie jedem. Ich kann Lernzettel anschauen und suchen. Ich kann sie im Fachordner speichern. Ich kann sie jederzeit wiederholen, wenn ich zurückkomme. Wenn du diese App noch nicht ausprobiert hast, verpasst du wirklich was.
Basil
Android-Nutzer
Diese App hat mich so viel selbstbewusster in meiner Klausurvorbereitung gemacht, nicht nur durch die Stärkung meines Selbstvertrauens durch die Features, die es dir ermöglichen, dich mit anderen zu vernetzen und dich weniger allein zu fühlen, sondern auch durch die Art, wie die App selbst darauf ausgerichtet ist, dass du dich besser fühlst. Sie ist einfach zu bedienen, macht Spaß und hilft jedem, der in irgendeiner Weise Schwierigkeiten hat.
David K
iOS-Nutzer
Die App ist einfach super! Ich muss nur das Thema in die Suche eingeben und bekomme sofort eine Antwort. Ich muss nicht mehr 10 YouTube-Videos schauen, um etwas zu verstehen, und spare dadurch richtig viel Zeit. Sehr empfehlenswert!
Sudenaz Ocak
Android-Nutzerin
In der Schule war ich echt schlecht in Mathe, aber dank der App bin ich jetzt besser geworden. Ich bin so dankbar, dass ihr die App gemacht habt.
Greenlight Bonnie
Android-Nutzerin
sehr zuverlässige App, um deine Ideen in Mathe, Englisch und anderen verwandten Themen zu verbessern. bitte nutze diese App, wenn du in bestimmten Bereichen Schwierigkeiten hast, diese App ist dafür der Schlüssel. wünschte, ich hätte früher eine Bewertung geschrieben. und sie ist auch kostenlos, also mach dir darüber keine Sorgen.
Rohan U
Android-Nutzer
Ich weiß, dass viele Apps gefälschte Accounts nutzen, um ihre Bewertungen zu pushen, aber diese App verdient das alles. Ursprünglich hatte ich eine 4 in meinen Englisch-Klausuren und dieses Mal habe ich eine 2 bekommen. Ich wusste erst drei Tage vor der Klausur von dieser App und sie hat mir SEHR geholfen. Bitte vertrau mir wirklich und nutze sie, denn ich bin sicher, dass auch du Fortschritte sehen wirst.
Xander S
iOS-Nutzer
DIE QUIZZE UND KARTEIKARTEN SIND SO NÜTZLICH UND ICH LIEBE Knowunity KI. ES IST AUCH BUCHSTÄBLICH WIE CHATGPT ABER SCHLAUER!! HAT MIR AUCH BEI MEINEN MASCARA-PROBLEMEN GEHOLFEN!! SOWIE BEI MEINEN ECHTEN FÄCHERN! NATÜRLICH 😍😁😲🤑💗✨🎀😮
Elisha
iOS-Nutzer
Diese App ist echt der Hammer. Ich finde Lernen so langweilig, aber diese App macht es so einfach, alles zu organisieren und dann kannst du die kostenlose KI bitten, dich abzufragen, so gut, und du kannst einfach deine eigenen Sachen hochladen. sehr empfehlenswert als jemand, der gerade Probeklausuren schreibt
Paul T
iOS-Nutzer